第1章蛋白质组成成分和氨基酸
- 格式:ppt
- 大小:2.14 MB
- 文档页数:163


第一章氨基酸与蛋白质上册 P1231. 1 氨基酸①①①蛋白质水解最后成为氨基酸混合物酸水解得19种 L-AA,色氨酸破坏。
碱水解得色氨酸,其余氨基酸消旋破坏。
酶水解不消旋破坏,但水解不彻底。
①①①α-氨基酸的一般结构生物体内已发现氨基酸180种,常见氨基酸20种1. 2 氨基酸的分类:常见蛋白质氨基酸,不常见蛋白质氨基酸,非蛋白氨基酸①①①常见蛋白质氨基酸,或称基本氨基酸。
每个氨基酸可用三个字母或单字母简写表示。
按侧链R基不同进行分类。
①1①按R基化学结构分类1.脂肪族氨基酸15个①.中性氨基酸5个甘氨酸 Glycine 氨基乙酸 Gly G 无旋光丙氨酸 Alanine α-氨基丙酸 Ala A缬氨酸 Valine α-氨基-β-甲基丁酸 Val V亮氨酸 Leusine α-氨基-γ-甲基戊酸 Leu L异亮氨酸 Isoleucine α-氨基-β-甲基戊酸 Ile I①.含羟基或硫氨基酸4个丝氨酸 Serine α-氨基-β-羟基丙酸 Ser S苏氨酸 Threonine α-氨基-β-羟基丁酸 Thr T半胱氨酸 Cysteine α-氨基-β-基丙酸 Cys C甲硫氨酸 Methionine α-氨基-γ-甲硫基丁酸 Met M③.酸性氨基酸及其酰胺4个天冬氨酸 Aspartic acid α-氨基丁二酸 Asp D谷氨酸 Glutamic acid α-氨基戊二酸 Glu E天冬酰胺 Asparagine α-氨基丁二酸一酰胺 Asn N谷氨酸胺 Glutamine α-氨基戊二酸一酰胺 Gln Q④. 碱性氨基酸2个赖氨酸 Lysine α,ε-二氨基已酸 Lys K精氨酸 Arginine α-氨基-δ-胍基戊酸 Arg R2.芳香族氨基酸3个苯丙氨酸 Phenylalanine α-氨基-β-苯基丙酸 Phe F酪氨酸 Tyrosine α-氨基-β-对羟苯基丙酸 Tyr Y色氨酸 Tryptophan α-氨基-β-吲哚基丙酸 Trp W3.杂环族氨基酸2个组氨酸 Histidine α-氨基-β-咪唑基丙酸 His H脯氨酸 Proline α-吡咯烷羧酸 Pro P①2①按R基极性性质分类1.非极性R基8个Ala(A) Val(V) Leu(L) Ile(I) Pro(P)Phe(F) Trp(W) Met(M)1。
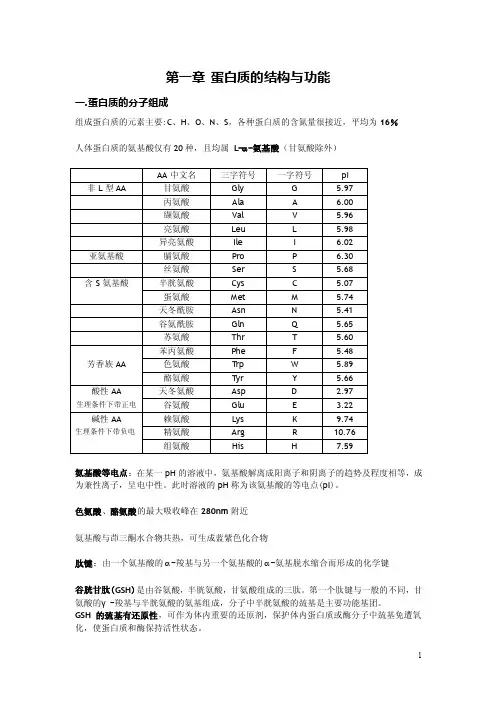
第一章蛋白质的结构与功能一.蛋白质的分子组成组成蛋白质的元素主要:C、H、O、N、S,各种蛋白质的含氮量很接近,平均为16%人体蛋白质的氨基酸仅有20种,且均属L-α-氨基酸(甘氨酸除外)氨基酸等电点:在某一pH的溶液中,氨基酸解离成阳离子和阴离子的趋势及程度相等,成为兼性离子,呈电中性。
此时溶液的pH称为该氨基酸的等电点(pI)。
色氨酸、酪氨酸的最大吸收峰在280nm附近氨基酸与茚三酮水合物共热,可生成蓝紫色化合物肽键:由一个氨基酸的α-羧基与另一个氨基酸的α-氨基脱水缩合而形成的化学键谷胱甘肽(GSH)是由谷氨酸,半胱氨酸,甘氨酸组成的三肽。
第一个肽键与一般的不同,甘氨酸的γ-羧基与半胱氨酸的氨基组成,分子中半胱氨酸的巯基是主要功能基团。
GSH的巯基有还原性,可作为体内重要的还原剂,保护体内蛋白质或酶分子中巯基免遭氧化,使蛋白质和酶保持活性状态。
二.蛋白质的分子结构α-螺旋的结构特点:1.多个肽键平面通过α-碳原子旋转,相互之间紧密盘曲成稳固的右手螺旋2.主链呈螺旋上升,每3.6个氨基酸残基上升一圈,相当于0.54nm,这与X线衍射图符合3.相邻两圈螺旋之间借肽键中C=O和NH形成许多链内氢健,这是稳定α-螺旋的主要键4.肽链中氨基酸侧链R分布在螺旋外侧,其形状、大小及电荷影响α-螺旋的形成基团影响α-螺旋的稳定性包括以下三个方面:1.酸性或碱性氨基酸集中区域(两种电荷相互排斥)2.脯氨酸不利于α-螺旋的形成3.较大R基团侧链集中区域(空间位阻效应)β-折叠要点:1.是肽链相当伸展的结构,肽链平面之间折叠成锯齿状2.依靠两条肽链或一条肽链内的两段肽链间的C=O与H形成氢键,使构象稳定3.氨基酸残基的R侧链伸出在锯齿的上方或下方4.两段肽链可以是平行的,也可以是反平行的超二级结构有三种基本形式:1.α-螺旋组合(αα)2.β-折叠组合(ββ)3.α-螺旋β-折叠组合(βαβ)三.蛋白质结构与功能的关系镰刀形红细胞贫血:血红蛋白有2个α亚基和2个β亚基组成,其中β亚基的第六个氨基酸谷氨酸突变成缬氨酸。


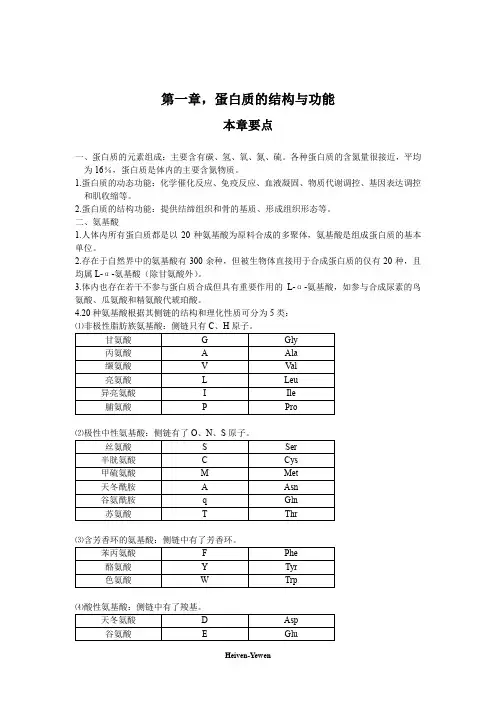
第一章,蛋白质的结构与功能本章要点一、蛋白质的元素组成:主要含有碳、氢、氧、氮、硫。
各种蛋白质的含氮量很接近,平均为16%,蛋白质是体内的主要含氮物质。
1.蛋白质的动态功能:化学催化反应、免疫反应、血液凝固、物质代谢调控、基因表达调控和肌收缩等。
2.蛋白质的结构功能:提供结缔组织和骨的基质、形成组织形态等。
二、氨基酸1.人体内所有蛋白质都是以20种氨基酸为原料合成的多聚体,氨基酸是组成蛋白质的基本单位。
2.存在于自然界中的氨基酸有300余种,但被生物体直接用于合成蛋白质的仅有20种,且均属L-α-氨基酸(除甘氨酸外)。
3.体内也存在若干不参与蛋白质合成但具有重要作用的L-α-氨基酸,如参与合成尿素的鸟氨酸、瓜氨酸和精氨酸代琥珀酸。
4.20种氨基酸根据其侧链的结构和理化性质可分为5类:⑴非极性脂肪族氨基酸:侧链只有C、H原子。
⑶含芳香环的氨基酸:侧链中有了芳香环。
⑷酸性氨基酸:侧链中有了羧基。
芳香族氨基酸中苯基的疏水性较强,酚基和吲哚基在一定条件下可解离;酸性氨基酸的侧链都含有羧基;而碱性氨基酸的侧链分别含有氨基、胍基或咪唑基。
5.20种氨基酸具有共同或特异的理化性质:⑴氨基酸具有两性解离的性质。
①所有氨基酸都含有碱性的α-氨基和酸性的α-羧基,可在酸性溶液中与质子(H+)结合呈带正电荷的阳离子(),也可在碱性溶液中与(OH-)结合,失去质子变成带负电荷的阴离子()。
②氨基酸是一种两性电解质,具有两性解离的特性。
③在某一PH的溶液中,氨基酸解离成阳离子和阴离子的趋势及程度相等,成为兼性离子,呈电中性,此时溶液的PH称为该氨基酸的等电点。
④取兼性离子两边的pK值的平均值,即为此氨基酸的pI值:pI=1/2(pK1+pK2)⑵含共轭双键的氨基酸具有紫外线吸收性质①含有共轭双键的色氨酸、酪氨酸的最大吸收峰在280nm波长附近。
②由于大多数蛋白质含有酪氨酸和色氨酸残基,所以测定蛋白质溶液280nm的光吸收值,是分析溶液中蛋白质含量的快速简便的方法。

第⼀篇⽣物⼤分⼦的结构与功能第⼀章氨基酸和蛋⽩质⼀、组成蛋⽩质的20种氨基酸的分类1、⾮极性氨基酸包括:⽢氨酸、丙氨酸、缬氨酸、亮氨酸、异亮氨酸、苯丙氨酸、脯氨酸2、极性氨基酸极性中性氨基酸:⾊氨酸、酪氨酸、丝氨酸、半胱氨酸、蛋氨酸、天冬酰胺、⾕氨酰胺、苏氨酸酸性氨基酸:天冬氨酸、⾕氨酸碱性氨基酸:赖氨酸、精氨酸、组氨酸其中:属于芳⾹族氨基酸的是:⾊氨酸、酪氨酸、苯丙氨酸属于亚氨基酸的是:脯氨酸含硫氨基酸包括:半胱氨酸、蛋氨酸注意:在识记时可以只记第⼀个字,如碱性氨基酸包括:赖精组⼆、氨基酸的理化性质1、两性解离及等电点氨基酸分⼦中有游离的氨基和游离的羧基,能与酸或碱类物质结合成盐,故它是⼀种两性电解质。
在某⼀PH的溶液中,氨基酸解离成阳离⼦和阴离⼦的趋势及程度相等,成为兼性离⼦,呈电中性,此时溶液的PH称为该氨基酸的等电点。
2、氨基酸的紫外吸收性质芳⾹族氨基酸在280nm波长附近有的紫外吸收峰,由于⼤多数蛋⽩质含有这些氨基酸残基,氨基酸残基数与蛋⽩质含量成正⽐,故通过对280nm波长的紫外吸光度的测量可对蛋⽩质溶液进⾏定量分析。
3、茚三酮反应氨基酸的氨基与茚三酮⽔合物反应可⽣成蓝紫⾊化合物,此化合物吸收峰在570nm波长处。
由于此吸收峰值的⼤⼩与氨基酸释放出的氨量成正⽐,因此可作为氨基酸定量分析⽅法。
三、肽两分⼦氨基酸可借⼀分⼦所含的氨基与另⼀分⼦所带的羧基脱去1分⼦⽔缩合成最简单的⼆肽。
⼆肽中游离的氨基和羧基继续借脱⽔作⽤缩合连成多肽。
10个以内氨基酸连接⽽成多肽称为寡肽;39个氨基酸残基组成的促肾上腺⽪质激素称为多肽;51个氨基酸残基组成的胰岛素归为蛋⽩质。
多肽连中的⾃由氨基末端称为N端,⾃由羧基末端称为C端,命名从N端指向C端。
⼈体内存在许多具有⽣物活性的肽,重要的有:⾕胱⽢肽(GSH):是由⾕、半胱和⽢氨酸组成的三肽。
半胱氨酸的巯基是该化合物的主要功能基团。
GSH的巯基具有还原性,可作为体内重要的还原剂保护体内蛋⽩质或酶分⼦中巯基免被氧化,使蛋⽩质或酶处于活性状态。



第一篇蛋白质的结构与功能(第一~四章小结)第一章氨基酸氨基酸是一类同时含有氨基和羧基的有机小分子。
组成多肽和蛋白质的氨基酸除Gly外,都属于L型的α- 氨基酸(Pro为亚氨基酸)。
氨基酸不仅可以作为寡肽、多肽和蛋白质的组成单位或生物活性物质的前体,也可以作为神经递质或糖异生的前体,还能氧化分解产生ATP。
目前已发现蛋白质氨基酸有22种,其中20种最为常见,而硒半胱氨酸和吡咯赖氨酸比较罕见。
非蛋白质氨基酸通常以游离的形式存在,作为代谢的中间物和某些物质的前体,具有特殊的生理功能。
22种标准氨基酸可使用三字母或单字母缩写来表示。
某些标准氨基酸在细胞内会经历一些特殊的修饰成为非标准蛋白质氨基酸。
氨基酸有多种不同的分类方法:根据R基团的化学结构和在pH7时的带电状况,可分为脂肪族氨基酸、不带电荷的极性氨基酸、芳香族氨基酸、带正电荷的极性氨基酸和带负电荷的极性氨基酸;根据R基团对水分子的亲和性,可分为亲水氨基酸和疏水氨基酸;根据对动物的营养价值,可分为必需氨基酸和非必需氨基酸。
氨基酸的性质由其结构决定。
其共性有:缩合反应、手性(Gly除外)、两性解离、具有等电点,以及氨基酸氨基和羧基参与的化学反应,包括与亚硝酸的反应、与甲醛的反应、Sanger反应、与异硫氰酸苯酯的反应和与茚三酮的反应等。
与亚硝酸的反应可用于Van Slyke定氮,与甲醛的反应可用于甲醛滴定,Sanger反应和与异硫氰酸苯酯的反应可用来测定N-端氨基酸。
只有脯氨酸和羟脯氨酸与茚三酮反应产生黄色物质,其余生成蓝紫色物质,利用此反应可对氨基酸进行定性或定量分析。
多数氨基酸的侧链可能发生特殊的反应,可以此鉴定氨基酸。
不同氨基酸在物理、化学性质上的差异可用来分离氨基酸,其中最常见的方法是电泳和层析。
第二章蛋白质的结构肽是氨基酸之间以肽键相连的聚合物,它包括寡肽、多肽和蛋白质。
氨基酸是构成肽的基本单位。
线形肽链都含有N端和C端,书写一条肽链的序列总是从N端到C端。

蛋⽩质结构与功能-----氨基酸蛋⽩质结构与功能——氨基酸2010遗传学Chapter 1 氨基酸I 蛋⽩质的天然组成天然蛋⽩质⼏乎都是由18种普通的氨基酸组成:L-氨基酸,L-亚氨基酸(脯氨酸)和⽢氨酸。
⼀些稀有的氨基酸在少量的蛋⽩质中结合了L-硒代胱氨酸。
II 氨基酸的结果每种氨基酸(除了脯氨酸):都有⼀个羧基,⼀个氨基,⼀个特异性的侧链(R基)连接在α碳原⼦上。
在蛋⽩质中,这些羧基和氨基⼏乎全部都结合成肽键。
在⼀般情况下,除了氢键的构成以外,是不会发⽣化学反应的。
氨基酸的侧链残基(R基)提供了多种多样的功能基团,这些基团赋予蛋⽩质分⼦独特的性质,导致:A.⼀种独特的折叠构象B.溶解性的差异C.聚集态D.和配基或其他⼤分⼦构成复合物的能⼒,酶活性等等。
蛋⽩质的功能是与蛋⽩质氨基酸排列顺序和每个氨基酸残基的特征有关。
那些残基赋予蛋⽩质独⼀⽆⼆的功能。
氨基酸的分类是依照它的侧链性质的A.⾮极性侧链的氨基酸B.不带电的极性侧链氨基酸C.酸性侧链的氨基酸D .碱性侧链的氨基酸A.⾮极性侧链氨基酸⾮极性氨基酸在蛋⽩质中的位置:在可溶性蛋⽩质中,⾮极性氨基酸链趋向于集中在蛋⽩质内部。
⽢氨酸(Gly G ) 结构:最简单的氨基酸,在蛋⽩质氨基酸当中,是唯⼀缺乏⾮对称结构的氨基酸。
特征:⽢氨酸在蛋⽩质结构中起到⼀个很重要的作⽤,与其它氨基酸残基相⽐,由于缺少β-碳原⼦,它在蛋⽩质的构象上有很⼤的灵活性和更容易达到它的空间结构。
功能和位置:1. ⽢氨酸经常位于紧密转⾓;和出现在⼤分⼦侧链产⽣空间位阻影响螺旋的紧密包装处(如胶原)和结合底物的地⽅。
2. 由于缺乏空间位阻侧链,所以⽢氨酸在邻近的肽键的位置有更强化学反应活性。
例如:Asn-Gly3. ⽢氨酸也出现在酶催化蛋⽩质特异性修饰的识别位点,例如N 端的⼗四酰基化(CH2(CH2)12CO -)和精氨酸甲基化的信号序列。
丙氨酸 (Ala A )结构:是20种氨基酸中最没有“个性”的氨基酸,没有长侧链,没有特别的构象性质,可以出现在蛋⽩质结构的任何部位。
第一章蛋白质学习要点一、元素组成特点:含氮量较恒定,蛋白质系数( 6.25 )二、氨基酸1.蛋白氨基酸:氨基酸(20种)——组成蛋白质的基本单位(1)特点:—L —型氨基酸;(2 )表示:中,英:三字母;(3)分类:原则:生理pH (中性)条件下R—基的带电性;类别(4类):非极性R基氨基酸,极性不带电荷R基氨基酸,负电荷R基氨基酸(酸性氨基酸),正电荷R基氨基酸(碱性氨基酸)2. 性质:(1)两性解离和等电点:两性解离:氨基酸可酸性和碱性解离,解离状态不同,所带电荷不同,酸正碱负等电点(pl )定义:净电荷等于零时的环境pH值等电点时的特点:溶解度下降pl计算法(2 )重要反应:茚三酮反应(氨基酸定性定量)3. 分离方法分配层析,离子交换层析三、肽1.概念:N端、C端;主肽链2. 书写方式:左T右,N R C四、蛋白质结构 1. 一级结构:定义特点:基础结构,稳定结构一级结构与功能的关系:一级结构不同功能可能不同2. 二级结构:(1)概念:二级结构定义;肽键平面(不能自由旋转)(2)种类(4类):—螺旋:要点:单链、右旋,众多氢键;-折叠:肽链伸展,形成链间氢键(成为片层)有平行和反平行两种;—转角(回折):肽链180°旋转,氢键连接;无规则卷曲。
3. 超二级结构:定义4. 结构域:定义5. 三级结构:定义;特点:外亲内疏6. 四级结构:定义,亚基与肽链的区别7. 维持蛋白质空间结构的作用力:氢键、盐键、疏水作用力、二硫键、范德华引力8. 空间结构与功能的关系:一定的结构,一定的功能;结构变化,功能变化;结构破坏,功能破坏六、蛋白质性质 1.两性解离等电点:(1)两性解离:酸、碱解离,酸正碱负(2)等电点(pl )定义:蛋白质净电荷等于零时的环境pH值特点:溶解度降低(3)电泳:原理:不同蛋白的电荷正负和数量不同,分子量不同,形状不同,因此在电场中的运动速度不同。
方向与速度的鉴别:pl —pH,正负决定方向,数值为速度。
第一章蛋白质·蛋白质(protein)就是由许多氨基酸(amino acids)通过肽键(prpide bond)相连形成得高分子含氮化合物。
·具有复杂空间结构得蛋白质不仅就是生物体得重要结构物质之一,而且承担着各种生物学功能,其动态功能包括:化学催化反应、免疫反应、血液凝固、物质代谢调控、基因表达调控与肌收缩等;就其结构功能而言,蛋白质提供结缔组织与骨得基质、形成组织形态等。
·显而易见,普遍存在于生物界得蛋白质就是生物体得重要组成成分与生命活动得基本物质基础,也就是生物体中含量最丰富得生物大分子(biomacromolecule)·蛋白质就是生物体重要组成成分。
分布广:所有器官、组织都含有蛋白质;细胞得各个部分都含有蛋白质含量高:蛋白质就是细胞内最丰富得有机分子,占人体干重得45%,某些组织含量更高,例如:脾、肺及横纹肌等高达80%。
·蛋白质具有重要得生物学功能。
1)作为生物催化剂(酶)2)代谢调节作用3)免疫保护作用4)物质得转运与存储5)运动与支持作用6)参与细胞间信息传递·氧化功能第一节蛋白质得分子组成(The Molecular Structure of Protein)1、组成元素:C(50%-55%)、H(6%-7%)、O(19%-24%)、N(13%-19%)、S(0-4%)。
有些但被指含少量磷、硒或金属元素铁、铜、锌、锰、钴、钼,个别还含碘。
2、各蛋白质含氮量接近,平均为16%。
100g样品中蛋白质得含量(g%)=每克样品含氮克数*6、25*100,即每克样品含氮克数除以16%。
凯氏定氮法:在有催化剂得条件下,用浓硫酸消化样品将有机氮都转化为无机铵盐,然后在碱性条件下将铵盐转化为氨,随水蒸气蒸馏出来并为过量得硼酸液吸收,再以标准盐酸滴定,就可计算出样品中得氮量。
此法就是经典得蛋白质定量方法。
一、氨基酸——组成蛋白质得基本单位存在于自然界得氨基酸有300余种,但组成人体蛋白质得氨基酸仅有20种,且均属L-氨基酸(甘氨酸除外),手性,具有旋光性(甘氨酸除外,甘氨酸R基团为-H)。