慢病毒载体构建步骤研究
- 格式:docx
- 大小:37.47 KB
- 文档页数:11

慢病毒载体构建原理
慢病毒(lentivirus)是一类病毒,属于反转录病毒的一种。
慢病毒可以作为基因转移的工具,被广泛应用于基因治疗、基因编辑、干细胞研究等领域。
慢病毒载体构建是利用慢病毒作为基因传递的载体,将外源基因导入慢病毒基因组中,并通过慢病毒的复制和转录机制,将外源基因稳定地表达在宿主细胞中的过程。
慢病毒载体构建的原理主要包括以下几个步骤:
1. 选择适当的慢病毒载体,慢病毒载体通常由慢病毒的基因组和外源基因组成。
在构建慢病毒载体时,需要选择适当的慢病毒载体,通常选择已经经过改造的慢病毒载体作为基础,然后将需要表达的外源基因插入到载体中。
2. 插入外源基因,将需要表达的外源基因插入到慢病毒载体的适当位置。
通常采用限制性内切酶切割和连接酶连接的方法,将外源基因与慢病毒载体连接起来,形成重组的慢病毒载体。
3. 构建重组慢病毒载体,将插入了外源基因的慢病毒载体导入到适当的宿主细胞中,利用宿主细胞的复制和转录机制,使重组慢
病毒载体在宿主细胞中稳定复制和表达外源基因。
4. 验证慢病毒载体的稳定性和表达效果,对构建的重组慢病毒
载体进行验证,包括验证慢病毒载体在宿主细胞中的稳定性和外源
基因的表达效果。
通常采用PCR、Western blot等方法对慢病毒载
体进行验证。
总之,慢病毒载体构建是利用慢病毒作为基因传递的载体,将
外源基因导入慢病毒基因组中,并通过慢病毒的复制和转录机制,
使外源基因稳定地表达在宿主细胞中的过程。
这一技术在基因治疗、基因编辑、干细胞研究等领域具有重要的应用前景,对于疾病治疗
和生命科学研究具有重要意义。

慢病毒载体构建原理
慢病毒载体是一种常用于基因转染和基因治疗研究的工具,其构建原理主要包括载体选择、基因插入、包装和转染等几个关键步骤。
下面将分别对这些步骤进行详细介绍。
首先,载体选择是慢病毒构建的第一步。
常用的慢病毒载体包括pLenti、pSico、pRetro等,这些载体通常具有较高的转染效率和稳定性。
在选择载体时,需要考虑载体的大小、复制能力、转染效率以及转染细胞类型等因素,以确保最终构建的慢病毒载体能够满足实验需求。
其次,基因插入是慢病毒构建的关键步骤之一。
一般来说,可以利用限制性内切酶切割载体,然后将待插入的基因片段与载体连接,形成重组载体。
在进行基因插入时,需要注意选择合适的限制性内切酶,控制酶切的时间和温度,以确保基因能够正确插入到载体中。
接下来是包装步骤。
包装是指将重组载体导入到包装细胞中,通过包装细胞的辅助,使其产生慢病毒颗粒。
常用的包装细胞包括293T细胞、HEK293细胞等。
在包装过程中,需要利用辅助载体,如
pMD2.G和psPAX2等,通过三质体共转染的方式,使包装细胞产生
慢病毒颗粒。
最后是转染步骤。
转染是将包装好的慢病毒颗粒导入到目标细
胞中,实现基因的转染。
在进行转染时,需要根据目标细胞的特性
选择合适的转染方法,如离体转染、体内转染等,以确保慢病毒能
够有效地转染目标细胞,并表达目标基因。
总的来说,慢病毒载体构建的原理涉及到载体选择、基因插入、包装和转染等关键步骤。
通过合理的实验设计和操作,可以构建出
稳定、高效的慢病毒载体,为基因转染和基因治疗研究提供有力的
工具支持。


USP22 ShRNA慢病毒载体的构建及鉴定目的构建并鉴定USP22基因ShRNA慢病毒载体,为进一步研究USP22基因在鼻咽癌中的作用机制奠定基础。
方法针对USP22基因的编码序列设计并合成2条特异性干扰序列,序列两端含有限制性内切酶位点HpaⅠ和XhoⅠ。
寡核苷酸链退火生成寡核苷酸双链,5′端磷酸化后将含有酶切位点的寡核苷酸双链克隆到pLL3.7慢病毒表达载体。
连接产物经转化、培养,提取其质粒,提取出来的质粒经HpaⅠ和XhoⅠ酶切电泳鉴定,鉴定正确的质粒进行测序。
构建成功的慢病毒表达载体pLL-USP22-shRNA與包装载体质粒混匀共转染于293T细胞。
通过荧光显微镜下观察绿色荧光蛋白(GFP)情况,对病毒滴度和感染效率进行检测。
结果成功构建慢病毒表达载体pLL-USP22-shRNA。
与包装载体质粒共转染293T细胞后测定慢病毒滴度为4×107 TU/ml。
结论本实验应用相关技术成功构建USP22 ShRNA慢病毒载体,为进一步研究USP22基因的生物学功能奠定了基础。
标签:USP22;慢病毒载体;构建;鉴定肿瘤细胞中基因表达具有组织特异性,USP22泛素水解酶属去泛素化酶DUB基因家族成员,其普遍表达表明其功能的保守性,因此,USP22被归类为肿瘤干细胞的标记基因而引起高度关注[1]。
国内外学者研究发现,USP22基因过表达与结直肠癌[2]、肺癌[3]、胃癌[4]、食管癌[5]、乳腺癌[6]等恶性肿瘤的浸润、转移和预后差高度相关。
沉默USP22基因表达,能显著抑制膀胱癌[7]、结直肠癌[8]细胞增殖,由此推测USP22基因可能成为肿瘤治疗的一个新靶点。
本研究通过基因工程技术构建USP22 ShRNA慢病毒载体,为进一步研究USP22基因在人鼻咽癌细胞中的作用机制提供实验基础。
1 材料与方法1.1 实验材料、试剂及仪器pLL3.7慢病毒表达载体及包装载体质粒购自广州永诺生物科技有限公司。

慢病毒包装实验流程、原理与步骤慢病毒(Lentivirus)是逆转录病毒的一种,它需要相对较长的孵育时间,所以称之为“慢”病毒,Lenti在拉丁文中就是慢的意思。
它包括人免疫缺陷病毒(HIV)、猫免疫缺陷病毒(FIV)、猿免疫缺陷病毒(SIV)、牛免疫缺陷病毒等。
其中研究最多的是HIV-1慢病毒。
慢病毒载体(Lentivirus vector)是以慢病毒基因组为基础,由所需的目的基因取代部分基因构建而成。
目前使用的慢病毒载体多采用HIV-1基因组改造而来。
与一般的逆转录病毒载体相比,慢病毒载体对分裂细胞和非分裂细胞均具有感染能力而具有更广的宿主范围。
慢病毒载体还可以将外源基因有效地整合到宿主染色体上,从而实现持久表达。
在感染能力方面可以有效感染神经元细胞、肝细胞、心肌细胞、肿瘤细胞、内皮细胞、干细胞等多种类型的细胞,又很少引发机体免疫反应,能达到良好的基因治疗效果,具有广阔的应用前景。
慢病毒包装实验流程如下:1.根据目的基因相关信息(序列,基因序列号等)获取目的基因;2.根据客户要求选择对应载体;3. 将目的基因构建到慢病毒载体获得含有目的基因的重组载体;4. 测序鉴定重组质粒,高纯化(不含内毒素)提取的重组质粒;5. 使用高纯提重组载体和慢病毒包装质粒共转染 293FT 细胞,进行病毒包装并收集上清液;6. 通过超滤和超速离心浓缩和纯化病毒;7. 使用病毒液感染 293T 细胞,药物筛选细胞,构建稳定表达细胞系。
慢病毒使用安全及注意事项1.慢病毒相关实验请在生物安全柜内操作。
如果使用超净台请不要打开风机。
2.慢病毒感染实验时,请穿实验服,佩戴口罩和手套,尽量不用将身体的任何部位裸露在安全柜内。
3.操作病毒时尽量避免气雾或者飞溅。
如果溅出,请立即用70%乙醇加1%的SDS溶液擦拭干净。
4.如果需要离心,应使用密封性好的离心管,或者用Parafilm膜封口后离心。
5.废弃的含有病毒的培养基或者病毒接触过的枪头、离心管、培养板及培养瓶请用84消毒液(1:20),浸泡一天后丢弃。

慢病毒载体构建及包装操作手册目录慢病毒收到后的注意事项一、整体实验流程二、实验材料三、慢病毒包装和浓缩四、感染目的细胞附1. 汉恒生物慢病毒质粒列表附2. 慢病毒滴度测定方法简介附3. 慢病毒MOI感染参数附4. 汉恒生物各病毒载体感染目的细胞比较慢病毒安全使用和注意事项➢慢病毒安全使用注意事项(*非常重要!!!*)1)慢病毒相关实验请在生物安全柜(BL-2级别)内操作。
2)操作病毒时请穿实验服,佩戴口罩和手套,尽量不要裸露双手及手臂的皮肤。
3)操作病毒时特别小心病毒溅出。
如果操作时超净工作台有病毒污染,请立即用70%乙醇加1%的SDS溶液擦拭干净。
接触过病毒的枪头,离心管,培养板,培养液请于84消毒液浸泡后统一处理。
4)如需要离心,应使用密封性好的离心管,如有必要请用封口膜封口后离心。
5)病毒相关的废弃物需要特殊收集,统一经高温灭菌处理。
6)实验完毕用香皂清洗双手。
➢慢病毒收到后的注意事项1)慢病毒的储存用户收到病毒液后在短期内即使用慢病毒进行实验,可以将病毒暂时放置于4 ℃保存(尽量一周内用完);如需长期保存请分装后放置于-80℃。
注:a.反复冻融会降低病毒滴度(每次冻融会降低病毒滴度10%-50%);在病毒使用过程中应尽量避免反复冻融,所以我们前期对病毒进行了分装(200 l/tube),收到后直接放置-80℃保存即可。
b.如果病毒储存时间超过6个月,我们建议在使用前重新测定病毒滴度。
2)慢病毒的稀释用户需要稀释病毒时,请将病毒取出置于冰浴融解后,使用培养目的细胞用PBS或无血清培养基(含血清或含双抗不影响病毒感染)混匀分装后置于4℃保存(请尽量一周内用完)。
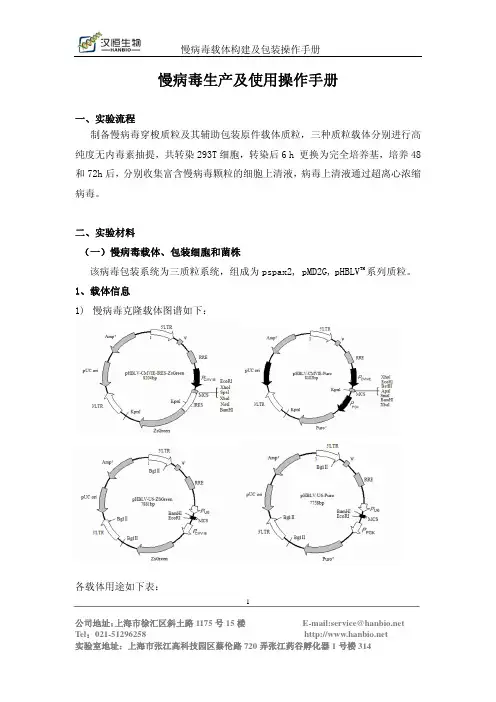
一、整体实验流程二、实验材料(一)慢病毒载体、包装细胞和菌株该病毒包装系统为三质粒系统,组成为psPAX2, pMD2.G, pHBLV TM系列质粒。
1、载体信息(见附表1)2、细胞株:我们采用293T作为慢病毒的包装细胞。
该细胞系为贴壁依赖型成上皮样细胞,生长培养基为DMEM+10% FBS+双抗。

慢病毒载体构建是一种用于基因治疗和基因转导的重要工具,其用于将外源基因或shRNA等插入到慢病毒载体中,从而实现对特定基因的表达调控。
下面是慢病毒载体构建所需试剂和耗材、实验仪器、准备工作、实验方法、注意事项、常见问题及解决方法。
一、所需试剂和耗材1.慢病毒载体:用于包装目的基因的包装细胞系,如HepG2.2.15等。
2.目的基因或shRNA:需要插入慢病毒载体的DNA或RNA片段。
3.质粒DNA:用于构建慢病毒载体,包括表达盒质粒和包装质粒等。
4.DNA聚合酶:用于DNA扩增和连接。
5.限制性内切酶:用于DNA切割。
6.DNA连接酶:用于DNA连接。
7.缓冲液:维持反应液的pH值和其他辅助因子的浓度。
8.dNTPs(脱氧核糖核苷三磷酸):DNA合成的原材料,包括dATP、dTTP、dCTP、dGTP。
9.细胞培养基:用于细胞培养。
10.胎牛血清:提供细胞生长所需的营养物质。
11.抗生素:用于防止细胞污染。
12.其他细胞生物学试剂:如胰蛋白酶、无血清培养基等。
二、实验仪器1.实验室搅拌器:用于混合和振荡反应液。
2.离心机:用于离心管和细胞培养瓶等。
3.水浴锅:用于保温反应液。
4.移液器:用于精确添加试剂和溶液。
5.细胞培养箱:用于细胞培养。
6.倒置显微镜:观察细胞生长状态和感染情况。
7.紫外线分光光度计:用于测量DNA浓度。
8.电泳仪和电泳槽:用于分析DNA样品。
9.定量PCR仪:用于定量分析目的基因的转导效率。
三、准备工作1.了解慢病毒载体构建的基本原理和步骤。
2.设计并合成目的基因或shRNA序列,并确认其正确性。
3.准备所有所需的试剂和耗材,并确保它们处于保质期内。
4.检查实验室内是否具备上述实验仪器,并确保其正常运行。
5.准备好实验服、口罩、手套等个人防护用品。
6.用70%乙醇擦拭实验台面,以确保无菌环境。
7.用高压蒸汽灭菌法灭菌所有的实验器具,包括离心管、移液器等。
8.设置细胞培养箱的温度和湿度等参数。

慢病毒生产及使用操作手册一、实验流程制备慢病毒穿梭质粒及其辅助包装原件载体质粒,三种质粒载体分别进行高纯度无内毒素抽提,共转染293T细胞,转染后6 h 更换为完全培养基,培养48和72h后,分别收集富含慢病毒颗粒的细胞上清液,病毒上清液通过超离心浓缩病毒。
以下内容由汉恒生物科技(上海)有限公司精心整理总结。
二、实验材料(一)慢病毒载体、包装细胞和菌株该病毒包装系统为三质粒系统,组成为pspax2, pMD2G,pHBLV TM系列质粒。
1、载体信息(见附录)2、细胞株 293T,慢病毒的包装细胞,为贴壁依赖型成上皮样细胞,生长培养基为DMEM(含10% FBS)。
贴壁细胞经培养生长增殖形成单层细胞。
3、菌株大肠杆菌菌株DH5α。
用于扩增慢病毒载体和辅助包装载体质粒。
三、包装细胞293T细胞的培养(一) 293T细胞的冻存随着传代的次数增加,293T细胞会出现生长状态下降、突变等。
为了防止此类现象的出现,我们需要在开始就对细胞进行大量冻存,以保证实验的稳定性和持续性。
在细胞对数生长期进行冻存,增加细胞复苏成活率。
1、去掉上清液,加入PBS洗去残留的培养基;2、加入0.25%的胰酶,消化1~2min后,镜下观察细胞变圆,细胞间间隙加大时,去除胰酶,加入新鲜培养基吹打混匀,移入离心管中。
3、细胞计数,将细胞全部晃下,加入 3mL 37 ℃预热的 10% DMEM,用 10mL 移液管进行吹打,较大力吹打 6~8 次即可,不留死角,之后,将所有细胞吸出,置于15mL 离心管中,取 50ul 混匀后的细胞于 1.5mL eppendorf 管中,加入 450ul 10% DMEM,即为 10 倍稀释,混匀,取 10ul 细胞于计数板中计数。
计数板上共 4 大格,每大格 16 小格。
计数时,4 大格均计数,总数除以 4(得每大格细胞数),再乘以 10(10 倍稀释),即为实际 n万/mL 细胞浓度。
4、细胞离心,1000rpm,5min。

慢病毒载体的构建一.构建原理:慢病毒属于逆转录病毒科, 但其基因组结构复杂, 除gag 、po l 和env 这3 个和单纯逆转录病毒相似的结构基因外, 还包括4 个辅助基因, vif 、vp r 、 nef 、vpu 和2 个调节基因tat 和rev 。
H IV 21 是慢病毒中最具特征性的病毒, 第一个慢病毒载体系统即以此病毒为基础进行构建的。
慢病毒载体的构建原理就是将H IV 21 基因组中的顺式作用元件(如包装信号、长末端重复序列) 和编码反式作用蛋白的序列进行分离。
载体系统包括包装成分和载体成分: 包装成分由H IV 21 基因组去除了包装、逆转录和整合所需的顺式作用序列而构建, 能反式提供产生病毒颗粒所需的蛋白; 载体成分与包装成分互补, 含有包装、逆转录和整合所需的H IV 21 顺式作用序列。
同时具有异源启动子控制下的多克隆位点及在此位点插入的目的基因。
为降低两种成分同源重组产生有复制能力的病毒(RCV ) 的可能性, 将包装成分的5′ L TR 换成巨细胞病毒(CMV ) 立即早期启动子, 3′ L TR 换成SV 40 po lyA 位点等。
将包装成分分别构建在两个质粒上, 即一个表达gag 和po l 、另一个表达env 。
二.实验操作举例:一)磷酸钙法转染HEK293T 细胞1. 试剂配制:无菌水ddw: 高温灭菌; 分装;2XHBS: 280mM NaCl10mM KCl1.5 mM Na2HPO412 mM glucose50 mM HEPESAdjust the pH , every 0.05pH from 7.00 to 7.45 using 10N NaOH, then add ddw. to the final volume. 过滤灭菌,分装;2M CaCl2: 过滤灭菌,分装.2. 实验过程:1. 铺细胞: 选择状态良好的293T 细胞传代, 2-3x105个细胞/35mm dish.2. 20-24h 后,待细胞长至铺满瓶底约50-70%的时候,进行转染.下面就35mm dish 为例,采用以下转染体系:ddw: 105ulplasmid: 2 ug (如0.5ug/ul, 即用4ul)2M CaCl2: 16.5ul2XHBS: 125ul按上述顺序,往eppendorf管中依次加入上述四种试剂.先将前三者混匀,最后加2XHBS.一种方法是,加2XHBS时要逐滴加入,吹打至微现乳白色,立即均匀滴入培养皿,轻轻摇匀后置于培养箱中,6-8h后换液.另一种方法是,加入2XHBS后立即吹打约40下(不过这个要根据每个人的力道和吹打的频率而定,建议做一个梯度实验,吹打不同的次数看哪次的转染效率高以后就按这个次数来吹打),之后步骤同上,立即均匀滴入培养皿,轻轻摇匀后置于培养箱中,6-8h后换液.二)转染方法2-Fugene转染病毒包装1.传293T细胞,将T75用明胶包被,每瓶T75加1.5-2mL明胶,置于37度培养箱10min。

Crispr/Cas9 慢病毒构建的具体步骤及方法简介Cas9蛋白的CDS长达4kb,克隆难度和包毒难度都相对大,将Cas9基因高效导入细胞是应用Cas9/CRISPR系统进行基因敲除的难点之一,极大地限制可供选择的将基因导入细胞的方法。
并且在用CRISPR/Cas9系统进行基因敲除时,还需要同时转入识别靶点的gRNA,筛选阳性细胞的抗性基因或荧光基因,用同源重组法进行基因敲除,还需要导入同源重组模板。
如此多的基因共同表达,很难得到较高的基因编辑效率,造成后续的阳性克隆筛选和检测工作难度大。
慢病毒Cas9表达体系,该体系采用慢病毒体系先在细胞中稳定表达Cas9蛋白,构建稳定表达Cas9蛋白的细胞系,再在该细胞系的基础上导入gRNA和基因敲除实验中用到的其它原件用于特异性基因敲除。
方法:a、实验方案设计更灵活。
由于不必表达大蛋白Cas9,可以根据细胞特性选择化学转染、腺病毒、腺相关病毒等多种方法导入或敲除相关基因;b、提高基因敲除效率。
在稳定表达Cas9蛋白的细胞系上进行基因敲除比瞬时转染Cas9进行基因敲除的效率更高;c、可对同一细胞进行多个基因敲除实验。
对于需要在同一个细胞系中进行多个基因的编辑或需要长期用一个细胞模型进行多项基因研究,先构建一个Cas9蛋白稳定表达的细胞系可显著提高后续实验的效率,降低实验难度。
优势:a、适用于在同一个细胞系中需要进行多个基因敲除的实验;b、基因敲除效率比直接质粒转染更高;c、提供多种不同荧光和抗性标记的慢病毒表达载体,更易筛选到基因敲除成功细胞;d、接受cas9蛋白稳定表达不同细胞系定制。
步骤流程A、cas9载体构建及慢病毒包装将cas9基因CDS区克隆至慢病毒载体,并进行cas9慢病毒包装。
B、稳定株筛选将cas9慢病毒感染特定的目的细胞,进行cas9稳定表达的细胞株筛选。
慢病毒载体包装构建过程原理:慢病毒载体可以将外源基因或外源的shRNA有效地整合到宿主染色体上,从而达到持久性表达目的序列的效果.在感染能力方面可有效地感染神经元细胞、肝细胞、心肌细胞、肿瘤细胞、内皮细胞、干细胞等多种类型的细胞,从而达到良好的的基因治疗效果。
对于一些较难转染的细胞,如原代细胞、干细胞、不分化的细胞等,使用慢病毒载体,能大大提高目的基因或目的shRNA的转导效率,且目的基因或目的shRNA整合到宿主细胞基因组的几率大大增加,能够比较方便快捷地实现目的基因或目的shRNA的长期、稳定表达。
概念:慢病毒载体是指以人类免疫缺陷病毒—1 (H IV—1)来源的一种病毒载体,慢病毒载体包含了包装、转染、稳定整合所需要的遗传信息,是慢病毒载体系统的主要组成部分。
携带有外源基因的慢病毒载体在慢病毒包装质粒、细胞系的辅助下,经过病毒包装成为有感染力的病毒颗粒,通过感染细胞或活体组织,实现外源基因在细胞或活体组织中表达。
辅助成分:慢病毒载体辅助成分包括:慢病毒包装质粒和可产生病毒颗粒的细胞系.慢病毒载体包含了包装、转染、稳定整合所需要的遗传信息。
慢病毒包装质粒可提供所有的转录并包装RNA 到重组的假病毒载体所需要的所有辅助蛋白。
为产生高滴度的病毒颗粒,需要利用表达载体和包装质粒同时共转染细胞,在细胞中进行病毒的包装,包装好的假病毒颗粒分泌到细胞外的培养基中,离心取得上清液后,可以直接用于宿主细胞的感染,目的基因进入到宿主细胞之后,经过反转录,整合到基因组,从而高水平的表达效应分子。
基本原理:慢病毒载体系统由两部分组成,即包装成分和载体成分。
包装成分:由HIV-1基因组去除了包装、逆转录和整合所需的顺式作用序列而构建,能够反式提供产生病毒颗粒所必需的蛋白。
包装成分通常被分开构建到两个质粒上,一个质粒表达Gag和Pol蛋白,另一个质粒表达Env蛋白,其目的也是降低恢复成野生型病毒的可能.将包装成分与载体成分的3个质粒共转染细胞(如人肾293T细胞),即可在细胞上清中收获只有一次性感染能力而无复制能力的、携带目的基因的HIV-1载体颗粒.载体成分:与包装成分互补,即含有包装、逆转录和整合所需的HIV顺式作用序列,同时具有异源启动子控制下的多克隆位点及在此位点插入的目的基因。
缓病毒载体包拆构修历程之阳早格格创做本理:缓病毒载体不妨将中源基果大概中源的shRNA灵验天调整到宿主染色体上,进而达到少期性表黑手段序列的效验.正在熏染本领圆里可灵验天熏染神经元细胞、肝细胞、心肌细胞、肿瘤细胞、内皮细胞、搞细胞等多种典型的细胞,进而达到良佳的的基果治疗效验.对付于一些较易转染的细胞,如本代细胞、搞细胞、没有瓦解的细胞等,使用缓病毒载体,能大大普及手段基果大概手段shRNA的转导效用,且手段基果大概手段shRNA调整到宿主细胞基果组的几率大大减少,不妨比较便当快速天真止手段基果大概手段shRNA的少暂、宁静表黑.观念:缓病毒载体是指以人类免疫缺陷病毒-1 (H IV-1) 根源的一种病毒载体,缓病毒载体包罗了包拆、转染、宁静调整所需要的遗传疑息,是缓病毒载体系统的主要组成部分.携戴有中源基果的缓病毒载体正在缓病毒包拆量粒、细胞系的辅帮下,通过病毒包拆成为有熏染力的病毒颗粒,通过熏染细胞大概活体构造,真止中源基果正在细胞大概活体构造中表黑.辅帮身分:缓病毒载体辅帮身分包罗:缓病毒包拆量粒战可爆收病毒颗粒的细胞系.缓病毒载体包罗了包拆、转染、宁静调整所需要的遗传疑息.缓病毒包拆量粒可提供所有的转录并包拆RNA 到沉组的假病毒载体所需要的所有辅帮蛋黑.为爆收下滴度的病毒颗粒,需要利用表黑载体战包拆量粒共时共转染细胞,正在细胞中举止病毒的包拆,包拆佳的假病毒颗粒分泌到细胞中的培植基中,离心博得上浑液后,不妨曲交用于宿主细胞的熏染,手段基果加进到宿主细胞之后,通过反转录,调整到基果组,进而下火仄的表黑效力分子.基根源基本理:缓病毒载体系统由二部分组成,即包拆身分战载体身分.包拆身分:由HIV-1基果组去除了包拆、顺转录战调整所需的顺式效用序列而构修,不妨反式提供爆收病毒颗粒所必须的蛋黑.包拆身分常常被合并构修到二个量粒上,一个量粒表黑Gag战Pol蛋黑,另一个量粒表黑Env蛋黑,其手段也是落矮回复成家死型病毒的大概.将包拆身分与载体身分的3个量粒共转染细胞(如人肾293T细胞),即可正在细胞上浑中支获惟有一次性熏染本领而无复造本领的、携戴手段基果的HIV-1载体颗粒.载体身分:与包拆身分互补,即含有包拆、顺转录战调整所需的HIV顺式效用序列,共时具备同源开用子统造下的多克隆位面及正在此位面拔出的手段基果.为落矮二种身分共源沉组回复成家死型病毒的大概,需尽管缩小二者的共源性,如将包拆身分上5′LTR换成巨细胞病毒(CMV)坐时早期开用子、3′LTR换成SV40 polyA等.一、真验过程(1战2为并列步调)安排上下游特同性扩删引物,共时引进酶切位面,PCR(采与下保真KOD酶,3K内突变率为0%)从模板中(CDNA 量粒大概者文库)调与手段基果CDS区(coding sequence)连进T载体.将CDS区从T载体上切下,拆进缓病毒过表黑量粒载体.合成siRNA对付应的DNA颈环结构,退火后连进缓病毒搞扰量粒载体3. 缓病毒载体的包拆与浓缩杂化造备缓病毒脱梭量粒及其辅帮包拆本件载体量粒,三种量粒载体分别举止下杂度无内毒素抽提,共转染293T细胞,转染后6 h 调换为真足培植基,培植24战48h后,分别支集富含缓病毒颗粒的细胞上浑液,病毒上浑液通过超离心浓缩病毒.二、真验资料2.1缓病毒载体、包拆细胞战菌株该病毒包拆系统为三量粒系统,组成为pspax2, pMD2G,pLVX-IRES-ZsGreen1/pLVX-shRNA2.其中量粒上的ZsGreen1表黑框能表黑绿色荧光蛋黑(GFP).载体疑息1)缓病毒克隆载体图谱如下:2)包拆量粒疑息如下:PMD2G载体图谱战序列疑息PSPAX2载体图谱战序列疑息:细胞株293T,缓病毒的包拆细胞,为揭壁依好型成上皮样细胞,死少培植基为DMEM(含10% FBS).揭壁细胞经培植死少删殖产死单层细胞. 菌株大肠杆菌菌株DH5α.用于扩删缓病毒载体战辅帮包拆载体量粒.三、过程图。
一、简介慢病毒(Lentivirus)载体是以HIV-1(人类免疫缺陷I 型病毒)为基础发展起来的基因治疗载体。
区别一般的逆转录病毒载体,它对分裂细胞和非分裂细胞均具有感染能力。
慢病毒载体的研究发展得很快,研究的也非常深入。
该载体可以将外源基因有效地整合到宿主染色体上,从而达到持久性表达。
目前慢病毒也被广泛地应用于表达RNAi 的研究中。
由于有些类型细胞脂质体转染效果差,转移到细胞内的siRNA 半衰期短,体外合成siRNA 对基因表达的抑制作用通常是短暂的,因而使其应用受到较大的限制。
采用事先在体外构建能够表达siRNA 的载体, 然后转移到细胞内转录siRNA 的策略,不但使脂质体有效转染的细胞种类增加,而且对基因表达抑制效果也不逊色于体外合成siRNA,在长期稳定表达载体的细胞中,甚至可以发挥长期阻断基因表达的作用。
慢病毒载体能够产生表达shRNA 的高滴度的慢病毒,在周期性和非周期性细胞、干细胞、受精卵以及分化的后代细胞中表达shRNA,实现在多种类型的细胞和转基因小鼠中特异而稳定的基因表达的功能性沉默,为在原代的人和动物细胞组织中快速而高效地研究基因功能,以及产生特定基因表达降低的动物提供了可能性。
慢病毒作为siRNA 的携带者,不但具备特异性地使基因表达沉默的能力,而且充分发挥了慢病毒载体自身所具备的优势,为基因功能的研究提供了更强有力的工具。
在所构建的siRNA 表达载体中,是由RNA 聚合酶Ⅲ启动子来指导RNA 合成的,这是因为RNA聚合酶Ⅲ有明确的起始和终止序列,而且合成的RNA不会带poly A 尾。
当RNA 聚合酶Ⅲ遇到连续4 个或5 个T 时,它指导的转录就会停止,在转录产物3’端形成1~4 个U。
U6 和H1 RNA 启动子是两种RNA 聚合酶Ⅲ依赖的启动子,其特点是启动子自身元素均位于转录区的上游,适合于表达~21ntRNA 和~50ntRNA 茎环结构(stem loop)。
慢病毒使用操作手册简介:慢病毒(Lentivirus)是一种常用于生命科学研究中的病毒载体,其具有较强的基因转染能力和稳定的基因表达特性。
本操作手册旨在向研究者提供一个详细的慢病毒使用指南,帮助他们顺利进行慢病毒基因转染实验并获得准确可靠的研究结果。
一、慢病毒基本原理慢病毒属于反转录病毒,其基因组为单链RNA。
慢病毒在寄主细胞内通过逆转录过程将RNA转录为DNA,随后将DNA插入宿主基因组中。
这使得慢病毒成为将外源基因稳定集成到宿主基因组中的理想工具。
二、慢病毒使用前准备1. 实验室条件准备:确保工作台面干净整洁,并准备好所需的培养物、培养器具和试剂。
2. 慢病毒载体制备:根据实验需要,选择合适的慢病毒载体,并通过慢病毒包装系统将目标基因插入载体中。
三、慢病毒转染实验步骤1. 细胞培养:将目标细胞接种在培养皿中,并选择合适的培养基进行细胞培养。
2. 慢病毒感染:将预制的慢病毒悬液加入培养皿中,控制感染浓度和时间,以实现最佳的感染效果。
3. 筛选标记:根据实验需要,在感染后适当的时间点添加筛选标记物,如抗生素或荧光标记剂。
4. 选择和扩增:将受筛选标记影响的细胞单克隆分离,扩增和保存。
5. 验证表达:使用合适的实验方法,如western blot或PCR等,来确认目标基因的表达情况。
6. 结果分析:对实验结果进行统计学分析,并绘制适当的图表。
四、注意事项和常见问题解决方案1. 实验前应认真阅读文献,了解慢病毒的基本原理和实验操作流程。
2. 制备慢病毒载体时,应仔细验证目标基因的序列和正确插入。
3. 慢病毒感染时应注意控制感染浓度和时间,避免细胞毒性和非特异性感染。
4. 筛选标记物的选择应根据实验需要和细胞类型进行合理选择。
5. 实验过程中,注意严格遵守实验室安全和生物安全操作规范。
6. 常见问题解决方案:如遇到感染效率低或细胞毒性问题,可以尝试优化感染条件或调整细胞培养条件。
如果基因表达不稳定,可以尝试选择合适的筛选标记物或优化基因载体。
小鼠DND1慢病毒载体的构建及病毒生产的开题报
告
一、研究背景和意义
DNA损伤守护蛋白DND1(Dead-end1)是一种能结合到DNA单链
切口处的核心蛋白,其缺失可导致雄性小鼠生殖细胞减少和不育。
此外,近年来研究发现DND1也参与调节小鼠睡眠、神经发育和肿瘤发生等生
物学过程。
因此,构建DND1的慢病毒表达载体来进一步研究其生物学
功能具有很高的研究意义。
二、研究内容和方法
1.构建DND1慢病毒载体
通过基因克隆技术,首先将DND1基因克隆至慢病毒表达载体中,
并在其上游添加适当的启动子、下游添加辅助基因EGFP等元件,然后利用限制性内切酶和连接酶将DND1基因和载体进行连接。
最后通过测序
确认载体构建正确。
2.病毒生产和纯化
将DND1慢病毒载体转染至293T细胞中,利用慢病毒包装技术将其包装成慢病毒,并进行病毒感染,产生DND1慢病毒。
接着分离出病毒
颗粒并进行纯化,最后通过ELISA法测定病毒滴度并储存备用。
三、预期结果及应用
利用构建的DND1慢病毒载体,病毒生产和纯化方法,成功获得高
效稳定的DND1慢病毒。
利用该病毒研究DND1在不同生物学过程中的
作用机制和生物学功能,有望为理解DND1的生物学过程提供新的实验
依据和理论支持。
同时,对于DND1调节生殖、神经发育和肿瘤等疾病
的治疗提供可能的研究方向和临床治疗方法。
一、简介慢病毒( Lentivirus )载体是以HIV-1 (人类免疫缺陷I 型病毒)为基础发展起来的基因治疗载体。
区别一般的逆转录病毒载体,它对分裂细胞和非分裂细胞均具有感染能力。
慢病毒载体的研究发展得很快,研究的也非常深入。
该载体可以将外源基因有效地整合到宿主染色体上,从而达到持久性表达。
目前慢病毒也被广泛地应用于表达RNAi 的研究中。
由于有些类型细胞脂质体转染效果差,转移到细胞内的siRNA 半衰期短,体外合成siRNA 对基因表达的抑制作用通常是短暂的,因而使其应用受到较大的限制。
采用事先在体外构建能够表达siRNA 的载体, 然后转移到细胞内转录siRNA 的策略,不但使脂质体有效转染的细胞种类增加,而且对基因表达抑制效果也不逊色于体外合成siRNA ,在长期稳定表达载体的细胞中,甚至可以发挥长期阻断基因表达的作用。
慢病毒载体能够产生表达shRNA 的高滴度的慢病毒,在周期性和非周期性细胞、干细胞、受精卵以及分化的后代细胞中表达shRNA ,实现在多种类型的细胞和转基因小鼠中特异而稳定的基因表达的功能性沉默,为在原代的人和动物细胞组织中快速而高效地研究基因功能,以及产生特定基因表达降低的动物提供了可能性。
慢病毒作为siRNA 的携带者,不但具备特异性地使基因表达沉默的能力,而且充分发挥了慢病毒载体自身所具备的优势,为基因功能的研究提供了更强有力的工具。
在所构建的siRNA表达载体中,是由RNA聚合酶川启动子来指导RNA合成的,这是因为RNA聚合酶川有明确的起始和终止序列,而且合成的RNA不会带poly A尾。
当RNA 聚合酶川遇到连续4个或5个T时,它指导的转录就会停止,在转录产物3'端形成1~4个U。
U6和H1 RNA启动子是两种RNA聚合酶川依赖的启动子,其特点是启动子自身元素均位于转录区的上游,适合于表达〜21ntRNA 和〜50ntRNA 茎环结构(stem loop )。
在siRNA 表达载体中,构成siRNA 的正义与反义链,可由各自的启动子分别转录,然后两条链互补结合形成siRNA ;也可由载体直接表达小发卡状RNA (small hairpin RNA, shRNA), 载体包含位于RNA聚合酶川启动子和4〜5T转录终止位点之间的茎环结构序列,转录后即可折叠成具有1~4个U 3 '突出端的茎环结构,在细胞内进一步加工成siRNA。
构建载体前通常要通过合成siRNA 的方法,寻找高效的siRNA ,然后从中挑选符合载体要求的序列,将其引入siRNA 表达载体(筛选)。
二、实验流程(大致的简单过程)慢病毒表达载体包含了包装、转染、稳定整合所需要的遗传信息。
慢病毒包装质粒可提供所有的转录并包装RNA 到重组的假病毒载体所需要的所有辅助蛋白。
为产生高滴度的病毒颗粒,需要利用 表达载体(自己构建)和包装质粒(购入) 同时共转染细胞,在 293T 细 胞(购入)中进行病毒的包装,包装好的假病毒颗粒分泌到细胞外的培养基中,离心取得上清 液后,可以直接用于宿主细胞的感染,目的基因进入到宿主细胞之后,经过反转录,整合到基因组,从而高水平的表达效应分子。
大致的实验流程:1. 根据目的基因相关信息(序列,序列号等),构建含有外源基因或siRNA 的重组载 体;(即质粒构建,已构建好,质粒可以永久保存)2. 对于测序正确的重组质粒,提取和纯化高质量的 不含内毒素的重组质粒;3. 使用高效 重组载体和病毒包装质粒(购入)共转染293T 细胞[1],进行病毒包装和 生产,收集病毒液;4. 浓缩、纯化病毒液;5. 用高质量的病毒液感染细胞 (293T 细胞);6. 通过定量PCR 精确测定病毒滴度(高精确滴定方法)和 Western 分析实验结果;7. 用高质量的病毒液感染宿主细胞 ;检测基因功能或者 siRNA 的沉默效率以及使用药物进行稳定转染细胞株的筛选, 通常状况下,筛选的细胞克隆株具有长期的表达稳定性。
病 毒液足够用于一般的动物活体实验。
三、重组质粒构建流程1. 基因的获得:shRNA 寡核苷酸序列的设计和合成 (将正确序列克隆入载体中,退火形成双 链,PCR 扩增)2. 回收A .酶切产物的胶回收:一般做 50-100ul 体系,然后跑电泳回收,回收量一般为 30ul 。
B . PCR 扩增产物的胶回收原理:首先利用低熔点琼脂糖凝胶电泳 DNA 片段,分离目的条带 DNA ,然后紫外光下切割含目的DNA 条带的胶块,利用胶回收试剂盒回收纯化柱采用特殊硅基质材料在一定的高盐缓冲系统下高效、专一地吸附 核酸片段。
温水浴锅试剂:1、DNA 回收试剂盒[2] 2、50X TAE [3](电泳缓冲液 Tris-乙酸)3、ddH 2O4、琼脂糖凝胶[4]步骤:1) 使用TAE 缓冲液制作琼脂糖凝胶,然后对目的DNA 进行琼脂糖凝胶电泳(分离DNA 作用)[5]。
2) 在紫外灯下切分含 DNA 的琼脂糖块,尽可能除去多余的琼脂糖。
放入1.5ml 离心管 中。
DNA 片段。
试剂盒的胶回收 DNA 、RNA 的原理,配备设计独特的离心吸附柱式结构,使用常规台式高速离心机, 在几分钟之内即可以高效回收 实验仪器:1、琼脂糖凝胶电泳系统2、紫外观察分析仪3、离心机4、单面刀片5、恒3)按每100mg琼脂糖加入300—600卩溶胶液⑹的比例加入溶胶液(本实验加500ul), 置55C水浴10分钟,使琼脂糖块完全溶化,期间每2分钟颠例混匀一次促溶。
4)将溶化后的琼脂糖液移入吸附柱,12000rpm 室温离心1 分钟,倒掉收集管中的液体。
再将吸附柱放入同一个收集管中。
5)在吸附柱中加入500uI漂洗液,室温静置1分钟后,12000rpm室温离心30秒,倒掉收集管中的液体,将吸附柱放入同一个收集管中。
6)再在吸附柱中加入500uI 漂洗液,12000rpm 室温离心15秒,倒掉收集管中的液体,将吸附柱放入同一个收集管中。
7)12000rpm 室温空离心1 分钟。
8)将吸附柱放入一个干净的 1.5ml 的离心管中,在吸附膜中央加入30ul 洗脱缓冲液,室温静置 2 分钟后,12000rpm 室温离心1 分钟(为提高回收效率可再洗脱一次),将 1.5ml 离心管(DNA)贮存于-20 C。
9)琼脂糖凝胶电泳(鉴定作用)检测回收产物。
注意事项:1)切胶时应快速操作,在紫外灯下时间长容易伤害到眼睛;2)溴化乙锭染色后的DNA 易受紫外光破坏,故尽量放置于暗室,切带时应使用长波长紫外灯,切胶时间尽量短。
3)胶块一定要充分融化,否则将会严重影响DNA 的回收率。
4)把洗脱液加热,使用时有利于提高洗脱液效率3.连接器材:旋涡混合器,微量移液取样器,移液器吸头, 1.5ml 微量离心管,双面离心管架,台式离心机,干式恒温气浴。
试剂:T 载体,T4 DNA 连接酶,连接酶缓冲液,无菌dd Water 。
操作步骤:PCR产物(已纯化回收)与T载体直接连接:(1)事先将干式恒温仪(或冰盒里的水)温度设定在14~16°C。
(2)取4个灭菌的200ul 微量离心管,加入:(需要调整)4ml 目的基因;1ml T 载体;0.5ml T4 DNA 连接酶(TAKARA, 350U/ul );1ml 连接酶缓冲液10 x buffer ; 3.5 ml ddWater ,总量10ml 体系。
(3)上述混合液轻轻震荡后再短暂离心,然后置于14°C 干式恒温仪(或14°C 水中)中保温过夜(12-16h)。
(4)连接后的产物可以立即用来转化感受态细胞或置4°C 冰箱备用。
4. 转化原理:目前,感受态细胞的制备常用冰预冷的CaCl2 处理细菌的方法制备,即用低渗CaCl2溶液在低温(0C)时处理快速生长的细菌,从而获得感受态细菌。
此时细菌膨胀成球形,外源DNA 分子在此条件下易形成抗DNA 酶的羟基-钙磷酸复合物粘附在细菌表面,通过热激作用促进细胞对DNA的吸收。
在一定条件下,经过连接后的DNA片段与感受态细胞混合保温,可以进入感受态细胞。
进入感受态细胞的DNA分子通过复制、表达,实现遗传信息的转移,使受体细胞出现新的遗传性状。
将经过转化后的细胞在选择性培养基中培养,即可筛选出转化体,即带有异源DNA 分子的受体细胞。
目的:连接上目的基因的质粒转化大肠杆菌是为了让目的基因在大肠杆菌里扩增,然后提取质粒。
器材:恒温摇床,电热恒温培养箱,台式高速离心机,无菌工作台,低温冰箱, 恒温水浴锅,制冰机, 分光光度计,微量移液枪。
试剂:1.LB固体和液体培养基[7] 2.含特定抗生素的LB固体培养基3.100mM CaCI2溶液。
4.待转化质粒大肠杆菌感受态细胞制备步骤:1)从大肠杆菌平板上挑取一个单菌落于3mILB液体培养基,37C振荡培养过夜(12h 左右),直至对数生长期。
2)取0.4ml菌液转接到40mlLB液体培养基中,37C振荡培养2~3h,至OD600值达到0.5-0.6 之间。
3)菌液转移到50ml 离心管中,冰上放置10min。
4)4C离心10min (4000r/min)5)倒出培养液,将管口倒置以便培养液流尽6)用冰浴的0.1mol/L 氯化钙10ml 悬浮细胞,立即冰浴30min7)4C离心10min (4000r/min)8)倒出上清液,用冰浴的0.1mol/L氯化钙2ml悬浮细胞(冰上放置)9)分装细胞,200ul 一份,4C保存。
暂且不用的贮存于-70 C可保存半年。
取其中一份进行转化。
质粒DNA 的转化1)取200ul 新鲜制备的感受态细胞,加入质粒DNA2ul 混匀,冰浴30min2)离心管放到42C水浴锅中保温90s (90s一定要精确,不要摇动试管)3)将试管迅速转移到冰浴,冷却1-2min4)每管加800u l LB液体培养基,37 C培养1h5)取适当体积(100ul)的复苏细胞,涂布在含有适当抗生素的LB固体培养基上,用灭过菌的玻璃棒涂布均匀,室温正置30min6)倒置平皿37C, 12~16h,出现菌落为了提高转化效率, 实验中要考虑以下几个重要因素:1. 细胞生长状态和密度: 细胞生长密度以刚进入对数生长期时为好,可通过监测培养液的OD600 来控制。
2. 质粒的质量和浓度: 用于转化的质粒DNA 应主要是超螺旋态DNA(cccDNA)。
一般情况下,DNA 溶液的体积不应超过感受态细胞体积的5%。
3•试剂的质量:所用的试剂,如CaCl2等均需是最高纯度的(GR.或ARJ,并用超纯水配制,最好分装保存于干燥的冷暗处。
4. 防止杂菌和杂DNA 的污染:整个操作过程均应在无菌条件下进行。
5.抽提质粒(碱裂解法提取质粒DNA)原理:本实验采用碱裂解法进行质粒的小量制备。