大学化学课件 第三章 氧化还原反应 电化学
- 格式:ppt
- 大小:6.92 MB
- 文档页数:50



氧化还原反应与电化学课件第一部分:氧化还原反应基础氧化还原反应,又称为化学电子转移反应,是化学反应中普遍存在的一种类型。
在氧化还原反应中,物质的氧化态或还原态发生变化,其中一个物质将电子转移给另一个物质。
这种电子转移过程导致原子或离子的氧化态发生改变,因此称为氧化还原反应。
1.1 氧化还原反应的基本概念在氧化还原反应中,我们需要关注两个重要的概念:氧化和还原。
- 氧化:物质失去电子,氧化态增大。
- 还原:物质获得电子,氧化态减小。
1.2 氧化还原反应的示例举例来说,我们可以观察以下氧化还原反应:Cu + 2Ag+ -> Cu2+ + 2Ag在这个反应中,Cu从0价氧化态变为+2价氧化态,被氧化,而Ag+离子从+1价还原态变为0价还原态,被还原。
在这个反应中,Cu失去了电子,被氧化,而Ag+获得了电子,被还原。
第二部分:电化学基础2.1 电化学的概念电化学是研究化学反应和电流之间相互转化的科学。
它研究物质在电化学过程中的氧化还原反应以及与之相关的电流和电势。
2.2 电化学的应用电化学在我们的日常生活和工业生产中有着广泛的应用。
- 电解池中的电化学过程被应用于电镀、电解和电池等行业。
- 电化学还应用于环境保护,例如电化学处理废水和废气等。
- 电化学还在药物研发和分析仪器等领域有着重要的应用。
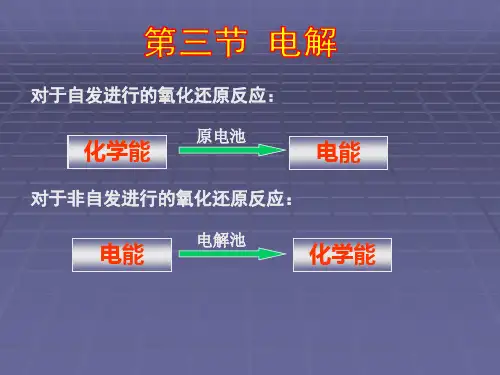
第三部分:电池和电解池3.1 电池的概念和分类电池是一种将化学能转化为电能的装置。
根据电池内部反应的性质,电池可以分为干电池和液电池两种类型。
3.2 电解池的概念电解池是一种在外部电流的作用下,将电能转化为化学能的装置。
它是电池的反向过程。
第四部分:课件设计4.1 课件设计的重要性课件设计是教学中不可或缺的一部分。
通过合理的课件设计,可以更好地呈现和组织知识内容,提高学生对氧化还原反应和电化学的理解程度。
4.2 课件设计的要点在氧化还原反应与电化学课件的设计中,应注意以下要点:- 简洁明了的页面布局,避免信息过载。


氧化还原反应与电化学氧化还原反应(Redox Reaction)是化学反应中常见的一种类型,也是电化学的基础。
在氧化还原反应中,物质会发生电荷转移过程,其中一个物质被氧化(失去电子),另一个物质被还原(获得电子)。
这种电荷转移过程伴随着电流的流动,因此氧化还原反应与电化学密切相关。
1. 氧化还原反应的基本原理在氧化还原反应中,常常可以观察到电子的转移与氧原子的参与。
在一些反应中,物质会失去电子,被称为氧化剂(Oxidizing Agent),而另一些物质则会获得电子,被称为还原剂(Reducing Agent)。
这种电子的转移与氧原子的参与使得物质的氧化态和还原态发生变化。
2. 氧化还原反应的重要性氧化还原反应在生活和工业中具有广泛的应用。
例如,我们所熟悉的腐蚀现象就是一种氧化还原反应。
金属物质在与氧气接触时会发生氧化反应,形成金属氧化物。
此外,氧化还原反应还被广泛应用于电池、电解、电镀等方面。
3. 电化学的基本概念电化学是研究化学反应与电流之间关系的学科。
它主要涉及电解反应(Electrolysis)和电化学电池(Electrochemical Cell)两个方面。
3.1 电解反应电解反应是在外加电压的作用下,将化学反应逆转的过程。
电解反应的基本原理是利用外部电压提供能量,使得自发不利反应变得可逆,从而实现物质的分解或转化。
3.2 电化学电池电化学电池是将化学能转化为电能的装置。
它由两个半电池组成,分别包含一个氧化反应和一个还原反应。
这两个半电池通过电解质溶液(Electrolyte)或电解质桥(Salt Bridge)连接起来,形成一个闭合的电路。
4. 电化学电池的工作原理电化学电池中,氧化反应和还原反应在两个半电池中同时进行。
在氧化反应中,电子流从还原剂移动到电解质溶液中;而在还原反应中,电子从电解质溶液流向氧化剂。
这一过程中,电子的流动经过外部电路,形成了电流。
根据电化学电池反应的性质和电流的方向,我们可以将电化学电池分为两类:电解池(Electrolytic Cell)和电池(Galvanic Cell)。

第3章第3节 氧化还原反应1.认识元素在物质中可以具有不同价态,可通过氧化还原反应实现含有不同价态同种元素的物质的相互转化。
2.认识有化合价变化的反应是氧化还原反应,了解氧化还原反应的本质是电子的转移,知道常见的氧化剂和还原剂。
1.本部分知识在高考中一般与元素化合物、电化学、流程图题相结合进行考查,难度中等。
2.对氧化还原反应概念的复习,首先要抓住概念的本质,建立氧化还原反应的观点,通过分析、推理等方法认识氧化还原反应的特征和实质,建立氧化还原反应计算、配平以及书写陌生方程式的思维模型。
3.能从氧化还原反应的角度,设计探究方案,进行实验探究,加深对物质氧化性、还原性的理解。
内容索引第一环节 必备知识落实第二环节 关键能力形成第三环节 核心素养提升第一环节 必备知识落实1氧化还原反应的相关概念及电子转移的表示方法知识筛查1.氧化还原反应的本质和特征2.相关概念及其关系简单概括为“升失氧、降得还,剂性一致、其他相反”。
3.氧化还原反应中电子转移的表示方法(1)双线桥法。
Cu与稀硝酸的反应中电子转移的方向和数目可表示为:(2)单线桥法。
Cu与稀硝酸的反应中电子转移的方向和数目可表示为:4.氧化还原反应与四种基本反应类型间的关系知识巩固1.判断正误,正确的画“√”,错误的画“×”。
(1)反应2Na 2O 2+2H 2O ══4NaOH+O 2↑与反应Cl 2+H 2O HCl+HClO 均为水做还原剂的氧化还原反应。
( )(2)将KI 和FeCl 3溶液在试管中混合后,加入CCl 4,振荡,静置,下层溶液显紫红色,说明氧化性Fe 3+>I 2。
( )(3)Cl 2+2Br -══2Cl -+Br 2,Zn+Cu 2+══Zn 2++Cu 均为单质被还原的置换反应。
( )(4)某元素从游离态变为化合态,该元素可能被氧化也可能被还原。
( )(5)铜与浓硝酸的反应中电子转移的方向和数目可表示为×√×√√2.(1)用双线桥法标出下列反应的电子转移情况。