肺炎支原体培养药敏试剂介绍
- 格式:ppt
- 大小:860.00 KB
- 文档页数:13

肺炎支原体培养及药敏试验结果分析摘要:目的对咽拭子标本进行肺炎支原体(MP)培养,分析阳性率及药敏情况,为临床诊治提供依据。
方法随机选取2018年11月至2019年12月医院2186例呼吸科呼吸道感染患者送检的咽拭子标本,将这些标本进行肺炎支原体培养和药敏试验,分析患者MP感染情况,以及采用何种药物治疗效果最好。
结果经肺炎支原体培养和药敏试验,我们发现2186例标本中,肺炎支原体培养结果显示阳性的有303例,阳性检出率为13.9%。
结论经过肺炎支原体培养和药敏试验可以得出,治疗药物中大环内酯类(依托红霉素、红霉素、罗红霉素、阿奇霉素)、克林霉素、克拉霉素对肺炎支原体有较强的抗菌性,喹诺酮类抗菌药物(环丙沙星、左氧氟沙星)耐药性有所增加,而四环素类抗菌药物(强力霉素、美满霉素)耐药情况较为严峻,耐药性逐渐增加,因此临床应根据药敏结果调整用药,首选大环内酯类抗菌药物,加大针对肺炎支原体感染的防控力度。
关键词:肺炎支原体;药敏试验;耐药性肺炎支原体(MP)为临床常见的病原体之一,主要侵犯呼吸系统,导致患者发生肺炎支原体感染,是我国社区获得性肺炎(CAP)的首位致病菌。
MP感染的主要治疗药物为大环内酯类、四环素类等抗菌药物,但随着抗菌药物的滥用及临床用药不规范,逐渐导致MP感染患者出现相应的耐药性。
近年来多名国内外相关学者针对MP感染的耐药性做出多方面的探究,并在临床分离出对大环内酯类抗菌药物耐药的MP耐药菌株,但仍然存在不同地区的耐药菌株具有差异性[2]。
本文通过肺炎支原体培养和药敏试验,分析引起成人呼吸道感染的主要病原体和针对性用药,作以下分析。
1资料与方法1.1标本来源选取2018年11月至2019年12月医院2186例呼吸科下呼吸道感染患者送检的咽拭子标本。
1.2标本采集在患者进行治疗前,采集患者呼吸道咽拭子。
在采集标本前,用生理盐水漱口,用无菌拭子来回擦拭悬雍垂附近数次。
所采集标本应尽快接种,室温放置不得超过4个小时。

肺炎支原体抗体( IgM )检测试剂盒(胶体金法)说明书【产品名称】肺炎支原体抗体(IgM )检测试剂盒(胶体金法)【包装规格】40 人份 /盒或 20 人份 / 盒(详细规格见试剂盒包装标签)【预期用途】定性检测人血清中的肺炎支原体IgM 抗体,可用于支原体肺炎的协助诊疗。
【查验原理】本品应用间接法的胶体金标志免疫斑点渗滤原理,质控线采纳双抗夹心的胶体金标志免疫斑点渗滤原理。
该试剂盒里的斑点反响板上的微孔滤膜固相有肺炎支原体P1 蛋白抗原斑点,当待检测的血清中含有肺炎支原体IgM 抗体时,与微孔滤膜上的肺炎支原体P1 蛋白抗原抗原形成复合物,胶体金标志的羊抗人IgM 抗体与上述抗原抗体复合物联合,形成肉眼可见的红色斑点,即为阳性结果,不然为阴性结果。
微孔滤膜上的质控线含有羊抗人IgM 抗体,当待测血清加入后,人血清中的IgM 抗体与质控线上羊抗人IgM 抗体形成复合物,胶体金标志的羊抗人IgM 抗体再与上述复合物联合,形成肉眼可见的红色质控线。
【主要构成成份】1.斑点反响板: 40 块(或 20 块),每块斑点反响板主要由含固相肺炎支原体P1 蛋白抗原斑点的硝酸纤维膜和吸水纸构成。
2.试剂 A: 1 瓶,约 10ml (或 5 ml),无色澄清溶液,主要成份为PH7.4PBS 缓冲液、吐温-20、硫柳汞( 0.1%)。
3.试剂 B: 1 瓶,约 8ml(或 4ml),深红色澄清溶液,主要成份为胶体金标志的羊抗人IgM 抗体、牛血清白蛋白、硫柳汞(0.1%)。
【储藏条件及有效期】试剂盒一般采纳冷链运输,并采纳最迅速的运输方式,缩短运输时间;冬季运输应注意防备制品冻结。
试剂盒储藏条件为2℃~8℃,有效期为8 个月。
【样本要求】1.本试剂盒产品仅合用于对血清样本的检测,其余样本(如,胸腹水、脑脊液、尿液等)未经过产品预期用途的有关研究,不合用于本产品的检测。
2. 样本收集:采纳静脉血于干净离心管中,不加任何抗凝剂、保护剂,置于37℃水浴 20~ 30 分钟(或置室温 1 小时以上),待纤维蛋白原充足凝结后离心(4000 转/ 分, 5~ 10 分钟)分别血清。
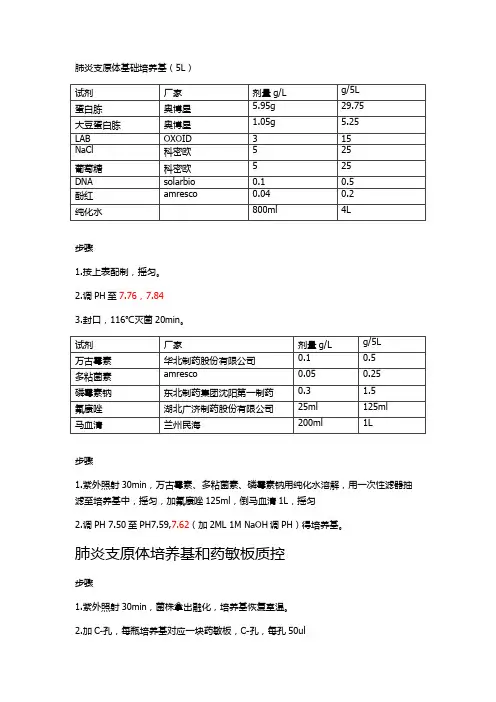
肺炎支原体基础培养基(5L)
步骤
1.按上表配制,摇匀。
2.调PH至7.76,7.84
3.封口,116℃灭菌20min。
步骤
1.紫外照射30min,万古霉素、多粘菌素、磷霉素钠用纯化水溶解,用一次性滤器抽滤至培养基中,摇匀,加氟康唑125ml,倒马血清1L,摇匀
2.调PH 7.50至PH7.59,7.62(加2ML 1M NaOH调PH)得培养基。
肺炎支原体培养基和药敏板质控
步骤
1.紫外照射30min,菌株拿出融化,培养基恢复室温。
2.加C-孔,每瓶培养基对应一块药敏板,C-孔,每孔50ul
3.摇匀菌株,每瓶培养基加200ul菌液,摇匀,加样,每孔50ul
4.每孔滴两滴石蜡油,盖药敏盖,37℃培养。
配制肺炎支原体试剂盒所需抗生素试剂
一、母液的配制
ERY、ROX、JOS.CLA,AZI,ACE,MIN,DOX,CLI,SPA,CIP.LEV,GAT,每种抗生素10mg,至小玻璃瓶中,洗净30个100ml的玻璃瓶,用无水乙醇洗一遍,每瓶加130ml无水乙醇
二、包被
每孔50ul。

肺炎支原体培养药敏检测试剂盒
(微生物检验法)
2.性能指标
2.1外观与结构
2.1.1培养液应透明、呈红色、清亮,无沉淀、无凝块、无絮状物。
2.1.2药敏微孔板应透明,无明显裂纹、气泡、锋棱及毛刺。
板盖与板体嵌接应紧密。
2.1.3试剂盒的文字和标记应清晰、准确、牢固。
2.2性能
2.2.1酸碱度:选择培养液、药敏培养液在25℃时的 pH 值应为7.3±0.5。
2.2.2培养灵敏度:选择培养液、药敏培养液接种终浓度为 103CCU 的目的菌株应可生长。
2.2.3培养选择性:选择培养液、药敏培养液接种终浓度为 104CCU 的非目的菌株不应生长。
2.2.4培养鉴别药敏重复性:
2.2.4.1批内重复性
2.2.4.1.1Mp 选择培养型:Mp 质控菌株培养重复率应达 100%;
2.2.4.1.2Mp 培养药敏型:Mp 质控菌株鉴别重复率应达 100%,药敏重复率应达 95%。
2.2.4.2批间重复性
2.2.4.2.1Mp 选择培养型:Mp 质控菌株培养重复率应达 100%;
2.2.4.2.2Mp 培养药敏型:Mp 质控菌株鉴别重复率应达 100%,药敏重复率应达 95%。
2.3微生物污染
培养液应无微生物污染。
2.4装量最大允许偏差
2.4.1Mp选择培养液装量允许最大偏差为1.4ml+0.3ml。
2.4.2Mp药敏培养液装量允许最大偏差为
3.6ml+0.3ml。
1。




小儿肺炎支原体培养及药敏试验分析李健茹;陈世豪;邱仲柳【摘要】目的培养肺炎支原体(MP)并进行药敏试验,帮助鉴别诊断小儿肺炎病因并选择适合小儿的敏感药物进行治疗.方法对356例小儿肺炎患儿的咽拭子进行肺炎支原体鉴定培养并对9种抗生素进行药敏试验.结果 MP阳性55例,阳性率为15.4%,耐药性由高到低为罗红霉素(54.5%)>克拉霉素(32.7%)=阿奇霉素(32.7%)>虹霉素(21.8%)=加替沙星(21.8%)>克林霉素(20.0%)>乙酰螺旋霉素(9.1%)>司帕沙星(1.8%)>左氧氟沙星(0%).结论培养能对MP引起的肺炎进行确诊,临床治疗MP选择药物时,MP对药物的耐药性不容忽视,应该根据药敏试验结果选用药物,使病患得到正确及时的治疗,并减缓耐药株出现.【期刊名称】《中国医药指南》【年(卷),期】2011(009)003【总页数】2页(P32-33)【关键词】肺炎支原体;培养;抗生素;耐药性【作者】李健茹;陈世豪;邱仲柳【作者单位】广东省江门市南方医科大学附属新会医院检验科,广东,江门,529100;广东省江门市南方医科大学附属新会医院检验科,广东,江门,529100;广东省江门市南方医科大学附属新会医院检验科,广东,江门,529100【正文语种】中文【中图分类】R375+.2;R725.6肺炎支原体(mycoplasma pneumoniae,MP)是我国急性呼吸道感染的常见病原体,由口、鼻分泌物经空气传播。
临床多表现为咳嗽、发热、头痛、咽喉疼痛和肌肉酸痛等。
本文对356例少儿肺炎感染患儿进行肺炎支原体培养鉴定以及药敏试验,现将分析情况报道如下。
广东省江门市南方医科大学附属新会医院2010年4月至8月收治的儿科住院及门诊呼吸道感染患儿356例,平均(6.2±1.9)岁,年龄最小的92d,年龄最大的14岁。
男孩226例,女孩90例。
取患儿咽拭子做液体培养基检测,试剂由陕西百盛园生物科技信息有限公司提供,对红霉素(ERY)、罗红霉素(ROX)、克拉霉素(CLA)、阿奇霉素(AZI)、乙酰螺旋霉素(ACE)、克林霉素(CLI)、左氧氟沙星(LEV)、加替沙星(GAT)、司帕沙星(SPA)9种药物进行药敏试验,操作及结果判读严格按试剂说明书进行。


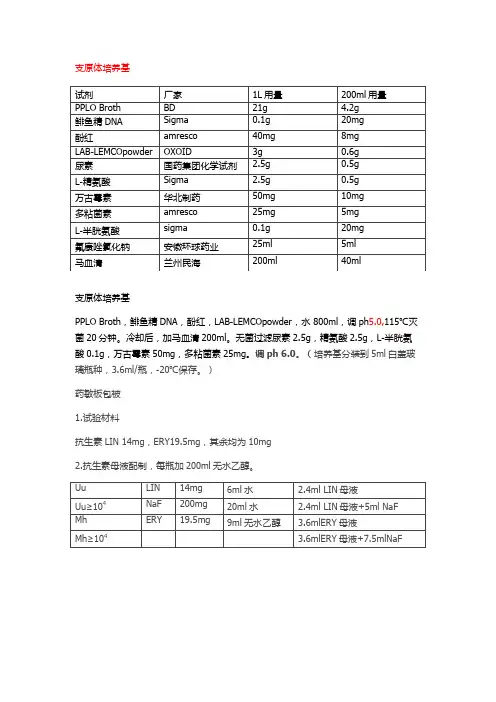
支原体培养基支原体培养基PPLO Broth,鲱鱼精DNA,酚红,LAB-LEMCOpowder,水 800ml,调ph5.0,115℃灭菌20分钟。
冷却后,加马血清200ml。
无菌过滤尿素2.5g,精氨酸2.5g,L-半胱氨酸0.1g,万古霉素50mg,多粘菌素25mg。
调ph 6.0。
(培养基分装到5ml白盖玻璃瓶种,3.6ml/瓶,-20℃保存。
)药敏板包被1.试验材料抗生素LIN 14mg,ERY19.5mg,其余均为10mg2.抗生素母液配制,每瓶加200ml无水乙醇。
其他孔药敏板质控1.紫外灯照射至少30min,菌株拿出融化,标记药敏板。
2.加C-孔,每块药敏板对应一瓶培养基,每孔100ul。
3.菌液稀释:摇匀解脲或人型支原体菌株,取4个空瓶,标记10-1至10-4,每瓶加3.6ml生理盐水,摇匀菌液,吸400ul至10-1,依次稀释至10-4,。
4.加药敏板:加入对应浓度菌液至空白培养基,每孔100ul,加样出C-孔的所有孔。
5.加完后,分别滴两滴石蜡油,盖药敏板,放37℃培养箱培养24h,48h,观察结果。
解脲支原体人型支原体菌株活化保存1.紫外照射30min,培养基提前放37℃培养箱,菌株拿出活化。
2.解脲支原体菌株:吸出5ml加至200ml培养基中摇匀,37℃培养。
3. 人型支原体菌株:吸出7.5ml加至200ml培养基中摇匀,37℃培养。
4.观察颜色发红,开始分装,每支500ul。
Uu菌株保存400ul菌液加入到200ml培养基中(下午4:30),摇匀,37度,第二天8:30拿出,观察颜色偏红,分装至1.5mlPE管中,每管500ul,放超低温。
检测解脲支原体菌活力和人型支原体CCU一.试验材料解脲支原体菌株,人型支原体菌株,药敏板,培养基,生理盐水二.步骤1.紫外30分钟,板子做uu,1个浓度1块,标记2.Uu:稀释10-1至10-4 4个浓度的菌液(3.6ml+0.4ml),分别加至对应浓度的空白培养基,摇匀,加药敏板上,滴两滴石蜡油培养。
支原体药敏检测的实验药物浓度和报告方式探讨支原体是一类常见的病原微生物,可导致多种感染疾病,如尿道炎、阴道炎、肺炎等。
为了对支原体感染进行准确的诊断和治疗,药敏检测是一种重要的手段。
药敏检测可以帮助医生选择合适的药物来治疗感染,提高治疗效果。
本文将探讨支原体药敏检测中实验药物浓度和报告方式的相关问题。
首先是实验药物浓度的探讨。
在进行药敏检测时,需要选择合适的药物浓度来进行实验。
常用的方法是通过微量稀释法来确定药物的最低抑菌浓度(MIC,Minimal Inhibitory Concentration)。
MIC是指药物能有效抑制病原微生物生长的最低浓度。
在支原体药敏检测中,常用的实验药物包括阿奇霉素、多西环素等。
这些药物的实验浓度应该根据临床的需要和病原微生物的特点来确定。
对于支原体药物浓度的选择,应该参考多方面的因素。
首先是临床的需要。
药敏检测的目的是为了指导临床治疗,因此实验药物的浓度应该与临床使用的浓度相符合。
其次是支原体的特点。
不同的支原体对药物的敏感性有所不同,因此在选择实验药物浓度时,应该考虑到不同支原体的特点。
最后是实验条件。
药物在不同的实验条件下可能会有不同的抑菌效果,因此在选择实验药物浓度时,应该参考实验条件来进行调整。
其次是报告方式的探讨。
药敏检测的结果应该以清晰、准确的方式向临床医生报告。
常用的报告方式包括抗生素敏感、抗生素中度敏感和抗生素耐药。
抗生素敏感表示该药物对病原微生物具有较好的抑制作用,可以作为临床治疗的药物选择。
抗生素中度敏感表示该药物对病原微生物的抑制作用较弱,可能需要较高浓度的药物来治疗。
抗生素耐药表示该药物对病原微生物的抑制作用较差,通常不建议作为治疗的药物选择。
在支原体药敏检测中,报告方式的选择应该考虑到临床的需要和病原微生物的特点。
对于临床需要高度依赖特定药物治疗的情况,应该将抗生素敏感和抗生素中度敏感分开报告,以便医生选择合适的治疗方案。
对于抗生素耐药的情况,应该指导医生选择其他合适的药物进行治疗。