常用化学反应方程式
- 格式:doc
- 大小:32.50 KB
- 文档页数:3
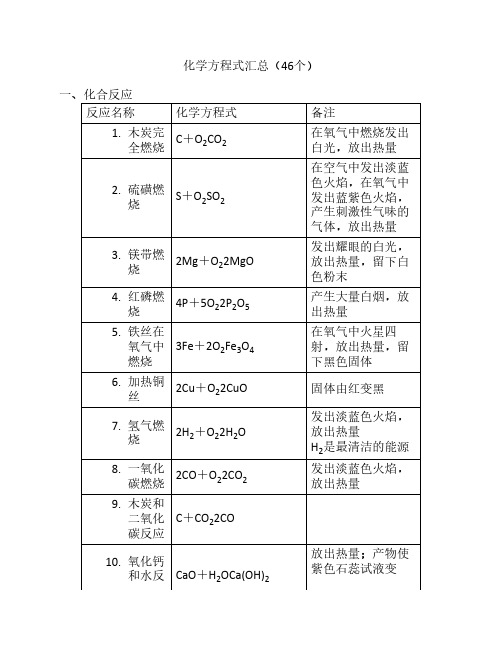
化学方程式汇总(46个)一、化合反应反应名称化学方程式备注1. 木炭完全燃烧C+O2CO2在氧气中燃烧发出白光,放出热量2. 硫磺燃烧S+O2SO2在空气中发出淡蓝色火焰,在氧气中发出蓝紫色火焰,产生刺激性气味的气体,放出热量3. 镁带燃烧2Mg+O22MgO发出耀眼的白光,放出热量,留下白色粉末4. 红磷燃烧4P+5O22P2O5产生大量白烟,放出热量5. 铁丝在氧气中燃烧3Fe+2O2Fe3O4在氧气中火星四射,放出热量,留下黑色固体6. 加热铜丝2Cu+O22CuO固体由红变黑7. 氢气燃烧2H2+O22H2O发出淡蓝色火焰,放出热量H2是最清洁的能源8. 一氧化碳燃烧2CO+O22CO2发出淡蓝色火焰,放出热量9. 木炭和二氧化碳反应C+CO22CO10. 氧化钙和水反CaO+H2OCa(OH)2放出热量;产物使紫色石蕊试液变应蓝,使无色酚酞试液变红11. 二氧化碳和水反应CO2+H2OH2CO3产物使紫色石蕊试液变红12. 硫酸铜粉末和水反应CuSO4+5H2OCuSO4·5H2O白色粉末变成蓝色晶体,放出热量CuSO4粉末用于检验物质是否含有水二、分解反应反应名称化学方程式备注13. 碳酸受热分解H2CO3H2O+CO2↑H2CO3不稳定14. 电解水2H2O2H2↑+O2↑正负极都产生气泡,负极产生的气体体积是正极产生气体的2倍负氢正氧,氢二氧一;工业上生产H215. 高温煅烧大理石或石灰石CaCO3CaO+CO2↑工业上生产CaO16. 过氧化氢在二氧化锰的催化作用下分解2H2O22H2O+O2↑产生大量气泡,放出热量实验室制取O217. 加热氯酸钾和二氧化锰的混合物2KClO32KCl+3O2↑实验室制取O218. 加热硫酸铜晶体CuSO4·5H2OCuSO4+5H2O蓝色晶体变成白色粉末,试管口产生无色液体三、置换反应反应名称化学方程式备注19. 木炭还原氧化铜C+2CuO2Cu+CO2↑产生红色固体20. 氢气还原氧化铜H2+CuOCu+H2O产生红色固体,试管口产生无色液体H2有还原性,用于冶炼金属21. 镁带在二氧化碳中燃烧2Mg+CO22MgO+C产生黑色和白色固体22. 锌粒和稀盐酸反应Zn+2HClZnCl2+H2↑实验室制取H223. 锌粒和稀硫酸反应Zn+H2SO4ZnSO4+H2↑实验室制取H224. 铁钉和稀盐酸反应Fe+2HClFeCl2+H2↑Fe元素从0价变成+2价25. 铁钉和稀硫酸Fe+H2SO4FeSO4+H2↑26. 铁丝和硫酸铜溶液反应Fe+CuSO4FeSO4+Cu铁丝表面产生红色固体27. 铜丝和硝酸银溶液反应Cu+2AgNO3Cu(NO3)2+2Ag铜丝表面产生银白色固体四、复分解反应反应名称化学方程式备注28. 氢氧化镁治疗胃“泛酸”Mg(OH)2+2HClMgCl2+2H2O29. 大理石或石灰石和稀盐酸反应CaCO3+2HClCaCl2+H2O+CO2↑实验室制取CO230. 硝酸银溶液和稀盐酸反应AgNO3+HClAgCl↓+HNO3产生白色沉淀31. 氯化钡溶液和稀硫酸反应BaCl2+H2SO4BaSO4↓+2HCl产生白色沉淀32. 硫酸铜溶液和氢氧化钠溶液反应CuSO4+2NaOHCu(OH)2↓+Na2SO4产生蓝色沉淀33. 氯化铁溶液和氢氧化钠溶液FeCl3+3NaOHFe(OH)3↓+3NaCl产生红褐色沉淀34. 碳酸钠溶液和石灰水反应Na2CO3+Ca(OH)2CaCO3↓+2NaOH35. 硫酸铜溶液和熟石灰制取农药波尔多液CuSO4+Ca(OH)2Cu(OH)2↓+CaSO436. 碳酸钠溶液和足量盐酸反应Na2CO3+2HCl2NaCl+H2O+CO2↑37. 氯化钠溶液和硝酸银溶液反应NaCl+AgNO3AgCl↓+NaNO3AgCl不溶于HNO338. 硫酸钠溶液和氯化钡溶液反应Na2SO4+BaCl2BaSO4↓+2NaClBaSO4不溶于HNO3五、其他反应反应名称化学方程式备注39. 甲烷燃烧CH4+2O2CO2+2H2O产生淡蓝色火焰40. 少量二氧化碳通入石灰水CO2+Ca(OH)2CaCO3↓+H2O产生白色沉淀;石灰水在空气中变质;石灰水用于检验CO241. 少量二氧NaOH在空气中变化碳和氢氧化钠溶液反应CO2+2NaOHNa2CO3+H2O质;NaOH溶液用于吸收CO242. 氢氧化钠溶液吸收二氧化硫SO2+2NaOHNa2SO3+H2ONa2SO3名称是亚硫酸钠43. 一氧化碳还原氧化铜CO+CuOCu+CO2产生红色固体尾气需要燃烧处理,防止CO污染空气44. 一氧化碳还原氧化铁3CO+Fe2O32Fe+3CO2工业炼铁的主要反应45. 盐酸除铁锈Fe2O3+6HCl2FeCl3+3H2O溶液变成棕黄色46. 硫酸溶解氧化铜固体CuO+H2SO4CuSO4+H2O溶液变成蓝色*固体小颗粒分散到气体中形成烟;小液滴分散到气体中形成雾。

化学反应方程式1.Pb(NO3)2 + 2KI ==== 2KNO3 + PbI2↓硝酸铅( n ) 碘化钾( n )硝酸钾碘化铅( y )2.Na2CO3 + Ca(OH)2 ===== CaCO3↓+ 2NaOH碳酸钠( w )3.FeCl3+3KSCN ==== Fe(SCN)3+3KCl氯化铁( y ) 硫氰化钾( n ) 硫氰化铁( r )[检验三价铁离子的存在][Fe(SCN)3---血红色胶状物质]4.CuSO4+2NaOH ==== Cu(OH)2↓+Na2SO4硫酸铜( s )氢氧化钠( b ) ( b ) ( s )[Cu(OH)2---蓝色絮状沉淀]5.1氯化氢气体溶于水生成盐酸;纯盐酸——无色透明;工业用——淡黄色(含三价铁离子等物质);浓盐酸——有挥发性,刺激性气味,瓶口有雾(酸雾)5.2 纯硫酸——无色、黏稠、油状的液体;有很强腐蚀性,沾到皮肤上应用小苏打(NaHCO3)溶液冲洗;具有吸水性,可用作某些气体的干燥剂;具有脱水性,是有机物的O、H脱出成水而炭化;不能将水倒入浓硫酸稀释酸反应化学方程式[酸电离生成的阳离子都是氢离子][酸的PH值低于7,可使紫色石蕊试液变红色,无色酚酞试液不变色]6.acid+salt→Nacid+Nsalt(复分解反应)E.g. (1)CaCO3+2HCl ==== CaCl2+H2O+CO2↑(2)HCl+AgNO3 ==== AgCl↓+HNO3[AgCl---白色沉淀,不溶于稀硝酸][检验HCl或一价氯离子的存在](3)H2SO4+BaCl2 ==== BaSO4↓+2HCl[产生不溶于稀硝酸的白色沉淀(BaSO4)][可用硝酸银溶液和稀硝酸鉴别一价氯离子的存在][硫酸根离子可用硝酸钡溶液(氯化钡溶液)和稀硝酸看是否声称不溶于稀硝酸的白色沉淀]7.acid+base→salt+H2O(中和反应)(复分解反应)E.g. (1)NaOH+HCl ==== NaCl+H2O(2)Al(OH)3+3HCl ===== AlCl3+3H2O(3)H2SO4+2NaOH ==== Na2SO4+2H2O(4)3H2SO4+2Al(OH)3 ==== 6H2O8.acid+某些金属氧化物→salt+H2O(复分解反应)E.g. (1)Fe2O3+6HCl ==== 2FeCl3+3H2O[工业上除锈][铁锈渐渐溶解,溶液变成黄色(FeCl3)](2)CuO+2HCl ==== CaCl2+H2O[CuO---褐色][CaCl2---蓝色](3)2HCl+CaCO3 ==== CaCl2+H2O+CO2↑(4)Fe2O3+3H2SO4 ==== Fe2(SO4)3+3H2O[铁锈渐渐溶解,溶液变成黄色(Fe2(SO4)3)](5)H2SO4+CuO ==== CuSO4+H2O9.acid+活泼金属→salt+H2(置换反应)E.g. (1)Zn+HCl ==== ZnCl2+H2↑[实验室制氢气](2)Fe+2HCl ==== FeCl2+H2↑[溶液变成浅绿色][生成氯化亚铁](3)Zn+H2SO4 ==== ZnSO4+H2↑[锌粒表面产生气泡][试管壁变热]碱化学反应方程式[碱电离生成的阴离子都是氢氧根离子][碱PH值高于7,使紫色石蕊试液变蓝色,无色酚酞试液变红色] 10.氢氧化钠俗称烧碱、苛性钠;吸水性——易潮解,常用作氧气、氢气的干燥剂,有滑腻感;腐蚀性——能溶解有机物;溶解性——极易溶于水,并放出大量的热11.氢氧化钙俗称熟石灰或消石灰,水溶液称为石灰水12.可溶解性碱:氢氧化钠,氢氧化钾,氢氧化钡,氢氧化钙13.可溶base+非金属氧化物→salt+H2OE.g. (1)Ca(OH)2+CO2 ==== CaCO3↓+H2O[用于检验二氧化碳的存在][产生白色絮状沉淀](2)2NaOH+SO2 ==== Na2SO3+H2O[工业上用碱溶液来吸收有毒的酸性气体](3)2NaOH+CO2 ==== Na2CO3+H2O[氢氧化钠不能敞口放置](4)SiO2+2NaOH ==== Na2SiO3+H2O[氢氧化钠不可用玻璃瓶塞放置]14.base+某些可溶salt→Nbase+NsaltE.g.(1)Ca(OH)2+Na2CO3 ==== CaCO3↓+2NaOH[用碳酸钠溶液可以区分氢氧化钠和熟石灰](2)CuCl2+2NaOH ==== Cu(OH)2↓+2NaCl(3)CuCl2+Ca(OH)2 ==== Cu(OH)2↓+CaCl2[蓝色溶液中出现蓝色絮状沉淀][可用于检验二价铜离子的存在](4)FeCl3+3NaOH ==== Fe(OH)3↓+3NaCl(5)2FeCl3+3Ca(OH)2 ==== 2Fe(OH)3↓+ 3CaCl2[黄色溶液中出现红褐色沉淀][可用于检验三价铁离子的存在] *【碱与盐反应时,两者均可溶,同时生成物中必有一种沉淀产生】15.base+acid→salt+H2OE.g.(1)H2SO4+2NaOH ==== 2H2O+NaSO4(2)2HCl+Ca(OH)2 ==== CaCl2+2H2O[农业上用熟石灰降低土壤酸性](3)3HCl+Al(OH)3 ==== AlCl3+3H2O[医学上用氢氧化铝中和过多的胃酸]。

方程式共14个.化合反应:1. 红磷在空气中燃烧生成五氧化二磷:4P + 5O2= 2P2O5冒大量的白烟,生成白色固体,放出热量2. 硫粉在氧气中燃烧生成二氧化硫:S + O2= SO2明亮蓝紫色的火焰,生成刺激性气味的气体3. 碳在氧气中燃烧生成二氧化碳:C + O2= CO2燃烧更旺,白光,产生无色无味使石灰水变浑浊的气体4. 镁在空气中燃烧生成氧化镁:2Mg + O2= 2MgO剧烈燃烧.耀眼白光.生成白色固体.放热.产生大量白烟5. 氢气中空气中燃烧生成水:2H2 + O2= 2H2O发出淡蓝色的火焰,放出热量,有水雾生成6. 铁在氧气中燃烧四氧化三铁:3Fe + 2O2 =Fe3O4剧烈燃烧,火星四射,生成黑色固体.分解反应:7. 加热高锰酸钾生成锰酸钾、二氧化锰和氧气:2KMnO4= K2MnO4 + MnO2 + O2↑8. 加热氯酸钾生成氯化钾和氧气:2KClO3= 2KCl + 3O2 ↑9. 实验室用双氧水制氧气:2H2O2= 2H2O+ O2↑10. 水在直流电的作用下分解:2H2O 通电= 2H2↑+ O2 ↑.置换反应:11.锌和稀硫酸生成硫酸锌和氢气:Zn + H2SO4 = ZnSO4 + H2↑12.铁和硫酸铜生成硫酸亚铁和铜:Fe+CuSO4==FeSO4+Cu.复分解反应:13.碳酸钠与浓盐酸反应:Na2CO3 + 2HCl === 2NaCl + H2O + CO2↑白色粉末消失,无色无味气体产生14.硫酸铜与氢氧化钠生成氢氧化铜和硫酸钠:CuSO4+2NaOH==Cu(OH)2 ↓+Na2SO4蓝色溶液变成蓝色沉淀二.概念:1、化学是一门研究物质的组成、结构、性质以及变化规律的以实验为基础自然科学。
2、化学变化和物理变化的根本区别是:有没有新物质的生成。
化学变化中伴随发生一些如放热、发光、变色、放出气体、生成沉淀等现象。
3、物理性质——状态、气味、熔点、沸点、硬度、密度、延展性、溶解性、挥发性、导电性、吸附性等。

常用化学方程式化学方程式是化学反应的一种表现形式,被广泛应用于各种化学实验、工业生产、环境保护等领域。
本文将介绍几种常用的化学方程式,包括酸碱反应、氧化还原反应、气体反应等。
一、酸碱反应酸碱反应是化学反应中最为基础的类型之一,常见的酸碱反应方程式如下:1.强酸和强碱的反应:HCl + NaOH → NaCl + H2O2.弱酸和强碱的反应:CH3COOH + NaOH → CH3COONa + H2O3.弱碱和强酸的反应:NH3 + HCl → NH4Cl二、氧化还原反应氧化还原反应(简称氧化反应和还原反应)是指在化学反应中,发生氧元素的转移的反应。
常见的氧化还原反应方程式如下:1.金属氧化反应:2Al + 3O2 → 2Al2O32.金属还原反应:CuO + H2 → Cu + H2O3.半反应式:Cu2+ + 2e- → CuFe → Fe2+ + 2e-三、气体反应气体反应指的是通过反应得到气体产物的化学反应,常见的气体反应方程式如下:1.燃烧反应:C2H2 + 2.5O2 → 2CO2 + H2O2.分解反应:2H2O → 2H2 + O23.合成反应:N2 + 3H2 → 2NH3四、其它反应除了上述反应,化学反应还包括复分解反应、酸碱中和反应等,常见的方程式如下:1.复分解反应:Ba(NO3)2 + Na2SO4 → BaSO4 ↓ + 2NaNO32.酸碱中和反应:NaOH + HCl → NaCl + H2O通过以上方程式的介绍,我们可以发现化学反应无处不在,它们在生产、环保等各个领域中起着重要的作用。
能够对化学反应的了解不仅能够提高我们的科学素养,还可以让我们更好地理解周围的世界。

初三化学反应式大全一、氧化还原反应(Redox Reactions)1. 金属与非金属氧化物反应:M + O₂ → MO例如:2Na + O₂ → 2Na₂O2. 非金属与非金属氧化物反应:N₂O₅ + H₂O → 2HNO₃例如:CO₂ + H₂O → H₂CO₃3. 金属与酸反应:2Fe + 6HCl → 2FeCl₃ + 3H₂例如:Zn + H₂SO₄ → ZnSO₄ + H₂4. 还原剂与氧化剂的反应:H₂O₂ + 2KI → I₂ + 2KOH例如:KMnO₄ + 5HCl → KCl + MnCl₂ + 3H₂O + Cl₂5. 氧化剂与还原剂的反应:Cl₂ + 2KI → 2KCl + I₂例如:HNO₃ + 3Cu → 3Cu(NO₃)₂ + H₂O + 2NO 二、酸碱反应(Acid-Base Reactions)1. 强酸与强碱的反应:HCl + NaOH → NaCl + H₂O例如:HNO₃ + KOH → KNO₃ + H₂O 2. 强酸与碱性氧化物的反应:HCl + Na₂O → 2NaCl + H₂O例如:HCl + CaO → CaCl₂ + H₂O3. 酸与碱的中和反应:H₂SO₄ + 2NaOH → Na₂SO₄ + 2H₂O例如:HNO₃ + NH₃ → NH₄NO₃4. 酸与金属的反应:2HCl + Zn → ZnCl₂ + H₂例如:2HCl + Mg → MgCl₂ + H₂5. 酸与金属碱的反应:2HNO₃ + Ca(OH)₂ → Ca(NO₃)₂ + 2H₂O 例如:HCl + NaOH → NaCl + H₂O三、沉淀反应(Precipitation Reactions)1. 双盐交换反应:AgNO₃ + NaCl → AgCl + NaNO₃例如:CaCl₂ + Na₂CO₃ → CaCO₃ + 2NaCl2. 酸与相应的盐反应:2HCl + Ba(OH)₂ → BaCl₂ + 2H₂O例如:2HCl + Cu(OH)₂ → CuCl₂ + 2H₂O3. 溶液中的钠盐与其他金属盐反应:Na₂S + Cd(NO₃)₂ → CdS↓ + 2NaNO₃例如:Na₂S + Pb(NO₃)₂ → PbS↓ + 2NaNO₃4. 氨与金属离子反应:2NH₃ + Cu²⁺ → Cu(NH₃)₄²⁺例如:2NH₃ + Fe³⁺ → Fe(NH₃)₆³⁺四、酸、碱、盐的相关反应(Acid, Base, Salt Reactions)1. 酸钠与碳酸钙的反应:2HCl + Na₂CO₃ → 2NaCl + H₂O + CO₂例如:2HCl + CaCO₃ → CaCl₂ + H₂O + CO₂2. 硝酸银与氯化钠的反应:AgNO₃ + NaCl → AgCl + NaNO₃例如:AgNO₃ + KCl → AgCl + KNO₃综上所述,初三化学反应式大全包含了氧化还原反应、酸碱反应、沉淀反应以及酸、碱、盐的相关反应。

高中化学反应方程式高中化学反应方程式:1、硝酸银与盐酸及可溶性盐酸盐溶液:Ag++Cl- =AgCl↓2、钠与水反应:2Na+2H2O=2Na++2OH –+H2↑3、钠与硫酸铜溶液:2Na+2H2O+Cu2+=2Na++Cu(OH)2↓+H2↑4、过氧化钠与水反应:2Na2O+2H2O=4Na++4OH –+O2↑5、碳酸氢盐溶液与强酸溶液混合:HCO3- +H+=CO2↑+H2O6、碳酸氢盐溶液与醋酸溶液混合:HCO3- +CH3COOH=CO2 ↑+H2O+CH3COO -7、氢氧化钙溶液与碳酸氢镁反应:Ca2++2OH-+2HCO3- +Mg2+=Mg(OH)2↓+CaCO3↓8、向碳酸氢钙溶液中加入过量的氢氧化钠:2HCO3-+Ca2++2OH –=CaCO3↓+2H2O+CO32–9、向碳酸氢钙溶液中加入少量的氢氧化钠:Ca2++HCO3-+OH –=CaCO3↓+H2O10 、澄清石灰水与少量小苏打溶液混合:Ca2++OH –+HCO3- =CaCO3↓+H2O11 、澄清石灰水通入少量CO2:Ca2++2OH –+CO3=CaCO3↓+H2O12 、澄清石灰水通入过量CO2:OH–+CO2=HCO3-13 、碳酸氢钠溶液与少量石灰水反应:Ca2++2OH –+2HCO3- =CaCO3↓+CO32– +2H2O14 、碳酸氢钠溶液与过量石灰水反应:HCO3-+OH –+Ca2+=CaCO3↓+H2O15 、等物质的量氢氧化钡溶液与碳酸氢铵溶液混合:Ba2++2OH –+NH4++HCO3- =BaCO3↓+H2O+NH3?H2O16 、碳酸钠溶液与盐酸反应:CO32–+H+=HCO3- 或 CO32–+2H+=CO2↑+H2O17 、向氢氧化钠溶液中通入少量的CO2?:CO2+2OH–=CO32 –+H2O18 、过量的 CO2 通入氢氧化钠溶液中:CO2+OH–=HCO3-19 、碳酸氢铵溶液中加入过量氢氧化钠溶液:NH4++HCO3-+2OH –=NH3↑+CO32–+2H2O20 、碳酸钙与盐酸反应:CaCO3+2H+=Ca2++CO2↑+H2O21 、碳酸钙与醋酸反应:CaCO3+2CH3COOH=Ca2++2CH3COO- +CO2↑+H2O。
1.碳与氧气(不足)的反应2C+O2==== 2CO碳与氧气(充足)的反应C+O2==== CO22.一氧化碳与氧气的反应2CO+O2==== 2CO23.二氧化碳与碳的反应CO2+C==== 2CO4.碳酸氢钠与盐酸的反应NaHCO3+HCl==== NaCl+H2O+CO2↑5.碳酸钠与盐酸的反应Na2CO3+ 2HCl==== 2NaCl+ H2O+ CO2↑6.碳酸钙与盐酸的反应CaCO3+2HCl==== CaCl2+ H2O+ CO2↑7.碳酸氢钠与氢氧化钠的反应NaHCO3+NaOH==== Na2CO3 +H2O8.碳酸钠与氢氧化钙的反应Na2CO3+Ca(OH)2==== CaCO3↓+ 2NaOH9.碳酸氢钠(少量)与氢氧化钙的反应NaHCO3+ Ca(OH)2==== CaCO3↓+NaOH+ H2O碳酸氢钠(过量)与氢氧化钙的反应2NaHCO3+ Ca(OH)2==== CaCO3↓+Na2CO3+2H2O10.碳酸氢钠加热的反应2NaHCO3==== Na2CO3+ H2O+CO2↑11.碳酸氢钙加热的反应Ca(HCO3)2==== CaCO3↓+H2O+CO2↑12.碳酸钙加热的反应CaCO3==== CaO+CO2↑13.二氧化碳(过量)通入氢氧化钙溶液中的反应Ca(OH)2+2CO2==== Ca(HCO3)2二氧化碳(少量)通入氢氧化钙溶液中的反应Ca(OH)2+CO2==== CaCO3↓+H2O14.氮气与氧气的反应N2+O2==== 2NO15.一氧化氮与氧气的反应2NO+O2==== 2NO216.二氧化氮与水的反应3NO2+ H2O==== 2HNO3+ NO17.氮气与氢气的反应N2+3H2========= 2NH318.氨气与水的反应NH3+H2O==== NH3?H2O19.氨气与盐酸的反应NH3+HCl==== NH4Cl20.氨气与硫酸的反应2NH3+H2SO4==== (NH4)2SO421.氨气与强酸的离子的反应NH3+H+==== NH4+22.氨的催化氧化的反应4NH3+5O2====== 4NO+6H2O23.碳酸氢铵加热的反应NH4HCO3==== NH3↑+CO2↑+H2O24.氯化铵加热的反应NH4Cl==== NH3↑+HCl↑25.碳酸铵加热的反应(NH4)2CO3==== 2NH3↑+CO2↑+H2O26.氯化铵与氢氧化钙的反应2NH4Cl+ Ca(OH)2==== CaCl2+2NH3↑+2H2O27.氯化铵与氢氧化钠的反应NH4Cl+ NaOH==== NaCl+NH3↑+H2O28.碳酸氢铵与氢氧化钠的反应NH4HCO3+2NaOH==== Na2CO3+NH3↑+2H2O29.碳酸氢铵与氢氧化钙的反应NH4HCO3+Ca(OH)2==== CaCO3↓+NH3↑+2H2O30.硝酸的分解的反应4HNO3========= 4NO2↑+O2↑+2H2O31.铜与浓硝酸的反应Cu+4HNO3(浓)==== Cu(NO3)2+2NO2↑+2H2O32.铜与稀硝酸的反应3Cu+8HNO3(稀)==== 3Cu(NO3)2+2NO↑+4H2O33.铁与浓硝酸的反应Fe+6HNO3(浓)==== Fe(NO3)3+3NO2↑+3H2O34.铁与稀硝酸的反应Fe+4HNO3(稀)==== Fe(NO3)3+NO↑+2H2O35.碳与浓硝酸的反应C+4HNO3(浓)==== CO2↑+4NO2↑+2H2O36.一氧化氮与一氧化碳的反应2NO+2CO====== N2+2CO237.一氧化氮与氧气和水的反应4NO+3O2+2H2O==== 4HNO338.二氧化氮与氧气和水的反应4NO2+O2+2H2O==== 4HNO339.氢氧化钠吸收二氧化氮和一氧化氮的反应2NaOH+NO2+NO==== 2NaNO2+ H2O40.氨气(过量)与氯气的反应8NH3+3Cl2==== 6NH4Cl+N2氨气(少量)与氯气的反应2NH3+3Cl2==== 6HCl+N241.二氧化氮生成四氧化二氮的反应2NO2==== N2O442.硫与铜的反应S+2Cu==== Cu2S43.硫与铁的反应S+Fe==== FeS44.硫与钠的反应S+2Na==== Na2S45.硫与铝的反应3S+2Al==== Al2S346.硫与汞的反应S+Hg==== HgS47.硫与氧气的反应S+O2==== SO248.硫与氢气的反应S+H2==== H2S49.硫与氢氧化钠的反应3S+6NaOH==== 2Na2S+Na2SO3+3H2O50.硫与浓硫酸的反应S+2H2SO4(浓)==== 3SO2+2H2O51.黑火药点燃S+2KNO3+3C==== K2S+3CO2↑+N2↑52.二氧化硫(少量)与氢氧化钠的反应SO2+2NaOH==== Na2SO3+H2O 二氧化硫(过量)与氢氧化钠的反应SO2+NaOH==== NaHSO353.二氧化硫与氢氧化钙的反应SO2+Ca(OH)2==== CaSO3↓+H2O54.二氧化硫与亚硫酸钙溶液的反应SO2+CaSO3+H2O ==== Ca(HSO3)255.二氧化硫与水的反应SO2+H2O==== H2SO356.二氧化硫与硫化氢的反应SO2+2H2S==== 3S↓+2H2O57.二氧化硫与氧气的反应2SO2+O2====== 2SO358.二氧化硫与过氧化钠的反应SO2+Na2O2==== Na2SO459.二氧化硫与氯水的反应SO2+ Cl2+2H2O==== H2SO4+2HCl60.三氧化硫与水的反应SO3+H2O==== H2SO461.亚硫酸与氧气的反应2H2SO3+O2==== 2H2SO462.亚硫酸钠与氧气的反应2Na2SO3+O2==== 2Na2SO463.浓硫酸与铜的反应2H2SO4(浓)+Cu==== CuSO4+SO2↑+2H2O64.浓硫酸与碳的反应2H2SO4(浓)+C==== CO2↑+2SO2↑+2H2O寿65.工业制备硫酸(初步) 4FeS2+11O2==== 8SO2+2Fe2O366.实验室制备硫酸(初步) Na2SO3+H2SO4(浓)==== Na2SO4+SO2↑+H2O67.硫化氢(少量)与氢氧化钠的反应H2S+2NaOH==== Na2S+2H2O硫化氢(过量)与氢氧化钠的反应H2S+NaOH==== NaHS+H2O68.硫化氢(少量)与氨气的反应H2S+2NH3==== (NH4)2S硫化氢(过量)与氨气的反应H2S+NH3==== NH4HS69.硫化氢与氧气(不足)的反应2H2S+O2==== 2S↓+2H2O 2H2S+O2==== 2S+2H2O硫化氢与氧气(充足)的反应2H2S+3O2==== 2SO2+2H2O70.硫化氢与氯气的反应H2S+Cl2==== 2HCl+S↓71.硫化氢与浓硫酸的反应H2S+H2SO4(浓)==== S↓+SO2↑+2H2O72.硫化氢的制备FeS+H2SO4==== FeSO4+H2S↑73.电解饱和食盐水(氯碱工业) 2NaCl+2H2O==== 2NaOH+H2↑+Cl2↑74.电解熔融状态氯化钠(制单质钠) 2NaCl==== 2Na+Cl2↑75.海水制镁(1) CaCO3==== CaO+CO2(2) CaO+H2O==== Ca(OH)2(3) Mg2++2OH2-==== Mg(OH)2↓(4) Mg(OH)2+2HCl==== MgCl2+2H2O(5) MgCl2==== Mg+C l2↑76.镁在空气中燃烧(与氧气的反应) 2Mg+O2==== 2MgO(与氮气的反应) 3Mg+N2==== Mg3N2(与二氧化碳的反应) 2Mg+CO2==== 2MgO+C77.镁与氯气的反应Mg+Cl2==== MgCl278.镁与水的反应Mg+2H2O==== Mg(OH)2+H2↑79.镁与盐酸的反应Mg+2HCl==== MgCl2+H2↑80.镁与氢离子的反应Mg+2H+==== Mg2++H2↑81.二氮化三镁与水的反应Mg3N2+6H2O==== 3M g(OH)2↓+2NH3↑82.镁与溴水的反应(颜色退去) Mg+Br2==== MgBr2(产生气泡) Mg+2HBr==== MgBr2+H2↑83.溴与水的反应Br2+H2O==== HBr+HBrO84.溴与氢氧化钠的反应Br2+2NaOH==== NaBr+NaBrO+H2O85.溴与氢气的反应Br2+H2==== 2HBr86.溴与铁的反应3Br2+2Fe==== 2FeBr387.碘与铁的反应I2+Fe==== FeI288.溴与碘化钾的反应Br2+2KI==== 2KBr+I289.氯气与溴化钾的反应2KBr+Cl2==== 2KCl+Br2第四章90.硅与氧气的反应Si+O2==== SiO291.硅与氯气的反应Si+2Cl2==== SiCl492.硅与氢气的反应Si+2H2===== SiH493.二氧化硅与氟的反应Si+2F2==== SiF494.硅与碳的反应Si+C==== SiC95.硅与氢氧化钠溶液的反应Si+2NaOH+H2O==== Na2SiO3+2H2↑96.硅与氢氟酸的反应Si+4HF==== SiF4+2H2↑97.单质硅的制备(1.制备)SiO2+2C==== Si+2CO(2.提纯)Si+2Cl2==== SiCl4(3.提纯)SiCl4+2H2==== Si+4HCl98.二氧化硅与氢氧化钠的反应SiO2+2NaOH==== Na2SiO3+H2O99.二氧化硅与氧化钠的反应SiO2+Na2O==== Na2SiO3100.二氧化硅与碳酸钠的反应SiO2+Na2CO3==== Na2SiO3+ CO2↑ 101.二氧化硅与氧化钙的反应SiO2+CaO==== CaSiO3102.二氧化硅与碳酸钙的反应SiO2+CaCO3==== CaSiO3+CO2↑ 103.二氧化硅与氢氟酸的反应SiO2+4HF==== SiF4+2H2O104.硅酸的制备Na2SiO3+ CO2+H2O==== H2SiO3↓+ Na2CO3105.硅酸加热分解H2SiO3==== SiO2+H2O106.铝与氧气的反应4Al+3O2==== 2Al2O3107.铝与氯气的反应2Al+3Cl2==== 2AlCl3108.铝与盐酸的反应2Al+6HCl==== 2AlCl3+3H2↑109.铝与氢氧化钠的反应2Al+2NaOH+6H2O==== 2Na[Al(OH)4]+3H2↑ 110.铝与水的反应2Al+6H2O==== 2Al(OH)3+3H2↑111.铝与三氧化二铁的反应(铝热反应)2Al+Fe2O3==== 2Fe+Al2O3 112.铝与二氧化锰的反应(铝热反应)4Al+3MnO2==== 3Mn+2AlO3113.氧化铝与盐酸的反应Al2O3+6HCl==== 2AlCl3+3H2O114.氧化铝与氢氧化钠的反应Al2O3+2NaOH+3H2O==== 2Na[Al(OH)4] 115.电解氧化铝2Al2O3==== 4Al+3O2↑116.硫酸与与一水合氨的反应Al2(SO4)3+6NH3?H2O==== 2Al(OH)3↓+3(NH4)2SO4117.氯化铝与一水合氨的反应AlCl3+3NH3?H2O==== Al(OH)3↓+3NH4Cl118.氯化铝与氢氧化钠(少量)的反应AlCl3+3NaOH==== Al(OH)3↓+3NaCl119.氢氧化铝与氢氧化钠的反应Al(OH)3+NaOH==== Na[Al(OH)4] 120.氯化铝与氢氧化钠(过量)的反应AlCl3+4NaOH==== Na[Al(OH)4]+3NaCl121.四羟基合氯酸钠与盐酸(少量)的反应Na[Al(OH)4]+HCl==== Al(OH)3↓+NaCl+H2O122.氢氧化铝与盐酸的反应Al(OH)3+3HCl==== AlCl3+3H2O123.四羟基合氯酸钠与盐酸(过量)的反应Na[Al(OH)4]+4HCl==== AlCl3+NaCl+4H2O124.四羟基合氯酸钠与氯化铝的反应3Na[Al(OH)4]+AlCl3==== 4Al(OH)3↓+3NaCl125.向四羟基合氯酸钠中通入过量二氧化碳Na[Al(OH)4]+CO2==== Al(OH)3↓+NaHCO3126.铜在潮湿空气中被腐蚀2Cu+O2+H2O+CO2==== Cu2(OH)2CO3 127.铜与氧气的反应2Cu+O2==== 2CuO128.铜与氯气的反应Cu+Cl2==== CuCl2129.铜氧化在高温下转化4CuO==== 2Cu2O+O2↑130.硫酸铜与水的反应CuSO4+5H2O==== CuSO4?5H2O。
1.碳与氧气(不足)的反应2C+O2==== 2CO碳与氧气(充足)的反应C+O2==== CO22.一氧化碳与氧气的反应2CO+O2==== 2CO23.二氧化碳与碳的反应CO2+C==== 2CO4.碳酸氢钠与盐酸的反应NaHCO3+HCl==== NaCl+H2O+CO2↑5.碳酸钠与盐酸的反应Na2CO3+ 2HCl==== 2NaCl+ H2O+ CO2↑6.碳酸钙与盐酸的反应CaCO3+2HCl==== CaCl2+ H2O+ CO2↑7.碳酸氢钠与氢氧化钠的反应NaHCO3+NaOH==== Na2CO3 +H2O8.碳酸钠与氢氧化钙的反应Na2CO3+Ca(OH)2==== CaCO3↓+ 2NaOH9.碳酸氢钠(少量)与氢氧化钙的反应NaHCO3+ Ca(OH)2==== CaCO3↓+NaOH+ H2O碳酸氢钠(过量)与氢氧化钙的反应2NaHCO3+ Ca(OH)2==== CaCO3↓+Na2CO3+2H2O10.碳酸氢钠加热的反应2NaHCO3==== Na2CO3+ H2O+CO2↑11.碳酸氢钙加热的反应Ca(HCO3)2==== CaCO3↓+H2O+CO2↑12.碳酸钙加热的反应CaCO3==== CaO+CO2↑13.二氧化碳(过量)通入氢氧化钙溶液中的反应Ca(OH)2+2CO2==== Ca(HCO3)2二氧化碳(少量)通入氢氧化钙溶液中的反应Ca(OH)2+CO2==== CaCO3↓+H2O14.氮气与氧气的反应N2+O2==== 2NO15.一氧化氮与氧气的反应2NO+O2==== 2NO216.二氧化氮与水的反应3NO2+ H2O==== 2HNO3+ NO17.氮气与氢气的反应N2+3H2========= 2NH318.氨气与水的反应NH3+H2O==== NH3?H2O19.氨气与盐酸的反应NH3+HCl==== NH4Cl20.氨气与硫酸的反应2NH3+H2SO4==== (NH4)2SO421.氨气与强酸的离子的反应NH3+H+==== NH4+22.氨的催化氧化的反应4NH3+5O2====== 4NO+6H2O23.碳酸氢铵加热的反应NH4HCO3==== NH3↑+CO2↑+H2O24.氯化铵加热的反应NH4Cl==== NH3↑+HCl↑25.碳酸铵加热的反应(NH4)2CO3==== 2NH3↑+CO2↑+H2O26.氯化铵与氢氧化钙的反应2NH4Cl+ Ca(OH)2==== CaCl2+2NH3↑+2H2O27.氯化铵与氢氧化钠的反应NH4Cl+ NaOH==== NaCl+NH3↑+H2O28.碳酸氢铵与氢氧化钠的反应NH4HCO3+2NaOH==== Na2CO3+NH3↑+2H2O29.碳酸氢铵与氢氧化钙的反应NH4HCO3+Ca(OH)2==== CaCO3↓+NH3↑+2H2O30.硝酸的分解的反应4HNO3========= 4NO2↑+O2↑+2H2O31.铜与浓硝酸的反应Cu+4HNO3(浓)==== Cu(NO3)2+2NO2↑+2H2O32.铜与稀硝酸的反应3Cu+8HNO3(稀)==== 3Cu(NO3)2+2NO↑+4H2O33.铁与浓硝酸的反应Fe+6HNO3(浓)==== Fe(NO3)3+3NO2↑+3H2O34.铁与稀硝酸的反应Fe+4HNO3(稀)==== Fe(NO3)3+NO↑+2H2O35.碳与浓硝酸的反应C+4HNO3(浓)==== CO2↑+4NO2↑+2H2O36.一氧化氮与一氧化碳的反应2NO+2CO====== N2+2CO237.一氧化氮与氧气和水的反应4NO+3O2+2H2O==== 4HNO338.二氧化氮与氧气和水的反应4NO2+O2+2H2O==== 4HNO339.氢氧化钠吸收二氧化氮和一氧化氮的反应2NaOH+NO2+NO==== 2NaNO2+ H2O40.氨气(过量)与氯气的反应8NH3+3Cl2==== 6NH4Cl+N2氨气(少量)与氯气的反应2NH3+3Cl2==== 6HCl+N241.二氧化氮生成四氧化二氮的反应2NO2==== N2O442.硫与铜的反应S+2Cu==== Cu2S43.硫与铁的反应S+Fe==== FeS44.硫与钠的反应S+2Na==== Na2S45.硫与铝的反应3S+2Al==== Al2S346.硫与汞的反应S+Hg==== HgS47.硫与氧气的反应S+O2==== SO248.硫与氢气的反应S+H2==== H2S49.硫与氢氧化钠的反应3S+6NaOH==== 2Na2S+Na2SO3+3H2O50.硫与浓硫酸的反应 S+2H2SO4(浓)==== 3SO2+2H2O51.黑火药点燃S+2KNO3+3C==== K2S+3CO2↑+N2↑52.二氧化硫(少量)与氢氧化钠的反应SO2+2NaOH==== Na2SO3+H2O二氧化硫(过量)与氢氧化钠的反应SO2+NaOH==== NaHSO353.二氧化硫与氢氧化钙的反应SO2+Ca(OH)2==== CaSO3↓+H2O54.二氧化硫与亚硫酸钙溶液的反应SO2+CaSO3+H2O ==== Ca(HSO3)255.二氧化硫与水的反应SO2+H2O==== H2SO356.二氧化硫与硫化氢的反应SO2+2H2S==== 3S↓+2H2O57.二氧化硫与氧气的反应2SO2+O2====== 2SO358.二氧化硫与过氧化钠的反应SO2+Na2O2==== Na2SO459.二氧化硫与氯水的反应SO2+ Cl2+2H2O==== H2SO4+2HCl60.三氧化硫与水的反应SO3+H2O==== H2SO461.亚硫酸与氧气的反应2H2SO3+O2==== 2H2SO462.亚硫酸钠与氧气的反应2Na2SO3+O2==== 2Na2SO463.浓硫酸与铜的反应 2H2SO4(浓)+Cu==== CuSO4+SO2↑+2H2O64.浓硫酸与碳的反应 2H2SO4(浓)+C==== CO2↑+2SO2↑+2H2O寿65.工业制备硫酸(初步) 4FeS2+11O2==== 8SO2+2Fe2O366.实验室制备硫酸(初步) Na2SO3+H2SO4(浓)==== Na2SO4+SO2↑+H2O67.硫化氢(少量)与氢氧化钠的反应H2S+2NaOH==== Na2S+2H2O硫化氢(过量)与氢氧化钠的反应H2S+NaOH==== NaHS+H2O68.硫化氢(少量)与氨气的反应H2S+2NH3==== (NH4)2S硫化氢(过量)与氨气的反应H2S+NH3==== NH4HS69.硫化氢与氧气(不足)的反应2H2S+O2==== 2S↓+2H2O 2H2S+O2==== 2S+2H2O硫化氢与氧气(充足)的反应2H2S+3O2==== 2SO2+2H2O70.硫化氢与氯气的反应H2S+Cl2==== 2HCl+S↓71.硫化氢与浓硫酸的反应 H2S+H2SO4(浓)==== S↓+SO2↑+2H2O72.硫化氢的制备FeS+H2SO4==== FeSO4+H2S↑73.电解饱和食盐水(氯碱工业) 2NaCl+2H2O==== 2NaOH+H2↑+Cl2↑74.电解熔融状态氯化钠(制单质钠) 2NaCl==== 2Na+Cl2↑75.海水制镁(1) CaCO3==== CaO+CO2(2) CaO+H2O==== Ca(OH)2(3) Mg2++2OH2-==== Mg(OH)2↓(4) Mg(OH)2+2HCl==== MgCl2+2H2O(5) MgCl2==== Mg+Cl2↑76.镁在空气中燃烧(与氧气的反应) 2Mg+O2==== 2MgO(与氮气的反应) 3Mg+N2==== Mg3N2(与二氧化碳的反应) 2Mg+CO2==== 2MgO+C77.镁与氯气的反应Mg+Cl2==== MgCl278.镁与水的反应Mg+2H2O==== Mg(OH)2+H2↑79.镁与盐酸的反应Mg+2HCl==== MgCl2+H2↑80.镁与氢离子的反应Mg+2H+==== Mg2++H2↑81.二氮化三镁与水的反应Mg3N2+6H2O==== 3Mg(OH)2↓+2NH3↑82.镁与溴水的反应(颜色退去) Mg+Br2==== MgBr2(产生气泡) Mg+2HBr==== MgBr2+H2↑83.溴与水的反应Br2+H2O==== HBr+HBrO84.溴与氢氧化钠的反应Br2+2NaOH==== NaBr+NaBrO+H2O85.溴与氢气的反应Br2+H2==== 2HBr86.溴与铁的反应3Br2+2Fe==== 2FeBr387.碘与铁的反应I2+Fe==== FeI288.溴与碘化钾的反应Br2+2KI==== 2KBr+I289.氯气与溴化钾的反应2KBr+Cl2==== 2KCl+Br2第四章90.硅与氧气的反应Si+O2==== SiO291.硅与氯气的反应Si+2Cl2==== SiCl492.硅与氢气的反应Si+2H2===== SiH493.二氧化硅与氟的反应Si+2F2==== SiF494.硅与碳的反应Si+C==== SiC95.硅与氢氧化钠溶液的反应Si+2NaOH+H2O==== Na2SiO3+2H2↑96.硅与氢氟酸的反应Si+4HF==== SiF4+2H2↑97.单质硅的制备(1.制备)SiO2+2C==== Si+2CO(2.提纯)Si+2Cl2==== SiCl4(3.提纯)SiCl4+2H2==== Si+4HCl98.二氧化硅与氢氧化钠的反应SiO2+2NaOH==== Na2SiO3+H2O99.二氧化硅与氧化钠的反应SiO2+Na2O==== Na2SiO3100.二氧化硅与碳酸钠的反应SiO2+Na2CO3==== Na2SiO3+ CO2↑101.二氧化硅与氧化钙的反应SiO2+CaO==== CaSiO3102.二氧化硅与碳酸钙的反应SiO2+CaCO3==== CaSiO3+CO2↑103.二氧化硅与氢氟酸的反应SiO2+4HF==== SiF4+2H2O104.硅酸的制备Na2SiO3+ CO2+H2O==== H2SiO3↓+ Na2CO3 105.硅酸加热分解H2SiO3==== SiO2+H2O106.铝与氧气的反应4Al+3O2==== 2Al2O3107.铝与氯气的反应2Al+3Cl2==== 2AlCl3108.铝与盐酸的反应2Al+6HCl==== 2AlCl3+3H2↑109.铝与氢氧化钠的反应2Al+2NaOH+6H2O==== 2Na[Al(OH)4]+3H2↑110.铝与水的反应2Al+6H2O==== 2Al(OH)3+3H2↑111.铝与三氧化二铁的反应(铝热反应)2Al+Fe2O3==== 2Fe+Al2O3 112.铝与二氧化锰的反应(铝热反应)4Al+3MnO2==== 3Mn+2AlO3113.氧化铝与盐酸的反应Al2O3+6HCl==== 2AlCl3+3H2O114.氧化铝与氢氧化钠的反应Al2O3+2NaOH+3H2O==== 2Na[Al(OH)4] 115.电解氧化铝2Al2O3==== 4Al+3O2↑116.硫酸与与一水合氨的反应Al2(SO4)3+6NH3?H2O==== 2Al(OH)3↓+3(NH4)2SO4117.氯化铝与一水合氨的反应AlCl3+3NH3?H2O==== Al(OH)3↓+3NH4Cl 118.氯化铝与氢氧化钠(少量)的反应AlCl3+3NaOH==== Al(OH)3↓+3NaCl119.氢氧化铝与氢氧化钠的反应Al(OH)3+NaOH==== Na[Al(OH)4] 120.氯化铝与氢氧化钠(过量)的反应AlCl3+4NaOH==== Na[Al(OH)4]+3NaCl121.四羟基合氯酸钠与盐酸(少量)的反应Na[Al(OH)4]+HCl==== Al(OH)3↓+NaCl+H2O122.氢氧化铝与盐酸的反应Al(OH)3+3HCl==== AlCl3+3H2O123.四羟基合氯酸钠与盐酸(过量)的反应Na[Al(OH)4]+4HCl==== AlCl3+NaCl+4H2O124.四羟基合氯酸钠与氯化铝的反应3Na[Al(OH)4]+AlCl3==== 4Al(OH)3↓+3NaCl125.向四羟基合氯酸钠中通入过量二氧化碳Na[Al(OH)4]+CO2==== Al(OH)3↓+NaHCO3126.铜在潮湿空气中被腐蚀2Cu+O2+H2O+CO2==== Cu2(OH)2CO3127.铜与氧气的反应2Cu+O2==== 2CuO128.铜与氯气的反应Cu+Cl2==== CuCl2129.铜氧化在高温下转化4CuO==== 2Cu2O+O2↑130.硫酸铜与水的反应CuSO4+5H2O==== CuSO4?5H2O。
常见化学反应化学方程式A、化合反应A+B → AB1、红磷在空气中燃烧:4P + 5O2 2P2O52、硫粉在空气中燃烧:S + O2 SO23、铁在氧气中燃烧:3Fe + 2O2 Fe3O44、镁在空气中燃烧:2Mg + O2 2MgO5、碳在充足氧气中充分燃烧: C + O2 CO26、碳在氧气不足时燃烧:2C + O2 2CO7、一氧化碳在氧气中燃烧:2CO + O2 2CO2 8、氢气在空气中燃烧:2H2 + O2 2H2O9、氢气在氯气中燃烧:H2 + Cl2 2HCl 10、二氧化碳通过灼热碳层: C + CO2 2CO11、二氧化碳和水反应生成碳酸(二氧化碳通入紫色石蕊试液):CO2 + H2O == H2CO312、氧化钙(生石灰)与水反应生成氢氧化钙(熟石灰):CaO + H2O == Ca(OH)213、铝在空气中表面形成致密氧化铝薄膜:4Al + 3O2 2Al2O3B、分解反应AB → A+B14、红色的氧化汞加热生成汞和氧气:2HgO 2Hg + O2↑15、过氧化氢(双氧水)用二氧化锰催化生成水和氧气:2H2O2 2H2O+ O2↑ 16、高锰酸钾加热生成锰酸钾和二氧化锰和氧气:2KMnO4 K2MnO4 + MnO2 + O2↑ 17、氯酸钾用二氧化锰催化并加热生成氯化钾和氧气:2KClO3 2KCl+ 3O2↑18、水通直流电分解成氢气和氧气:2H2O 2H2↑+ O2 ↑ 19、碳酸不稳定而分解生成水和二氧化碳:H2CO3 == H2O + CO2↑ 20、高温煅烧石灰石生成氧化钙和二氧化碳(二氧化碳工业制法):CaCO3 CaO + CO2↑ C、置换反应A+BC → AC+B21、锌加稀硫酸生成硫酸锌加氢气(实验室制氢气):Zn + H2SO4 == ZnSO4 + H2↑ 22、铁加稀硫酸生成硫酸亚铁加氢气:Fe + H2SO4 == FeSO4 + H2↑ 23、镁加稀硫酸生成硫酸镁加氢气:Mg + H2SO4 == MgSO4 + H2↑ 24、铝加稀硫酸生成硫酸铝加氢气:2Al +3H2SO4 == Al2(SO4)3 +3H2↑ 25、锌加稀盐酸生成氯化锌加氢气:Zn + 2HCl == ZnCl2 + H2↑26、铁加稀盐酸生成氯化亚铁加氢气:Fe + 2HCl == FeCl2 + H2↑ 27、镁加稀盐酸生成氯化镁加氢气:Mg+ 2HCl == MgCl2 + H2↑28、铝加稀盐酸生成氯化铝加氢气:2Al + 6HCl == 2AlCl3 + 3H2↑ 29、铁和硫酸铜溶液反应生成铜和硫酸亚铁:Fe + CuSO4 == Cu + FeSO430、氢气加氧化铜加热生成铜和水:H2 + Cu O Cu + H2O31、氢气加氧化铁加热生成铁和水:3H2 + Fe2O3 2Fe +3 H2O32、木炭与氧化铜在高温下生成铜和二氧化碳:C+ 2CuO 2Cu + CO2↑33、木炭与氧化铁在高温下生成铁和二氧化碳:3C+ 2 Fe2O3 4Fe+ 3CO2↑34、铝与硫酸铜溶液反应生成铜和硫酸铝:2Al + 3CuSO4 == 3Cu+ Al2(SO4)335、铜与硝酸银溶液反应生成银和硝酸铜:Cu+ 2AgNO3 == 2Ag+Cu(NO3)2D、复分解AB+CD → AD+CB36、氢氧化钠溶液与硫酸铜溶液反应生成氢氧化铜沉淀加硫酸钠:2NaOH+CuSO4 == Cu(OH)2↓+Na2SO437、石灰石(大理石)与稀盐酸反应(CO2的实验室制法):CaCO3 + 2HCl =CaCl2 + H2O + CO2↑ 38、除铁锈:氧化铁加稀盐酸生成氯化铁加水:Fe2O3 + 6HCl == 2FeCl3 + 3H2O39、氧化铁加稀硫酸生成硫酸铁加水:Fe2O3 + 3H2SO4 == Fe2(SO4)3 + 3H2O40、稀盐酸和氢氧化钠反应生成氯化钠加水:HCl + NaOH == NaCl +H2O41、稀盐酸和氢氧化钙反应生成氯化钙加水:2HCl + Ca(OH)2 == CaCl2 + 2H2O42、稀盐酸和氢氧化镁反应生成氯化镁加水:2HCl + Mg(OH)2 == MgCl2 + 2H2O43、稀盐酸和氢氧化铝反应生成氯化铝加水:3HCl + Al(OH)3 == AlCl3 + 3H2O44、稀硫酸和氢氧化钠反应生成硫酸钠加水:H2SO4 + 2NaOH == Na2SO4 + 2H2O45、碳酸钠与稀盐酸反应生成氯化钠加水加二氧化碳:Na2CO3 + 2HCl == 2NaCl + H2O + CO2↑ 46、碳酸氢钠与稀盐酸反应生成氯化钠加水加二氧化碳:NaHCO3 +HCl == NaCl + H2O + CO2↑47、氢氧化钙与碳酸钠反应生成碳酸钙沉淀和氢氧化钠:Ca(OH)2 + Na2CO3 == CaCO3↓+ 2NaOH。
九年级所有化学方程式总汇全一、化学反应类型1. 置换反应金属置换反应:例如,铁与硫酸铜反应硫酸亚铁和铜。
Fe + CuSO₄ → FeSO₄ + Cu非金属置换反应:例如,氯气与溴化钠反应氯化钠和溴。
Cl₂ + 2NaBr → 2NaCl + Br₂2. 复分解反应中和反应:例如,氢氧化钠与盐酸反应氯化钠和水。
NaOH + HCl → NaCl + H₂O盐与盐的反应:例如,硫酸钠与氯化钡反应硫酸钡和氯化钠。
Na₂SO₄ + BaCl₂ → BaSO₄↓ + 2NaCl3. 分解反应热分解:例如,碳酸钙在高温下分解氧化钙和二氧化碳。
CaCO₃ → CaO + CO₂↑光解:例如,氯酸钾在光照下分解氯化钾和氧气。
2KClO₃ → 2KCl + 3O₂↑4. 合成反应燃烧反应:例如,碳与氧气反应二氧化碳。
C + O₂ → CO₂氢化反应:例如,氮气与氢气反应氨气。
N₂ + 3H₂ → 2NH₃二、化学方程式实例1. 氢气与氧气反应水2H₂ + O₂ → 2H₂O2. 铁与硫酸铜反应硫酸亚铁和铜Fe + CuSO₄ → FeSO₄ + Cu3. 氢氧化钠与盐酸反应氯化钠和水NaOH + HCl → NaCl + H₂O4. 碳酸钙在高温下分解氧化钙和二氧化碳 CaCO₃ → CaO + CO₂↑5. 氯酸钾在光照下分解氯化钾和氧气2KClO₃ → 2KCl + 3O₂↑6. 氮气与氢气反应氨气N₂ + 3H₂ → 2NH₃7. 碳与氧气反应二氧化碳C + O₂ → CO₂8. 氯气与溴化钠反应氯化钠和溴Cl₂ + 2NaBr → 2NaCl + Br₂9. 硫酸钠与氯化钡反应硫酸钡和氯化钠 Na₂SO₄ + BaCl₂ → BaSO₄↓ + 2NaCl 10. 氢气与氯气反应氯化氢H₂ + Cl₂ → 2HCl九年级所有化学方程式总汇全三、氧化还原反应1. 氧化反应例如,铁在氧气中燃烧四氧化三铁。
3Fe + 2O₂ → Fe₃O₄2. 还原反应例如,氧化铜在氢气中还原铜和水。
常用化学反应方程式
化学1常用化学反应方程式
一、钠及其化合物
1、钠在空气中燃烧(黄色的火焰)2Na + O2 Na2O2
2、钠与水反应(浮、熔、游、响、红)2Na + 2H2O = 2NaOH + H2 ↑
2Na + 2H2O = 2Na+ + 2OH - + H2 ↑
3、过氧化钠与水的反应(放热反应、Na2O2是强氧化剂,用于漂白)
2Na2O2 + 2H2O = 4NaOH + O2 ↑
2Na2O2 + 2H2O = 4Na+ + 4OH - +O2 ↑
4、过氧化钠可用在呼吸面具和潜水艇中作为氧气来源,原因是:2Na2O2 + 2CO2 = 2Na2CO3 + O2
5、苏打(纯碱)与盐酸反应
①盐酸中滴加纯碱溶液Na2CO3 + 2HCl = 2NaCl + H2O + CO2↑
CO32- + 2H+ = H2O + CO2↑
②纯碱溶液中滴加少量盐酸Na2CO3 + HCl = NaHCO3 + NaCl
CO32- + H+ = HCO3-
6、小苏打受热分解2NaHCO3 Na2CO3 + H2O +CO2 ↑
7、固体氢氧化钠和碳酸氢钠混合物在密闭容器中加热NaHCO3 + NaOH Na2CO3 + H2O HCO3-+ OH - = H2O + CO32-(若是溶液中反应有离子方程式)
二、氯及其化合物
8、金属钠在氯气中燃烧(白烟)2 Na + Cl2 2NaCl
9、铜丝在氯气中剧烈燃烧(燃烧,棕黄色烟,蓝绿色溶液)Cu + Cl2 CuCl2
10、铁在氯气中剧烈燃烧(燃烧,棕色烟,棕黄色溶液)2Fe + 3Cl2 3FeCl3
11、氢气在氯气中燃烧(苍白色火焰,颇愫泌有白雾产生,有刺激性气味气体生成)H2 + Cl2 2HCl
12、氯气溶于水(新制氯水中含H+ 、Cl - 、ClO - 、OH-、Cl2、HClO、H2O)
Cl2 + H2O = HCl + HClO
Cl2 + H2O = H+ + Cl - + HClO
13、次氯酸见光分解(强氧化剂、杀菌消毒,漂白剂)2HClO 2HCl + O2↑
14、工业制漂白粉的原理
2Ca(OH)2 + 2Cl2 ===Ca(ClO)2 + CaCl2 + 2H2O
2Ca(OH)2 + 2Cl2 ===2Ca2++2ClO- + 2Cl -+ 2H2O
漂白粉的失效Ca(ClO)2 + CO2 + H2O =CaCO3↓+ 2HClO 2HClO 2HCl + O2↑
Ca2++2ClO- + CO2 + H2O =CaCO3↓+ 2HClO
15、氯气与NaOH的反应Cl2+2NaOH==NaCl+NaClO+H2O
Cl2+2OH-=Cl-+H2O+ ClO-
16、氯气的实验室制法:(仪器:分液漏斗,圆底烧瓶)
MnO2 + 4HCl(浓) MnCl2 +Cl2↑+ 2H2O
MnO2 + 4H+ +2Cl- Mn2+ + Cl2↑+ 2H2O
17、新制氯水注入盛溴化钠溶液的试管中Cl2 + 2NaBr = Br2 + 2NaCl
Cl2 + 2Br- = Br2 + 2Cl-
三、硫及其化合物
18、二氧化硫制三氧化硫(无色固体,熔点16.8℃)2SO2 + O2 2SO3
19、铜与浓硫酸反应:Cu + 2H2SO4 (浓)CuSO4 + 2H2O+SO2 ↑
20、碳与浓硫酸反应: C + 2H2SO4(浓)2H2O+CO2↑+2SO2↑
21、工业制单质硅(碳在高温下还原二氧化硅)SiO2 + 2C Si + 2CO↑
22、二氧化硅与氢氧化钠反应SiO2 + 2NaOH = Na2SiO3 + H2O
SiO2 + 2OH - = SiO32- + H2O
四、氮及其化合物
23、氮气和氢气反应(工业合成氨)N2 + 3H2 2NH3
24、氮气和氧气放电下反应N2 + O2 2NO
2NO + O2 2NO2
25、二氧化氮溶于水3NO2 + H2O 2HNO3 + NO
3NO2 + H2O 2H+ + 2NO3- + NO
26、NO2 、O2 的混合气通入水中无剩余气体4NO2 + O2 + 2H2O = 4 HNO3
27、NO 、O2 的混合气通入水中无剩余气体4NO + 3O2 + 2H2O = 4 HNO3
28、Cu与稀硝酸反应3Cu+8HNO3======3Cu(NO3)2+2NO↑+4H2O
29、Cu与浓硝酸反应Cu+4HNO3(浓)=Cu(NO3)2+2NO↑+2H2O硫酸、硝酸都是浓的溶液氧化性比稀的溶液强
30、C与浓硝酸反应C+4HNO3(浓)4NO2↑+CO2↑+2H2O
31. 氨的催化氧化4NH3 +5O2 4NO + 6H2O
32. 碳酸氢铵受热分解NH4HCO3 NH3 ↑+ H2O↑+ CO2 ↑
33. 用浓盐酸检验氨气(白烟生成)HCl + NH3 = NH4Cl
34. 硫酸铵溶液与氢氧化钠溶液混合加热
(NH4)2SO4 + 2NaOH 2NH3↑+ Na2SO4 + 2H2O
NH4+ + OH - NH3 ↑+ H2O
35. 硝酸铵溶液与氢氧化钠溶液混合(不加热)
NH4NO3 + NaOH = NH3.H2O + NaNO3
NH4+ + OH- = NH3.H2O
五、铝及其化合物
36. 铝箔在氧气中剧烈燃烧4Al + 3O2 2Al2O3
37. 铝片与稀盐酸反应2Al + 6HCl = 2AlCl3 + 3H2↑
2Al + 6H+ = 2Al3+ +3H2↑
38. 铝与氢氧化钠溶液反应2Al + 2NaOH + 2H2O = 2NaAlO2 + 3H2↑
2Al + 2OH - + 2H2O = 2AlO2- + 3H2↑
39. 镁在二氧化碳中燃烧2Mg + CO2 2MgO + C
40、氧化铝溶于稀盐酸Al2O3 + 6HCl = 2AlCl3 + 3 H2O
Al2O3 + 6H+ = 2Al3+ +3 H2O
41. 氧化铝溶于氢氧化钠溶液Al2O3 + 2NaOH 2NaAlO2 +H2O
Al2O3 + 2OH - === 2AlO2- + H2O
42. 硫酸铝溶液中滴过量氨水Al2(SO4)3 +6NH3.H2O = 2Al(OH)3↓+ 3(NH4)2SO4
Al3+ + 3 NH3.H2O = Al(OH)3↓+ 3NH4+
43. ①氢氧化铝溶液中加盐酸Al(OH)3 + 3HCl = AlCl3 + 3H2O
Al(OH)3 + 3H+ = Al3+ + 3H2O
②Al(OH)3与NaOH溶液反应:Al(OH)3 + NaOH NaAlO2 +2 H2O
Al(OH)3 + OH- ===== AlO2- +2 H2O
铁及其化合物
44.高温下铁与水反应3Fe + 4H2O(g) Fe3O4 + 4H2
45. 铁与盐酸反应Fe + 2HCl = FeCl2 + H2↑
Fe + 2H+ = Fe2+ + H2↑
46. 氧化铁溶于盐酸中Fe2O3 + 6HCl = 2FeCl3 + 3H2O
Fe2O3 + 6H+ = 2Fe3+ + 3H2O
47. 氯化铁中滴入氢氧化钠溶液(红褐色沉淀)FeCl3 + 3NaOH = Fe(OH)3 ↓+ 3NaCl
Fe3+ + 3OH - = Fe(OH)3 ↓
48. 氢氧化亚铁在空气中被氧化(白色沉淀变为红褐色沉淀)4Fe (OH)2 + O2 + 2H2O = 4Fe (OH)3
49. 氯化亚铁溶液中通入氯气2FeCl2 + Cl2 = 2FeCl3
2 Fe2+ + Cl2 = 2 Fe3+ + 2Cl-
50. 氯化铁溶液中加入铁粉2FeCl3 + Fe = 3FeCl2
2Fe3+ + Fe = 3Fe2+。