NSCLC诊断及治疗进展
- 格式:ppt
- 大小:1.83 MB
- 文档页数:54


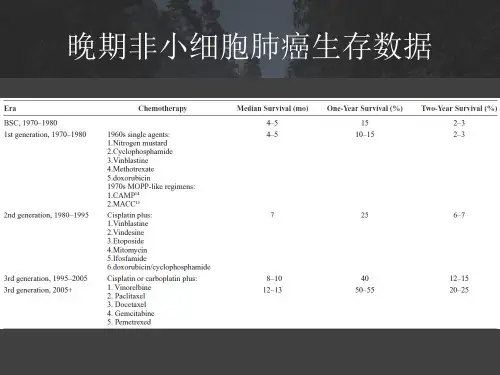
非小细胞肺癌诊疗现状与展望肺癌是世界范围内最常见的致死性恶性肿瘤之一,据统计每年全球新发肺癌病例约为180万,其中非小细胞肺癌(NSCLC)占80%至85%。
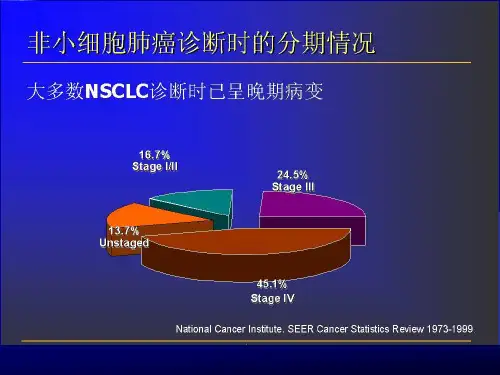
NSCLC不仅有较高的发病率和死亡率,而且此病患者大多已处于较晚期就诊,加之临床症状与体征不显著,因此极具挑战性。
本文旨在探讨NSCLC的诊断与治疗现状,以及未来的发展方向。
一、 NSCLC的分类与分期NSCLC包括腺癌、鳞癌和大细胞癌等亚型,其中腺癌是最常见的类型。
分期是NSCLC的关键因素之一,可以指导患者接受合理的治疗方案。
临床上常用的分期方法包括TNM分期和分子分期。
TNM分期主要依据肺癌的肿物大小(T)、淋巴结转移情况(N)和是否有血管内转移(M)等三个参数来分期,而分子分期则基于分子标志物对肿瘤进行分类和分期。
二、 NSCLC的临床症状与诊断NSCLC的临床症状常不明显,仅有乏力、咳嗽、胸闷等轻微体征,并且多出现在晚期。
因此,只有通过严谨的诊断程序才能确诊。
诊断过程通常包括肺部影像学和组织学检查,如X线、CT、MRI、PET-CT等检查。
此外,该疾病的确诊还需通过活检和组织学检查,以明确肺癌类型和分期。
三、 NSCLC的治疗现状NSCLC的治疗方案既包括手术、放疗、化疗等传统的治疗手段,也包括分子靶向治疗、免疫治疗等新型治疗手段。
对于不同层次的患者,治疗方案也存在相应的变化。
对于早期的NSCLC患者,手术是最主要也是最有效的治疗手段;对于中晚期患者,传统的化疗和放疗等手段常被用于综合治疗和缓解症状;而对于EGFR突变、ALK、ROS1重排等NSCLC患者,分子靶向治疗能够非常明显地提高生存率和治疗效果;最新的免疫治疗也已成为NSCLC治疗的新指南,该治疗方式通过抑制恶性肿瘤细胞的免疫逃逸,增强机体免疫应答,达到治疗效果。
四、 NSCLC治疗展望尽管现有的治疗手段已经取得了很大的进展和成就,但仍然有很多未解决的问题。
其中,如何精准分期和诊断、如何选择最佳治疗方案、如何提高治疗精准度和效果等问题是最紧迫的。

驱动基因阴性晚期NSCLC一线免疫治疗肺癌作为发病率第一的肿瘤,严重威胁人们的健康。
近年来,肺癌的诊疗从化疗到靶向治疗再到免疫治疗,引领肿瘤的精准治疗模式。
对于驱动基因阴性晚期非小细胞肺癌( non-small-cell lung cancer,NSCLC) 患者,多种程序性死亡受体 1( programmed death 1,PD-1) 和程序性死亡配体 1( programmed death-ligand 1,PD-L1) 抑制剂取得显著疗效,在晚期 NSCLC 一线、二线治疗中获得适应证,并丰富了从单药治疗到联合治疗的格局,使得“chemo- free”有望成为可能。
免疫治疗为肺癌治疗模式带来改变的同时,也对肺癌治疗方案、生物标志物的选择和相关不良反应的治疗带来一定的挑战。
2011 年 Nature 发表的《Cancer immunotherapy comes of age》点燃了免疫治疗的燎原之火,众多研究陆续推出,主要集中于程序性死亡受体1( programmed death 1,PD-1) 、程序性死亡配体1( programmed death-ligand 1,PD-L1) 和细胞毒性 T 淋巴细胞相关抗原-4( cytotoxic T lympho- cyte-associated antigen 4,CTLA-4) 抑制剂。
自 2013年美国《科学》杂志将癌症免疫治疗评为“重大突破”以来,PD-1 /PD-L1 抑制剂作为免疫治疗中的主力军,在癌症治疗领域备受瞩目。
2014 年美国食品药品监督管理局( Federal Food and Drug Adminstra- tion,FDA) 首先批准pembrolizumab 和nivolumab 用于晚期黑色素瘤治疗,其适应证不扩大。
其中,对非小细胞肺癌( non-small-cell lung cancer,NSCLC) 治疗的不断探索:从二线到一线,从晚期到局部晚期再到早期,从单药到联合,从泛人群到精准治疗,使得免疫治疗遍地开花。


非小细胞肺癌2017版NCCN治疗指南中文版非小细胞肺癌(NSCLC)是肺癌中最常见的类型,约占肺癌总数的80%至 85%。
对于 NSCLC 的治疗,科学合理的方案至关重要。
2017版 NCCN 治疗指南为临床医生提供了重要的参考和指导。
首先,我们来了解一下 NSCLC 的基本情况。
NSCLC 包括腺癌、鳞状细胞癌和大细胞癌等多种亚型。
其发病与吸烟、环境因素、遗传因素等密切相关。
患者在早期可能没有明显症状,随着病情进展,可能会出现咳嗽、咯血、胸痛、呼吸困难等表现。
在诊断方面,影像学检查如胸部 X 线、CT 扫描等是常用的方法。
对于疑似病例,往往需要进行病理活检来明确诊断和确定肿瘤的亚型。
此外,还会进行一系列的评估,包括肿瘤的大小、位置、是否有转移等,以制定个性化的治疗方案。
2017 版 NCCN 治疗指南对于早期 NSCLC 的治疗有明确的建议。
对于可手术的早期 NSCLC(IA、IB、IIA 和 IIB 期),手术切除是主要的治疗手段。
手术方式包括肺叶切除术、全肺切除术等,并可能会进行淋巴结清扫。
术后,根据肿瘤的病理特征和患者的具体情况,可能会考虑辅助化疗或放疗,以降低复发风险。
对于局部晚期 NSCLC(IIIA 和 IIIB 期),治疗方案则相对复杂。
对于一些可切除的病例,手术联合术前新辅助治疗或术后辅助治疗是常见的策略。
新辅助治疗通常包括化疗、放疗或同步放化疗,目的是缩小肿瘤体积,提高手术切除的成功率。
对于不可切除的局部晚期NSCLC,同步放化疗是主要的治疗方法。
晚期 NSCLC(IV 期)的治疗则侧重于全身性治疗。
化疗是常用的治疗手段之一,但随着医学的发展,靶向治疗和免疫治疗也在 NSCLC的治疗中发挥着越来越重要的作用。
靶向治疗是针对肿瘤细胞特定的分子靶点进行治疗。
例如,对于存在 EGFR 基因突变的患者,EGFR 酪氨酸激酶抑制剂(如吉非替尼、厄洛替尼等)可能会取得较好的疗效。
对于ALK 融合基因阳性的患者,ALK 抑制剂(如克唑替尼等)则是有效的治疗选择。


驱动基因阴性晚期NSCLC 一线免疫治疗肺癌作为发病率第一的肿瘤,严重威胁人们的健康。
近年来,肺癌的诊疗从化疗到靶向治疗再到免疫治疗,引领肿瘤的精准治疗模式。
对于驱动基因阴性晚期非小细胞肺癌 ( non-small-cell lung cancer,NSCLC) 患者,多种程序性死亡受体 1( programmed death 1,PD-1) 和程序性死亡配体 1( programmed death-ligand 1,PD-L1) 抑制剂取得显著疗效,在晚期NSCLC 一线、二线治疗中获得适应证,并丰富了从单药治疗到联合治疗的格局,使得“chemo- free”有望成为可能。
免疫治疗为肺癌治疗模式带来改变的同时,也对肺癌治疗方案、生物标志物的选择和相关不良反应的治疗带来一定的挑战。
20n 年 Nature 发表的《Cancer immunotherapy comes of age》点燃了免疫治疗的燎原之火,众多研究陆续推出,主要集中于程序性死亡受体1( programmed death 1,PD-1) 、程序性死亡配体1( programmed death-ligand 1 PD-L1)和细胞毒性 T 淋巴细胞相关抗原-4( cytotoxic T lympho- cyte-associated antigen 4,CTLA-4) 抑制剂。
自 2013年美国《科学》杂志将癌症免疫治疗评为“重大突破”以来,PD-1/PD-L1抑制剂作为免疫治疗中的主力军,在癌症治疗领域备受瞩目。
2014 年美国食品药品监督管理局( Federal Food and Drug Adminstra- tion,FDA) 首先批准pembrolizumab 和nivolumab用于晚期黑色素瘤治疗,其适应证不扩大。
其中,对非小细胞肺癌(non-small-cell lung cancer NSCLC)治疗的不断探索:从二线到一线,从晚期到局部晚期再到早期,从单药到联合,从泛人群到精准治疗,使得免疫治疗遍地开花。


非小细胞肺癌EGFR基因靶向治疗研究进展一、本文概述非小细胞肺癌(NSCLC)是全球范围内发病率和死亡率均较高的恶性肿瘤之一。
表皮生长因子受体(EGFR)是非小细胞肺癌中常见的异常表达基因之一,因此,针对EGFR的靶向治疗已成为非小细胞肺癌治疗的重要手段。
本文旨在全面综述非小细胞肺癌EGFR基因靶向治疗的研究进展,包括EGFR基因突变与表达的研究、EGFR抑制剂的研发与临床应用、EGFR靶向治疗的耐药机制以及联合治疗策略等方面的最新成果和进展。
通过本文的阐述,期望能够为非小细胞肺癌EGFR基因靶向治疗的深入研究与实践提供有益的参考和启示。
二、EGFR基因及其与NSCLC的关系EGFR,即表皮生长因子受体,是一种关键的跨膜蛋白酪氨酸激酶受体,主要参与细胞生长、增殖、分化和凋亡等过程。
在人体中,EGFR 基因位于第七号染色体上,其编码的EGFR蛋白广泛存在于上皮组织,尤其在肺、脑和乳腺等组织中表达最为丰富。
近年来,大量的研究表明,EGFR与NSCLC的发生和发展密切相关。
NSCLC细胞常常存在EGFR基因的突变或过度表达,这些变化导致EGFR蛋白的持续激活,从而引发细胞的无序增殖和肿瘤的形成。
EGFR突变最常见的是酪氨酸激酶域的突变,这些突变能够增加EGFR 的活性,使细胞对EGFR配体的反应增强,导致细胞增殖失控。
EGFR作为NSCLC的重要治疗靶点,其靶向药物的开发和应用已经成为NSCLC治疗领域的研究热点。
目前,针对EGFR的靶向药物主要包括酪氨酸激酶抑制剂(TKIs)和单克隆抗体两大类。
这些药物通过抑制EGFR的活性或阻断其与配体的结合,从而抑制肿瘤细胞的增殖和转移,提高NSCLC患者的生存质量和生存期。
然而,尽管EGFR靶向治疗在NSCLC治疗中取得了显著的成效,但仍存在一些问题。
如部分患者对EGFR靶向药物不敏感,部分患者在初始敏感后会出现耐药性等。
这些问题的存在提示我们,对EGFR 及其与NSCLC关系的深入研究,以及新的靶向药物的研发,仍然是NSCLC治疗领域的重要任务。
非小细胞肺癌NCCN指南2024版解读
非小细胞肺癌(NSCLC)是一种常见的恶性肿瘤,近年来发病率和死
亡率均有明显升高,因此研究不同诊断、治疗的规范化管理指南就显得尤
为重要。
2024年,由美国全国癌症网(NCCN)发布的NSCLC诊疗指南已
经进入其第六版,此版规定了明确的治疗步骤。
下面简要介绍此版诊疗指南。
一、诊断
1、临床表现:NSCLC的主要症状为咳嗽、血痰、气促、体重减轻以
及痰中带有血液。
此外,也可能伴有胸膜及淋巴结游离性的包块,以及呼
吸困难、极重的咳嗽等其他非特异性症状。
2、检查鉴别诊断:通过胸部X线、血常规检查、肺动脉造影、肺切
片以及肿瘤标志物等物理检查,来确诊NSCLC,其中肺部CT扫描是确诊NSCLC的主要方法。
3、病理诊断:如果肺部CT扫描可以诊断出NSCLC,那么将通过痰液
的细胞学检查,肺部CT检查可能提示局部的肿瘤,有可能进行肺部减毒
术或者是内镜抽穿分活检,来病理诊断NSCLC。
二、治疗
1、手术治疗:通常而言,NSCLC的治疗的重点是手术治疗,但是特
别是小肺坏疽的肿瘤,或者是中晚期肿瘤手术前治疗进展较为明显的病例,术前诊断的检查便成为特别重要的步骤。