工业盐酸的浓度检测
- 格式:docx
- 大小:23.89 KB
- 文档页数:2

稀盐酸浓盐酸的浓度范围稀盐酸和浓盐酸是化学实验室中常用的化学试剂,它们在许多化学实验和工业生产中都起着重要的作用。
本文将介绍稀盐酸和浓盐酸的浓度范围及其在实验和工业中的应用。
一、稀盐酸的浓度范围稀盐酸是指盐酸溶液中盐酸的浓度较低的情况。
通常情况下,我们用质量分数来表示稀盐酸的浓度。
质量分数是指溶液中溶质的质量与溶液总质量之比。
稀盐酸的浓度通常在0.1%到3%之间,其中0.1%的稀盐酸表示溶液中盐酸的质量占总质量的0.1%。
浓度为3%的稀盐酸表示溶液中盐酸的质量占总质量的3%。
稀盐酸的浓度越高,溶液中盐酸的含量越多。
二、稀盐酸的应用1.实验室中的应用稀盐酸在实验室中有广泛的应用。
它常用于酸碱中和反应、金属的腐蚀性测试、沉淀的溶解等实验中。
例如,在酸碱中和反应中,稀盐酸可以与碱反应生成盐和水。
在金属的腐蚀性测试中,将金属置于稀盐酸中,观察是否发生气体的产生以及金属的腐蚀情况。
此外,稀盐酸还可以用于沉淀的溶解实验中,将沉淀溶解后可以得到溶液。
2.工业中的应用稀盐酸在工业生产中也有许多应用。
其中一个重要的应用是作为化学品的原料。
稀盐酸可以用于生产盐酸盐和其他化学品。
此外,稀盐酸还可以用于金属的清洗和酸洗过程。
将金属置于稀盐酸中,可以去除金属表面的氧化物和其他杂质,使金属表面更加光滑和干净。
三、浓盐酸的浓度范围浓盐酸是指盐酸溶液中盐酸的浓度较高的情况。
同样,我们用质量分数来表示浓盐酸的浓度。
浓盐酸的浓度通常在35%到38%之间,其中35%的浓盐酸表示溶液中盐酸的质量占总质量的35%。
浓度为38%的浓盐酸表示溶液中盐酸的质量占总质量的38%。
浓盐酸的浓度越高,溶液中盐酸的含量越多。
四、浓盐酸的应用1.实验室中的应用浓盐酸在实验室中也有许多应用。
它常用于有机合成实验中,可以用作酸催化剂。
此外,浓盐酸还可以用于制备其他化学试剂,如盐酸酯、盐酸醛等。
2.工业中的应用浓盐酸在工业生产中有着广泛的应用。
它常用于金属表面的处理,可以去除金属表面的氧化物和其他杂质,使金属表面更加光滑和干净。

盐酸浓度检测仪安全操作及保养规程盐酸浓度检测仪是一种常用的检测和测量盐酸浓度的设备。
使用该仪器要注意安全,正确保养,这样才能更好地发挥其作用。
以下是盐酸浓度检测仪的安全操作及保养规程。
安全操作1.在操作检测仪之前,应认真阅读使用说明书,并熟悉仪器的各部分。
2.在进行检测时,应将检测仪放在平稳的底座上,并确保仪器的插头牢固。
3.进行检测时,应佩戴安全眼镜,手套,口罩等适当的个人保护装备,以免受到盐酸的溅射。
4.在设备连接和操作过程中,应注意保持干燥,避免水和其他液体进入到接口中。
5.当使用完毕后,应将仪器上电源关闭,并拔掉电源插头。
从操作位置清除盐酸残留物,并对仪器进行必要的清洁和消毒。
保养规程1.在使用检测仪之前,应检查设备是否完好无损。
如发现设备有损坏,应及时修理或更换。
2.在使用过程中,应仔细查看设备上是否有盐酸残留物,并定期清洁和消毒设备。
3.检测仪上的电池应按照使用说明书的提示进行更换。
4.仪器长期不用时,应将电源关闭和电池取出。
5.检测仪应妥善保管,放在干燥,通风的地方。
避免长时间沾染水或湿气。
6.定期检测和校准仪器,以确保设备的准确性和可靠性。
总结盐酸浓度检测仪不仅在化工,水处理等行业有广泛的应用,而且也可以在实验室等领域使用。
在使用过程中,应注重安全操作和仪器保养,避免因设备未经保养而导致的效率低下和错误测试结果。
本文介绍的安全操作和保养规程只是一些基本方法,每个用户应根据具体需要,也可以根据仪器说明书使用其他保养和安全操作方法。

盐酸检验报告
报告编号:20210001
委托方:XXX有限公司
检测单位:XXX检测中心
检测日期:2021年1月1日
样品名称:盐酸
样品来源:委托方提供的样品
检测目的:确认样品的纯度和质量是否符合标准要求检测方法:采用滴定法进行检测
检测结果:
样品盐酸的浓度为0.99mol/L,符合GB/T 6227-2017《盐酸》的要求,检测结果如下表所示:
指标名称检测结果检测方法
浓度 0.99mol/L 滴定法
结论:
样品盐酸的质量完全符合GB/T 6227-2017《盐酸》的要求,检测结果可信,委托方可放心使用。
备注:本检测报告仅对所提供样品的检测结果负责,其他有关事宜不在本检测报告范围内。
XXX检测中心
2021年1月1日。

盐酸的标定1. 介绍盐酸(化学式:HCl)是一种常见的无机酸,它在化学实验和工业生产中有广泛的应用。
为了确保盐酸的浓度准确,需要进行盐酸的标定。
盐酸的标定是通过与已知浓度的标准溶液反应,从而确定盐酸溶液的浓度。
2. 标定原理盐酸的标定原理是利用酸碱中和反应,根据反应的化学方程式和已知浓度的标准溶液的体积,计算出未知盐酸溶液的浓度。
盐酸与碱溶液(如氢氧化钠溶液)发生中和反应,生成盐和水。
反应方程式如下:HCl + NaOH → NaCl + H2O根据反应的化学方程式可以知道,1 mol的盐酸与1 mol的碱溶液完全反应,生成1 mol的盐和1 mol的水。
根据化学计量关系,可以推导出标定盐酸的公式:C1V1 = C2V2其中,C1是标准溶液的浓度,V1是标准溶液的体积,C2是盐酸溶液的浓度,V2是盐酸溶液的体积。
3. 实验步骤3.1 准备工作•配置标准溶液:根据实验要求和需要,配置一定浓度的标准溶液,如0.1 mol/L的氢氧化钠溶液。
•准备盐酸溶液:根据实验要求和需要,配制一定浓度的盐酸溶液,如未知浓度的盐酸溶液。
3.2 标定操作1.使用容量瓶准确称取一定体积的标准溶液(V1)。
2.将标准溶液倒入锥形瓶中。
3.使用滴定管取适量的盐酸溶液(V2)。
4.加入几滴酚酞指示剂,溶液变成粉红色。
5.慢慢滴加盐酸溶液,同时轻轻摇晃锥形瓶,直到溶液由粉红色变为无色。
6.记录滴定过程中盐酸溶液的体积(V2’)。
3.3 数据处理根据标定原理中的公式C1V1 = C2V2,可以计算出盐酸溶液的浓度。
C2 = (C1V1) / V2’其中,C1是标准溶液的浓度,V1是标准溶液的体积,V2’是盐酸溶液的滴定体积。
4. 实验注意事项•实验前要进行充分的准备,确保实验所需的试剂和设备齐全。
•实验过程中要注意安全,佩戴实验室必要的防护用品,如实验手套、护目镜等。
•滴定过程中要控制滴液的速度,避免滴液过快导致误差。
•滴定过程中要充分摇晃锥形瓶,使反应充分进行。

中国药典中稀盐酸浓度中国药典(Chinese Pharmacopoeia)是我国药品质量标准的法定性文件,是我国药品监管的基础依据。
它规定了各种药品的质量要求、检验方法、使用规范等内容,为保证药品的安全性、有效性和合理使用提供了科学依据。
在中国药典中,稀盐酸浓度也有相应的规定。
稀盐酸(hydrochloric acid)是一种常见的无机酸,化学式为HCl。
它是一种无色、有刺激性气味的液体,在化学实验、工业生产和医疗领域中都有广泛的应用。
稀盐酸可以与碱反应生成盐和水,是一种常见的酸碱中和反应。
在中国药典中,对于稀盐酸浓度的要求有如下规定:1. 稀盐酸浓度的检测方法:中国药典规定了稀盐酸浓度的检测方法,主要包括酸度滴定法、气相色谱法等。
这些方法可以准确地测定稀盐酸溶液中酸性物质的含量,保证了稀盐酸浓度的准确性和可靠性。
2. 稀盐酸浓度的要求:根据中国药典的规定,稀盐酸溶液的浓度应符合特定的要求。
一般来说,药品中所使用的稀盐酸浓度应在1%至10%之间。
这个范围内的稀盐酸溶液既可以满足药品生产和制备的需要,又可以保证药品的质量和安全性。
3. 稀盐酸浓度的控制:在药品生产和制备过程中,对稀盐酸浓度的控制非常重要。
合理控制稀盐酸浓度可以保证药品的质量和稳定性,同时也可以避免对人体的不良影响。
因此,在药品生产过程中,需要严格按照中国药典的规定进行稀盐酸浓度的控制和调整。
总之,中国药典对稀盐酸浓度有明确的规定,包括检测方法、要求和控制等方面。
这些规定的制定旨在保证药品质量和安全性,为药品监管提供科学依据。
只有严格按照中国药典的要求进行稀盐酸浓度的控制和调整,才能保证药品的质量和有效性,保障人民群众的用药安全。


33%的盐酸摩尔浓度盐酸是一种强酸,普遍应用于化学合成、工业加工和实验室等领域中。
在化学反应中,盐酸的摩尔浓度测量是非常重要的,因为它能够影响反应的速率、平衡和产量。
本文将讨论33%盐酸的摩尔浓度以及它的相关特性和应用。
33%盐酸的摩尔浓度是指盐酸溶液中每升溶液中盐酸分子的摩尔数。
换句话说,它是盐酸溶液中盐酸和水的比例。
在33%盐酸中,摩尔浓度约为11.7M。
这个数字很高,说明这个溶液有很强的酸性。
与其他摩尔浓度相比,33%的盐酸溶液是浓缩的。
普通的盐酸溶液通常只有10%到20%的浓度,因此,33%的盐酸溶液更加强酸性,具有更高的反应活性。
这也使得33%盐酸在化学合成和实验室反应的中应用广泛。
盐酸溶液的酸性程度可以使用pH值来表达。
pH值越低,溶液越酸性。
在33%盐酸溶液中,pH约为0.2。
这个数字非常低,反映了这个溶液的极强酸性。
在实验室和工业生产中,这种极强酸性的溶液通常用于酸化、酸溶和化学反应。
除了酸性之外,33%盐酸还有其他一些特性,包括其物理特性和化学特性。
它是一种无色、有刺激性气味的液体,可以溶解许多无机物和有机物。
33%盐酸的密度约为1.18g/cm3,在室温下为液体。
在实验室和工业生产中,33%盐酸作为强酸,被广泛用于酸性溶液的制备,例如电池电解液、清洁剂和消毒剂等。
它还常被用于化学分析和纯化分离等领域。
另一个常见的应用是在医药领域,盐酸常被用作药物盐酸盐的制备剂。
例如,氨碘必利(Amitriptyline)鸟苷(Nucleosides)等药物的盐酸盐制剂是最常用的有效物质。
盐酸还被广泛用于人工呼吸机进行清洗和消毒。
总结一下,33%的盐酸的摩尔浓度是一种强酸性的溶液,拥有很强的反应活性和极低的pH值。
由于其物理、化学和酸性特性,33%盐酸在化学合成、工业加工、实验室和医药制剂等领域中得到了广泛的应用。
同时,也需要注意到33%盐酸在使用时可能引起严重的风险和危险。
人们需要在使用时提高警惕,并且遵守安全操作规程,确保工作场所和过程的安全性。
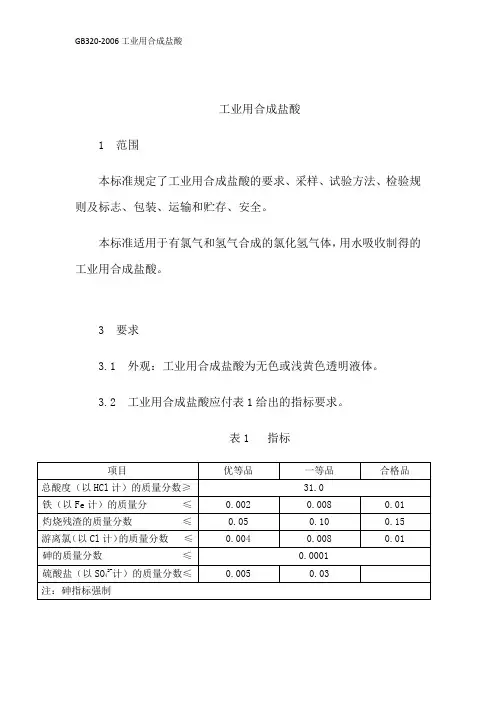
工业用合成盐酸1 范围本标准规定了工业用合成盐酸的要求、采样、试验方法、检验规则及标志、包装、运输和贮存、安全。
本标准适用于有氯气和氢气合成的氯化氢气体,用水吸收制得的工业用合成盐酸。
3 要求3.1 外观:工业用合成盐酸为无色或浅黄色透明液体。
3.2 工业用合成盐酸应付表1给出的指标要求。
表1 指标4 采样4.1 产品按批检验。
生产企业以每一成品槽或每一生产周期生产的工业用合成盐酸为一批。
用户以每次收到的同一批次的工业用合成盐酸为一批。
4.2 工业用合成盐酸从槽车或贮槽xx采样时,宜用GB/T6680xx规定的适宜的耐酸采样器自上、xx、下三处采取等量的有代表性样品。
生产企业可将槽车或贮槽内的工业用合成盐酸混匀后于采样口采取有代表性样品,进行检测。
4.3 工业用合成盐酸从塑料桶或陶瓷坛xx采样时,按GB/T6678xx规定的采样单元数随机抽样,拆开包装,宜采用GB/T6680xx规定的适宜耐酸采样器自上、xx、下三处采取等量的有代表性样品。
4.4 将采取的样品混匀,装于清洁、干燥的塑料瓶或具磨口塞的玻璃瓶中,xx。
样品量不少于500mL。
样品瓶上应贴上标签并注明:生产企业名称、产品名称、批号或生产日期、采样日期及采样人。
5 试验方法除非另有说明,在分析xx仅使用确认为分析纯试剂和GB/T6682xx规定的三级水或相当纯度的水。
试验中所需标准溶液、制剂及制品,在没有其他规定时,均按GB/T601、GB/T602、GB/T603规定制备。
5.1 外观目视观察5.2 总酸度的测定滴定法5.2.1 原理试料溶液以溴甲酚绿为指示液,用氢氧化钠标准滴定溶液滴定至溶液由黄色变为蓝色为终点。
反应式如下:H++OH-→H2O5.2.2 试剂5.2.2.1 氢氧化钠标准滴定溶液:c(NaOH)=1mol/L5.2.2.2 溴甲酚绿指示液:1g/L。
5.2.3 仪器一般的实验室仪器和以下仪器。
5.2.3.1 锥形瓶,100mL(具磨口塞)。

编辑:自由小五001目录1、 氢氧化钠标准溶液标定2、 混合碱的测定(双指示剂法)3、 0.2mol/L HCl 标准溶液标定4、 工业醋酸含量测定5、 0.1mol/L Na 2CO 3标准溶液的配制6、 混合碱的测定氢氧化钠标准溶液标定一. 实验目的1. 学习碱标准溶液浓度的标定方法。
2. 进一步练习滴定操作和减量法称量。
3. 初步掌握酸碱指示剂的选择方法。
二. 实验原理酸碱标准溶液是采用间接法配制的,其准确浓度必须依靠基准物进行标定。
标定碱溶液用的基准物很多,下面为最为常用的邻苯二甲酸氢钾方法:邻苯二甲酸氢钾,是一种二元弱酸的共轭碱,它的酸性较弱,在标定 NaOH 溶液到达等当点时反应产物是邻苯二甲酸钾钠,在水溶液中显微碱性,化学计量点pH=9.1,pH 图越范围在8.1~10.1, 因此可用酚酞为指示剂,反应如下:结果计算:M=204.2g/mol三. 仪器与试剂1.1000)(-⨯=L m ol V M mC NaOHNaOH邻苯二甲酸氢钾COOH COOK+NaOHCOOKCOONa +H 2O仪器:电光分析天平(0.1mg),滴定管(碱式,50mL)。
试剂:NaOH 标准溶液(0.2mol / L),邻苯二甲酸氢钾(基准试剂),酚酞指示剂(0.2%)。
四. 实验步骤1. 按仪器洗涤的标准方法,将所要使用的锥形瓶、碱式滴定管、移液管、量筒洗干净,并检查碱式滴定管是否漏水,移液管是否完整。
2. 用减量法准确称取邻苯二甲酸氢钾1g(准确至小数点后4位),置于250 ML洗净的锥形瓶中。
3. 加入50 ML 蒸馏水溶解,必要时可用小火温热溶解。
冷却后,加酚酞指示剂1~2 滴。
4. 用氢氧化钠溶液洗涤碱式滴定管三次,每次使用约5-8mL,洗涤时,将氢氧化钠溶液从尖嘴放出,洗涤结束后,加入氢氧化钠溶液到0刻度线上方,观察是否有气泡,若有,按正确排气泡方式,赶出气泡,调节液面到0刻度。
5. 将滴定管放在裴氏夹的右边,一边摇荡,一边滴定用氢氧化钠溶液滴定,滴定速度不易太快,最快只能成串滴出。

工业盐酸标准工业盐酸是一种常用的化工原料,广泛应用于化工、冶金、医药、石油、农药、染料等领域。
作为一种强酸,工业盐酸的质量标准显得尤为重要。
本文将对工业盐酸的标准进行详细介绍,以便相关行业的生产和使用单位参考。
一、外观与性状。
工业盐酸应为无色透明的液体,无悬浮物和杂质。
其气味刺激,呈强酸性。
在常温下,应为液态,不得凝固或结晶。
二、主要成分。
工业盐酸的主要成分为盐酸(HCl),其含量应符合国家标准或企业标准的要求。
同时,其他成分的含量也需要在规定范围内,以确保产品质量稳定。
三、理化指标。
1. 盐酸浓度,工业盐酸的浓度应符合国家标准或企业标准的规定,通常为浓盐酸(≥30%)和稀盐酸(<30%)两种类型。
2. 密度,工业盐酸的密度应在规定范围内,通常为1.15g/cm³左右。
3. PH值,工业盐酸的PH值应在强酸性范围内,通常为0-1之间。
4. 游离氯离子含量,工业盐酸中游离氯离子的含量应符合规定,以免对环境和人体造成危害。
四、杂质含量。
工业盐酸中的杂质包括铁、硫酸盐、硫化物等,其含量应在规定范围内。
特别是对于铁离子的含量,需要严格控制,以免影响产品的质量和使用效果。
五、包装与储存。
工业盐酸应采用塑料桶或槽车进行包装和运输,包装物应干燥、清洁、密封良好。
在储存过程中,应远离火源、避免阳光直射,存放在阴凉干燥处,远离易燃、易氧化物品。
六、安全注意事项。
1. 在生产和使用工业盐酸时,应佩戴防护眼镜、防护手套等个人防护用品,避免接触皮肤和眼睛。
2. 工业盐酸属于腐蚀性物质,应远离食品、饮用水等,防止误食和误触。
3. 在工业盐酸泄漏或溅洒时,应立即用大量清水冲洗,并及时向有关部门报告,以便进行应急处理和处置。
七、质量控制。
为了确保工业盐酸的质量稳定,生产企业应建立健全的质量管理体系,严格执行国家标准或企业标准的要求,加强原材料的采购检验和生产过程的控制,确保产品符合标准要求。
八、结语。
工业盐酸作为一种重要的化工原料,在各个行业都有着广泛的应用。

工业用合成盐酸检测标准1 范围本规范规定了工业用合成盐酸的要求、采样、试验方法、检验规则及标志、包装、运输和贮存、安全。
本规范适用于由氯气和氢气合成的氯化氢气体,用水吸收制得的工业用合成盐酸。
2 规范性引用文件下列文件中的条款通过本规范的引用而成为本规范的条款。
凡是注日期的引用文件,仅所注日期的版本适用于本文件。
凡是不注日期的引用文件,其最新版本(包括所有的修改单)适用于本文件。
GB 190 危险货物包装标志GB/T 191 包装储运图示标志(GB/T 191_2000,eqv ISO780:1997)GB/T 601 化学试剂规范滴定溶液的制备GB/T 602 化学试剂杂质测定用规范溶液的制备(GB/T603-2002,ISO 6353-1982,NEO)GB/T 1250 极限数值的表示方法和判定方法GB/T 6678 化工产品采样总则(GB/T 6678—1986,neq ASTM E300:1983)GB/T 6680 液体化工产品采样通则(GB/T 6680_1986,neq BS5309:1976)GB/T 6682 分析实验室用水规格和试验方法(GB/T 6682—1992,eqv ISO 3696:1987)GB 320-2006 工业用合成盐酸3 要求3.1 外观:工业用合成盐酸为无色或浅黄色透明液体。
3.2 工业用合成盐酸应符合表 1 给出的指标要求。
表1 盐酸技术指标指标项目优等品一等品总酸度(以HCl 计)的质量分数,% ≥31铁(以Fe 计)的质量分数,% ≤0.002 ≤0.008灼烧残渣的质量分数,% ≤0.05 ≤0.10游离氯(以Cl 计)的质量分数,% ≤0.004 ≤0.008砷的质量分数,% ≤0.0001硫酸盐(以SO42-计)的质量分数,% ≤0.005 ≤0.03 注:砷指标强制。
4 采样4.1 产品按批检验。
生产企业以每一成品槽或每一生产周期生产的工业用合成盐酸为一批。
纯盐酸浓度全文共四篇示例,供读者参考第一篇示例:纯盐酸是一种无机酸,化学式为HCl,是普遍应用的一种电解质强酸。
在工业上,纯盐酸主要用于金属表面处理、盐酸盐制备、染料、药物、冶金和橡胶工业等。
在实验室中,纯盐酸常用于调节溶液的酸碱度、沉淀分析和中和反应等。
而对于纯盐酸的浓度,则会直接影响到其在各种应用场合中的效果,因此了解纯盐酸浓度的重要性是至关重要的。
纯盐酸的浓度可以通过不同的方法来进行测定。
最常用的方法是以质量分数(w/w%)或体积分数(v/v%)表示。
质量分数表示的是纯盐酸中盐酸的质量与总质量之比,而体积分数则是表示纯盐酸中盐酸的体积与总体积之比。
在实际操作中,我们可以通过滴定法、密度法、电导率法、气相色谱法等方法来测定纯盐酸的浓度。
通过滴定法测定纯盐酸浓度是最常见的方法之一。
滴定法利用一种已知浓度的溶液去溶解待测物,并在滴加到一定数量后达到中和反应的终点。
这时,记录下所需的滴定量即可计算出待测物的浓度。
通常情况下,我们会用氢氧化钠(NaOH)作为滴定试剂,因为它是一种强碱,与盐酸呈酸碱中和反应。
另一种测定纯盐酸浓度的方法是通过密度法。
密度法实际上是一种间接测定方法,通过测量溶液的密度,根据溶液的密度与浓度之间的关系,可以计算出溶液的浓度。
在进行密度法测定时,需要事先确定不同浓度的盐酸溶液的密度与浓度之间的关系,以便后续的实验操作。
电导率法也是一种常用的测定纯盐酸浓度的方法。
电导率法利用溶液中的电解质导电的特性来测定其浓度。
由于盐酸是一种强电解质,当浓度增大时,溶液的电导率也会增大。
通过测量溶液的电导率,可以间接得出溶液的浓度。
电导率法适用于浓度较大的盐酸溶液的测定,但在低浓度下的准确度可能会有所下降。
除了传统的测定方法,近年来气相色谱法也逐渐被应用于纯盐酸浓度的测定。
气相色谱法通过检测气相中有机物质的挥发性来测定溶液中有机物质的浓度。
当盐酸浓度较高时,可以通过气相色谱法对溶液中盐酸的浓度进行快速准确地测定,为相关工业和实验室提供了便利。
纯盐酸浓度-概述说明以及解释1.引言1.1 概述在概述部分,我们需要介绍纯盐酸浓度的背景和基本概念。
下面是一个概述部分的简单示例:在化学领域中,纯盐酸浓度是指盐酸溶液中所含盐酸的量与溶液总体积的比例。
纯盐酸浓度是衡量盐酸溶液中溶质含量的一个重要指标,它对于化学实验、工业生产以及日常生活中的一些应用都具有重要意义。
随着科学技术的发展,人们对纯盐酸浓度的研究越来越深入。
准确地了解和控制纯盐酸浓度可以促进实验结果的准确性和可重复性,对于化学反应速率、生成物的质量和产率等方面都有着重要的影响。
此外,在某些工业生产过程中,如金属腐蚀防护、酸碱中和反应等,纯盐酸浓度的控制也显得尤为关键。
然而,纯盐酸浓度受到多种因素的影响,如溶液的温度、压力、反应时间等。
因此,准确测量和控制纯盐酸浓度具有一定的挑战性。
为了解决这一问题,科学家们开展了大量的研究,并提出了各种测量方法和技术。
本文的目的是系统地介绍纯盐酸浓度的定义、意义以及影响纯盐酸浓度的因素。
同时,我们还将探讨一些常用的测量方法,并总结纯盐酸浓度的重要性。
最后,我们将提出一些建议,以促进对纯盐酸浓度的进一步研究。
通过深入研究纯盐酸浓度,我们可以更好地理解和应用盐酸溶液在化学领域中的特性,为实验和工业生产提供更科学、高效的指导。
同时,对于探索更多纯盐酸浓度相关的领域和问题也大有裨益。
文章结构部分的内容应该对整篇文章的构成进行简要介绍,指导读者在阅读过程中能够清楚地了解文章的组织和内容安排。
以下是文章结构部分的一个可能写法:1.2 文章结构本文分为引言、正文和结论三个主要部分。
引言部分概述了纯盐酸浓度的定义和意义,解释了为什么纯盐酸浓度对于某些领域至关重要。
此外,引言部分还列出了本文的目的,即探讨影响纯盐酸浓度的因素以及测量纯盐酸浓度的方法。
正文部分主要包括三个小节。
首先,我们将在2.1节中详细阐述纯盐酸浓度的定义与意义,以帮助读者全面理解这个概念。
然后,在2.2节中,我们将探讨影响纯盐酸浓度的因素,从而揭示了为什么纯盐酸在不同条件下具有不同浓度。
工业盐酸浓度检测方法
工业盐酸浓度常用的检测方法有以下几种:
1. 中和法:将待测的盐酸溶液与已知浓度的标准碱溶液反应,根据反应前后的酸碱溶液体积变化计算待测盐酸的浓度。
2. 硬度法:利用盐酸对含钙、镁的水样中的碳酸盐进行中和反应,根据所需的酸量反推出盐酸的浓度。
3. 电导法:通过测量盐酸溶液的电导率来间接判断盐酸的浓度,浓度越高,电导率越大。
4. pH法:使用酸度计或pH计来测量盐酸溶液的酸度或pH值,根据测量值对照标准曲线或表格,确定盐酸的浓度。
5. 光度法:利用化学试剂与盐酸发生反应后产生的颜色变化,通过比色计测量溶液的吸光度来确定盐酸的浓度。
需要根据实际情况选择合适的检测方法,并注意使用过程中的安全操作。
氯化氢HCL检测仪重点技术参数氯化氢(HCl)检测仪是一种用于检测空气中HCl浓度的仪器。
根据不同的应用需求,HCl检测仪的技术参数可能会有所不同,下面是一些可能的重点技术参数(超过1200字):1. 测量范围:HCl检测仪的测量范围通常是根据应用需求而确定的。
一般来说,测量范围可以从低至几ppb(parts per billion)到高至几百ppm(parts per million)。
这样的范围可以覆盖从环境空气中微量HCl浓度到工业气体中高浓度HCl的测量。
2. 灵敏度:灵敏度是指HCl检测仪能够检测到的最低浓度。
灵敏度通常以ppb或ppm为单位。
高灵敏度的仪器可以检测到更低浓度的HCl,这对于一些环境监测和安全监测应用来说是非常关键的。
3.响应时间:响应时间是指HCl检测仪从感知到HCl存在到发出相应信号所需的时间。
响应时间短的仪器可以更快地检测到HCl的存在并及时采取相应的措施。
在一些需要实时监测的应用,如工业过程控制和紧急应急响应中,快速响应时间是非常重要的。
4. 精确度:精确度是指HCl检测仪测量结果与真实值之间的偏差。
精确度通常以百分比或ppm为单位。
高精确度的仪器能够提供更准确的测量结果,减少误判和误报的可能性。
5.分辨率:分辨率是指HCl检测仪能够分辨的最小浓度差异。
较高的分辨率意味着仪器可以检测到更小的浓度变化,提供更多的信息。
对于一些需要对HCl浓度进行细致调控的应用,如工业过程控制,高分辨率的仪器非常重要。
6.可重复性:可重复性是指HCl检测仪在相同浓度下进行多次测量时,测量结果的一致性。
较高的可重复性表示仪器的测量结果较为稳定和可靠。
7.温度和湿度范围:HCl检测仪应当能够在广泛的温度和湿度条件下正常工作。
一般来说,仪器应当能够在温度范围从-20℃至50℃,湿度范围为0-95%RH(相对湿度)时正常工作。
8.输出接口:HCl检测仪通常提供各种输出接口,以便与其他系统进行数据交互。
盐酸浓度盐酸(HCl)是一种常见的无机强酸,其化学式为HCl。
盐酸在许多领域都有广泛的应用,如化学工业、食品加工、医药等。
盐酸的浓度是指其质量或摩尔数与溶液总体积的比率,通常以质量百分比或摩尔浓度表示。
盐酸的浓度根据其应用场景和需求而有所不同。
一般来说,盐酸的浓度范围可以从低浓度的稀盐酸到高浓度的浓盐酸。
在化学工业中,盐酸的浓度通常为37%左右,这是因为该浓度的盐酸具有较好的腐蚀性和溶解性,适用于许多化学反应和清洗过程。
除了质量百分比表示外,盐酸还可以用摩尔浓度来表示。
摩尔浓度是指溶质在溶液中的摩尔数与溶液总体积的比率。
对于盐酸,其摩尔浓度可以通过测量其氢离子浓度来计算。
盐酸的浓度对溶液的性质和反应速率有着重要的影响。
在某些化学反应中,需要使用高浓度的盐酸来提高反应速率或促进化学反应的进行。
然而,高浓度的盐酸也具有较高的腐蚀性和危险性,因此在使用时需要特别注意安全和防护措施。
此外,盐酸的浓度还与其生产方法和纯度有关。
不同的生产方法和纯度会导致盐酸的浓度有所差异。
例如,工业盐酸通常含有较多的杂质和其他盐类物质,因此其浓度相对较低。
而高纯度的盐酸则具有较高的浓度和纯度,适用于一些特殊的应用场景。
在使用盐酸时,需要注意安全和防护措施。
盐酸具有强烈的腐蚀性和刺激性气味,会对皮肤、眼睛和呼吸道造成伤害。
因此,在使用盐酸时需要佩戴防护眼镜、手套和口罩等防护用品。
同时,还需要注意盐酸的储存和使用方法,避免泄漏和误食等情况的发生。
总之,盐酸是一种重要的无机强酸,其浓度和应用场景广泛。
在使用盐酸时需要注意安全和防护措施,并选择适合自己应用场景的盐酸浓度和质量。