Folin-Wu法定量测定血糖的含量(精)
- 格式:doc
- 大小:21.00 KB
- 文档页数:4



folin吴法测血糖实验报告一、实验目的血糖的测定在医学诊断和糖尿病的监测中具有重要意义。
本实验旨在通过 folin 吴法测定血糖浓度,掌握该实验的原理、操作步骤及注意事项,并对实验结果进行分析和讨论。
二、实验原理folin 吴法是一种常用的血糖测定方法。
其原理基于葡萄糖在碱性溶液中与硫酸铜反应生成氧化亚铜,氧化亚铜与磷钼酸试剂反应生成蓝色的钼蓝。
颜色的深浅与葡萄糖的含量成正比,通过比色法可测定血糖浓度。
三、实验材料1、仪器分光光度计、离心机、恒温水浴锅、移液器、试管、刻度吸管等。
2、试剂(1)10%钨酸钠溶液(2)033mol/L 硫酸溶液(3)碱性硫酸铜溶液(4)磷钼酸试剂3、样本待测血液样本四、实验步骤1、样本处理(1)取适量待测血液,加入 10%钨酸钠溶液和 033mol/L 硫酸溶液,摇匀后离心,取上清液备用。
2、反应(1)取两支试管,分别标记为测定管和空白管。
(2)向测定管中加入处理后的上清液和碱性硫酸铜溶液,混匀后置于沸水浴中加热 8 分钟,取出后迅速冷却。
(3)向空白管中加入蒸馏水和碱性硫酸铜溶液,同样进行沸水浴加热和冷却处理。
3、显色(1)向测定管和空白管中分别加入磷钼酸试剂,充分混匀。
4、比色测定(1)使用分光光度计,以空白管调零,在波长 620nm 处测定测定管的吸光度值。
五、实验结果根据标准曲线或计算公式,将测定管的吸光度值转换为血糖浓度。
六、注意事项1、样本采集和处理要严格按照操作规程进行,避免溶血和污染。
2、试剂的配制要准确,保存条件要符合要求,避免失效。
3、反应过程中的温度和时间要控制准确,以保证反应的充分进行。
4、比色测定时要注意仪器的校准和调零,确保结果的准确性。
七、实验讨论1、实验结果的准确性分析可能影响实验结果准确性的因素,如样本采集、处理和保存不当,试剂质量问题,操作误差等,并提出相应的改进措施。
2、与其他血糖测定方法的比较简要介绍其他常见的血糖测定方法,如葡萄糖氧化酶法、己糖激酶法等,并比较它们与 folin 吴法的优缺点。




18生物化学实验--吴宪-Folin法测定血糖含量标题:18生物化学实验——吴宪-Folin法测定血糖含量一、实验目的1.掌握吴宪-Folin法测定血糖含量的原理和方法。
2.学习使用分光光度计测量样品吸光度。
3.了解血糖的生理意义及其调节机制。
二、实验原理吴宪-Folin法是一种利用邻甲苯胺和硫酸铜反应生成紫红色络合物的原理,通过测量该络合物在特定波长下的吸光度来测定血糖含量的方法。
由于葡萄糖分子中含有醛基,因此可以利用这一特性进行测定。
本实验采用吴宪-Folin法进行血糖含量的测定。
三、实验步骤1.样品准备:收集受试者在禁食12小时后的静脉血,分离血清备用。
2.试剂准备:将邻甲苯胺、硫酸铜、碳酸钠等试剂按照配方准确称量,溶解定容,现配现用。
3.测定步骤:将试剂和样品按照规定比例混合,在规定温度下静置一段时间,用分光光度计在特定波长下测量吸光度,记录数据。
4.数据处理:根据吸光度和标准曲线计算血糖浓度。
四、实验结果与数据分析1.数据记录:记录受试者血糖吸光度数据(表1)。
表1:血糖吸光度数据记录表表2:血糖浓度计算表3.数据统计:对所有受试者的血糖浓度进行平均值和标准差统计(表3)。
表3:血糖浓度统计表平均值:x̄= ΣC/n (mg/dl) 标准差:s= [Σ(C-x̄)²/n]½五、结论总结与讨论根据实验数据,我们得出以下结论:1.所有受试者的血糖浓度均处于正常范围内。
这表明受试者在禁食12小时后的血糖水平处于生理正常范围。
这一结果与我们所知的人体在禁食状态下的血糖调节机制相符。
当人体处于禁食状态时,胰高血糖素分泌增加,促进肝糖原分解,使血糖水平维持在正常范围。
2.实验结果存在一定差异。
这可能与个体差异、采血时间、实验操作等因素有关。
为了获得更为准确的数据,需要进一步改进实验方法,提高操作精度和标准化程度。
此外,对于不同个体之间的比较,应考虑个体差异对实验结果的影响。
3.吴宪-Folin法是一种灵敏度高、操作简便的血糖测定方法。

中国海洋大学实验报告姓名庞裕智专业年级生命基地班2011 题目血糖的定量测定(Folin-Wu法)学号************科目生物化学实验时间周一90节同组者田特一、实验目的1、掌握Folin-Wu法测定血糖含量的原理和方法。
2、学会制备无蛋白血滤液。
3、掌握7200型可见分光光度计的使用方法。
二、实验原理葡萄糖是一种多羟基的醛类化合物。
其醛基具有还原性,与碱性铜试剂混合加热,葡萄糖分子中的醛基被氧化成羧基,Cu2+即被葡萄糖还原成Cu+(Cu2O)而沉淀。
Cu2+(CuSO4) + 葡萄糖 Cu+ (Cu2O)无蛋白血滤液中的葡萄糖和酸性钼酸盐溶液共热反应, Cu2O又把酸性钼酸试剂(Mo6+)还原成低价的蓝色钼化合物——钼蓝。
Cu2O+酸性钼酸试剂蓝色钼化合物 OD420比色血滤液中葡萄糖的含量与产生的Cu2O成正比,而Cu2O的量与产生的钼化合物的量成正比。
可用比色法定量的测定。
三、实验仪器1、25mL血糖管×3支;2、血糖管橡胶塞×3个;3、1mL胖肚吸管×1支;4、100mL锥形瓶×2个;5、漏斗架×1个;6、普通漏斗×2个;7、水浴锅×1个;8、电炉×1个;9、移液管1mL×2支;2mL×3支;5mL×2支;10mL×1支;10、滤纸×1盒;11、吸耳球×2个;12、7200型分光光度计×1台;13、表面皿×1个。
四、实验试剂1、标准葡萄糖溶液(0.1mg/ml)(1)1%葡萄糖母液:称取1.000g葡萄糖,溶于蒸馏水,稀释并定容至100ml。
(2)葡萄糖标准液:取1.0ml葡萄糖母液于100ml容量瓶中,加蒸馏水定容。
2、10%钨酸钠溶液:称取钨酸钠10g,溶于蒸馏水并定容至100毫升。
3、0.33mol/L H2SO4溶液:于53ml蒸馏水中加入1ml的浓硫酸。


18 生物化学实验--吴宪-Folin法测定血糖含量吴宪 -Folin 法测定血糖含量【目的】1 (掌握吴宪 -Folin 法测定血糖含量的实验方法。
2 (熟悉吴宪 -Folin 法测定血糖含量的实验原理。
【原理】钨酸钠( Na 2 WO 4 )和硫酸作用,生成钨酸,可沉淀血液样品中的蛋白质滤除蛋白质沉淀即可制得无蛋白血滤液,此血滤液中的葡萄糖具有还原性与硷性铜试剂共热可使兰色的二价铜离子( Cu 2+ )还原成红色的氧化亚铜( Cu 2 O )沉淀。
氧化亚铜再使无色的磷钼酸还原成兰色的钼兰。
颜色深浅与葡萄糖含量成正比。
因此,将血滤液和经同样处理的标准葡葡萄溶液分别进行比色,即可求出血糖含量。
其反应如下:1 (硷性铜试剂内的反应2 (定糖显色反应【器材】1 ( Folin- 吴氏定糖管2 (中号试管3 (电炉及加热器4 ( 刻度吸管5 (微量移液器6 (漏斗of the reform of distribution system, linked to the implementation of goals, tasks, benefits, payroll management by objectives approach, effectively mobilized the enthusiasm of the staff. Meanwhile, strengthened cost management, focus on staffTraining, employee skills, service quality has been significantly improved, saving7 (分光光度计【试剂】1 ( 1/3mol/L 硫酸溶液2 ( 10% 钨酸钠3 (碱性铜试剂取无水碳酸钠 40g 溶解于 400ml 蒸馏水中,再加入酒石酸 7.5g ,溶解后定量地移入 1000ml 量瓶中,再加入结晶硫酸铜 4.5g (可先用热水浴稍微加热),待其完全溶解后加蒸馏水至刻度,混匀贮于棕色瓶中保存。
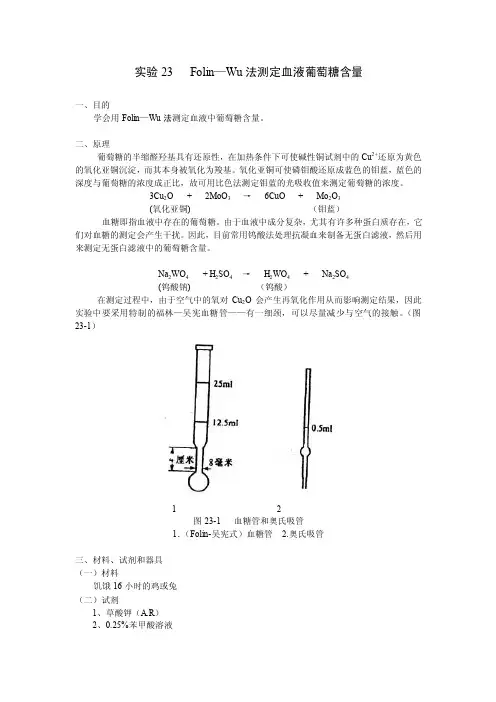
实验23 Folin—Wu法测定血液葡萄糖含量一、目的学会用Folin—Wu法测定血液中葡萄糖含量。
二、原理葡萄糖的半缩醛羟基具有还原性,在加热条件下可使碱性铜试剂中的Cu2+还原为黄色的氧化亚铜沉淀,而其本身被氧化为羧基。
氧化亚铜可使磷钼酸还原成蓝色的钼蓝,蓝色的深度与葡萄糖的浓度成正比,故可用比色法测定钼蓝的光吸收值来测定葡萄糖的浓度。
3Cu2O + 2MoO3 →6CuO + Mo2O3(氧化亚铜) (钼蓝)血糖即指血液中存在的葡萄糖。
由于血液中成分复杂,尤其有许多种蛋白质存在,它们对血糖的测定会产生干扰。
因此,目前常用钨酸法处理抗凝血来制备无蛋白滤液,然后用来测定无蛋白滤液中的葡萄糖含量。
Na2WO4+ H2SO4→H2WO4+ Na2SO4(钨酸钠) (钨酸)在测定过程中,由于空气中的氧对Cu2O会产生再氧化作用从而影响测定结果,因此实验中要采用特制的福林—吴宪血糖管——有一细颈,可以尽量减少与空气的接触。
(图23-1)1 2图23-1 血糖管和奥氏吸管1.(Folin-吴宪式)血糖管 2.奥氏吸管三、材料、试剂和器具(一)材料饥饿16小时的鸡或兔(二)试剂1、草酸钾(A.R)2、0.25%苯甲酸溶液3、10%钨酸钠溶液称取10g钨酸钠,用双蒸水溶解后定容至100ml。
4、1/3mol/L硫酸溶液5、标准葡萄糖溶液(0.1mg/ml)称取1.000g无水葡萄糖,用苯甲酸水溶液溶解后定容至1000ml,其浓度为1mg/ml。
可长期保存使用。
使用时用蒸馏水稀释,配成0.1mg/ml的葡萄糖溶液。
6、碱性铜试剂分别称取40g无水碳酸钠、7.5g酒石酸、4.5g硫酸铜结晶,用蒸馏水溶解后混合,定容至1000ml。
本试剂于室温下可长期保存使用,若有沉淀产生,应过滤后再使用。
7、磷钼酸试剂称取70g钼酸、10g钨酸钠,量取10%氢氧化钠400ml及蒸馏水400ml,于烧杯中混合加热20~40min(以除去可能夹杂于钼酸中的氨),冷却后加入85%磷酸250ml,混匀后定溶至1000ml..(三)器具1、剪刀2、烧杯3、试管与试管架4、玻璃棒5、奥氏吸量管(见图23—1)6、血糖管(见图23—1)7、小漏斗8、可见光分光光度计9、水浴锅10、移液管11、电炉12、天平13、容量瓶四、操作步骤(一)制备无蛋白滤液1.杀鸡取血后立即按2g草酸钾/L血液的比例加入草酸钾,以制备抗凝血。
血糖含量的定量测定 (Folin-Wu 法一、目的1、掌握 Folin - Wu法测定血糖含量的原理和方法。
2、学会制备无蛋白血滤液。
3、掌握 7200 型可见分光光度计的使用方法。
二、实验原理葡萄糖是一种多羟基的醛类化合物。
其醛基拥有复原性,与碱性铜试剂混淆加热,葡萄糖分子中的醛基被氧化成羧基,,Cu2+即被葡萄糖复原成 Cu+(Cu2O)而积淀。
无蛋白血滤液中的葡萄糖和酸性钼酸盐溶液共热反响, Cu2O 又把酸性钼酸试剂( Mo6+)复原成廉价的蓝色钼化合物—钼蓝。
血滤液中葡萄糖的含量与产生的 Cu2O成正比,而 Cu2O的量与产生的钼化合物的量成正比。
可用比色法定量的测定。
3、实验仪器1、25mL血糖管×3 支;2、血糖管橡胶塞×3 个;3、1mL胖肚吸管×1 支;4、100mL锥形瓶×2 个;5、漏斗架×1 个;6、一般漏斗×2 个;7、水浴锅×1 个;8、电炉×1 个;9、移液管 1mL×2 支; 2mL ×3 支;5 mL ×2 支;10 mL×1 支 ; 10 、滤纸×1 盒;11、吸耳球×2 个;12、7200 型分光光度计×1 台 ;13、表面皿×1 个4、实验试剂1、标准葡萄糖溶液( 0.1mg/ml )(11%葡萄糖母液:称取 1.000g 葡萄糖,溶于蒸馏水,稀释并定容至100ml。
(2 葡萄糖标准液:取 1.0ml 葡萄糖母液于100ml 容量瓶中,加蒸馏水定容。
2、碱性硫酸铜溶液A 液:无水碳酸钠35g,酒石酸钠 13g 及碳酸氢钠 11g 溶于蒸馏水,稀释定容至1000ml.B 液:硫酸铜晶体5g,溶于蒸馏水并定容至100ml。
临用时, A 液: B 液=9:1 混淆(体积比),混淆液于冰箱中保留(4℃)。
3、10%钨酸钠溶液:称取钨酸钠10g,溶于蒸馏水并定容至100 毫升。
folin吴法测血糖实验报告Folin吴法测血糖实验报告一、实验目的掌握 Folin吴法测定血糖的原理和方法,熟悉实验操作过程,准确测定血液中葡萄糖的含量。
二、实验原理Folin吴法是一种常用的测定血糖的化学方法。
其原理是葡萄糖在碱性溶液中加热,能将斐林试剂中的铜离子还原为氧化亚铜沉淀。
然后用酸性的三价铁离子将氧化亚铜氧化为二价铜离子,同时三价铁离子被还原为亚铁离子。
亚铁离子与亚铁氰化钾反应生成普鲁士蓝,其颜色的深浅与葡萄糖的含量成正比。
通过比色法测定溶液的吸光度,即可计算出血糖的浓度。
三、实验材料与设备1、材料新鲜血液样本标准葡萄糖溶液斐林试剂(甲液:硫酸铜溶液;乙液:氢氧化钠与酒石酸钾钠溶液)三氯化铁溶液亚铁氰化钾溶液蒸馏水2、设备分光光度计恒温水浴锅移液器容量瓶试管刻度吸管四、实验步骤1、标准曲线的绘制准备一系列不同浓度的标准葡萄糖溶液,浓度分别为 0、01、02、03、04、05mg/ml。
向每支试管中加入 1ml 相应浓度的标准葡萄糖溶液,再加入 1ml 斐林试剂甲液和 1ml 斐林试剂乙液,摇匀后在沸水浴中加热 10 分钟。
取出试管,迅速冷却后加入 2ml 三氯化铁溶液和 05ml 亚铁氰化钾溶液,摇匀。
使用分光光度计,以蒸馏水为空白对照,在波长 620nm 处测定各管溶液的吸光度。
以葡萄糖浓度为横坐标,吸光度为纵坐标,绘制标准曲线。
2、样品测定吸取 01ml 血液样本,用蒸馏水稀释至 10ml,摇匀。
吸取 1ml 稀释后的血液样本,按照与绘制标准曲线相同的步骤进行操作,测定吸光度。
五、实验结果与计算1、实验结果标准曲线的相关数据如下:|葡萄糖浓度(mg/ml)|吸光度|||||0|0||01|012||02|025||03|038||04|051||05|065|样品测定的吸光度为 042。
2、计算根据标准曲线,找到吸光度为 042 所对应的葡萄糖浓度。
由于血液样本进行了 100 倍稀释,所以计算出血糖浓度的实际值。
血糖含量的定量测定(Folin-Wu法
一、目的
1、掌握Folin-Wu法测定血糖含量的原理和方法。
2、学会制备无蛋白血滤液。
3、掌握7200型可见分光光度计的使用方法。
二、实验原理
葡萄糖是一种多羟基的醛类化合物。
其醛基具有还原性,与碱性铜试剂混合加热,葡萄糖分子中的醛基被氧化成羧基,,Cu2+即被葡萄糖还原成Cu+(Cu2O)而沉淀。
无蛋白血滤液中的葡萄糖和酸性钼酸盐溶液共热反应, Cu2O又把酸性钼酸试剂(Mo6+)还原成低价的蓝色钼化合物—钼蓝。
血滤液中葡萄糖的含量与产生的Cu2O成正比,而Cu2O的量与产生的钼化合物的量成正比。
可用比色法定量的测定。
3、实验仪器
1、25mL血糖管×3支;
2、血糖管橡胶塞×3个;
3、1mL胖肚吸管×1支;
4、100mL锥形瓶×2个;
5、漏斗架×1个;
6、普通漏斗×2个;
7、水浴锅×1个;
8、电炉×1个;
9、移液管 1mL×2支; 2mL×3支;5 mL×2支;
10 mL×1支; 10、滤纸×1盒;
11、吸耳球×2个;
12、7200型分光光度计×1台;
13、表面皿×1个
4、实验试剂
1、标准葡萄糖溶液(0.1mg/ml)
(11%葡萄糖母液:称取1.000g葡萄糖,溶于蒸馏水,稀释并定容至100ml。
(2葡萄糖标准液:取1.0ml葡萄糖母液于100ml容量瓶中,加蒸馏水定容。
2、碱性硫酸铜溶液
A液:无水碳酸钠35g,酒石酸钠13g及碳酸氢钠11g溶于蒸馏水,稀释定容至1000ml.
B液:硫酸铜晶体5g,溶于蒸馏水并定容至100ml。
临用时,A液:B液=9:1混合(体积比),混合液于冰箱中保存(4℃)。
3、10%钨酸钠溶液:称取钨酸钠10g,溶于蒸馏水并定容至100毫升。
4、0.33mol/LH2SO4溶液:于53ml蒸馏水中加入1ml的浓硫酸。
5、酸性钼酸盐溶液:
称取钼酸钠600g,用少量蒸馏水溶解后倾入2000ml 的容量瓶中,加蒸馏水至刻度,摇匀,倾入另一较大的试剂瓶中,加溴水0.5ml,摇匀,静止数小时后取上清夜500ml,于1000ml容量瓶中,徐徐加入225ml85%磷酸,边加边摇匀,再加25%硫酸150ml。
置暗处次日,用空气将剩余的溴赶去。
然后加99%醋酸75ml,摇匀,用蒸馏水稀释定容至1000ml,贮于棕色瓶中。
5、实验步骤
1、无蛋白血滤液的制备:
氏吸管吸取全血(已加抗凝剂)1ml,缓缓放入100ml锥形瓶中,加蒸馏水7ml,摇匀,溶血后(血液变为红色透明)加10%钨酸钠1ml,摇匀.。
再加0.33mol/L H2SO41ml,边加边摇,加毕充分摇匀,放置5~15分钟,至沉淀变为暗棕色(如不变色可再加0.33mol/L H2SO41-2滴)。
用干滤纸过滤。
先倾入少许,待滤纸湿润后在全部倒入,如滤液不清需重新过滤。
每毫升无蛋白血滤液相当于1/10ml全血。
2、血糖的定量测定:
1、取25ml的血糖管3支,编号。
第一支血糖管中加入2ml蒸馏水(空白管);第二支血糖管中加2ml标准葡萄糖液;用吸管吸取无蛋白血滤液2ml,放入第三支血糖管中。
2、然后向三支血糖管中各加入2ml新配制的碱性硫酸铜溶液,同时置于沸水浴中8分钟,取出,在流水中迅速冷却后,勿摇动,各加4ml酸性钼酸盐溶液。
3、一分钟后,用蒸馏水稀释至25ml,混匀,用7200分光光度计在420nm波长处比色,以空白管调节零点。
六、实验结果
样品A1(吸光度)标准液A0
(吸光度)
水
(吸光度)
10.1690.1300.000 20.1900.1350.000 30.1940.1280.000平均值0.1840.1310.000
m=A1/A2*C*10*100
m代表100ml全血中含血糖毫克数
C0代表标准液葡萄糖含量(0.1mg/ml)
A1代表样品液光吸收值
A0代表标准液光吸收值
所以可得出m=0.184/0.131*0.1*10*100=140.4580153···约等于140.458mg。
7、实验分析
1、实验过程中哪些操作可能影响实验结果的准确性?
在沉淀不完全时过滤,吸管中放出血液太快使大量血液黏在吸管内壁,或有亚铜离子氧化成铜离子,比色测量时也可能会出现误差。
2、实验中,血糖管有什么作用?
可减少亚铜离子与空气的接触,防止氧化成铜离子。
3、实验过程中,为什么要用流水冷却加入碱性硫酸铜液反应后的血糖管?
流水冷却比较稳定,可以迅速降温。
如不冷却会继续反应造成误差。