无机化学武大吉大第三版答案_31-45
- 格式:pdf
- 大小:1.02 MB
- 文档页数:15



第16章硼组元素一、选择题1.下列酸中属于一元酸的是()。
【答案】A【解析】H3BO3在水中电离的方程式为:H3BO3+H2O =B(OH)4-+H+,而B(OH)4-不再电离,所以H3BO3为一元酸。
2.硼酸的分子式常写成H3BO3,它是()。
A.二元弱酸B.一元弱酸C.三元弱酸D.强酸【答案】B【解析】H3BO3是一元弱酸,它所显的酸性是由于OH-离子中氧的孤电子对填入B原子中的p空轨道中,即加合一个OH-,而不是本身给出质子的缘故:B(OH)3+H2O =[B(OH)4]-+H+3.()不是CO的等电子体。
A.NO B.NO+C.N2D.CN一【答案】A【解析】等电子体是指价电子数和原子数(氢等轻原子不计在内)相同的分子、离子或基团。
4.下列化合物不属子缺电子化合物的是( )。
A .BCl 3 B .HBF 4 C .B 2H 6D .Al (OH )3 【答案】B【解析】缺电子化合物是由价电子数少于价层轨道的缺电子原子形成的化合物。
A 项和D 项是由缺电子原子与多电子原子化合物形成的配键化合物;C 项为缺电子原子与等电子原子化合形成的缺电子分子。
5.在硼砂珠试验中,硼砂与氧化钴(Ⅱ)产生的颜色是( )。
A .蓝色 B .棕色 C .黑色 D .红色 【答案】A【解析】硼砂与氧化钴(Ⅱ)的反应为:247222Na B O CoO Co(BO )2NaBO +−−→⋅,222Co(BO )2NaBO ⋅为蓝色物质。
6.某硼氢合物(B x H y 与过量的水反应,得到30.9mg 硼酸和30.26mL 干燥氢气(在22℃,730mmHg 柱),该硼氢化物的实验式为(B 的原子量为10.811)( )。
【答案】C【解析】B x H y + H 2O → H 3BO 3 + H 2,由n (H 3BO 3) = 0.0005 mol ,n (H 2)= 0.0012 mol 得n (H 3BO 3):n (H 2) = 5:12。


无机化学第三版课后答案【篇一:武大吉大第三版无机化学教材课后习题答案02-11】2.一敝口烧瓶在280k时所盛的气体,需加热到什么温度时,才能使其三分之一逸出? 解3.温度下,将1.013105pa的n2 2dm3和0.5065pa的o23 dm3放入6 dm3的真空容器中,求o2和n2的分压及混合气体的总压。
解4.容器中有4.4 g co2,14 g n2,12.8g o2,总压为2.02610pa,求各组分的分压。
解55.在300k,1.013105pa时,加热一敝口细颈瓶到500k,然后封闭其细颈口,并冷却至原来的温度,求这时瓶内的压强。
解在此过程中,液体损失0.0335 g,求此种液体273k时的饱和蒸汽压。
解7.有一混合气体,总压为150pa,其中n2和h2的体积分数为0.25和0.75,求h2和n2的分压。
解完全吸水后,干燥空气为3.21 g,求291k时水的饱和蒸汽压。
解而不致发生危险?解(1)两种气体的初压;(2)混合气体中各组分气体的分压;(3)各气体的物质的量。
解用作图外推法(p对?/p)得到的数据求一氯甲烷的相对分子质量。
2.4-3-5-12.22.00.00.20.40.60.81.01.2p (10pa)5解可得出一氯甲烷的相对分子质量是50.49512.(1)用理想气体状态方程式证明阿佛加德罗定律;(2)用表示摩尔分数,证明xi =?i v总(3)证明2=3ktm证明:(1)pv=nrt当p和t一定时,气体的v和n成正比可以表示为v∞n(2)在压强一定的条件下,v总=v1+v2+v3+----- 根据分体积的定义,应有关系式p总vi=nrt混合气体的状态方程可写成p总v总=nrtnivi= nv总ni?=xi 所以 xi = inv总又(3)mb?a=ma?b又pv=1n0m(?2)2 33pv3rt= n0mm2=所以?2=3ktm【篇二:第3版的无机化学_课后答案】3.解:一瓶氧气可用天数n1(p?p1)v1(13.2?103-1.01?103)kpa?32l???9.6dn2p2v2101.325kpa?400l ? d-1pvmpv?nrmr= 318 k ?44.9℃4.解:t?5.解:根据道尔顿分压定律pi?p(n2) = 7.6?104 pa p(o2) = 2.0?104 pa p(ar) =1?103 panip n6.解:(1)n(co2)? 0.114mol; p(co2)? 2.87 ? 104 pa(2)p(n2)?p?p(o2)?p(co2)?3.79?104pan(o2)p(co2)2.67?104pa(3)???0.286np9.33?104pa7.解:(1)p(h2) =95.43 kpapvm(2)m(h2) = = 0.194 grt8.解:(1)? = 5.0 mol(2)? = 2.5 mol结论: 反应进度(?)的值与选用反应式中的哪个物质的量的变化来进行计算无关,但与反应式的写法有关。

第十二章1.卤素中哪些元素最开朗?为何有氟至氯开朗性变化有一个突变?答:单质的开朗性序次为:F2>>Cl 2>Br 2>I 2—从 F2到 Cl 2开朗性突变,其原由归纳为 F 原子和 F 离子的半径特别小。
r/pmF Cl Br I F64 99 114 133 136181—Cl —195216Br—I—(1)因为 F 的原子半径特别小,F—F原子间的斥力和非键电子对的斥力较大,使解离能( 155KJ/mol )远小于Cl 2的解离能( 240KJ/mol )。
F2的(2)因为 F-离子半径特别小,所以在形成化合物时,氟化物的离子键更强,键能或晶格能更大。
因为 F-离子半径特别小,F-的水合放热比其余卤素离子多。
2.举例说明卤素单质氧化性和卤离子X-复原性递变规律,并说明原由。
答:氧化性次序为:F2> Cl 2 >Br2>I 2; 复原性次序为:I ->Br- >Cl - >F- .只管在同族中氯的电子亲合能最高,但最强的氧化剂倒是氟卤素单质是很强的氧化剂, 跟着原子半径的增大, 卤素的氧化能力挨次减弱。
只管在同族中氯的电子亲合能最高, 但最强的氧化剂倒是氟。
一种氧化剂在常温下, 在水溶液中氧化能力的强弱 , 可用其标准电极电势值来表示,值的大小和以下过程相关(见课本P524)3.写出氯气与钛、铝、氢、水和碳酸钾作用的反响式,并注明必需的反响条件。
答:( 1) 2Cl 2+Ti =TiCl4( 2) 3Cl 2+2Al =2AlCl3( 3) Cl 2+H2 =2HCl( 4) 3Cl 2+2P(过度 )=2PCl 35Cl 2( 过度 )+2P=2PCl 5加热,干燥加热,干燥点燃干燥干燥(5) Cl 2+H2O=HClO +HCl(6)Cl 2+2KCO3+H2O=KCl+KClO+2KHCO34.试解说以下现象:( 1)I 2溶解在 CCl4中获取紫色溶液,而I 2在乙醚中倒是红棕色。

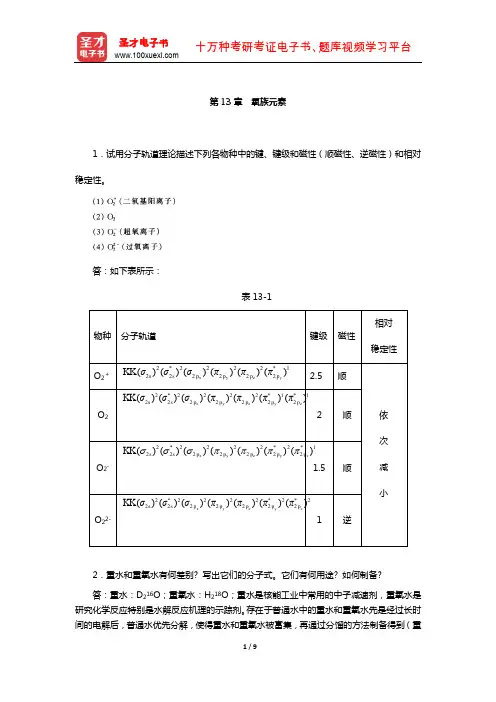
第13章氧族元素1.试用分子轨道理论描述下列各物种中的键、键级和磁性(顺磁性、逆磁性)和相对稳定性。
答:如下表所示:表13-12.重水和重氧水有何差别? 写出它们的分子式。
它们有何用途? 如何制备?答:重水:D216O;重氧水:H218O;重水是核能工业中常用的中子减速剂,重氧水是研究化学反应特别是水解反应机理的示踪剂。
存在于普通水中的重水和重氧水先是经过长时间的电解后,普通水优先分解,使得重水和重氧水被富集,再通过分馏的方法制备得到(重水和重氧水的沸点都高于普通水)。
3.解释为什么O 2分子具有顺磁性,O 3具有反磁性?答:O 2的分子轨道式为:2*2222*1*12222222()()()()()()()x y z y z s s p p p p p KK σσσππππ,可见O 2分子中有2个单电子,因而具有顺磁性。
O 3分子中没有单电子,只存在大π键43Π,因而具有反磁性。
4.在实验室怎样制备O 3? 它有什么重要性?答:在实验室里制备臭氧主要靠紫外光(<185 nm )照射氧或使氧通过静电放电装置而获得臭氧与氧的混合物,臭氧的含量可达10%,反应方程式为:3O 2=2O 3(放电条件下)。
O 3是大气层中主要的吸收紫外线的物质,使人类避免受到紫外线照射的伤害。
5.油画放置久后为什么会发暗、发黑? 为什么可用H 2O 2来处理? 写出反应方程式。
答:油画放置久后会变黑,发暗,原因是油画中的白色颜料中含有PbSO 4,遇到空气中的H 2S 生成黑色的PbS 造成的,反应方程式为:PbSO 4 +H 2S = PbS (黑)+ H 2SO 4。
用H 2O 2处理又重新变白,是因为发生以下反应:2242PbS 4H O PbSO 4H O +=+。
6.比较氧族元素和卤族元素氢化物在酸性、还原性、热稳定性方面的递变规律。
答:氧族元素的氢化物有H 2O ,H 2S ,H 2Se 和H 2T e 。


1.什么叫稀溶液的依数性?试用分子运动论说明分子的几种依数性?答2.利用溶液的依数性设计一个测定溶质分子量的方法。
答3.溶液与化合物有什么不同?溶液与普通混合物又有什么不同?答4.试述溶质、溶剂、溶液、稀溶液、浓溶液、不饱和溶液、饱和溶液、过饱和溶液的含意。
答为溶质。
体系叫溶液。
5.什么叫做溶液的浓度?浓度和溶解度有什么区别和联系?固体溶解在液体中的浓度有哪些表示方法?比较各种浓度表示方法在实际使用中的优缺点。
答6.如何绘制溶解度曲线?比较KNO3、NaCl和NaSO4的溶解度曲线,说明为什么着三条曲线的变化趋势(及斜率)不一样?答以溶解度为纵坐标,以温度为横坐标所做出的溶解度随温度变化的曲线叫做溶解度曲线。
KNO3溶解度随温度升高而增大;NaCl溶解度随温度升高几乎不变; NaSO4溶解度随温度升高而减小。
7.为什么NaOH溶解于水时,所得的碱液是热的,而NH4NO3溶解与水时,所得溶液是冷的?答8.把相同质量的葡萄糖和甘油分别溶于100g水中,问所得溶液的沸点、凝固点、蒸汽压和渗透压相同否?为什么?如果把相同物质的量的葡萄糖和甘油溶于100g水中,结果又怎样?说明之。
答9.回答下列问题:(a)提高水的沸点可采用什么方法?(b)为什么海水鱼不能生活在淡水中?(c)气体压强和溶液渗透压有何差别?(d)为什么临床常用质量分数为%生理食盐水和用质量分数为5%葡萄糖溶液作输液?(e)为什么浮在海面上的冰山其中含盐极少?(f)试述亨利(Henry)定律和拉乌尔(Raoult)定律的适用范围是。
答(a)增大水的蒸气压;(b)因为渗透压不同;(c) =CRT稀溶液的渗透压与溶液的浓度和温度的关系同理想气体方程式一致。
(d)在一定条件下,难挥发非电解质稀溶液的渗透压与溶液中溶质的浓度成正比,而与溶质的本性无(e)非极性或弱极性的固态物质溶于弱极性溶剂而难溶于强极性溶剂。
(f)亨利(Henry)定律的适用范围是中等强度;拉乌尔(Raoult)定律的适用范围是任何强度。

第5章氢和稀有气体一、填空题1.人们将氢化物分为______氢化物,______氢化物和______氢化物三种类型。
【答案】离子型,分子型,金属型。
2.拉姆齐和雷利在1894年从空气中第一次分离出的稀有气体是______;l962年巴特利特第一次合成出来的稀有气体化合物是______,该化合物是模仿______合成出来的。
【答案】Ar(或氩);3.用Xe和F2直接反应合成出的化合物有______、______和______。
【答案】三、完成方程式并配平1.氙的化合物与水反应。
答:2.氢化物LiH与下列化合物反应。
答:3.完成下列氟化物与水反应的方程式。
答:4.完成并配平下列反应方程式。
答:四、问答题1.举例说明氢气都有哪些重要的化学性质。
答:氢气的化学性质主要有以下几种:(1)与活泼金属在加热条件下反应,生成离子型氢化物。
(2)与非金属元素形成分子型氢化物。
H2与氧化能力强的F2在低温下即可剧烈反应。
存光照或引燃的条件下,H2与Cl2和O2等反应。
H2是合成氨的重要原料,与N2在高温、加压和催化剂存在的条件下反应。
(3)在加压条件下与过渡金属形成金属型氢化物。
(4)在高温条件下,H2作为反应的还原剂。
(5)利用H2在有机合成中进行加氢反应,在催化剂作用下合成特定的化合物。
2.氢作为能源,其优点是什么?目前开发中的困难是什么?答:氢作为能源其优点如下:(1)原料来源于地球上储量丰富的水,因而资源不受限制;(2)氢气燃烧时放出的热量很大;(3)作为燃料的最大优点是燃烧后的产物为水,不会污染环境;(4)有可能实现能量的储存,也有可能实现经济高效的输送。
发展氢能源需要解决三个方面的问题:氢气的发生,氢气的储备和氢气的利用。
3.由氙的元素电势图计算的值。
答:酸性溶液中氙的元素电势图为说明H4XeO4具有很强的氧化性。
4.为什么XeOF4不能用玻璃容器储存?并指出应该用什么容器储存?答:XeOF4会与SiO2发生如下反应:可用镍容器(因氟与镍反应生成致密的保护膜)和某些塑料容器(如聚四氟乙烯)。
第四部分模拟试题武汉大学、吉林大学《无机化学》(第3版)配套模拟试题及详解一、填空题(20*1=20分)1.在中,具有顺磁性的是______。
【答案】【解析】当原子或离子核外轨道中有单电子时则具有顺磁性。
价电子结构式:的d 轨道中均有单电子。
2.BrF 3和XeOF 4分子的几何构型分别为______和______。
【答案】T 形;四方锥形【解析】根据价层电子对理论,前者有5对价层电子,3对共用电子对,两对孤对电子,sp 3d 杂化分子为T 形;后者有6对价层电子,5对共用电子对,一对孤对电子,本为八面体,但有一孤对电子从锥低伸向与锥体相反的方向,使其变形。
3.已知226Ra 的半衰期为1590年,则此一级反应的速率常数为______。
【答案】6-11.1910d -⨯【解析】一级反应的半衰期为:1/21ln 2t =k ,故6-111/2ln 2ln 2= 1.1910d t 1590365k -==⨯⨯。
4.已知K (HAc)=1.75×10-5,K (HNO 2)=7.2×10-4;K (HOCl)=2.8×10-8;在相同浓度的HAc、HNO 2、HOCl、HBr 溶液中,c (H +)由大到小的顺序是______;pOH 由大到小的顺序是______。
【答案】HBr>HNO 2>HAc>HOCl;HOCl>HAc>HNO 2>HBr【解析】HAc 在水中的解离平衡为:HAc Ac H -++ ;HNO 2在水中的解离平衡为:22HNO NO H -++ ;HBr 是强酸,在水中完全电离:HBr Br H -+→+,酸性最强,H +浓度最高;HOCl 在水中的解离平衡为:HOCl ClO H -++ ;根据解离平衡常数K (HNO 2)>K (HAc)>K (HOCl)的关系可知,三者溶液中H +浓度由大到小顺序为HNO 2>HAc>HOCl。
溶液中OH -的浓度与H +浓度相反。
第18章铜、锌副族1.用反应方程式说明下列现象:(1)铜器在潮湿空气中会慢慢生成一层铜绿;(2)金溶于王水;(3)在CuCl2浓溶液逐渐加入水稀释时,溶液颜色由黄棕色经绿色而变为蓝色;(4)当SO2通入CuSO4与NaCl的浓溶液中时析出白色沉淀;(5)往AgNO3溶液中滴加KCN溶液时,先生成白色沉淀而后溶解,再加入NaCl溶液时并无AgCl沉淀生成,但加入少许Na2S溶液时却析出黑色AgS沉淀。
答:(1)2Cu +O 2+H2O +CO2Cu2(OH)2CO3(2)Au +4HCl +HNO 3H[AuCl4] +NO↑+2H2O(3)[CuCl 4]2-+4H2O [Cu(H2O)4]2++4Cl-[CuCl4]2-为黄色,[Cu(H2O)4]2+为蓝色,而当这两种离子共存时溶液呈绿色。
(4)2Cu2++2Cl-+SO 2+2H2O 2CuCl↓+4H++SO42-(5)Ag++CN-AgCN↓(白)AgCN+CN- [Ag(CN)2]-(无色)2[Ag(CN)2]-+S2-Ag2S↓+4CN-2.解释下列实验事实:(1)焊接铁皮时,常先用浓ZnCl2溶液处理铁皮表面;(2)HgS不溶于HCl,HNO3和(NH4)2S中而能溶于王水或Na2S中;(3)HgC2O4难溶于水,但可溶于含有Cl-离子的溶液中;(4)热分解CuCl2·2H2O时得不到无水CuCl2。
(5)HgCl2溶液中有NH4Cl存在时,加入NH3水得不到白色沉淀NH2HgCl。
答:(1)ZnCl2+H2O =H[ZnCl2(OH)]H[ZnCl2(OH)]有显著的酸性,能清除金属表面的氧化物而不损害金属表面,如:FeO +2H[ZnCl2(OH)] =Fe[ZnCl2(OH)]2+H2O(2)HgS不溶于HCl溶液中是因为HgS的溶度积常数太小;HgS溶于王水,它与王水反应生成HgCl42-和S。
3HgS +8H++2NO3-+12Cl-=3HgCl42-+3S +2NO +4H2OHgS溶于Na2S溶液反应生成可溶性的HgS22-,反应式为:HgS +S2-=HgS22-。
武汉大学吉林大学等校编第三版答案全解第二章1.某气体在293K与9.97×104Pa时占有体积1.910-1dm3其质量为0.132g,试求这种气体的相对分子质量,它可能是何种气体?解2.一敝口烧瓶在280K时所盛的气体,需加热到什么温度时,才能使其三分之一逸出?解3.温度下,将1.013105Pa的N22dm3和0.5065Pa的O23dm3放入6dm3的真空容器中,求O2和N2的分压及混合气体的总压。
解4.容器中有4.4 gCO,14 gN,12.8gO,总压为2.026105Pa,求各组分的分压。
5.在解6.在78.在910.在用作图外推法(p对ρ/p)得到的数据求一氯甲烷的相对分子质量。
0.00.20.40.60.8 1.0 1.22.02.22.4ρ/P (g ·d m -3·10 -5 p a -1)又pV=31N 0m(2μ)2 2μ=mpV 0N 3=M RT 3 所以2μ=M kT 3 13.已知乙醚的蒸汽热为25900J ·mol -1,它在293K 的饱和蒸汽压为7.58×104Pa ,试求在308K 时的饱和蒸汽压。
解14.水的气化热为40kJ·mol-1,,求298K时水的饱和蒸汽压。
解15.如图所示是NaCl的一个晶胞,属于这个晶胞的Cl (用表示)和Na+(用表示)各多少个?解第三章晶体结构3-1给出金刚石晶胞中各原子的坐标。
1﹑解:0,0,0;1/4,1/4,1/4;3/4,1/4,3/4;3/4,3/4,1/4;1/4,3/4,3/4或0,0,0;3/4,1/4,1/4;3/4,3/4,1/4;1/4,1/4,3/4;3/4,3/4,3/4。
3-2给出黄铜矿晶胞(图3-48)中各种原子(离子)的坐标。
2﹑解:Cu0,0,0;1/2,1/2,1/2;0,1/2,1/4;1/2,0,3/4。
Fe1/2,1/2,0;1/2,0,1/4;0,0,1/2;0,1/2,3/4。