2017-2018学年河北省石家庄市第二中学高一12月月考化学试题
- 格式:doc
- 大小:348.50 KB
- 文档页数:8

石家庄二中2022级高一年级10月份月考地理试题(答案在最后)考试时间:40分钟;满分:60分第I卷(选择题)一、单选题(每题2分,共50分)天亮前后,东方地平线上有时会看到一颗特别明亮的“晨星”——金星,它不是光源,人们称它为“启明星”。
下图是太阳系部分行星绕日公转示意图。
读图,完成1~2题。
1.图中被称为“启明星”的是()A.MB.JC.VD.W2.“狮子座流星雨”来源于()A.M轨道与V轨道之间B.V轨道与地球轨道之间C.地球轨道与W轨道之间D.W轨道与J轨道之间蓝巨星是非常巨大的蓝色星球,亮度是太阳的五百倍以上,但其寿命却比太阳短得多;其引力较强,有时会吞噬行星。
宇宙中的蓝巨星很多,但一般认为,以其为中心绕转的天体存在生命的可能性极小。
完成3~4题。
3.蓝巨星属于()A.星云B.恒星C.行星D.卫星4.围绕蓝巨星运行的天体很难有生命存在的主要原因是()①光照条件差②宇宙环境不安全③体积太小④温度过高A.①②B.②③C.③④D.②④火星是地球的近邻,表面大气稀薄,大气成分以二氧化碳为主,昼夜长短接近地球,而昼夜温差却超过100℃。
北京时间2020年7月23日,我国“天问一号”火星探测器发射升空。
2021年2月10日,“天问一号”顺利实施近火制动,正式踏入环绕火星轨道。
5月15日,“天问一号”携带的“祝融号”火星车和及其着陆组合体,成功降落在火星北半球的乌托邦平原南部,实现了中国航天史无前例的突破:我国成为世界上第二个真正“踏上”火星的国家,也是首次火星探测即实现着陆的国家。
据此,完成5~6题。
5.火星表面昼夜温差远大于地球表面,主要原因是()A.太阳活动极强B.轨道半径很大C.距离太阳更远D.空气密度超低6.“天问一号”火星探测器进入环火星轨道后()①脱离了地月系②脱离了太阳系③始终在银河系④进入了河外星系A.①②B.①③C.②④D.③④2017年6月15日,我国成功发射首颗天文观测卫星“慧眼”,假设此卫星观测到一次剧烈的太阳活动,产生了巨大的发光现象(如图)。

河北省临漳县2017-2018学年高一化学上学期第一次月考试题(29-32班)(使用范围:29--32班,时间:90分钟,总分:60分)可能用到的相对原子质量:Ne—20 H—1 O—16 S—32 Zn—65C—12 N—7 Cl—35.5 Na—23第I卷(选择题,共30分)一、选择题(共15题,每小题2分,共30分,其中每小题只有一个选项符合题意)1.下列广告用语在科学性上没有错误的是()A.这种饮料中不含任何化学物质B.这种蒸馏水绝对纯净,其中不含任何微粒C.这种口服液含丰富的氮、磷、锌等微量元素D.没有水就没有生命2.“垃圾是放错了位置的资源”,应该分类回收。
生活中废弃的铁锅、铝制的易拉罐、铜导线等可以归为一类加以回收,它们属于()A.氧化物 B.盐 C.金属或合金 D.碱3.Na2CO3俗名纯碱,下面是对纯碱采用不同分类法的分类,不正确的是( ) A.Na2CO3是碱 B.Na2CO3是盐C.Na2CO3是钠盐D.Na2CO3是碳酸盐4.下列各组物质中,均为纯净物的一组是 ( ) A.碘酒、干冰 B.石油、液氧C.Na2CO3·10H2O、Na2CO3 D.石灰石、盐酸5.下列分散系不发生丁达尔效应的是()A.雾 B.硫酸铜溶液C.氢氧化铁胶体 D.碘化银胶体6.下列物质中属于纯净物、化合物、无机化合物、盐、钙盐的是()A.石灰石B.Ca(OH)2 C.CaCO3D.CH47.下列说法中正确的是()A.1 mol O的质量是16 g·mol-1B.Na+的摩尔质量是23 g·mol-1C.CO 2的摩尔质量是44 g ·mol -1D.氢的摩尔质量是2 g ·mol -18.相同状况下,下列气体所占体积最大的是( )A. 8.0g SO 3B. 1.6g O 2C. 3.2g H 2SD. 0.3g H 29.关于2mol 二氧化碳的叙述中,正确的是( )A .质量为44gB .有4mol 原子C .分子数为6.02×1023D .摩尔质量为44g/mol10.下列说法正确的是 ( )A.6.02×1023个鸡蛋为1mol 鸡蛋B.6.02×1023个氧为1mol O 2C.1molNa +中约含有6.02×1023个Na +D.1mol 硫酸溶液11.判断下列物质中属于电解质的是( )A .硝酸钾溶液B .蔗糖C .金属铜D .氢氧化钡12.下列各组物质中,含原子数最多的是 ( )A .0.4 mol NH 3B .4℃时5.4 mL 水C .10 g 氖气D .6.02×1023个硫酸分子13.下列反应属于氧化还原反应的是( )14.等物质的量的SO 2与SO 3 , 下列有关叙述中正确的是 ( ) A.所含硫原子个数相等 B.所含分子个数相等C.所含氧原子数相等D.所含电子数相等15.现有下列四种因素:① 温度和压强 ②微粒本身大小③所含微粒数④ 微粒间的距离,其中对气体物质体积有显著影响的是( )A .只②③④B .只②④C .只①③④D .①②③④全部A .CaCO 3=====高温CaO +CO 2↑B .2KClO 3=====MnO 2△2KCl +3O 2↑ C .MnO 2+4HCl(浓)=====△MnCl 2+Cl 2↑+2H 2OD .NaCl(s)+H 2SO 4(浓)=====△NaHSO 4+HCl ↑第Ⅱ卷(非选择题,共30分)二、判断题(4分)16.(4分)判断下列说法是否正确,正确的打√,错误的打×。
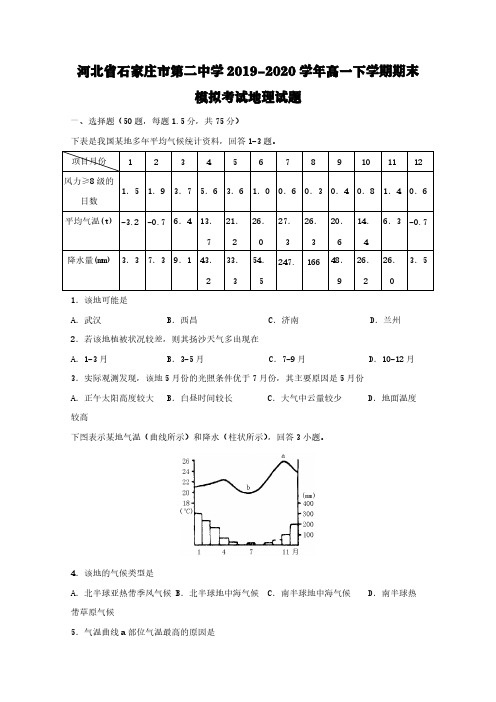
河北省石家庄市第二中学2019-2020学年高一下学期期末模拟考试地理试题一、选择题(50题,每题1.5分,共75分)下表是我国某地多年平均气候统计资料,回答1-3题。
项目月份123456789101112风力≥8级的日数1.51.93.75.63.61.00.60.30.40.81.40.6平均气温(t)-3.2-0.76.413.721.226.27.326.320.614.46.3-0.7降水量(mm)3.37.39.143.233.354.5247.16648.926.226.3.51.该地可能是A.武汉B.西昌C.济南D.兰州2.若该地植被状况较差,则其扬沙天气多出现在A.1-3月B.3-5月C.7-9月D.10-12月3.实际观测发现,该地5月份的光照条件优于7月份,其主要原因是5月份A.正午太阳高度较大B.白昼时间较长 C.大气中云量较少 D.地面温度较高下图表示某地气温(曲线所示)和降水(柱状所示),回答3小题。
4.该地的气候类型是 A.北半球亚热带季风气候 B.北半球地中海气候 C.南半球地中海气候 D.南半球热带草原气候5.气温曲线a部位气温最高的原因是 A.正午太阳高度大,天气晴朗少雨B.太阳直射点位于赤道C.气压带和风带北移D.受高原地形影响6.气温线b部位气温低的原因是A.太阳高度角小B.寒流影响C.云雨较多D.海陆位置影响读下图,甲、乙、丙、丁四个地区的气温雷达图和降水柱状图,回答2题。
7.从气候条件考虑,不适宜乙地区的农业地域类型是A.混合农业B.水稻种植业C.乳畜业D.园艺业8.四个地区中,地带性植被为亚热带常绿硬叶林的是A.甲B.乙C.丙D.丁读世界某地气候资料,回答3题。
9.该种气候类型可能分布在A.巴西利亚B.孟买C.新加坡D.首尔10.该地河流A.冬季有断流B.季节变化大C.有凌汛现象D.年际变化小11.该城市规划建设化学工业区的最理想区域位置是A.西北郊B.东北郊C.西南郊D.城区内下面是2019年“五一”节前几天,我国南、北方两地朋友微信对话截图,根据对话信息回答以下问题。

2019-2020学年河北省石家庄市第二中学高一上学期10月月考数学试题一、单选题1.设集合{}31,A n n k k ==-∈Z ,{}13B x x =-≤,则A B =( )A.{}1,2-B.{}2,1,1,2,4--C.{}1,4D.∅【答案】A【解析】解出集合B ,再根据交集的定义得出A B .【详解】解不等式13x -≤,即313x -≤-≤,解得24x -≤≤,则{}24B x x =-≤≤, 因此,{}1,2A B =-,故选:A.【点睛】本题考查集合的交集运算,同时也考查了绝对值不等式的解法,考查计算能力,属于基础题.2.下列四个函数中,在(0,)+∞上为增函数的是( ) A .()3f x x =- B .2()3f x x x =- C .()f x x =- D .1()1f x x =-+ 【答案】D【解析】根据常见函数的性质判断函数的单调性即可. 【详解】对于A :函数在R 递减,不符合题意; 对于B :函数的对称轴是x 32=,在(0,32)递减,不合题意;对于C :函数在(0,+∞)递减,不合题意;对于D :函数在(-1,+∞)递增,所以在(0,+∞)满足递增,符合题意; 故选:D . 【点睛】3.函数()g x x=的定义域为( )A.()(]2,00,1-UB.[)(]2,00,1-⋃ C.()(]1,00,1-U D.[)(]1,00,2-U【答案】B【解析】根据求函数定义域的基本原则列不等式组求出实数x 的取值范围,即可得出函数()y g x =的定义域. 【详解】由题意得220x x x ⎧--+≥⎨≠⎩,即2200x x x ⎧+-≤⎨≠⎩,解得21x -≤≤且0x ≠,因此,函数()y g x =的定义域为[)(]2,00,1-⋃,故选:B. 【点睛】本题考查具体函数定义域的求解,解题时要熟悉几条求函数定义域的基本原则,根据条件列出不等式求出自变量的取值范围,考查计算能力,属于基础题.4.已知集合A ={x|-3x<0},B ={1,a},且A∩B 有4个子集,则实数a 的取值范围是( ) A .(0,3) B .(0,1)∪(1,3) C .(0,1)D .(-∞,1)∪(3,+∞) 【答案】B【解析】试题分析:∵有4个子集,∴有2个元素,∴,∴且,即实数的取值范围是,故选B .【考点】本题主要考查集合的关系.5.若函数()125-=-f x x ,且()216f a -=,则a 等于( ) A.114B.74C.43D.73【答案】A【解析】利用换元法求出函数()y f x =的解析式,然后由()216f a -=求出a 的值.设1t x =-,则1x t =+,()()21523f t t t ∴=+-=-, 则()()212213456f a a a -=--=-=,解得114a =,故选:A. 【点睛】本题考查函数解析式的应用,利用换元法求出函数的解析式是解题的关键,考查运算求解能力,属于基础题.6.若函数()221f x x mx =-+在[)3,4上是单调函数,则实数m 的取值范围为( )A.3m ≤B.5m ≥C.3m ≤或4m ≥D.3m ≥【答案】C【解析】得出函数()y f x =的对称轴方程,对该函数的对称轴与区间[)3,4分三种位置进行讨论,分析函数()y f x =在区间[)3,4上的单调性,可得出实数m 的取值范围. 【详解】二次函数()221f x x mx =-+的图象开口向上,对称轴为直线x m =.①当3m ≤时,函数()221f x x mx =-+在区间[)3,4上单调递增,合乎题意;②当34m <<时,函数()221f x x mx =-+在区间[)3,m 上单调递减,在区间(),4m 上单调递增,此时,函数()y f x =在区间[)3,4上不单调,不合乎题意; ③当4m ≥时,函数()221f x x mx =-+在区间[)3,4上单调递减,合乎题意.综上所述,实数m 的取值范围是3m ≤或4m ≥,故选:C. 【点睛】本题考查二次函数的单调性与参数,解题时要分析二次函数图象的开口方向和对称轴,再者就是要讨论对称轴与定义域的位置关系,考查分类讨论思想的应用,属于中等题. 7.已知函数()()22435f x ax a x =+-+在区间(),3-∞上是减函数,则a 的取值范围是( ) A.30,4⎛⎫ ⎪⎝⎭B.3,4⎛⎤-∞ ⎥⎝⎦C.30,4⎡⎫⎪⎢⎣⎭D.30,4⎡⎤⎢⎥⎣⎦【答案】D【解析】分0a =、0a >、0a <三种情况,在0a ≠的前提下,讨论二次函数()y f x =图象的对称轴与定义域的位置关系,分析函数的单调性,可求出实数a 的取值范围.当0a =时,()125f x x =-+,此时,函数()y f x =在区间(),3-∞上是减函数,合乎题意;当0a >时,二次函数()y f x =的图象开口向上,对称轴为直线3ax a-=,若函数()y f x =在区间(),3-∞上是减函数,则33aa -≥,解得304a <≤; 当0a <时,二次函数()y f x =的图象开口向下,对称轴为直线30ax a-=<. 则函数()y f x =在区间3,a a -⎛⎫-∞ ⎪⎝⎭上单调递增,在3,3a a -⎛⎫⎪⎝⎭单调递减, 此时,函数()y f x =在区间(),3-∞上不单调,不合乎题意. 综上所述,实数a 的取值范围是30,4⎡⎤⎢⎥⎣⎦,故选:D.【点睛】本题考查二次函数的单调性与参数,解题时要分析二次函数图象的开口方向和对称轴,再者就是要讨论对称轴与定义域的位置关系,考查分类讨论思想的应用,属于中等题.8.函数()5f x =的单调减区间是( )A.[]1,2B.[]1,0-C.[]0,2D.[)1,+∞【答案】A【解析】先求出函数()y f x =的定义域,分离出内层函数22u x x =-和外层函数5y =,并分析内层函数和外层函数的单调性,利用同增异减法得出函数()y f x =的单调减区间.【详解】由220x x -≥,即220x x -≤,解得02x ≤≤,内层函数为22u x x =-,外层函数为5y =,内层函数22u x x =-的增区间为[]0,1,减区间为[]1,2,外层函数5y =为增函数,由复合函数同增异减法可知,函数()5f x =的单调减区间是[]1,2,故选:A. 【点睛】调区间时,要注意求出函数的定义域,要在函数定义域内得出单调区间,否则得到的单调区间无意义,考查分析问题和解决问题的能力,属于中等题.9.如图,不规则四边形ABCD 中,AB 和CD 是线段,AD 和BC 是圆弧,直线l AB ⊥于E ,当l 从左至右移动(与线段AB 有公共点)时,把四边形ABCD 分成两部分,设AE x =,左侧部分面积为y ,则y 关于x 的图像大致为( )A .B .C .D .【答案】C【解析】试题分析:直线l 从A 到D 的移动过程中,面积在增大并且面积的增大率在增加,即函数的导数为正且在变大,直线l 从D 到C 的移动过程中,面积在增大,但面积的增大率不变,所以导数为正的常数,直线l 从C 到B 的增大过程中,面积在增大,但面积的增大率在减小,所以导数为正但逐渐减小,综上可得函数为增函数,且函数的导数先增大后不变再减小,C 项符合要求 【考点】函数导数的几何意义及瞬时变化率 点评:函数在某点处的导数值等于该点处的切线斜率10.已知函数()32f x x =-,()2g x x =,构造函数()()()()()()(),,g x f x g x F x f x f x g x ⎧≥⎪=⎨<⎪⎩,那么函数()y F x =( ) A .有最大值1,最小值﹣1 B .有最小值﹣1,无最大值 C .有最大值1,无最小值 D .有最大值3,最小值1【答案】C【解析】根据函数()F x 的定义令()()0g x f x -≥,可得函数()y F x =的解析式,作函数的图象即可求解. 【详解】由()()2320g x f x x x -=-+≥得,1x ≥;故()21321x x F x x x ⎧≤⎪=⎨-≥⎪⎩,,,故可作()21321x x F x x x ⎧≤⎪=⎨-≥⎪⎩,,的图象如下,通过图象观察可得有最大值1,没有最小值,故选C . 【点睛】本题考查了函数的图象的应用,准确得到函数的解析式作出函数的图象是解题的关键,属于中档题.11.已知偶函数()f x 对于任意x ∈R 都有()()1f x f x +=-,且()f x 在区间[]0,1上是单调递增,则()6.5f -、()1f -、()0f 的大小关系是( ) A.()()()0 6.51f f f <-<- B.()()()6.501f f f -<<- C.()()()1 6.50f f f -<-< D.()()()10 6.5f f f -<<-【答案】A【解析】利用题中等式推导出函数()y f x =是以2为周期的周期函数,由函数的周期性和奇偶性得出()()6.50.5f f -=,()()11f f -=,再利用函数()y f x =在区间[]0,1上的单调性可得出()6.5f -、()1f -、()0f 三个数的大小关系.【详解】 对任意的x ∈R ,()()1f x f x +=-,()()()21f x f x f x ∴+=-+=,所以,函数()y f x =是周期为2的周期函数,又函数()y f x =为偶函数,()()()6.50.50.5f f f -=-=,()()11f f -=, 函数()y f x =在区间[]0,1上单调递增,所以,()()()00.51f f f <<,即()()()0 6.51f f f <-<-,故选:A.【点睛】本题考查利用奇偶性和周期性比较函数值的大小关系,要充分利用周期性和奇偶性将自变量置于同一单调区间,考查分析问题和解决问题的能力,属于中等题. 12.已知函数2()24(03)f x ax ax a =++<<,若12x x <,121x x a +=-,则 A.12()()f x f x < B.12()()f x f x =C.12()()f x f x >D.1()f x 与2()f x 的大小不能确定【答案】A 【解析】【详解】故选A.二、填空题13.已知函数()f x 是定义在R 上的奇函数,当(),0x ∈-∞时,()3221f x x x =+-,则当()0,x ∈+∞时,()f x =______.【答案】3221x x -+【解析】设()0,x ∈+∞,求出()f x -的表达式,再利用奇函数的定义得出()()f x f x =--,可得出函数()y f x =在()0,∞+上的解析式.【详解】设()0,x ∈+∞,则(),0x -∈-∞,则()()()32322121f x x x x x -=⋅-+--=-+-,函数()y f x =是R 上的奇函数,则当()0,x ∈+∞时,()()3221f x f x x x =--=-+.故答案为:3221x x -+. 【点睛】本题考查奇函数的解析式,利用对称转移法求解,首先先设自变量x 在所求区间,然后求出()f x -的表达式,再利用奇函数的定义()()f x f x =--可得出结果,考查运算求解能力,属于中等题.14.设函数()f x 对0x ≠的一切实数都有2019()2()3f x f x x+=,则(2019)f =___________【答案】-2017【解析】分别令1x =和2019x = 代入等式,解方程组得到()2019f 的值. 【详解】1x =时,()()1220193f f +=,当2019x =时,()()2019216057f f +=即()()()()12201932019216057f f f f ⎧+=⎪⎨+=⎪⎩ ,解得()20192017f =-.故填:-2017. 【点睛】本题考查了利用方程组求解析式,属于简单题型,一般求解析式的方法分为: 1.待定系数法,适应于已知函数类型;2.代入法,适用于已知()f x 的解析式,求()f g x ⎡⎤⎣⎦的解析式;3.换元法,适用于已知()f g x ⎡⎤⎣⎦的解析式,求()f x 的解析式;4.方程组法,适用于已知()f x 和1f x ⎛⎫⎪⎝⎭的方程,或()f x 和()f x -的方程. 15.已知函数()()24f x x g x =+,()g x 为奇函数且()f x 在区间11,22⎡⎤-⎢⎥⎣⎦上的最大值与最小值分别为M 和m ,则M m +=______. 【答案】8【解析】先推导出函数()y f x =的图象关于点()0,4对称,可得出函数()y f x =在区间11,22⎡⎤-⎢⎥⎣⎦上的最高点和最低点也关于点()0,4对称,由此可得出M m +的值. 【详解】函数()y g x =为奇函数,则()()g x g x -=-,()()()()2244f x x g x x g x ∴-=+-⋅-=-⋅,则()()8f x f x +-=,所以,函数()y f x =的图象关于点()0,4对称,则函数()y f x =在区间11,22⎡⎤-⎢⎥⎣⎦上的最高点和最低点也关于点()0,4对称,因此,8M m +=,故答案为:8. 【点睛】本题考查函数对称性的应用,利用题中等式推导出函数的对称性是解题的关键,考查分析问题和解决问题的能力,属于中等题.16.已知函数()2,04442,4x x f x x x ⎧-<≤⎪=⎨⎪->⎩,函数()()0h x x ≠为偶函数,且当0x >时,()()h x f x =,若()()2h t h >,则实数t 的取值范围为______.【答案】()()2,00,2-【解析】判断出函数()y h x =在()0,∞+上为减函数,再由该函数为偶函数,结合()()2h t h >可得出2t t ⎧<⎨≠⎩,解出即可得出实数t 的取值范围.【详解】当0x >时,()2,044x x h x ⎧-<≤⎪=⎨⎪,易知函数()y h x =在区间(]0,4和()4,+∞上均为减函数,又函数()y h x =在()0,∞+上连续,所以,函数()y h x =在()0,∞+上为减函数,函数()()0y h x x =≠为偶函数,由()()2h t h >,得()()2h t h >,20t t ⎧<∴⎨≠⎩,解得22t -<<且0t ≠,因此,实数t 的取值范围是()()2,00,2-,故答案为:()()2,00,2-.【点睛】本题考查利用函数的单调性与奇偶性解不等式,在涉及到偶函数的性质时,可充分利用性质()()h x h x =,可简化分类讨论,考查运算求解能力,属于中等题.17.如图1是某公共汽车线路收支差额y 元与乘客量x 的图象.由于目前本条线路亏损,公司有关人员提出了两种扭亏为赢的方案,根据图1上点A 、点B 以及射线AB 上的点的实际意义,用文字说明图2方案是______,图3方案是______.【答案】降低成本,票价不变 增加票价【解析】观察函数的图象可知,函数图象上的横坐标表示乘客量,纵坐标表示收支差额,结合图象可得出结论. 【详解】由图1可知,点A 表示无人乘车时收支差额为20-元,点B 表示有10人乘车时收支差额为零,线段AB 上的点表示亏损,AB 延长线上的点表示盈利.对于图2而言,与图1相比,两个一次函数的一次项系数没变,但无人乘车时收支差额变为10-元,差距在减少,则图2的方案是降低成本,票价不变;对于图3而言,与图1相比,图3对应的一次函数一次项系数增大了,但无人乘车时收支差额仍是20-元,则图3的方案是增加票价. 故答案为:降低成本,票价不变;增加票价. 【点睛】题中的意义,理解问题的叙述过程是解题的关键,考查分析问题和解决问题的能力,属于中等题.三、解答题18.已知集合{}2430A x x x =-+<,集合{}21B x m x m =≤≤-. (1)当1m =-时,求A B ;(2)若AB =∅,求实数m 的取值范围.【答案】(1){}23x x -≤<;(2)[)0,+∞.【解析】(1)解出集合A ,再将1m =-代入集合B ,再利用并集的定义求出集合AB ;(2)分B =∅和B ≠∅两种情况讨论,在B ≠∅的前提下,由题意得出11m -≤或23m ≥,由此可得出实数m 的取值范围.【详解】(1)解不等式2430x x -+<,得13x <<,{}13A x x ∴=<<, 当1m =-时,{}22B x x =-≤≤,因此,{}23A B x x ⋃=-≤<; (2)当B =∅时,21m m >-,得13m >,此时,A B =∅成立; 当B ≠∅时,21m m ≤-,得13m ≤, A B ⋂≠∅Q ,则11m -≤或23m ≥,解得0m ≥或32m ≥,此时,103m ≤≤. 综上所述,实数m 的取值范围是[)0,+∞. 【点睛】本题考查集合的并集运算,同时也考查了利用交集的运算结果求参数的取值范围,解题时要注意对集合分空集与非空集合两种情况讨论,考查分类讨论思想,考查运算求解能力,属于中等题.19.二次函数()f x 满足()()12f x f x x +-=,且()01f =. (1)求()f x 的解析式;(2)若在区间[]1,2上,不等式()2f x mx >恒成立,求实数m 的取值范围. 【答案】(1)()21f x x x =-+;(2)1,2⎛⎫-∞ ⎪⎝⎭. 【解析】(1)设()2f x ax bx c =++,由()01f =得出1c =,根据等式()()12f x f x x +-=列关于a 、b 的方程组,解出这两个未知数,可得出函数()y f x =的解析式;(2)当[]1,2x ∈时,由()2f x mx >利用参变量分离法得出121m x x<+-,并利用定义法证明出函数()11g x x x=+-在区间[]1,2上的单调性,求出函数()y g x =在区间[]1,2上的最小值,可求出实数m 的取值范围.【详解】(1)设()2f x ax bx c =++,则()01f c ==.()()()()()221111122f x f x a x b x ax bx ax a b x ⎡⎤+-=++++-++=++=⎣⎦,220a a b =⎧∴⎨+=⎩,解得11a b =⎧⎨=-⎩,因此,()21f x x x =-+; (2)当[]1,2x ∈时,由()2f x mx >,得221mx x x <-+,得121m x x<+-, 构造函数()11g x x x=+-,[]1,2x ∈,下面证明函数()y g x =在区间[]1,2上的单调性.任取1x 、[]21,2x ∈,且12x x <,即1212x x ≤<≤, 则()()()1212121212111111g x g x x x x x x x x x ⎛⎫⎛⎫⎛⎫-=+--+-=-+- ⎪ ⎪ ⎪⎝⎭⎝⎭⎝⎭()()()()1212211212121212111x x x x x x x x x x x x x x x x --⎛⎫-=-+=--=⎪⎝⎭, 1212x x ≤<≤Q ,120x x ∴-<,1210x x ->,120x x >,()()12g x g x ∴<,所以,函数()11g x x x=+-在区间[]1,2上单调递增,则()()min 11g x g ==,21m ∴<,解得12m <,因此,实数m 的取值范围是1,2⎛⎫-∞ ⎪⎝⎭.【点睛】本题考查利用待定系数法求二次函数的解析式,同时也考查了利用不等式恒成立问题求参数的取值范围,在含单参数的不等式中,利用参变量分离法进行求解,可避免分类讨论,考查分析问题和解决问题的能力,属于中等题.20.已知函数y =f (x )在定义域[-1,1]上既是奇函数,又是减函数. (1)求证:对任意x 1,x 2∈[-1,1],有[f (x 1)+f (x 2)]·(x 1+x 2)≤0; (2)若f (1-a )+f (1-a 2)<0,求实数a 的取值范围. 【答案】(1)见解析;(2)0≤a <1.【解析】试题分析:(1)由x 2∈[﹣1,1],可得﹣x 2∈[﹣1,1],利用函数y=f (x )在定义域[﹣1,1]上是奇函数,又是减函数,即可证明结论;(2)f (1﹣a )+f (1﹣a 2)<0,等价于a 2+a ﹣2<0,即可求出实数a 的取值范围. 解析:(1)证明:若x 1+x 2=0,显然不等式成立. 若x 1+x 2<0,则-1≤x 1<-x 2≤1,因为f (x )在[-1,1]上是减函数且为奇函数, 所以f (x 1)>f (-x 2)=-f (x 2),所以f (x 1)+f (x 2)>0. 所以[f (x 1)+f (x 2)](x 1+x 2)<0成立. 若x 1+x 2>0,则1≥x 1>-x 2≥-1, 同理可证f (x 1)+f (x 2)<0.所以[f (x 1)+f (x 2)](x 1+x 2)<0成立.综上得证,对任意x 1,x 2∈[-1,1],有[f (x 1)+f (x 2)]·(x 1+x 2)≤0恒成立. (2)因为f (1-a )+f (1-a 2)<0⇔f (1-a 2)<-f (1-a )=f (a -1),所以由f (x )在定义域[-1,1]上是减函数,得22211102{11 1 {02 1120a a a a a a a a -≤-≤≤≤-≤-≤⇒≤≤->-+-<解得0≤a <1.点睛:本题考查奇偶性与单调性的综合,考查学生分析解决问题的能力,属于中档题.解抽象函数不等式问题时,一般利用函数的奇偶性,和单调性转化为括号内的自变量的大小关系的比较。

石家庄二中2022级高一年级10月份月考化学试题(答案在最后)满分:100分考试时间:50分钟可能用到的相对原子质量:S 32 N 14 Na 23 I 127一、选择题(每题只有一个选项符合题意。
1-21题每题2分,22-25题每题3分,共54分。
)1.下列体系不属于分散系的是( )A.碘酒B.冰水C.泥浆D.鸡蛋清2.下列物质中,其水溶液能导电,但本身属于非电解质的是( )A.金属铁B.SO2C.酒精D.硫酸钡晶体3.下列装置工作原理与氧化还原反应无关的是( )A.臭氧消毒柜B.甲烷燃料电池C.太阳能集热器D.燃气灶4.下列电离方程式中,正确的是()A.Ca(OH)2=Ca2++OH-B.H2CO 32H++CO32-C.Na2O2=2Na++2O2-D.Al2(SO4)3=2Al3++3SO42-5.某中德联合研究小组设计制造了一种“水瓶”,用富勒烯(C60)的球形笼子作“瓶体”,一种磷酸盐作“瓶盖”,恰好可将一个水分子关在里面。
下列说法正确的是( ) A.“水瓶”、冰水混合物、CuSO4•5H2O都是混合物B.金刚石、石墨和C60互称为同素异形体,具备相同的性质C.磷酸钙可溶于水,水溶液能导电D.一定条件下石墨转化为C60是化学变化,属于有单质参加的非氧化还原反应6.下列关于胶体的认识正确的是( )A.纳米材料粒子直径一般从几纳米到几十纳米(1nm=10-9m),因此纳米材料属于胶体B.丁达尔效应可用于区别溶液和胶体,云、雾均能产生丁达尔效应C.将一束强光通过淀粉溶液,不能产生丁达尔效应D.空气中PM2.5(2.5微米以下的颗粒物)的存在能够形成丁达尔效应7.一种制备的流程如图所示,下列关于该流程的说法错误的是( )A.该流程中可循环利用的物质有CaCO3B.该流程不涉及氧化还原反应C.生石灰和熟石灰都能溶于稀盐酸,均属于碱性氧化物D.由制备流程可知,该流程中既含有化合反应,又含有分解反应8.下列离子方程式改写成化学方程式正确的是( )A.Mg2++2OH-=Mg(OH)2↓ MgSO4+Ba(OH)2=Mg(OH)2↓+BaSO4↓B.Fe+Cu2+=Fe2++Cu Fe+Cu(OH)2=Fe(OH)2+CuC.Ag++Cl-=AgCl↓ AgNO3+HCl=AgCl↓+HNO3D.CO2+2OH-=CO32-+H2O CO2+Ca(OH)2=CaCO3↓+H2O9.氧气转炉炼钢工艺可以利用废氧化铁经过必要的造球、码垛堆集或烧结工艺处理。

石家庄二中2022级高一年级10月份月考物理试题(答案在最后)一、单选题(1~8题为单选题,每题4分,共32 分)1、第24届冬奥会中的四个比赛项目,下列研究的问题中可把运动员视为质点的是( )A .研究U 型池技巧运动员的空中转体B .研究花样滑冰运动员的艺术表现C .研究短道速滑运动员的入弯道技术D .研究雪橇运动员的运动快慢2、关于速度、速度变化量、加速度,下列说法正确的是( )A .物体运动时,速度的变化量越大,它的加速度一定越大B .速度很大的物体,其加速度可能为零C .某时刻物体的速度为零,其加速度不可能很大D .加速度很大时,运动物体的速度一定很快变大3、如图所示,弹簧质量不计,劲度系数k =400 N/m,一端固定在P 点,另一端悬挂质量为1 kg 的物体M ,当M 静止时,弹簧的长度为10 cm,若将M 换为质量为2 kg 的物体N ,则N 静止时,弹簧的长度为(弹簧始终在弹性限度内,g =10 m/s 2) ( )A.10 cmB.12.5 cmC.15 cmD.20 cm4、物体以初速度v 0做匀减速直线运动,第1 s 内通过的位移为x 1=3 m ,第2 s 内通过的位移为x 2=2 m ,又经过位移x 3物体的速度减小为0,则下列说法中不正确...的是( ) A .加速度a 的大小为1 m/s 2B .初速度v 0的大小为2.5 m/sC .位移x 3的大小为98m D .位移x 3内的平均速度大小为0.75 m/s 5、在恶劣天气中,能见度很低,甲、乙两汽车在一条平直的单行道上,甲在前、乙在后同向行驶.某时刻两车司机听到前方有事故发生的警笛提示,同时开始刹车,两车刹车后的v -t 图像如图所示,下列说法正确的是( )A.甲车的加速度大于乙车的加速度B.若t=24 s时两车未发生碰撞,则此时两车相距最远C.为避免两车发生碰撞,开始刹车时两车的间距至少为48 mD.若两车发生碰撞,则可能是在开始刹车24 s以后的某时刻发生的6、甲、乙两物体从同一点出发且在同一条直线上运动,它们的位移—时间(x-t)图像如图所示,由图像可以看出在0~4 s内()A.甲、乙两物体始终同向运动B.第2 s末,甲、乙两物体间的距离最大C.甲的平均速度大于乙的平均速度D.乙物体一直做匀加速直线运动7、一个做匀加速直线运动的物体,先后经过相距为x的A、B两点时的速度分别为v和7v,从A到B的运动时间为t,则下列说法不正确...的是()A.前t2时间通过的位移比后t2时间通过的位移少1.5vtB.经过AB中间时刻的速度为4vC.通过前x2位移所需时间是通过后x2位移所需时间的2倍D.经过AB中点的速度为4v8、如图所示,位于水平桌面上的物块P,由跨过定滑轮的轻绳与物块Q相连,从滑轮到P和Q的两段绳都是水平的。
河北省石家庄市第二中学2023-2024高一上学期第一次诊断测评化学试题1.最近,华为Mate60 Pro上市,其搭载的新型麒麟9000s芯片,突破了美国的芯片封锁,实现了智能手机5G芯片国产化。
下列有关说法正确的是A.硅是芯片的主要成分之一,晶体硅是一种性能优良的半导体材料,它属于非电解质B.晶体硅和无定形硅是硅元素的同素异形体,二者化学性质完全不同C.光刻胶是制造芯片的关键材料,金属氧化物纳米颗粒光刻胶由金属氧化物纳米簇和溶剂等组成,是一种胶体D.工业粗硅的冶炼方法为SiO 2 +2C Si+2CO↑,在该反应中SiO 2作还原剂2.构建元素化合价和物质类别的二维图是学习化学的一种重要方法。
如图是碳元素的“价—类”二维图,下列说法错误的是A.a点对应的物质不充分燃烧可能得到c点对应的物质B.b点对应的物质不只一种C.c点对应的物质只具有还原性D.d点对应的物质可与碱反应得到f点对应的物质3.宋代著名法医学家宋慈的《洗冤集录》中有“银针验毒”的记载,“银针验毒”的原理是4Ag+2H2S+O2=2X+2H2O,下列说法错误的是A.X的化学式为Ag 2 SB.反应中Ag和H 2 S均是还原剂C.银针验毒时,空气中氧气得电子D.该反应中有三种物质是电解质4.下列各组离子在指定溶液中一定能大量共存的是A.无色溶液中MnO 、NH 、Mg 2+、SO B.在pH=1的溶液中Fe 3+、NO 、SO 、I -C.Na 2 CO 3溶液中OH -、K +、Cl -、SO D.NaHCO 3溶液中OH -、Ba 2+、NO 、Cl -5.下列说法正确的是①由一种元素组成的物质是单质②Al2(SO4)3•12H2O是混合物③含有氧元素的化合物是氧化物④强氧化剂与强还原剂混合一定发生氧化还原反应⑤酸性氧化物都是非金属氧化物⑥根据酸分子中含有H原子个数将酸分为一元酸、二元酸等⑦有单质参加或有单质生成的反应不一定是氧化还原反应⑧碱性氧化物一定是金属氧化物,但金属氧化物不一定是碱性氧化物⑨蔗糖和水分别属于非电解质和电解质⑩盐酸、纯碱、醋酸钠和生石灰分别属于酸、碱、盐和氧化物A.⑦⑧⑨B.①②③④⑤C.①⑧⑨⑩D.⑥⑦⑧⑨6.下列离子方程式书写正确的是(已知还原性强弱顺序:I->Fe2+>Br->Cl-)A.向澄清石灰水溶液中通入过量二氧化碳:Ca 2+ +2OH - +CO 2 =CaCO 3↓+H 2 OB.少量Cl 2通入FeI 2溶液中:Cl 2 +2I - =2Cl - +I 2C.碳酸氢钾溶液中滴少量氢氧化钡溶液:Ba 2+ +HCO +OH - =BaCO 3↓+H 2 OD.碳酸氢钠溶液中滴足量氢氧化钙溶液:Ca 2+ +2HCO +2OH - =CaCO 3↓+CO +2H 2 O7.已知反应:2FeSO4+6Na2O2=2Na2FeO4+2Na2O+2Na2SO4+O2↑,下列关于该反应的说法正确的是A.Na 2 O 2中的氧元素全部被还原B.氧化性:Na 2 O 2<Na 2 FeO 4C.每生成1个Na 2 FeO 4,反应有4个电子转移D.Na 2 O为还原产物8.在复杂的体系中,确认化学反应先后顺序有利于解决问题,下列化学反应先后顺序判断正确的是(已知氧化性强弱顺序:Cl2>Br2>Fe3+>I2)A.在含CO 、SO 、OH -的溶液中逐滴加入硫酸氢钠溶液:SO 、CO 、OH -B.含等量的FeBr 2、FeI 2的溶液中,缓慢通入氯气:I -、Br -、Fe 2+C.含等量的Ba(OH) 2、KOH的溶液中,缓慢通入CO 2:KOH、Ba(OH) 2D.在含Fe 3+、H +、NH 的溶液中逐滴加入烧碱溶液:H +、Fe 3+、NH9.已知2MO+5S2-+16H+=2M2++5S↓+8H2O,则MO中x的值为A.1 B.2 C.3 D.410.在稀硫酸中几种离子的转化关系如图所示:下列说法正确的是A.反应1的氧化剂为Ce 4+,还原产物为Mn 3+B.推测不可发生反应:Ce 4+ +Fe 2+ =Ce 3+ +Fe 3+C.反应3的离子方程式为:Fe 3+ +2I - =I 2 +Fe 2+D.氧化性由强到弱的顺序为:Ce 4+ >Mn 3+ >Fe 3+ >I 211.下列说法错误的是A.已知硝酸铵在400℃以上时,剧烈分解发生爆炸:4NH 4 NO 3 =3N 2↑+2NO 2↑+8H 2 O,其中被氧化的氮原子和被还原的氮原子的个数之比为1:1B.4Zn+10HNO 3 =4Zn(NO 3 ) 2 +NH 4 NO 3 +3H 2 O中,氧化剂和还原剂个数之比为5:2C.3I 2 +6KOH 5KI+KIO 3 +3H 2 O中,被氧化和被还原的碘原子个数之比为1:5D.2FeS+6H 2 SO 4 (浓) Fe 2 (SO 4 ) 3 +3SO 2↑+2S↓+6H 2 O中,反应中发生氧化反应和发生还原反应的硫原子个数之比为2:312.对于下列事实和相应解释有错误的是13.对于反应14CuSO4+5FeS2+12H2O=7Cu2S+5FeSO4+12H2SO4(FeS2中S为-1价),下列结论正确的是A.FeS 2既不是氧化剂,又不是还原剂B.Cu 2 S既是氧化产物,又是还原产物C.被氧化的硫和被还原的个数比是7:3D.被CuSO 4氧化的硫占全部被氧化的硫的14.小明为探究金属与盐的反应,将一定质量的某种金属的粉末放入与的混合溶液中,充分反应后发现,溶液呈现无色,溶液底部有少量固体粉末;过滤后在滤渣和滤液中分别加入适量稀盐酸,滤渣中有无色气体产生,滤液中无沉淀产生。
石家庄二中2013-2014学年第一学期十二月月考化学试题2013-12-3 可能用到了相对原子质量:H—1 C—12 N—14 O—16 Na—23 Mg—24 Al—27 Cl—35.5 K—39 Ca—40 Mn—55 Fe—56 Cu—64 Zn—65 Br—80 Ag—108第Ⅰ卷 (选择题共40分)一、选择题(本题包括20小题,每小题2分,共40分,每小题只有一个正确答案)1.下列说法不正确...的是 ( )A.蛋白质及其水解产物均是两性化合物B.用新制的Cu(OH)2可鉴别乙醇、乙醛和乙酸C.植物油的不饱和程度比动物油高,植物油更易氧化变质D.淀粉和纤维素均可用(C6H10O5)n表示,二者互为同分异构体2.下列说法正确的是( )A.右图可表示水分解过程中的能量变化B.若2C(s)+O2(g)=2CO(g) △H= -221.0 kJ/mol,则碳的燃烧热为110.5 kJ/molC.需要加热的反应一定是吸热反应,常温下能发生的反应一定是放热反应D.已知:Ⅰ:对于反应:H2(g)+Cl2(s)=2HCl (g)△H= - a kJ/mol,b kJ / mol且a、b、c均大于零,则断开1 mol H-Cl键所需的能量为- a-b-c3.下列叙述正确的是()A.Li在氧气中燃烧只生成Li2OB.将SO2通入过量BaCl2溶液可生成BaSO3沉淀C.新制氯水显酸性,向其中滴加少量紫色石蕊试液,充分振荡后溶液呈红色D.将稀硫酸滴加到Fe(NO3)2溶液中无明显现象4.用N A表示阿伏加德罗常数的值。
下列叙述正确的是( )A.常温常压下的33.6L氯气与27g铝充分反应,转移电子数为3N AB.标准状况下,22.4L己烷中共价键数目为19N AC.由CO2和O2组成的混合物中共有N A个分子,其中的氧原子数为2N AD.1mol Na2O2固体中含有O22-2 N A5. 用48 mL 0.1 mol/L的FeSO4溶液,恰好还原2.4×10-3 mol [RO(OH)2]+,则R元素的最终价态为() 价。
【良师益友】高一化学同步教学资源(人教版2019必修第一册)第三章 铁 金属材料第二节 金属材料第2课时 物质的量在化学方程式计算中的应用学校:___________班级:___________姓名:___________一、单选题1.将一定质量的铁片放入4100mLCuSO 溶液中,待充分反应后取出铁片,洗净后称量,发现铁片比原来增加了0.2g ,则该4CuSO 溶液的物质的量浓度为( ) A .10.25mol L -⋅B .10.1mol L -⋅C .10.15mol L -⋅D .11mol L -⋅2.一定量的镁和氧化镁的混合物中镁元素的质量分数为72%,取10g 加入足量的稀硫酸溶液,再向溶液中加入足量的氢氧化钠溶液,得到沉淀的质量为( ) A .17.4gB .10gC .7.2gD .5g3.设N A 为阿伏加德罗常数的值。
下列说法正确的是( ) A .标准状况下,1 mol 水的体积为22.4 LB .常温常压下,7.8 g 过氧化钠中含有阴离子的数目为0.2N AC .1.6 g 由氧气和臭氧组成的混合物中含有氧原子的数目为0.1N AD .标准状况下,22.4 L Cl 2与足量的铁充分反应,转移的电子数为3N A基础达标10.现有Fe 、FeO 、23Fe O 的混合物粉末3.44g ,加入含240.05molH SO 的稀硫酸恰好完全溶解,并收集到标准状况下气体224mL 。
向反应后的溶液中滴加KSCN 溶液,无明显变化。
若将4.30g 该混合物在高温下与足量的CO 充分反应,生成2CO 的质量为( )A .2.20gB .1.40gC .1.30gD .1.10g二、填空题11.一块表面已被氧化为氧化钠的钠块17.0 g ,投入50 g 水中,最多能产生0.2 g 气体,则: (1)涉及的化学方程式为 , 。
(2)钠块中钠的质量是 g 。
(3)钠块中氧化钠的质量是 g 。
邢台市八中2017-2018学年第一学期十二月月考高一年级化学试卷试卷满分100分考试时间90分钟命题人:杜翠乔注意事项:1、答题前填写好自己的姓名、班级、考号等信息 2、请将答案正确填写在答题卡上第I卷选择题一、选择题(每题只有一个正确答案,每小题3分,共48分)1、下列物质中符合如图所示阴影部分表示的分类标准是( )A. B.C. D.2、在如图所示电解质溶液的导电性装置中,若向某一电解质溶液中逐滴加入另一种溶液时,则灯光由亮变暗至熄灭后又逐渐变亮的是()A、盐酸中逐滴加入食盐溶液B、醋酸中逐滴加入氢氧化钠溶液C、氢氧化钡溶液中逐滴加入硫酸溶液D、醋酸中逐滴加入氨水3、下列各气体: ① 含个的; ② 标准状况下6.72的; ③3.4的; ④0.5。
四种物质所含的原子总数由少到多的正确顺序是( ) A.①< ③ < ④ < ② B.③< ① < ② < ④C.④< ① < ② < ③D.④< ② < ① < ③4、在水溶液中能大量共存的一组离子是( )A.、、、B.、、、C.、、、D.、、、5、下列化学方程式能用离子方程式表示的是( )A.B.C.D.6、能够用来鉴别、、三种无色溶液的试剂是( )A.溶液B.稀硫酸C.稀盐酸D.澄清石灰水7、下列有关胶体的性质与应用的说法中错误的是( )A.用可见光束照射以区别溶液和胶体B.胶体无色、透明,能产生丁达尔现象C.葡萄糖注射液不能产生丁达尔现象,不属于胶体D.盐卤可用于制豆腐8、下列实验装置图所示的实验操作或实验仪器,不能达到相应实验目的的是( )A.检查容量瓶是否漏水B.量取8.5盐酸C.向容量瓶中转移液体D.称量2.19、设代表阿伏加德罗常数,下列说法不正确的( )A. 在质量以克为单位时,醋酸的摩尔质量与个醋酸分子的质量在数值上相等B.个氧分子和个氢分子的质量比等于161C.28克氮气所含的原子数目为D. 在标准状况下,0. 5 个氯气分子所占体积约是11. 2升10、中含有个氢原子,则阿伏加德罗常数为( )A. B.C. D.11、以水为分散剂的分散系,按粒子直径由大到小的顺序排列的是()A. 溶液、胶体、浊液B. 浊液、胶体、溶液C. 胶体、浊液、溶液D. 浊液、溶液、胶体12、将饱和FeCl3溶液分别滴入下列溶液或水中,能形成胶体的是()A.冷水B.煮沸的蒸馏水C.NaOH浓溶液D.NaCl浓溶液13、下列溶液中物质的量浓度最大的是( )A.100 2B.1000 1. 5C.2501D.300514、粗盐中含有少量的、、等杂质,现采用①②③来除杂则这三种试剂添加的顺序为( )A.①②③B.③②①C.①③②D.②①③15、用表示阿伏加德罗常数的值,下列说法中正确的是( )A.1 所含有的原子数为B.标准状况下, 22.4 水中含有的水分子数为C.标准状况下,22.4 氯化氢所含的原子数为D.24分子和24分子所含的氧原子数目均为1.516、下列离子方程式正确的是( )A.铁片与氯化铜溶液反应:Fe +Cu2+ = Cu +Fe2+B.铁与稀硫酸反应:2Fe +6H+ = 2Fe3+ +3H2↑C.氢氧化镁溶于盐酸:Mg(OH)2+H+ = Mg2+ +2H2OD.Ba(OH)2溶液与稀H2SO4反应:Ba2+ + OH- + H+ +SO42- = H2O+BaSO4↓第II卷非选择题二、非选择题(共52分)17、(8分)根据所学知识,回答下列问题:在标准状况下,测得1. 92某气体的体积为672,此气体的相对分子质量为。
考试时间为60分钟总分100分可能用到的相对原子质量: H-1 C-12 N-14 O-16 S-32 Cl-35.5 K-39Fe-56 Cu-64 Al-27 Mg-24一、单选题(每个2分,共40分)1.下列物质中既能跟稀H 2SO 4反应,又能跟氢氧化钠溶液反应的酸式盐是①NaHCO 3 ②Al 2O 3 ③Al(OH)3 ④Al ⑤NaHSO 4 ⑥AlCl 3 ⑦NaAlO 2A. ①②B. ①②③⑥⑦C. ①D.全部2.下列离子方程式正确的是A.钠与水反应:Na+H 2O=Na+OH -+ H 2↑B.AlCl 3 溶液中加过量氨水Al 3++3OH -=Al(OH)3↓C.向氯化亚铁中通入氯气 Fe 2++ Cl 2= Fe3+ + 2Cl - D.铝粉投入到NaOH 溶液 2A1+ 2OH -+ 2H 2O=2AlO 2-+ 3H 2↑3.下列各组在溶液中的反应,无论谁过量,都可以用同一离子方程式表示的是A.Ba(OH)2 与NaHSO 4B.Ba(OH)2 与H 2SO 4C.石灰水和二氧化碳D.Ca(HCO 3)2 与NaOH4. 常温下,下列各组离子在指定溶液中一定能大量共存的是A.常温下pH=10 溶液中: Cl -、SO 42-、Na +、Fe 3+B.使石蕊试液变蓝色的溶液: K +、Ba 2+、NO 3-、I -C.能与Al 反应生成H2 的溶液: NH4+、K +、NO 3-、SO 42-D.加入KSCN 溶液变血红色的溶液中: S 2-、K +、Na +、SO 42-5.设N A 为阿伏加德罗常数,下列说法正确的是①标准状况下,11.2 L 以任意比例混合的氮气和氧气所含的原子数为N A②同温同压下,体积相同的氢气和氩气所含的分子数相等③2 mol/L 的氯化镁溶液中含氯离子为4N A④标准状况下,11.2 LCCl 4所含分子数为0.5N A⑤32gO 2和O 3混合气体中含有原子数为2N AA. ①②③B. ①②⑤C. ①③④D. ①③⑤6.科学家刚刚发现了某种元素的原子,其质量是ag,12C的原子质量是bg,N A是阿伏加德罗常数的值,下列说法不正确的是A.该原子的摩尔质量是aN A g/molB.Wg 该原子的物质的量一定是W/(aN A)molC.Wg该原子中含有W/a 个该原子D.N A=12/a7.在两个容积相同的容器中,一个盛有C2H4气体,另一个盛有N2和CO的混合气体。
在同温同压下,两容器内的气体一定具有相同的①分子数②密度③质量④质子数⑤原子数A. ①④⑤B. ①②⑤C. ③④⑤D. ①②③8.下列实验操作中错误的是A.分液时,分液漏斗下层液体从下口放出,上层液体从上口倒出B.蒸馏时,应使温度计水银球靠近蒸馏烧瓶支管口C.CO2中混有少量HCl气体可用饱和碳酸钠溶液除去D.用蒸馏的方法可将汽油和煤油进行分离9.已知常温下二氯化二硫(S2Cl2)为红棕色液体,(其结构式为Cl-S-S-C1)。
其制备反应及与水反应的化学方程式如下:①CS2+3Cl2CCl4+S2Cl2②2S2Cl2+2H2O=4HCl+SO2+ S↓,则下列说法正确的是A.反应①中CS2作氧化剂B.反应①中每生成lmol S2Cl2转移4mol 电子C.反应②中氧化产物与还原产物的物质的量之比为3:1D.反应②中S2Cl2既作氧化剂又作还原剂10. 将标准状况下的aL.HCl 气体溶于1000g水中,得到的盐酸密度为bg·cm-3,则该盐酸的物质的量浓度是A.a/22.4 mol/LB.ab /22400mol/LC.ab/22400+36.5a mol/LD.1000ab /22400+36.5a mol/L11. 己知在相同条件下,下列几种微粒的还原性强弱顺序为Cl-<Br-<Fe2+<I-<SO2。
由此判断下列反应不能发生的是A.2Fe3++SO2+2H2O =SO42-+4H++2Fe2+B.2Br-+SO42-+4H+= SO2+Br2+2H2OC.2Fe2++2Br-+2Cl2= 2Fe3++Br2+4Cl-D.2Fe3++ 2I-=2Fe2++I212.实验室可将氧气通过高压放电管来制取臭氧:3O2=2O3(反应条件为放电)。
在容积可变的密闭容器中,投入一定量O2可发生上述反应,反应一段时间后,有60%O2发生了转化,则此时O2的体积分数为A.30%B.40%C.50%D.60%13.今有下列三个氧化还原反应: ①2FeCl3+2KI=2FeC12+2KC1+I2,②2FeCl2+Cl2=2FeCl3, ③2KMnO4+ 16HCl(浓)= 2KCl+2MnCl2+8H2O+5Cl2↑。
若某溶液中有Fe2+、I-、Cl-共存,要除去I-而不影响Fe2+和Cl-,则可加入的试剂是A.Cl2B.KMnO4C.FeCl3D.HCl14.以下物质之间的每步转化中,都能通过一步实现的是①Fe→FeCl2→Fe(OH)2→Fc(OH)3②Na→Na2O→Na2CO3→NaHCO3→NaOH③Mg→MgCl2→Mg(OH)2④A1→Al2O3→A1(OH)3⑤A1→NaAlO2→Na2CO3A. ②③④B. ①③④⑤C. ①②③⑤D. ①②③④⑤l5.下列关于氧化性、还原性的判断正确的是A.B 的阳离子的氧化性比A 的阳离子强,说明A 元素的金属性一定比B 元素强B.发生氧化还原反应时,A 原子失去电子比B 原子多,则A 的金属性一定比B 强C.将少量Na2O2固体加入滴有酚酞的水中,溶液变为红色D.一定量的氯气通入30mL 10.00 mol/L 的氢氧化钠溶液中,加热后形成NaCl、NaClO、NaClO3共存的溶液,若反应中转移的电子为n mol,则0.15<n<0.2516.下列示意图与对应的反应情况正确的是A. Fe(NO3)3、Cu(NO3)2、HNO3 混合溶液中逐渐加入铁粉B.NaCO3、NaHCO3溶液中逐滴加入HClC.KAl(SO4)2溶液中逐滴加入Ba(OH)2溶液D.NaAlO2溶液中逐渐通入CO217.下列实验中,对应的现象及结论都正确且两者具有因果关系的是18.下列除杂或检验的方法正确的是A.向溶液中加入稀硝酸再加入氯化钡溶液产生白色沉淀说明有SO42-B.在溶液中加KSCN,溶液显红色,证明原溶液中有Fe3+,无Fe2+C.向溶液中加入过量的氨水先产生白色胶状沉淀后沉淀溶解说明有Al3+D.灼烧某白色粉末,火焰呈黄色,证明原粉末中含有Na+,无法确定是否含K+19.把200mLK2CO3和NH4HCO3的混合溶液分成四等份,取一份加入含0.35mo1HCl的盐酸恰好反应完全,另取一份加入含0.3 mol 氧氧化钾的溶液恰好反应完全,则该混合溶液中c (K+) 为A.1mol/LB.2 mol/LC.3 mol/LD.4 mol/L20.将百分比浓度为a%,物质的量浓度为c1 mol/L的NaC1稀溶液蒸发掉一定量的水,使之质量分数为2a%,此时物质的量浓度为c2 mol/L,则c1和c2的数值关系是A.c1>2c2B.c1<2c2C.c1<c2/2D.c1>c2/2二、选择题(每题3 分,共15 分)21.今有一混合物的水溶液,可能含有以下离子中的若干种: K+、NH4+、Cl-、Mg2+、Ba2+、CO32-、SO42-,现取三份100mL 该溶液进行如下实验:(1) 第一份加入AgNO3溶液有沉淀产生(2) 第二份加足量NaOH 溶液加热后,收集到气体0.04mol(3) 第三份加足量BaCl2溶液后,得干燥沉淀6.27g,经足量盐酸洗涤干燥后,沉淀质量为2.33g.根据上述实验,以下推测正确的是①K+一定存在②100mL 溶液中含0.01mol CO32-③Cl-可能存在④Ba2+一定不存在,Mg2+可能存在A. ①②③B. ①③C. ①②④D. ②③22.烧杯中盛有100mL1mo/L的NaHSO4溶液,向其中逐滴滴加1mol/L 的Ba(OH)2溶液,烧杯中某些物质(或微粒) 的物质的量的变化曲线如图。
下列说法中正确的是A.曲线a表示Na+的物质的量的变化B.曲线c 表示Ba2+的物质的量的变化C.加入50 mL Ba(OH)2溶液时反应的离子方程式为Ba2++2OH-+2H++SO42-= BaSO4↓+2H2OD.加入Ba(OH)2溶液体积大于50 mL后,反应的离子方程式为OH-+H+=H2O23.向一定量的NaOH 容液中逐滴加入AlCl3溶液,生成沉淀Al(OH)3的量随AlCl3加入量的变化关系如图所示。
则下列离子组在对应的溶液中一定能大量共存的是A.a点对应的溶液中: Na+、Fe3+、SO42-、HCO3-B.b点对应的溶液中: Na+、S2-、SO42-、Cl-C.c点对应的溶液中: Ag+、Ca2+、NO3-、F-D.d 点对应的溶液中: K+、NH4+、I-、CO32-24.一定条件下,硫的某种含氧酸H2SO x(x≤4)与H2S 可发生如下反应:H2S+H2SO x-----S+ (x-3)SO2+H2O(未配平)下列推断合理的是A.该反应中,一定有SO2B.该反应中,H2S作还原剂,H2SO x作氧化剂C.若x=3,则还原剂与氧化剂的物质的量之比为1:1D.若x=4,每生成1molS,转移的电子为6mol25.amolFeS 与bmo1FeO投入到VL c mol/L 的硝酸溶液中充分反应,产生NO气体,所得澄清溶液成分可看作是Fe(NO3)3、H2SO4混合液,则反应中未被还原的硝酸可能为①(3a+3b)mol ②[ Vc-(9a+b)/3]mol ③Vc-(a+b)/3 mol ④(a+b)×189gA. ①②④B. ①②C. ②④D. ②③④三、填空题(共4个小题,共45 分)26.(6分) (1) 在反应式: aFeCl2+bKNO3+cHCl=dFeCl3+eKCl+fX+gH2O中,若b=1,d=3,则X 的分子式为____________。
(2) 完成以下氧化还原反应的离子反应方程式,并标出电子转移的方向和数目:___CrI3+____Cl2+______——____K2CrO4+ ____KIO4+___KCl+______27.(20分) A、B、C、W均为中学常见的纯净物,它们之间有如下转化关系(其它产物及反应条件已略去,反应可以在水溶液中进行)。
(1) 若A、B、C 三种物质的溶液均显碱性,焰色反应均为黄色,C受热分解转化为B①A 与过量W转化为C的总反应的离子方程式_______________。