第五章--成分过冷与单相合金凝固教程文件
- 格式:ppt
- 大小:3.19 MB
- 文档页数:37

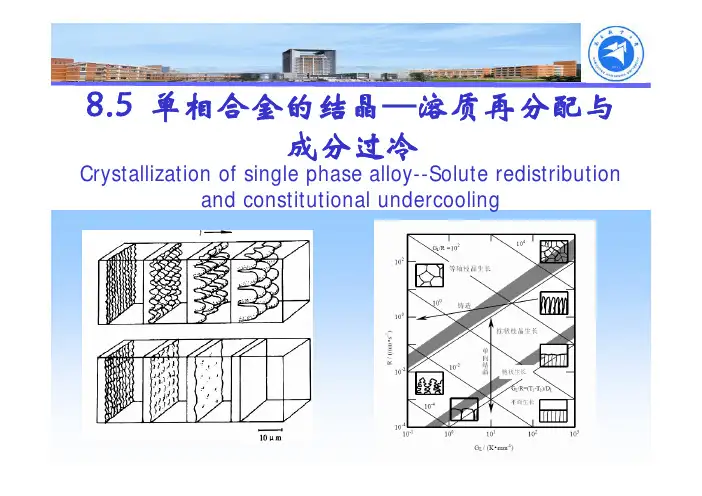
8.5 单相合金的结晶—溶质再分配与成分过冷Crystallization of single phase alloy--Solute redistribution and constitutional undercooling溶质再分配固液两相成分不同除纯金属外,单相合金的结晶是在固液两相区间内完成溶质再分配类似于凝固潜热的释放随着凝固过程的进行,由于固液两相成分差,越来越多的溶质原子被排出,释放到前方液相中与凝固潜热释放不同,液相中溶质扩散不可能很快均匀除间隙固溶体外,溶质原子在固相中扩散系数比液相低4个数量级液相中溶质扩散系数比热扩散系数也要低4个数量级溶质再分配具体分配形式与决定传质过程的动力学因素密切相关,决定着界面处,乃至固液两相内部成分变化溶质再分配影响到宏观及微观成分及偏析现象、晶体的生长形态、组织分布,一定程度上决定了材料各种性能同温度分布一样,溶质再分配也是合金结晶一大特点,二者共同控制晶体生长行为相图基本知识对于单相合金,将液相线和固相线近似看成直线当合金成分为C 0时液相线及液相线斜率m l 固相线及固相线斜率m s00*C m T T l l +=液相线温度00*C m T T s s +=固相线温度当合金成分为T 时()l l m T T C /0−=液相成分()ss m T T C /0−=固相成分平衡溶质分配系数平衡溶质分配系数s l ls m m c c k ==**0液固相直线:k 0为常数固相和液相内部的成分始终相等结晶初期,T = T L 时:C S *=C 0k 0,C L *=C 0结晶末期,T = T S 时:C S *=C 0,C L *=C 0/k 0平衡条件下溶质再分配-杠杆定律合金原始成分为C 0,固液两相在某一瞬间平衡成分为C S *与C l *,相应质量分数为f S *和f l *,则有:****c f c f c l l s s =+平衡结晶中溶质再分配;)1(10*00*k f k c c s s −−=)1(0*00*k f k c c l l−+=平衡条件下溶质再分配-杠杆定律A-B相图一部分液相线温度附近(凝固初期)固相线温度附近(凝固末期)液固相线区间内(中间阶段)近平衡/非平衡条件下溶质再分配一般条件下:溶质原子在液态金属中扩散系数为5×10-9m 2/s数量级溶质原子在固相中的扩散系数为5×10-12m 2/s数量级平衡凝固是指液、固相溶质成分完全达到平衡相图对应的平衡成分,即固、液相中成分均能及时充分扩散均匀平衡结晶极难实现,实际结晶过程都是近/非平衡结晶几种情况下溶质分配系数平衡凝固:平衡分配系数(界面与固液相内部均平衡)近平衡凝固:有效分配系数(仅界面处相平衡)非平衡凝固:非平衡分配系数(均不满足相平衡)近平衡凝固条件下溶质再分配-Scheil 公式凝固时,固相原子来不及扩散,液相中如存在足够对流和搅拌,任一温度下都能保证液相溶质原子的均匀分布,其成分沿着液相线变化除间隙固溶体外,溶质原子在固相中扩散系数比液相低四个数量级近平衡凝固条件下溶质再分配-Scheil 公式以水平圆棒自左向右单向结晶为例。








