化工原理-9章液体精馏-课件PPT
- 格式:ppt
- 大小:7.04 MB
- 文档页数:167



第9章液体精馏知识要点液体精馏是将挥发度不同的组分组成的混合液,在精馏塔中同时进行多次部分气化和部分冷凝,使其实现高纯度分离的过程。
实现精馏需要3个条件:①设备条件:精馏塔;②回流条件:塔底气相回流,塔顶液相回流;③相平衡条件:组分的挥发度有差异。
本章讨论重点为双组分精馏过程的计算,主要应掌握的内容包括:相平衡关系的表达和应用;精馏塔的物料衡算和操作关系;回流比的确定;理论板数的求法;影响精馏过程主要因素的分析等。
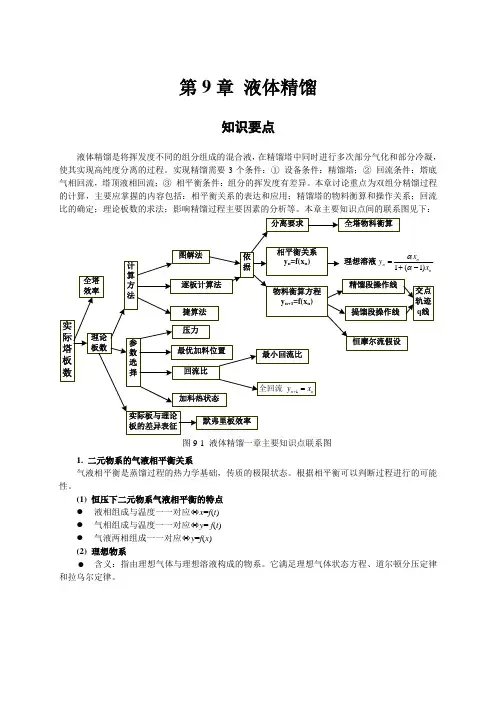
本章主要知识点间的联系图见下:图9-1 液体精馏一章主要知识点联系图1. 二元物系的气液相平衡关系气液相平衡是蒸馏过程的热力学基础,传质的极限状态。
根据相平衡可以判断过程进行的可能性。
(1) 恒压下二元物系气液相平衡的特点●液相组成与温度一一对应⇔x=f(t)●气相组成与温度一一对应⇔y= f(t)●气液两相组成一一对应⇔y=f(x)(2) 理想物系含义:指由理想气体与理想溶液构成的物系。
它满足理想气体状态方程、道尔顿分压定律和拉乌尔定律。
拉乌尔定律相对挥发度/1/1A A A B B B p x y xp x y xναν-===⋅- (9-1)11y xy xα-=⋅- (气相服从道尔顿分压定律) 相对挥发度α愈是大于1 ,则y 愈是大于x ,物系愈容易分离。
● 泡点方程x -toB ooA Bp p x p p -=- (9-2) ● 露点方程y -to A BA A Bp p p y p p p -=⋅- (9-3) ● 相平衡方程y-x()11xy xαα=+- (9-4)● t -y (x )相图两端点A 与B :端点A 代表纯易挥发组分A(x =1),端点B 代表纯难挥发组分B(x =0)。
两线:t -x 线为泡点线,泡点与组成x 有关;t-y 线为露点线,露点与组成y 有关。
3区:t -x 线以下为过冷液体区;t-y 线以上为过热蒸汽区;在t-x 与t -y 线之间的区域为气液共存区,只有体系落在气液共存区才能实现一定程度的分离。






思考题•精馏过程设计时,P增大,泡点,α,对分离。
P增大塔顶温度上升,塔釜温度上升。
若要降低塔釜温度,则可降低塔釜。
•精馏与蒸馏的区别——精馏有,蒸馏无。
平衡蒸馏与简单蒸馏的区别——前者,后者。
•摩尔流假定,主要依据各组分的。
但精馏段与提馏段的摩尔流量由于由于的不同而不一定相等。
•精馏过程设计时,P增大,泡点升高,α减小,对分离不利。
P增大塔顶温度上升,塔釜温度上升。
若要降低塔釜温度,则可降低塔釜压力。
•精馏与蒸馏的区别——精馏有回流,蒸——前者是连续过程,后者是间歇过程馏无回流。
平衡蒸馏与简单蒸馏的区别。
•摩尔流假定,主要依据各组分的摩尔潜热相等。
但精馏段与提馏段的摩尔流量由于由于进料状态q的不同而不一定相等。
9.5.4.2 多股加料浓度不同的料液在同一塔内分离。
回流比减小时,三操作线均向平衡线靠拢。
挟点位置有多种可能。
混合加料不利,能耗增加。
线与平衡线交点处。
例:图示为双组分混合液精馏塔。
塔顶采用全凝器, 泡点回流, 回流比为8。
系统相对挥发度α=2.5。
由塔上部抽出的侧线液相产品量为θ kmol/s, 其组成x θ= 0.9 。
进料F=10kmol/s, x f =0.5, 进料状态系饱和液体。
塔顶馏出液D=2kmol/s, x D =0.98,塔底残液组=0.05。
试求:成x w =0.05。
试求:(1)抽出液量θ;(2)由第三块理论板下降液体组成。
解:(1) F =D +θ+WF x f =Dx D +θx θ+W x w代入数据: 10=2+θ+W……(1)10×0.5=2×0.98+θ×0.9+W ×0.053.04=0.9θ+0.05W ……(2)联解(1)、(2), θ=3.106 kmol/s无回流的回收塔操作线x D 为max例如图所示的回收塔。
F=100kmol/h ,x f =0.4 (摩尔分率,下同),泡点进料,要求塔顶轻组分回收率为0.955,x W =0.05,系统的α=3。
