高考化学复习碳酸钠质量分数测定的实验探究【优秀课件】
- 格式:ppt
- 大小:2.11 MB
- 文档页数:16


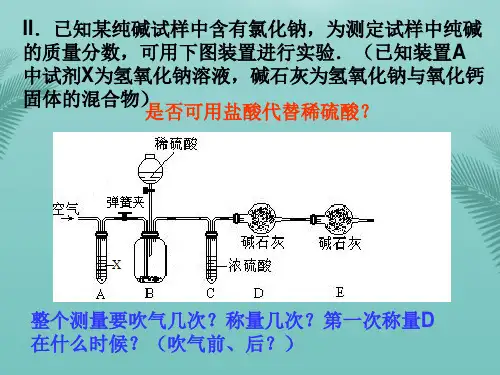





饼干中的碳酸氢钠和碳酸钠的含量测定---------13五年食品药品检验一班四组一实验项目※ 计算出饼干中的碳酸氢钠和碳酸钠的含量※ 掌握双指示剂滴定法的原理,操作和计算※ 熟练掌握用酚酞,甲基橙作指示剂判断※ 观看实验视频二实验器材与试剂♐实验仪器:♐分析天平,烧杯,碱式滴定管,♐锥形瓶,玻璃棒,漏斗,铁♐架台,移液管,洗耳球,滤纸,♐胶头滴管♐实验试剂:♐不含二氧化碳的去离子水,♐酚酞指示剂(10g/l乙醇),♐甲基橙指示剂(1g/l水溶液),♐0.1mol/l盐酸滴定液,饼干试样5g♐三实验原理♐碳酸钠,碳酸氢钠混合溶液用盐酸标准滴定溶液滴定到第♐一化学计量点,ph为8.31,选用酚酞或甲酚红-百里酚蓝混♐和指示液。
若用混和指示液并以相同浓度碳酸氢钠为参比液♐滴定,误差可达0.5%。
混合溶液用盐酸标准滴定溶液滴定到♐第二化学计量点时为3.89,选用甲基橙或甲基红-溴甲酚绿混♐和指示液三实验原理反应式如下:Na2Co3+Hcl→NaHCo3+NaCl NaHCo3+Hcl→NaCL+H2O+CO2 ↑四实验步骤(1) 准确称取5.0g饼干试样,用不含CO2的去离子水溶解,定量装移到250ML容量瓶中,并稀释至刻度,摇匀,静置。
(或过滤)(2)小心用移液管移取50.00ML上层清液(或滤液)于250ML锥形瓶中,加入3滴酚酞指示液(或5滴甲酚红-百里酚蓝混合指示剂),用0.1MOL/L盐酸标准滴定溶液滴定至淡粉色刚刚褪色(或溶液由红紫色变为樱桃色),记录消耗盐酸滴定溶液的体积V1。
(3)再加2滴甲基橙指示剂(或甲基红-溴甲酚绿混合指示剂),继续用盐酸标准滴定溶液滴定至由黄色变为橙色(或溶液由绿色变为暗红色),记录盐酸标准滴定溶液消耗的体积V2。
(4)平行测定3次,同时作空白试验。
饼干中的碳酸氢钠或碳酸钠的含量测定♐饼干试样中Na2Co3,NaHCo3的含量按下式计算:♐W(Na2Co3)={C×2V1×10‾³×M(½Na2CO3)}÷(M×50/250)×100% W(NaHCo3)={C(V1-V2)×10‾³×M(NaHCo3)}÷(M×50/250)×100%式中W(Na2Co3)--饼干试样中Na2Co3的质量分数;W(NaHCo3)--饼干试样中NaHCo3的质量分数;C--盐酸标准滴定溶液的浓度,MOL/L; V1--用酚酞作指示剂,消耗盐酸标准滴定溶液的体积,ML;V2--用甲基橙指示剂,消耗盐酸标准滴定溶液的体积,ML;M(½Na2CO3)--以½Na2CO3为基本单位的Na2CO3的摩尔质量,g/mol;M(NaHCo3)--NaHCo3的摩尔质量,g/mol;M--饼干试样的质量,g。


碳酸钠质量分数测定的实验探究李仕才测定碳酸钠质量分数的常用方法1.气体法(1)测定原理:Na 2CO 3+H 2SO 4===Na 2SO 4+H 2O +CO 2↑。
依据CO 2的体积确定Na 2CO 3的物质的量,进而确定纯碱中Na 2CO 3的含量。
(2)实验操作:向m g 纯碱样品中加入足量的稀硫酸,准确测量产生CO 2气体的体积为V mL(已折算为标准状况)。
(3)数据处理纯碱样品中Na 2CO 3的质量为V 22 400 mol ×106 g·mol -1=106V 22 400 g ,则纯碱样品中Na 2CO 3的质量分数为106V 22 400 g m g ×100%=53V 112m%。
2.沉淀法(1)测定原理:Na 2CO 3+BaCl 2===BaCO 3↓+2NaCl 。
依据BaCO 3沉淀的质量,确定Na 2CO 3的物质的量,进而确定纯碱中Na 2CO 3的含量。
(2)实验操作:先将m g 纯碱样品溶于水配成溶液,向溶液中加入过量的BaCl 2溶液,经过滤、洗涤、干燥得BaCO 3沉淀的质量为n g 。
(3)数据处理纯碱样品中Na 2CO 3的质量为n g197 g·mol -1×106 g·mol -1=106n 197 g ,则纯碱样品中Na 2CO 3的质量分数为106n 197 g m g ×100%=106n 197m×100%。
专题训练1.下列实验方案中,不能测定Na2CO3和NaHCO3混合物中Na2CO3质量分数的是( ) A.取a克混合物充分加热,减重b克B.取a克混合物与足量稀盐酸充分反应,加热、蒸干、灼烧,得b克固体C.取a克混合物与足量稀硫酸充分反应,逸出气体用碱石灰吸收,增重b克D.取a克混合物与足量Ba(OH)2溶液充分反应,过滤、洗涤、烘干,得b克固体答案 C解析取a克混合物充分加热,减重b克,根据差量法可求出NaHCO3的质量,从而求出Na2CO3的质量分数,A正确;取a克混合物与足量稀盐酸充分反应,加热、蒸干、灼烧,得b克固体氯化钠,列方程组即可求出,B正确;取a克混合物与足量稀硫酸充分反应,逸出气体用碱石灰吸收,增重b克,由于逸出气体中含有H2O(g),故无法求解,C错误;由于二者都能与Ba(OH)2溶液反应生成BaCO3沉淀,由Na2CO3→BaCO3、NaHCO3→BaCO3的转化关系,列方程组即可求出混合物中Na2CO3的质量分数,D正确。

推荐下载碳酸钠质量分数测定的实验探究李仕才测定碳酸钠质量分数的常用方法 1.气体法(1)测定原理:Na 2CO 3+H 2SO 4===Na 2SO 4+H 2O +CO 2↑。
依据CO 2的体积确定Na 2CO 3的物质的量,进而确定纯碱中Na 2CO 3的含量。
(2)实验操作:向m g 纯碱样品中加入足量的稀硫酸,准确测量产生CO 2气体的体积为V mL(已折算为标准状况)。
(3)数据处理纯碱样品中Na 2CO 3的质量为V 22 400 mol ×106 g·mol -1=106V 22 400 g ,则纯碱样品中Na 2CO 3的质量分数为106V22 400 g m g ×100%=53V112m %。
2.沉淀法(1)测定原理:Na 2CO 3+BaCl 2===BaCO 3↓+2NaCl 。
依据BaCO 3沉淀的质量,确定Na 2CO 3的物质的量,进而确定纯碱中Na 2CO 3的含量。
(2)实验操作:先将m g 纯碱样品溶于水配成溶液,向溶液中加入过量的BaCl 2溶液,经过滤、洗涤、干燥得BaCO 3沉淀的质量为n g 。
(3)数据处理纯碱样品中Na 2CO 3的质量为n g 197 g·mol -1×106g·mol -1=106n 197 g ,则纯碱样品中Na 2CO 3的质量分数为106n197 g m g ×100%=106n197m×100%。
专题训练1.下列实验方案中,不能测定Na 2CO 3和NaHCO 3混合物中Na 2CO 3质量分数的是( ) A .取a 克混合物充分加热,减重b 克B .取a 克混合物与足量稀盐酸充分反应,加热、蒸干、灼烧,得b 克固体C .取a 克混合物与足量稀硫酸充分反应,逸出气体用碱石灰吸收,增重b 克D .取a 克混合物与足量Ba(OH)2溶液充分反应,过滤、洗涤、烘干,得b 克固体 答案 C解析 取a 克混合物充分加热,减重b 克,根据差量法可求出NaHCO 3的质量,从而求出Na 2CO 3的质量分数,A 正确;取a 克混合物与足量稀盐酸充分反应,加热、蒸干、灼烧,得b 克固体氯化钠,列方程组即可求出,B 正确;取a 克混合物与足量稀硫酸充分反应,逸出气体用碱石灰吸收,增重b 克,由于逸出气体中含有H 2O(g),故无法求解,C错误;由于二者都能与Ba(OH)2溶液反应生成BaCO3沉淀,由Na2CO3→BaCO3、NaHCO3→BaCO3的转化关系,列方程组即可求出混合物中Na2CO3的质量分数,D正确。