产品放行审核单
- 格式:doc
- 大小:45.50 KB
- 文档页数:2


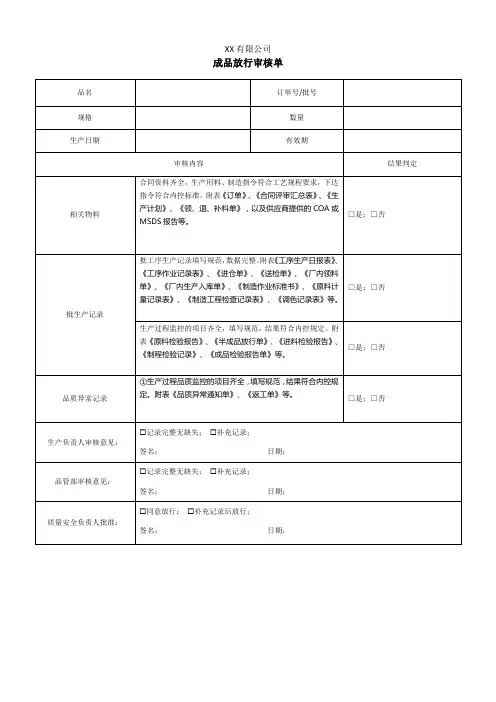

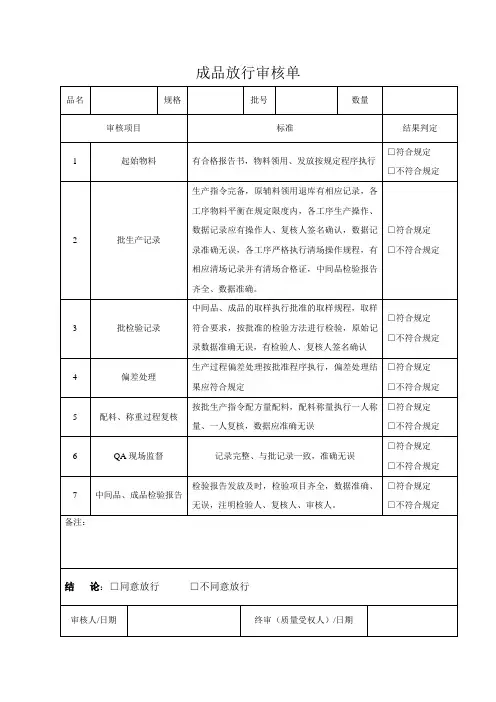
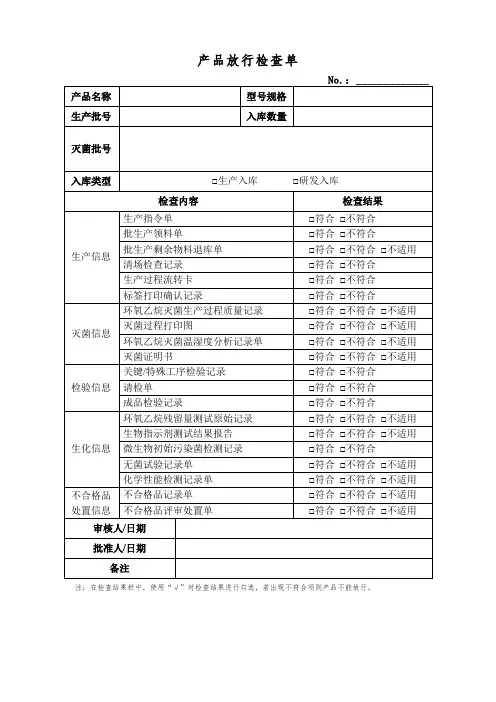

产品的放行审核记录应纳入批记录摘要:I.引言- 产品的放行审核记录的重要性II.什么是产品的放行审核记录- 定义和概念III.为什么产品的放行审核记录应纳入批记录- 法规要求- 质量控制- 产品追溯IV.产品的放行审核记录的具体内容- 审核过程- 审核内容V.产品的放行审核记录的管理- 管理流程- 保存期限VI.结论- 总结重要性正文:I.引言产品的放行审核记录是药品生产质量管理的重要环节,它对于保证药品的质量和安全具有重要意义。
在药品生产过程中,每一个生产批次都需要进行放行审核,以确保产品符合法规要求、质量标准以及客户的要求。
II.什么是产品的放行审核记录产品的放行审核记录是指在药品生产过程中,对生产批次进行审核、检查、批准等一系列活动的记录。
它包括了对生产过程的审核、对质量标准的检查、对生产记录的批准等。
III.为什么产品的放行审核记录应纳入批记录产品的放行审核记录应纳入批记录,这是由法规要求和质量管理要求决定的。
首先,药品生产质量管理规范(GMP) 要求药品生产企业必须建立和实施严格的质量管理体系,确保药品的质量和安全。
而产品的放行审核记录是质量管理体系的重要组成部分,它记录了药品生产过程中的关键信息,对于保证药品的质量和安全具有重要意义。
其次,产品的放行审核记录是产品追溯的重要依据。
在药品出现质量问题时,可以通过产品的放行审核记录追溯到生产过程中的问题环节,从而采取有效的措施解决问题。
IV.产品的放行审核记录的具体内容产品的放行审核记录应包括以下内容:- 审核过程的描述,包括审核人员、审核时间、审核结果等;- 审核内容的描述,包括产品名称、规格型号、生产批号、生产日期、生产过程、质量标准等;- 审核结论,包括是否批准放行、是否需要采取纠正措施等。
V.产品的放行审核记录的管理产品的放行审核记录应按照一定的流程进行管理,以确保记录的完整性和可追溯性。
首先,审核记录应保存在生产企业的质量管理部门,并由专人负责管理。

产品放行审核记录产品放行审核是指对产品的质量、安全、性能等方面进行审查和评估,以确定产品是否符合相应的技术规范和标准,可以正常投放市场和使用。
产品放行审核记录是对审核过程中所进行的各项测试、检验和评估的结果进行记录和总结。
1.确保产品质量安全:通过产品放行审核记录,可以明确产品是否符合相关的技术标准和规范。
只有通过审核的产品才能正常投放市场和使用,从而保证产品质量和安全。
2.追溯和溯源:产品放行审核记录可以作为产品质量的溯源依据,能够清晰地反映产品的检验过程和结果。
一旦产品质量出现问题,可以通过审核记录进行追溯,快速找到问题原因,采取相应的措施进行处理。
3.汇总和分析:通过产品放行审核记录的汇总和分析,可以及时发现和总结问题,为后续的质量改进提供参考。
同时,对审核记录进行统计和分析,可以为公司的质量管理提供数据支持和决策依据。
1.产品信息:记录产品的基本信息,如产品名称、型号、批次等。
同时,可以附上产品的技术标准和规范。
2.审核人员:记录参与产品放行审核的人员姓名、职务等信息。
其中,审核人员应具备相关的技术和专业知识,并独立、客观地进行审核。
3.审核流程:记录产品放行审核的全过程,包括检查、测试、评估等环节。
需要清楚地标明审核的先后顺序和时限。
4.审核结果:对每个审核环节进行详细的记录和评估,如测试数据、检验结果等。
需要准确地记录每项检验的内容和结果。
5.异常处理:记录在审核过程中出现的异常情况和处理措施。
当遇到问题时,需要及时记录并采取相应的措施进行处理,保证审核的准确性和可靠性。
6.审核结论:总结和评价产品的审核结果,根据审核结果判断产品是否符合放行要求,决定是否放行该批产品。
编写和管理产品放行审核记录的过程需要注意以下几点:1.规范和标准:在编写产品放行审核记录时,需要参考相关的技术标准和规范,确保审核内容的全面和准确。
2.现场记录:在进行实地审核时,需要及时记录下每个审核环节的情况和结果。
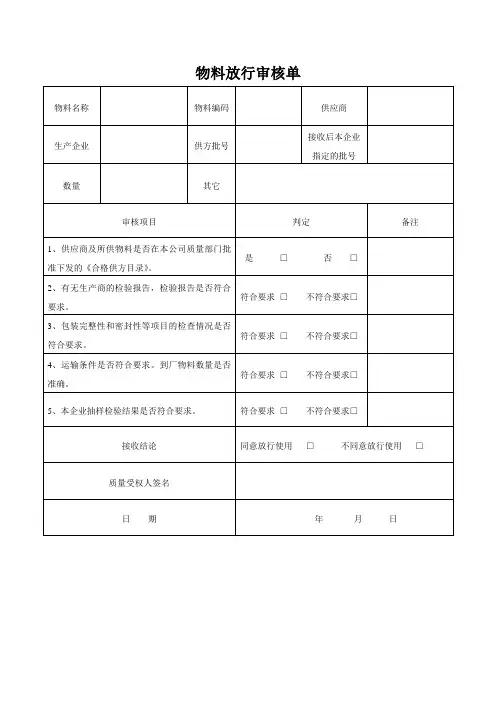

中药材放行审查单
XXXXXXXXXX有限企业
中药材放行审查单
编号:品名规格审查单号
编码入库数目物料代码
请验日期报告日期报告单编号
产地(供货单位)厂家编号复验期至
审查项目审查结果中药材供给商资质的采集能否齐备。
是□否□在库中药材的储藏条件能否与该中药材储藏条件相一致。
是□否□
中药材查验项目能否完好,查验结果能否切合规定的质量标准规定,各种查验记
QA是□否□录能否齐备。
监
中药材在进行入库查验前,其储藏条件能否切合该物料储藏条件要求。
是□否□督
GMP 规范要求。
中药材包装过程中标签的领用和使用能否符号是□否□员
在库中药材能否悬挂明确的物料状态。
是□否□审
能否做到帐、卡、物一致。
是□否□核
其余:
审查建议:
QA 监察员署名:年月日质量评论:
结
论
切合规定,赞同放行□不切合规定,不一样意放行□
质量授权人署名:年月日
备
注。
德信诚培训网
更多免费资料下载请进: 好好学习社区
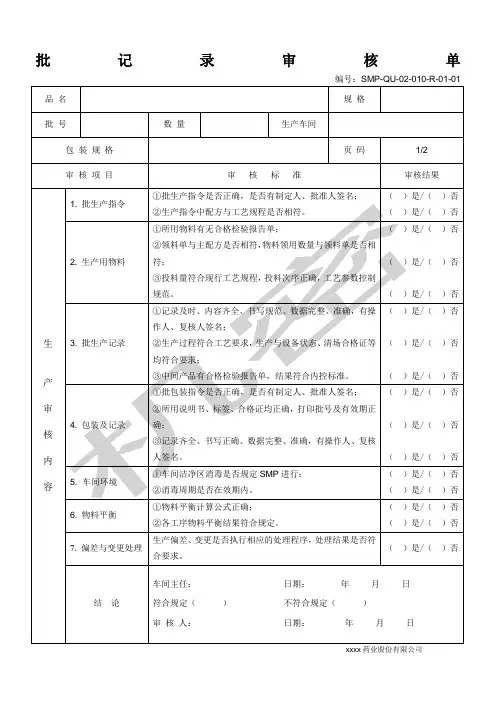
产品放行审核单
产品名称 批号
规格
包装规格
数量
审核内容
审核结果(打“√”)
1.起始物料均应有检验合格报告单 有 □ 无 □
2.配料、称重应执行复核制度 已复核 □ 未复核 □
3.生产记录应完整、真实
(应有配料指令、包装指令、各生产岗位原始记录等)
完整 □ 不完整 □ 4.清场
已清场 □ 未清场 □ 5.半成品质量检验结果:应符合内控标准
符合 □ 不符合 □ 6.偏差及异常情况
无偏差及异常情况 □
有偏差及异常情况 □ 同意处理意见 □ 不同意处理意见□ 7.成品质量检验结果:应符合标准
符合 □
不符合 □ 8.物料平衡情况 符合 □
不符合 □ 原因分析:
9.质管员现场监督记录应完整 符合 □ 不符合 □ 10.药品及其生产应符合注册批准的要求和质量标
准
符合 □
不符合 □
结论
符合标准,准予出厂 □
不符合标准,不准予出厂 □ 质量受权人:
年 月 日 备注。