第2章分子轨道理论
- 格式:pptx
- 大小:6.92 MB
- 文档页数:126



第二章分子结构第五节分子轨道理论2.5.2 分子轨道能级图及其应用分子轨道能级图及其应用1. 同核双原子分子轨道能级图a图:适合O2,F2 b图:适合N2,C2 ,B2N2和O2分子轨道与N、O原子轨道能级数据2. 同核双原子分子轨道电子排布式:◆H 22H 1s 1 →H 2H 2 [(σ1s )2] (分子轨道式)键级 = (相当于共价单键)◆H 2+(氢分子离子)H 2+ [(σ1s )1]键级 = 单电子键(VB 法和Lewis 理论无此说法)20122--==成键分子轨道电子数反键分子轨道电子数100.52-=◆He 2 [(σ1s )2 (σ*1s )2 ]键级 = (不成键),He 2不能稳定存在。
◆He +2 [(σ1s )2 (σ*1s )1 ]键级= , He 2+ 可以存在。
2202-=210.52-=2*22*24221s 1s 2s 2s 2p 2p N ()()()()(π)()σσσσσ⎡⎤⎣⎦键级 = 1/2( 10 - 4 ) = 3N 22*22*224*221s 1s 2s 2s 2p 2p 2p O ()()()()()(π)(π)σσσσσ⎡⎤⎣⎦键级= 1/2 ( 10 - 6 ) = 2O 2第二周期同核双原子分子的电子结构、键级、稳定性及磁性:3.异核双原子分子的分子轨道图及电子排布式: 分子轨道符号不再用下标1s、2s、2p等。
HF分子的电子构型:2224σσσ[123 1 π]CO与N2互为等电子体(14 e ),分子轨道能级相近。
CO [1σ2 2σ2 3σ2 4σ21π45σ2]键级= 3 相当于价键法:C ≡ O对比:N2 (σ1s) 2 (σ*1s) 2 (σ2s) 2 (σ*2s) 2 (π2p) 4 (σ2p) 2。

第章前线分子轨道理论什么是分子轨道理论分子轨道理论是描述分子内电子构型的一种理论。
在化学中,原子的价电子构型决定了化学反应和化学性质,而分子的电子构型又是决定分子性质和反应的关键因素。
因此,分析和理解分子的电子构型具有重要意义。
分子轨道理论通过将原子轨道合并形成分子轨道的方式来描述分子的电子构型。
在分子轨道理论中,分子中所有原子的原子轨道合并为一系列分子轨道,每个分子轨道可以容纳一对电子。
前线分子轨道理论前线分子轨道理论是分子轨道理论的一个重要分支。
在前线分子轨道理论中,我们关注的是分子中最外层的电子。
这些电子决定了分子的化学性质和反应活性。
因此,对于化学反应和分子中的电荷转移来说,前线分子轨道理论具有重要意义。
前线分子轨道理论中,我们通常关注两个参数:能量和对称性。
在分子中,前线分子轨道由接近原子核的、能级较低的σ轨道和能级较高的π轨道组成。
由于能量较低的σ轨道电子最相互靠近原子核,因此它们的相互作用能最大。
同时,它们的能量比较低,因此对于分子中电荷转移反应最具有反应性。
分子轨道理论的应用分子轨道理论具有广泛的应用。
在设计新的材料和药物时,分子轨道理论可以帮助我们预测分子的反应性和性能。
在催化剂的设计中,分子轨道理论可以帮助我们理解催化反应的机制和选择最适合的催化剂。
分子轨道理论还可以帮助我们理解一些化学现象。
如何在实验室中制备高能量化合物、如何控制分子中重要反应的速率和选择性和如何设计更有效的催化剂,都是分子轨道理论研究领域。
此外,分子轨道理论还可以在设计新型化学反应和控制分子反应中的选择性方面发挥重要的作用。
第章前线分子轨道理论是分子轨道理论中的重要分支,它可以帮助我们理解分子中最外层电子的性质和化学反应的机理。
分子轨道理论在新材料和药物的设计、催化剂的研究、化学反应的加速和选择性控制等方面都具有广泛的应用前景。
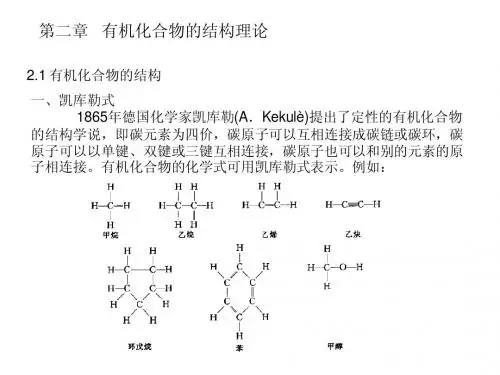





分子轨道理论1. 引言分子轨道理论是化学中的一种重要理论,它用量子力学的原理解释了分子的电子结构和化学性质。
本文将介绍分子轨道理论的基本概念、应用以及相关的计算方法。
2. 基本概念2.1 原子轨道在分子轨道理论中,首先要了解的是原子轨道。
原子轨道是描述单个原子中电子运动的波函数。
根据量子力学的原理,一个原子可以存在多个不同的原子轨道,每个原子轨道都对应着不同的能量状态。
2.2 分子轨道当两个或更多个原子靠近形成化学键时,原子轨道会互相重叠,形成新的分子轨道。
分子轨道描述的是电子在整个分子中的运动状态。
根据分子轨道理论,分子轨道可以分为两类:成键分子轨道和反键分子轨道。
成键分子轨道对应着电子的主要分布区域,而反键分子轨道则对应着电子分布相对较少的区域。
2.3 分子轨道能级分子轨道能级与原子轨道能级类似,分子轨道的能量随着轨道的能级增加而增加。
有时,分子轨道能级之间会有一定的能隙,这种能隙反映了分子稳定性的特征。
3. 分子轨道的应用分子轨道理论可以解释大量的化学现象和性质,下面列举了几个常见的应用:3.1 化学键的形成分子轨道理论提供了解释化学键产生的机制。
当两个原子靠近并形成化学键时,原子轨道会发生线性组合形成分子轨道。
通过分子轨道理论,我们可以理解不同类型的化学键(如共价键、离子键和金属键)是如何形成的以及其性质的差异。
3.2 分子轨道的能级顺序分子轨道理论还可以预测分子轨道的能级顺序,从而解释分子的化学性质。
能级较低的分子轨道通常具有较高的稳定性,从而决定了分子的化学反应性质。
3.3 分子光谱在分子光谱中,分子轨道理论被广泛应用。
分子轨道理论可以解释分子在吸收或发射光的过程中所发生的能级跃迁,从而解释不同光信号的产生和分子结构的变化。
4. 分子轨道的计算方法4.1 原子轨道模型著名的原子轨道计算方法包括Hartree-Fock方法和密度泛函理论。
这些方法通过求解原子的薛定谔方程,得到原子轨道及其能量。
第2章分子结构[教学要求]1.掌握离子键和共价键的基本特征和它们的区别。
2.掌握价键理论,杂化轨道理论。
3.掌握分子轨道理论的基本内容。
4.了解分子间作用力及氢键的性质和特点。
[教学重点] 1.VSEPR 2.VB法3.MO法[教学难点] MO法[教学时数] 6学时[主要内容]1.共价键:价键理论-电子配对法(本质,要点,饱和性,方向性,类型σ键、π键)。
2.VSEPR:价电子互斥理论的提出,价电子互斥理论的基本要点以及用价电子互斥理论分析各类分子和原子团的空间构型。
3.杂化轨道理论:杂化轨道理论的提出,杂化轨道理论的基本要点,杂化轨道的类型-sp、spd 等各种类型及举例。
4.分子轨道理论:分子轨道理论的基本要点,分子轨道的能级图,实例-同核:H2、He、O2、F2、N2;异核:NO、HF。
5.共价键的属性:键长,键角,键能,键级。
6.分子间的作用力和氢键。
[教学内容]上一章主要研究的是原子的结构与性质,本章进一步讨论原子同原子之间和分子之间靠什么力结合在一起?分子有什么性质?具体的讲2-1 路易斯结构式一、弗兰克兰结构式到19世纪时,化学家们已经知道了许多分子的成分,如氯化氢HCl、水H2O、二氧化碳CO2、氨NH3等,并用短棍线“—”的形式来描述分子中原子之间的相互结合“1价”,还总结出一些规律。
其中英国化学家弗兰克兰和瑞典化学家贝采尼乌斯贡献较大。
这些表达方式,在我们中学化学课本中还在沿用。
二、路易斯结构式1916年美国的著名化学家(加里福尼亚大学教授)路易斯利用原子结构知识对弗兰克兰结构式的短棍线“—”进行了解释,即“—”代表一对共用电子对,= 代表两对共用电子对,≡代表三对共用电子对,并进一步提出了键合电子和孤对电子的概念以及分子结构稳定性的“八隅律”—原子倾向于通过共用电子对使它们的最外层达到稀有气体的8电子稳定构型。
1923年路易斯进一步将化合物分子中两个原子在一起的共享电子对称为共价键,从而建立了路易斯共价键理论。