人教版高中化学必修二乙烯
- 格式:ppt
- 大小:2.22 MB
- 文档页数:32


第二节乙烯与有机高分子材料第1课时乙烯A级必备知识基础练1.(广东7月学考)乙烯是不饱和烃,下列说法正确的是( )A.乙烯和甲烷都是不饱和烃B.甲烷和乙烯互为同系物C.乙烯分子中只含碳碳单键D.乙烯能与H2O发生加成反应2.(湖南6月合格考)下列试剂中,能用于鉴别甲烷和乙烯的是( )A.水B.稀硫酸C.氢氧化钠溶液D.酸性高锰酸钾溶液3.(湖北襄阳高一期末)与乙烯所含碳、氢元素的百分含量相同,但与乙烯既不是同系物又不是同分异构体的是( )A.环丙烷()B.乙烷C.甲烷D.CH3CH CH24.(辽宁沈阳高一期末)甲烷和乙烯的混合气体5 L,完全燃烧消耗相同状况下O2 12 L,则甲烷和乙烯的体积比为( )A.2∶1B.1∶2C.3∶2D.2∶35.(湖南师大附中高一月考)下列化合物中,既能发生加成反应又能发生加聚反应的有( )A.CH3CH CHCH3B.CH3CH2CH3C.D.CH3CH36.(山西吕梁高一期末)使1 mol乙烯与氯气发生完全加成反应,然后使该加成反应的产物与氯气在光照条件下发生取代反应,则两个过程中消耗的氯气的总的物质的量是( )A.3 molB.4 molC.5 molD.6 mol7.(河北唐山高一期末)标准状况下,0.56 L CH4和C2H4的混合气体通入足量溴水中,溴水增重0.28 g(假设C2H4完全被吸收),则乙烯占混合气体体积的( )A.20%B.40%C.60%D.80%B级关键能力提升练8.(山东潍坊高一期末)乙烯的产量是衡量一个国家石油化工发展水平的重要标志之一,以乙烯为原料合成的部分产品如图所示。
下列有关说法正确的是( )A.加成反应有①、②,加聚反应有③B.氯乙烯、聚乙烯都能使酸性KMnO4溶液褪色C.反应①属于取代反应D.反应④中乙烯发生还原反应9.(山东省实验中学高一期末)如图所示为某有机物分子的球棍模型图,图中的“棍”代表单键或双键,不同大小的“球”代表三种不同的短周期元素的原子。


第二节 乙烯与有机高分子材料人非圣贤,孰能无过?过而能改,善莫大焉。
《左传》大地二中 张清泉第1课时 乙烯[核心素养发展目标] 1.掌握乙烯的组成及结构特点,体会结构决定性质的观念,增强“宏观辨识与微观探析”的能力。
2.掌握乙烯的化学性质,认识加成反应的特点,培养“证据推理与模型认知”能力。
3.了解乙烯在生产及生活中的应用,培养“科学态度与社会责任”。
(一)乙烯的分子组成与结构(二)乙烯的性质1.乙烯的物理性质2.乙烯的化学性质(1)氧化反应①燃烧:现象:火焰明亮,伴有黑烟。
化学方程式:C2H4+3O2――→点燃2CO2+2H2O 。
②和酸性KMnO4溶液反应现象:酸性KMnO4溶液褪色。
结论:乙烯能被酸性KMnO4溶液氧化。
(2)加成反应①将乙烯通入溴的四氯化碳溶液中现象:溴的四氯化碳溶液褪色。
化学方程式:。
②加成反应定义:有机物分子中的不饱和碳原子与其他原子或原子团直接结合生新的化合物的反应。
书写下列加成反应的化学方程式:(3)聚合反应①定义:由相对分子质量小的化合物分子互相结合成相对分子质量大的聚合物的反应。
②乙烯自身加成生成聚乙烯的方程式:该反应是聚合反应,同时也是加成反应,这样的反应又被称为加成聚合反应,简称加反应。
其中,—CH2—CH2—称为链节,n称为聚合度,小分子乙烯称为聚乙烯的单体。
(三)乙烯的用途1.乙烯是重要的化工原料,在一定条件下用来制聚乙烯塑料、聚乙烯纤维、乙醇等。
乙烯的产量可以用来衡量一个国家的石油化工发展水平。
2.在业生产中用作植物生长调节剂。
(1)乙烯的结构简式可书写为CH2CH2( ×)提示乙烯分子中含有,在书写时,官能团不能省略,应为CH2==CH2。
(2)乙烯是一种无色无味,易溶于水的气体( ×)提示乙是一种稍有气味,难溶水的气体。
(3)乙的化学性质比乙烷活泼( √)(4)乙烯能使酸性KMnO4溶液和溴水褪色,反应原理相同( × )提示 乙烯使酸性KMnO4溶液褪色发生的是氧化反应,乙烯使溴水褪色发生的为加成反应。


第七章有机化合物第二节乙烯与有机高分子材料第一课时《乙烯》学案【学习目标】1.从生活和生产实际出发,了解乙烯的来源,知道乙烯的物理性质。
2. 通过对乙烯的组成和分子结构模型的学习,了解乙烯分子中的碳原子的成键特点,构建常见有机物分子3. 的认知模型。
学会用分子式、结构式、结构简式、电子式、球棍模型和空间填充模型表示乙烯分子。
4. 了解乙烯的主要化学性质,分析乙烯的性质与其结构中碳碳双键(官能团)的关系。
通过学习乙烯的加聚反应,体会合成高分子材料与我们生活的关系。
【学习过程】【任务一】阅读材料,完成填空乙烯是世界上产量最大的化学产品之一,乙烯工业是石油化工产业的核心,乙烯产品占石化产品的75%以上,在国民经济中占有重要的地位。
通常情况下,乙烯是一种无色稍有气味的气体,无色气体,熔点-169.4 ℃,沸点-103.80 ℃。
略具烃类特有的臭味。
密度为1.178 g/L,比空气的密度略小,难溶于水,几乎不溶于水,难溶于乙醇,易溶于乙醚、丙酮和四氯化碳等有机溶剂。
乙烯是最简单的烯烃,少量存在于植物体内,是植物的一种代谢产物,能使植物生长减慢,促进叶落和果实成熟。
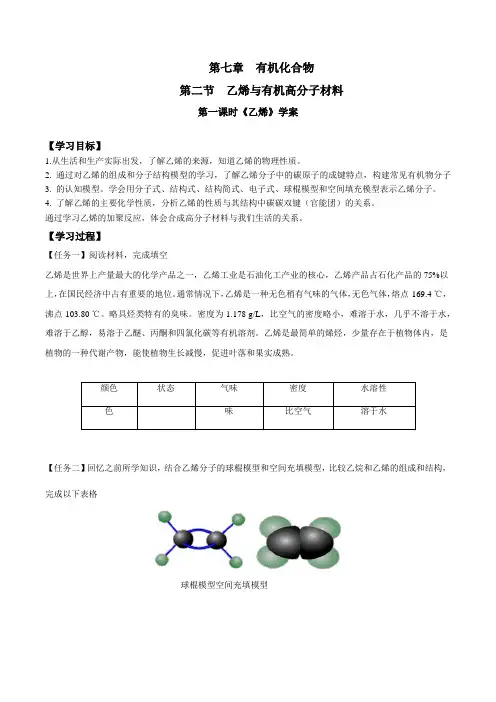
【任务二】回忆之前所学知识,结合乙烯分子的球棍模型和空间充填模型,比较乙烷和乙烯的组成和结构,完成以下表格球棍模型空间充填模型思考:乙烯和乙烷的组成和结构有什么相同点和不同点? 【任务三】阅读以下资料,分析乙烯分子中的碳碳双键的特点思考:乙烯分子中的碳碳双键有什么特点?【任务四】用乙烯进行如下实验,将实验现象填写在表格中思考:乙烯和酸性高锰酸钾溶液、溴的四氯化碳溶液的实验现象可能的产生原因?【任务五】乙烯在一定条件下,可以与Cl 2、H 2、HCl 、H 2O 等物质发生加成反应,请根据这些反应总结加成反应的反应规律CH 2===CH 2+Cl 2―→CH 2ClCH 2Cl CH 2===CH 2+H 2――→催化剂△CH 3CH 3CH 2===CH 2+HCl ――→催化剂△CH 3CH 2ClCH 2===CH 2+H 2O――→催化剂加热、加压CH 3CH 2OH【任务六】查阅教材,完成填空。



统编人教版高中化学(必修二)第七章第二节《乙烯与有机高分子材料》优质说课稿今天我说课的内容是统编人教版高中化学(必修二)第七章第二节《乙烯与有机高分子材料》。
第七章讲述有机化合物。
主要内容有:认识有机化合物、乙烯与有机高分子材料、乙醇与乙酸、基本营养物质。
碳在地壳中的含量很低,但是含有碳元素的有机化合物却分布极广。
有机化合物不仅构成了生机勃勃的生命世界,也是燃料、材料、食品和药物的主要来源。
与无机化合物相比,有机化合物的组成元素并不复杂,但化合物数量众多,性质各异。
对有机化合物的研究,需要在了解碳原子成键规律的基础上,认识有机化合物的分子结构,以及决定其分类与性质的特征基团,进而认识有机化学反应,实现有机化合物之间的转化,合成新的物质。
本课教学旨在引导学生学习掌握乙烯与有机高分子材料,培养学生化学学科核心素养。
教学承担着实现本单元教学目标的任务,为了更好地教学,下面我将从教材分析、教学目标和核心素养、教学重难点、学情分析、教学方法、教学准备、教学过程等方面进行说课。
一、说课程标准。
普通高中化学课程标准(2017版2020年修订):【内容要求】“4.2 典型有机化合物的性质:认识乙烯的结构及其主要性质与应用;知道氧化、加成、取代、聚合等有机反应类型。
知道有机化合物之间在一定条件下是可以转化的。
”二、说教材分析本节讲述了乙烯与有机高分子材料的知识。
本课以介绍乙烯与有机高分子材料的知识为载体,以探究、实验设计为核心,训练学生对已有知识进行分析综合、归纳演绎的思维能力以及解决实际问题的能力。
包括乙烯、烃、有机高分子材料三部分内容。
教材以文字介绍乙烯导入,正文部分以文字叙述为主,辅以图片。
另外教材还提供了“信息搜索、科学史话、科学技术与社会”,以丰富拓展教学内容。
教材设置“思考与讨论”相关栏目,引导学生探究实践。
三、说教学目标与核心素养(一)教学目标:1.掌握乙烯的用途和乙烯的分子结构。
2.掌握乙烯的物理性质、乙烯的化学性质(加成、氧化、聚合)。

课后作业(十五)[基础巩固]一、乙烯的结构1.下列说法正确的是()A.乙烯的电子式为B.乙烯的球棍模型为C.乙烯分子的碳碳双键中有一个键易断裂D.乙烯的分子式可表示为(CH2)2[解析]乙烯分子中碳原子间是双键,有两对共用电子对,A错误;碳原子半径应比氢原子大,B错误;乙烯分子中含有碳碳双键,其中有一个键容易断裂,而使乙烯的化学性质较为活泼,故C正确;分子式表示分子的组成即分子中原子的种类和个数,乙烯的分子式为C2H4,故D错误。
[答案] C2.能证明乙烯分子里含有一个碳碳双键的事实是()A.乙烯分子里碳氢个数比为1∶2B.乙烯完全燃烧生成的CO2和水的物质的量相等C.乙烯容易与溴的四氯化碳溶液发生加成反应,且1 mol乙烯完全加成需要消耗1 mol溴D.乙烯能使酸性高锰酸钾溶液褪色[解析]碳氢原子个数比为1∶2,是对乙烯的组成分析,而不是证明碳碳双键存在的事实;B与A的实质是一样的,根据生成的CO2和水的物质的量相等,也只能推断出碳、氢原子个数比为1∶2,A、B错误;加成反应是不饱和烃的特征性质,1 mol乙烯完全加成需要消耗1 mol溴,说明乙烯分子中含有一个碳碳双键,C正确;能够使酸性高锰酸钾溶褪色是不饱和烃的特征,并不能说明一定含有碳碳双键,也不能定量地说明乙烯分子的结构中只含有一个碳碳双键,D错误。
[答案] C3.下列说法不正确的是()A.乙烯属于不饱和链烃,乙烷属于饱和链烃B.乙烯分子中所有原子处于同一平面上,乙烷分子中所有原子不都在同一平面上C.1 mol乙烯所含C—H单键的数目与0.5 mol乙烷所含C—H 单键的数目相同D.根据乙烯的结构可知,乙烯也可能发生取代反应[解析]C2H4中含有碳碳双键,属于不饱和链烃,A项正确;乙烯为平面结构,所有原子共面,乙烷相当于2个—CH3结合而成,所有原子不可能共面,B项正确;1 mol C2H4含有4 mol C—H键,0.5 mol C2H6含有3 mol C—H键,C项错误;乙烯分子中的H原子在一定条件下也能被其他原子取代,D项正确。
第二节来自石油和煤的两种基本化工原料课时1 乙烯1.会写乙烯的分子式、结构式、结构简式、电子式,知道乙烯的结构特点,了解烯烃的概念。
2.知道乙烯能够发生氧化反应和加成反应。
(重点)3.知道乙烯发生加成反应时的断键和成键情况,会写乙烯与H2、HCl、Cl2、H2O发生加成反应的化学方程式。
(重难点)4.了解加成反应的含义与判断。
(重点)烯烃的组成与乙烯的结构[基础·初探]1.不饱和烃与烯烃2.乙烯的结构(1)分子结构分子式电子式结构式结构简式分子模型球棍模型比例模型C2H4分子结构立体构型乙烯为平面结构,2个碳原子和4个氢原子共面[题组·冲关]题组烯烃和乙烯的组成与结构1.下列有关说法不正确的是()A.由乙烯分子的组成和结构推测含一个碳碳双键的单烯烃通式为C n H2n B.乙烯的电子式为C.烯烃与烷烃中碳碳键不完全相同D.C3H6的分子结构可以是CH2===CHCH3和【解析】乙烯分子的C与C之间共用2对电子。
【答案】 B2.下列分子不是平面型分子的是()【导学号:30032052】A.H2O B.CH2===CH2C.CH2===CH—CH3D.CO2【解析】H2O、CO2为三点共面分子,CH2===CH2为平面6原子分子。
【答案】 C乙烯的性质及应用[基础·初探]1.乙烯的物理性质无色、稍有气味的气体,难溶于水,密度比空气小。
2.乙烯的化学性质(1)氧化反应(2)加成反应①乙烯通入溴的CCl4或溴水中,现象是溶液褪色,其化学方程式为CH2===CH2+Br2―→CH2Br—CH2Br,产物名称为1,2-二溴乙烷。
②写出CH2===CH2与H2、HCl、H2O反应的化学方程式CH2===CH2+H2――→催化剂△CH3—CH3,CH2===CH2+HCl――→催化剂CH3CH2Cl,CH2===CH2+H2O――→催化剂高温、高压CH3CH2OH。
③乙烯发生加成聚合反应生成聚乙烯,其反应方程式为n CH2===CH2――→催化剂CH2—CH2。
⼈教版⾼中化学必修2[知识点整理及重点题型梳理]_⼄烯(提⾼)H 两个未成对电⼦C C 精品⽂档⽤⼼整理⼈教版⾼中化学必修⼆知识点梳理重点题型(常考知识点)巩固练习⼄烯【学习⽬标】1、以⼄烯为例,加深认识有机化合物中结构—性质—⽤途的关系;2、了解⼄烯的分⼦结构,熟悉其主要性质和重要⽤途;3、初步掌握加成反应的概念。
【要点梳理】【⼄烯 ID :402314&⼄烯的分⼦组成及其结构】要点⼀、⼄烯的组成和结构1、⼄烯的组成⼄烯的分⼦式为 C 2H 4。
⽐较 C 2H 4 与 C 2H 6(⼄烷)可知,⼄烯分⼦⽐碳原⼦数相同的⼄烷分⼦少两个氢原⼦,我们可以这样理解:HH HH HHHCC H每个碳原⼦上失去1个氢原⼦H..结合成共价键 HCCHHH⼄烯即⼄烯分⼦中碳碳之间为双键,⼄烷分⼦中碳原⼦是“饱和”的,⼄烯分⼦中碳原⼦是“不饱和”的。
⼄烯的电⼦式为。
2、⼄烯的结构⼄烯的结构式为,结构简式为 CH 2=CH 2。
其分⼦中的 2 个碳原⼦和 4 个氢原⼦都处在同⼀平⾯上,它们彼此之间的键⾓为 120°,空间结构为。
⼄烯的两种分⼦模型如下图所⽰:要点⼆、⼄烯的性质1、⼄烯的物理性质⼄烯是⽆⾊、稍有⽓味的⽓体,标准状况下的密度为 1.25g ·L -1(略⼩于空⽓的密度),难溶于⽔,易溶于四氯化碳等有机溶剂。
2、⼄烯的化学性质与只含碳碳单键的烷烃相⽐,⼄烯分⼦中因碳碳双键的存在⽽表现出较活泼的化学性质。
实验探究:装置:实验步骤与现象:实验步骤将⽓体通⼊酸性⾼锰酸钾溶液中将⽓体通⼊溴的四氯化碳溶液中⽤排⽔法收集⽓体验纯后,点燃实验现象溶液褪⾊溶液褪⾊⽕焰明亮,伴有⿊烟结论⼀:⽯蜡油分解产⽣了能使⾼锰酸钾溶液、溴的四氯化碳溶液褪⾊的⽓态产物,由此可知产物中含有与烷烃性质(烷烃不能使酸性⾼锰酸钾溶液褪⾊)不同的烃。
结论⼆:研究表明,⽯蜡油分解的产物主要是⼄烯和烷烃的混合物。
要点诠释:a.碎瓷⽚起催化作⽤。