第12章d区元素和f区元素[1].
- 格式:ppt
- 大小:933.00 KB
- 文档页数:29

第12章d区元素和f区元素【12-1】试用d区元素价电子层结构的特点来说明d区元素的特性。
解:d 区元素最后一个电子填充到d 轨道上,其价层电子组态为:(n-1)d1-8ns1-2,位于周期表的中部,包括ⅢB -ⅦB和Ⅷ族元素,它们都是过渡元素,每个元素都有多种氧化值。
同周期过渡元素的原子半径随着原子序数的增加而缓慢地依次减小,到了第Ⅷ族元素后又缓慢增大。
同族过渡元素的原子半径,除了ⅢB外,自上而下随着原子序数的增大而增大。
各过渡系元素电离能随原子序数的增大,总的变化趋势是逐渐增大的。
同副族过渡元素的电离能递变不很规则。
熔点、沸点高, 密度大, 导电性、导热性、延展性好。
在化学性质方面,第一过渡系元素的单质比第二、三过渡系元素的单质活泼。
化学性质变化总趋势是同一过渡系单质的活泼性从左到右降低。
或:d 区元素价电子层结构是(n-1)d1-8ns1-2。
它们ns轨道上的电子数几乎保持不变,主要差别在于(n-1)d 轨道上的电子数不同。
又因(n-1)d轨道和ns轨道的能量相近,d电子可以全部或部分参与成键,由此构成了d区元素的一些特性:全部是金属,原子半径小,密度大,熔、沸点高,有良好的导热、导电性能,化学性质相近。
大多具有可变的氧化态。
由于d轨道有未成对电子,水合离子一般具有颜色。
由于所带电荷高,离子半径小,且往往具有未充满的d电子轨道,所以容易形成配合物。
【12-2】完成下列反应式:(1)TiO2+H2SO4(浓)→(2)TiO2++Zn+H+→(3)TiO2+C+Cl2→(4)V2O5+NaOH→(5)V2O5+H2SO4→(6)V2O5+HCl→(7)VO2++H2C2O4+H+→解:(1)TiO2 + H2SO4 (浓) = TiOSO4 + H2O(2)2TiO2+ + Zn + 4 H+ = 2 Ti3+ + Zn2+ +2 H2O(3)TiO2 + 2 C + 2 Cl2 (加热) = TiCl4 + 2 CO(4)V2O5 + 6 NaOH = 2 Na3VO4 + 3 H2O(5)V2O5 + H2SO4 = (VO2)2SO4 + H2O(6)V2O5 + 6 HCl = 2 VOCl2 + Cl2 + 3 H2O(7)2VO+ + H2C2O4 + 2 H+ = 2VO2+ + 2CO2 +2H2O【12-3】在酸性溶液中钒的电势图为已知φθ(Zn2+/Zn)=-0.76V, φθ(Sn2+/Sn)=-0.14V, φθ(Fe3+/Fe2+)=0.77V。


高中《无机化学》第十六至十八章测试题及答案(d区元素、f区元素)(总9页)-本页仅作为预览文档封面,使用时请删除本页-高中《无机化学》第十六至十八章测试题及答案(d区元素、f区元素)第十六章 d区元素(一)一、填空题1、在所有过渡元素中,熔点最高的金属是 W ,熔点最低的是 Hg ,硬度最大的是 Cr ,密度最大的是 Os ,导电性最好的是 Ag ,耐海水腐蚀的是Ti 。
2、分别写出下列离子的颜色:[Fe(H2O)6]2+淡绿色,FeO42-紫色,[FeCl4]-黄色,[Fe(H2O)6]3+淡紫色,[Ti(H2O)6]3+紫色,VO43-淡黄色,[Co(H2O)6]2+粉红色,[Mn(H2O)6]2+粉红色,[Ni(H2O)6]2+绿色。
3、CrCl3溶液与氨水反应生成灰绿色的 Cr(OH)3沉淀该产物与NaOH溶液反应生成亮绿色的 Cr(OH)4-。
4、锰在自然界主要以软锰矿的形式存在,在强氧化剂(如KClO3)作用下碱熔时只能得到 +6 价锰的化合物,而得不到高锰酸盐,这是因为后者在碱中和受热均分解。
5、K2Cr2O7(s)与浓H2SO4反应生成的氧化物为 CrO3,它为橙红色,遇酒精立即着火,生成铬的一种绿色氧化物,其化学式为 Cr2O3。
KMnO4(s)与浓H2SO4作用生成的氧化物为 Mn2O7;MnO2与浓H2SO4反应生成的气体是O2。
6、高锰酸钾是强氧化剂,它在酸性溶液中与H2O2反应的主要产物是 O2和 Mn2+,它在中性或弱碱性溶液中与Na2SO3反应的主要产物为 SO42-和MnO2。
7、在强碱性条件下,KMnO4溶液与MnO2反应生成绿色的 K2MnO4;在该产物中加入硫酸后生成紫色的 KMnO4和褐色的 MnO2。
8、三氯化铁蒸气中含有的聚合分子化学式为 Fe2Cl6,其结构与金属 Al 的氯化物相似。
FeCl3能溶于有机溶剂。
9、既可用于鉴定Fe3+,又可用于鉴定Co2+的试剂是 KCNS ,当Fe3+存在时,能干扰Co2+的鉴定,可加入 NaF 因生成 FeF63-而将Fe3+掩蔽起来,消除对Co2+鉴定的干扰。

周期表化学元素周期表图集(20张)的编排显示出不同元素的化学性质的周期性,在周期表中,元素按原子序(即原子核内的质子数目)递增次序排列,并分为若干列和栏,在同一行中的称为同一周期,根据量子力学,周期对应着元素原子的电子排布,显示出该原子的已装填电子层数目。
沿着周期表向下,周期的长度逐渐上升,并按元素的电子排布划分出s区元素、p区元素、d区元素和f区元素。
而同一栏中的则称为同一族,同一族的元素有着相似的化学性质。
在印刷的周期表中,会列出元素的符号和原子序数。
而很多亦会附有以下的资料,以元素X为例:A:质量数(Mass number) ,即在数量上等于原子核(质子加中子)的粒子数目。
Z:原子序数,即是质子的数目。
由于它是固定的,一般不会标示出来。
e:净电荷,正负号写在数字后面。
n:原子数目,元素在非单原子状态(分子或化合物)时的数目。
除此之外,部份较高级的周期表更会列出元素的电子排布、电负性和价电子数目。
元素读音第一周期元素:1 氢(qīng) 2 氦(hài) 元素周期表正确金属汉字写法第二周期元素:3 锂(lǐ) 4 铍(pí) 5 硼(péng) 6 碳(tàn) 7 氮(dàn) 8 氧(yǎng) 9 氟(fú) 10 氖(nǎi)第三周期元素:11 钠(nà) 12 镁(měi) 13 铝(lǚ) 14 硅(guī) 15 磷(lín) 16 硫(liú) 17 氯(lǜ) 18 氩(yà)第四周期元素:19 钾(jiǎ) 20 钙(gài) 21 钪(kàng) 22 钛(tài) 23 钒(fán) 24 铬(gè) 25 锰(měng) 26 铁(tiě) 27 钴(gǔ) 28 镍(niè) 29 铜(tóng) 30 锌(xīn) 31 镓(jiā) 32 锗(zhě) 33 砷(shēn) 34 硒(xī) 35 溴(xiù) 36 氪(kè)第五周期元素:37 铷(rú) 38 锶(sī) 39 钇(yǐ) 40 锆(gào) 41 铌(ní) 42 钼(mù) 43 锝(dé) 44 钌(liǎo) 45 铑(lǎo) 46 钯(bǎ) 47 银(yín) 48 镉(gé) 49 铟(yīn) 50 锡(xī) 51 锑(tī) 52 碲(dì) 53 碘(diǎn) 54 氙(xiān)第六周期元素:55 铯(sè) 56 钡(bèi) 57 镧(lán) 58 铈(shì) 59 镨(pǔ) 60 钕(nǚ) 61 钷(pǒ) 62 钐(shān) 63 铕(yǒu) 64 钆(gá) 65 铽(tè) 66 镝(dī) 67 钬(huǒ) 68 铒(ěr) 69 铥(diū) 70 镱(yì) 71 镥(lǔ) 72 铪(hā) 73 钽(tǎn) 74 钨(wū) 75 铼(lái) 76 锇(é) 77 铱(yī) 78 铂(bó) 79 金(jīn) 80 汞(gǒn g) 81 铊(tā) 82 铅(qiān) 83 铋(bì) 84 钋(pō) 85 砹(ài) 86 氡(dōng)H氢qīng He氦hàiLi锂lǐ Be铍pí B硼péng C碳tàn N氮dàn O氧yǎng F 氟fú Ne氖nǎi Na钠nà Mg镁měi Al铝lǚ Si硅guī P磷lín S硫liú Cl氯lǜ Ar 氩yà K钾jiǎ Ca钙gài Sc钪kàng Ti钛tài V钒fán Cr铬gè Mn锰měng Fe 铁tiě Co钴gǔ Ni镍niè Cu铜tóng Zn锌xīn Ga镓jiā Ge锗zhě As砷shēn Se 硒xīBr溴xiù Kr氪kè Rb铷rú Sr锶sī Y钇yǐ Zr锆gào Nb铌ní Mo钼mù Tc 锝dé Ru钌liǎo Rh铑lǎo Pd钯bǎ Ag银yín Cd镉gé In铟yīn Sn锡xī Sb锑tī Te碲dì I碘diǎn Xe氙xiān Cs铯sè Ba钡bèi La镧lán Hf铪hāTa钽tǎn W 钨wū Re铼lái Os锇é Ir铱yī Pt铂bó Au金jīn Hg汞gǒng Tl铊tā Pb铅qiān Bi铋bì Po钋pō At砹ài Rn氡dōng Fr钫fāng Ra镭léi Ac锕ā Ce铈shì Pr 镨pǔ Nd钕nǚ Pm钷pǒ Sm钐shān Eu铕yǒu Gd钆gá Tb铽tè Dy镝dī Ho 钬huǒ Er铒ěr Tm铥diū Yb镱yì Lu镥lǔ Th钍tǔ Pa镤pú U铀yóu Np镎náPu钚bù Am镅méi Cm锔jú Bk锫péi Cf锎kāi Es锿āi Fm镄fèi Md钔mén No 锘nuò Lr铹láo第一周期:氢氦---- 侵害第二周期:锂铍硼碳氮氧氟氖---- 鲤皮捧碳蛋养福奶第三周期:钠镁铝硅磷硫氯氩---- 那美女桂林留绿牙第四周期:钾钙钪钛钒铬锰---- 嫁给康太反革命铁钴镍铜锌镓锗---- 铁姑捏痛新嫁者砷硒溴氪---- 生气休克第五周期:铷锶钇锆铌---- 如此一告你钼锝钌---- 不得了铑钯银镉铟锡锑---- 老爸银哥印西提碲碘氙---- 地点仙第六周期:铯钡镧铪----(彩)色贝(壳)蓝(色)河钽钨铼锇---- 但(见)乌(鸦)(引)来鹅铱铂金汞砣铅---- 一白巾供它牵铋钋砹氡---- 必不爱冬(天)第七周期:钫镭锕---- 防雷啊!唉,没办法,这么难记的东东,又必须要背,就只能这样了。



元素周期表口诀歌元素周期表口诀歌元素周期表是学习化学必须掌握的一个知识点,接下来店铺搜集了元素周期表口诀歌,仅供大家参考,希望帮助到大家。
元素周期表口诀歌我是氢,我最轻,火箭靠我运卫星;我是氦,我无赖,得失电子我最菜;我是锂,密度低,遇水遇酸把泡起;我是铍,耍赖皮,虽是金属难电离;我是硼,有点红,论起电子我很穷;我是碳,反应慢,既能成链又成环;我是氮,我阻燃,加氢可以合成氨;我是氧,不用想,离开我就憋得慌;我是氟,最恶毒,抢个电子就满足;我是氖,也不赖,通电红光放出来;我是钠,脾气大,遇酸遇水就火大;我是镁,最爱美,摄影烟花放光辉;我是铝,常温里,浓硫酸里把澡洗;我是硅,色黑灰,信息元件把我堆;我是磷,害人精,剧毒列表有我名;我是硫,来历久,沉淀金属最拿手;我是氯,色黄绿,金属电子我抢去;我是氩,活性差,霓虹紫光我来发;我是钾,把火加,超氧化物来当家;我是钙,身体爱,骨头牙齿我都在;我是钛,过渡来,航天飞机我来盖;我是铬,正六铬,酒精过来变绿色;我是锰,价态多,七氧化物爆炸猛;我是铁,用途广,不锈钢喊我叫爷;我是铜,色紫红,投入硝酸气棕红;我是砷,颜色深,三价元素夺你魂;我是溴,挥发臭,液态非金我来秀;我是铷,碱金属,沾水烟花钾不如;我是碘,升华烟,遇到淀粉蓝点点;我是铯,金黄色,入水爆炸容器破;我是钨,高温度,其他金属早呜呼;我是金,很稳定,扔进王水影无形;我是汞,有剧毒,液态金属我为独;我是铀,浓缩后,造原子弹我最牛;我是镓,易融化,沸点很高难蒸发;我是铟,软如金,轻微放射宜小心;我是铊,能脱发,投毒出名看清华;我是锗,可晶格,红外窗口能当壳;我是硒,补人体,口服液里有玄机;我是铅,能储电,子弹头里也出现。
元素周期表相关记忆技巧1、化合价实质之歌化合价实质要记准,金正非负单质零;氢一氧二应记住,正负总价和为零;许多元素有变价,条件不同价不同。
注:“金正”指金属的化合价通常显正价:“非负”指非金属的化合价通常显负价。


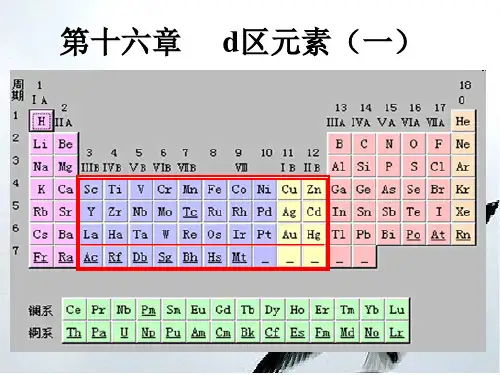
表格说明周期表化学元素周期表图集(20张)的编排显示出不同元素的化学性质的周期性,在周期表中,元素按原子序(即原子核内的质子数目)递增次序排列,并分为若干列和栏,在同一行中的称为同一周期,根据量子力学,周期对应着元素原子的电子排布,显示出该原子的已装填电子层数目。
沿着周期表向下,周期的长度逐渐上升,并按元素的电子排布划分出s区元素、p区元素、d区元素和f区元素。
而同一栏中的则称为同一族,同一族的元素有着相似的化学性质。
在印刷的周期表中,会列出元素的符号和原子序数。
而很多亦会附有以下的资料,以元素X为例:A:质量数(Mass number) ,即在数量上等于原子核(质子加中子)的粒子数目。
Z:原子序数,即是质子的数目。
由于它是固定的,一般不会标示出来。
e:净电荷,正负号写在数字后面。
n:原子数目,元素在非单原子状态(分子或化合物)时的数目。
除此之外,部份较高级的周期表更会列出元素的电子排布、电负性和价电子数目。
元素读音第一周期元素:1 氢(qīng) 2 氦(hài) 元素周期表正确金属汉字写法第二周期元素:3 锂(lǐ) 4 铍(pí) 5 硼(péng) 6 碳(tàn) 7 氮(dàn) 8 氧(yǎng) 9 氟(fú) 10 氖(nǎi) 第三周期元素:11 钠(nà) 12 镁(měi) 13 铝(lǚ) 14 硅(guī) 15 磷(lín) 16 硫(liú) 17 氯(lǜ) 18 氩(yà) 第四周期元素:19 钾(jiǎ) 20 钙(gài) 21 钪(kàng) 22 钛(tài) 23 钒(fán) 24 铬(gè) 25 锰(měng) 26 铁(tiě) 27 钴(gǔ) 28 镍(niè) 29 铜(tóng) 30 锌(xīn) 31 镓(jiā) 32 锗(zhě) 33 砷(shēn) 34 硒(xī) 35 溴(xiù) 36 氪(kè) 第五周期元素:37 铷(rú) 38 锶(sī) 39 钇(yǐ) 40 锆(gào) 41 铌(ní) 42 钼(mù) 43 锝(dé) 44 钌(liǎo) 45 铑(lǎo) 46 钯(bǎ) 47 银(yín) 48 镉(gé) 49 铟(yīn) 50 锡(xī) 51 锑(tī) 52 碲(dì) 53 碘(diǎn) 54 氙(xiān) 第六周期元素:55 铯(sè) 56 钡(bèi) 57 镧(lán) 58 铈(shì) 59 镨(pǔ) 60 钕(nǚ) 61 钷(pǒ) 62 钐(shān) 63 铕(yǒu) 64 钆(gá) 65 铽(tè) 66 镝(dī) 67 钬(huǒ) 68 铒(ěr) 69 铥(diū) 70 镱(yì) 71 镥(lǔ) 72 铪(hā) 73 钽(tǎn) 74 钨(wū) 75 铼(lái) 76 锇(é) 77 铱(yī) 78 铂(bó) 79 金(jīn) 80 汞(gǒng) 81 铊(tā) 82 铅(qiān) 83 铋(bì) 84 钋(pō) 85 砹(ài) 86 氡(dōng) 第七周期元素:87 钫(fāng) 88 镭(léi) 89 锕(ā) 90 钍(tǔ) 91 镤(pú) 92 铀(yóu) 93 镎(ná) 94 钚(bù) 95 镅(méi) 96 锔(jú) 97 锫(péi) 98 锎(kāi) 99 锿(āi) 100 镄(fèi) 101 钔(mén) 102 锘(nuò) 103 铹(láo) 104 鈩(lú) 105 (dù) 106 (xǐ) 107 (bō) 108 (hēi) 109 䥑(mài) 110 鐽(dá) 111 錀(lún) 112 鎶(gē)[暂定] 注:新元素汉字请使用Win7系统浏览,XP系统下无法显示。