第十五章 有机含氮化合物
- 格式:doc
- 大小:2.25 MB
- 文档页数:36


第十五章含氮有机合物(Nitrogenous Organic Compounds)授课对象:应用化学、制药工程、化学反应工程与工艺、药学学时安排:6h教材:《有机化学》(第四版)高鸿宾主编 2005年5月一、教学目的与要求1、掌握芳香硝基化合物的性质(吸电子硝基对苯酚、苯胺等酸碱性的影响),巩固学习掌握芳环上亲电取代反应机理。
2、掌握重氮化反应。
掌握胺的结构、分类和命名,胺的化学性质。
3、掌握重氮化反应,重氮盐的性质;重氮化合物在有机合成中的应用。
4、初步了解腈命名和性质。
二、教学重点1、芳香硝基化合物中芳环亲核取代反应机理。
2、胺的化学性质。
3、重氮盐在有机合成中的应用。
三、教学难点1、伯、仲、叔胺与亚硝酸的反应。
重氮盐在有机合成上的应用。
四、教学方法讲授法。
总结往届学生的教学反馈情况,拟具体采用如下教学方法,以突出重点,突破难点。
通过对比伯、仲、叔胺与亚硝酸的反应的不同点,帮助学生掌握不同类型的胺与亚硝酸的反应。
多练,多举些例题,帮助学生掌握重氮盐在有机合成上的应用。
五、教具电脑、投影仪、Powerpoint课件、教鞭。
六、教学步骤引言:胺属于有机含氮化合物,是一类很重要的化合物。
它们中有的严重危害人类健康如亚硝胺、海洛因等;有的对维护人类健康或在化学生产中有着重要的作用如胆胺、胆碱、肾上腺素、重氮化合物和偶氮化合物等。
15.1 芳香族硝基化合物一、芳香硝基化合物的表达方式与结构分子表达式:结构示意图:(硝基与苯环共轭)注意:硝基的电子效应:强吸电子基团(吸电子诱导、吸电子共轭)硝基的同分异构体:芳香硝基化合物与亚硝酸(芳基)酯是同分异构体。
Ar-NO2,Ar-O-N=O二、芳香硝基化合物的物理性质、光谱性质和用途1 物理性质:一元芳香硝基化合物是高沸点液体,多数是有机物的良好溶剂。
不溶于水,有毒。
二元和多元芳香硝基化合物为无色或黄色固体2 光谱性质:硝基的IR 在1365-1335 cm-1,1550-1510 cm-1 处有吸收峰。




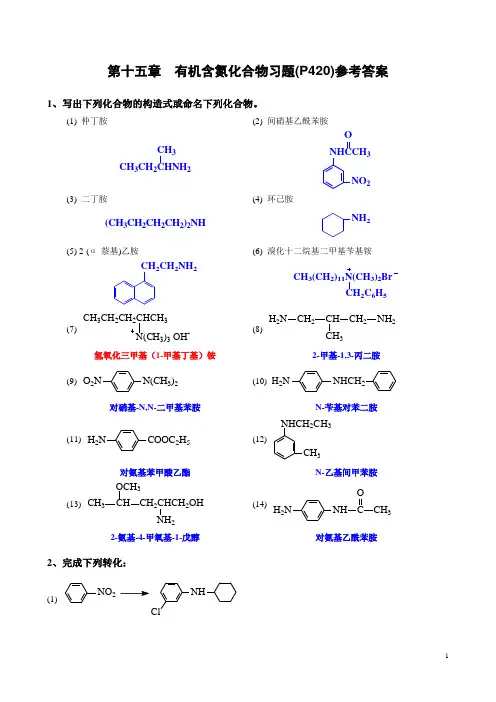
第十五章 有机含氮化合物习题(P420)参考答案1、写出下列化合物的构造式或命名下列化合物。
(1) 仲丁胺(2) 间硝基乙酰苯胺CH 3CH 2CHNH 2CH 3NHCCH 3NO 2O(3) 二丁胺(4) 环己胺(CH 3CH 2CH 2CH 2)2NHNH 2(5) 2-(α-萘基)乙胺(6) 溴化十二烷基二甲基苄基铵CH 2CH 2NH 2CH 3(CH 2)11N(CH 3)2BrCH 2C 6H 5(7)CH 3CH 2CH 2CHCH 3N(CH 3)3 OH-(8)H 2N CH 2CH CH 2NH 2CH 3氢氧化三甲基(1-甲基丁基)铵2-甲基-1,3-丙二胺(9) O 2NN(CH 3)2(10) H 2NNHCH 2对硝基-N,N-二甲基苯胺N-苄基对苯二胺(11) H 2NCOOC 2H 5(12) NHCH 2CH 3CH 3对氨基苯甲酸乙酯N-乙基间甲苯胺(13) CH 3CH CH 2CHCH 2OH 2OCH 3(14)H 2N NH C OCH 32-氨基-4-甲氧基-1-戊醇对氨基乙酰苯胺2、完成下列转化:(1)NO 2NHCl解:NO 2NHCl2Fe, HClNH2Cl(2) CH 2=CH CH=CH 2H 2N(CH 2)6NH 2解:CH 2=CH CH=CH 2H 2N(CH 2)6NH 22Cl CH 2CH=CHCH 2Cl2 Ni(3) 正丁醇正丁胺、正丙胺、正戊胺解:CH 3CH 2CH 2CH 22N - K +O ON OOCH 2CH 2CH 2CH 3CH 3CH 2CH 2CH 2NH 2H OCH 3CH 2CH 2CH 2OHCH 3CH 2CH 2NH 2(1) NH _(1) [O]2CH 3CH 2CH 2CH 2OHCH 3CH 2CH 2CH 2CH 2NH 2(1) SOCl (2) NaCNCH 3CH 2CH 2CH 2CN 2Ni(4) C 2H 5OH 、C 6H6C 6H 5CHCH 3NHC 2H 5解:C 2H 5OHHClNH 3C 2H 5NH 2或PCl 32C 2H 5CH3COOH P O (CH 3CO)2OCCH 3OCHCH 3NHC 2H 5[O]3、排序:(1) 将下列化合物按沸点由高到低顺序排列:(A) 丙胺 (B) 丙醇 (C) 甲乙醚 (D) 甲乙胺 (E) 三甲胺 解:(B )>(A)>(D)>(C)>(E)(2) 将下列化合物按亲核取代反应活性由高到低顺序排列:(A) 氯苯 (B) 对甲氧基氯苯 (C) 对硝基氯苯 (D) 2,4-二硝基氯苯 解:(D)>(C)>(A)>(B)(3) 将下列化合物按碱性由强到弱顺序排列:(A) (CH3)4NOH(B) C6H5NH2(C) C2H5NH2(D) C6H5NHCH3(E) CH3CONH2解:(A)>(C)>(D)>(B)>(E)(4) 将下列化合物按碱性由强到弱顺序排列:(A) CH3CH2CH2NH2(B) CH3CHCH2NH2OH(C)CH3CH2CH2NH2OH(D)CH3CH2CHNH2CH3解:(D)>(A)>(B)>(C)(5) 将下列化合物按碱性由强到弱顺序排列:(A) NHCOCH3(B) NHSO2CH3(C) NHCH3(D) N CH3(E) NH2解:(E)>(D)>(C)>(A)>(B)(6) 将下列化合物按碱性由强到弱顺序排列:(A) 对甲苯胺(B) 苄胺(C) 2,4-二硝基苯胺(D) 对硝基苯胺(E) 对氯苯胺解:(B)>(A)>(E)>(D)>(C)4、用简单的化学方法区别下列化合物:(1) (A) 硝基苯(B) 硝基环己烷(C) 间甲苯胺(D) N-甲基苯胺(E) N,N-二甲基苯胺解:ABCDE溶解不溶解溶解不溶解不溶解不溶解溶解硝基苯硝基环己烷清亮溶液油状物间甲苯胺N-甲基苯胺N,N-二甲基苯胺(2) (A) OH(B) NH2(C) N H(D) N CH3解:ABCD 溶解不溶解不溶解不溶解清亮溶液油状物苯胺环戊胺N-甲基环戊胺苯酚5、用简单的化学方法分离、提纯下列各组混合物:(1) (A) 苄胺(B) N-甲基环己胺(C) 苯甲醇(D) 对甲苯酚解:水层ABCD -油层水层有机层水层H+p-CH3-C6H4-OH (D) C6H5CH2OH (C)(2) 分液p-CH-C H-SO ClNaOH清亮溶液固体沉淀过滤C6H5CH2NH2NHCH3(1) H O/OH-, ∆干燥、蒸馏(1) HO/OH-, ∆干燥、蒸馏(A)(B)(2) N-甲基苯胺中混有少量N,N-二甲基苯胺,请设计实验方案提纯N-甲基苯胺。



第15章有机含氮化合物1.写出下列化合物的构造式或命名(1)仲丁胺(2)1,3-丙二胺(3)溴化四正丁铵(4)对氨基-N,N-二甲苯胺(5)(6)(7)(8)(9)解:(1)(2)(3)(4)(5)2-二甲氨基乙醇(6)N-苄基对苯二胺(7)氢氧化三甲基(1-甲基-2-苯基乙基)铵(8)2-对氨甲基苯基乙胺(9)2-(α-萘基)乙胺2.两种异构体(A)和(B),分子式都是,用发烟硝酸分别使它们硝化,得到同样产物。
把(A)和(B)分别氧化得到两种酸,它们分别与碱石灰加热,得到同样产S还原,则得间硝基苯胺。
写出(A)和(B)的构造式及各步物为,后者用Na反应式。
解:3.完成下列转变:(1)丙烯→异丙胺(2)正丁醇→正戊胺和正丙胺(3)3,5-二溴苯甲酸→3,5-二溴苯甲胺(4)乙烯→1,4一丁二胺(5)乙醇,异丙醇→乙基异丙基胺(6)苯,乙醇→α-乙氨基乙苯解:4.把下列各组化合物的碱性由强到弱排列成序:解:(1)(A)>(C)>(B)(2)(A)>(B)>(C)>(D)(3)(D)>(C)>(A)>(B)5.试拟一个分离环己基甲酸、三丁胺和苯酚的方法。
解:6.用化学方法区别下列各组化合物:(3)(A)硝基苯(B)苯胺(C)N-甲基苯胺(D)N,N-二甲苯胺解:7.试分别写出正丁胺、苯胺与下列化合物作用的反应式。
(1)稀盐酸(2)稀硫酸(3)乙酸(4)稀NaOH溶液(5)乙酐(6)异丁酰氯(7)苯磺酰氯+KOH(水溶液)(8)溴乙烷(9)过量的CH3I,然后加湿Ag2O(10)(9)的产物加强热(11)CH3COCH3+H2+Ni(12)HONO(即NaNO2+HCI),0℃(13)邻苯二甲酸酐(14)氯乙酸钠解:与正丁胺的反应产物:与苯胺的反应产物:8.写出下列反应的最终产物:解:9.解释下列实验现象:。
有机化学课程教案编写日期:2006 年 11月 9日章、节(或课题、单元)名称第十五章有机含氮化合物授课学时 6目的要求l、掌握硝基化合物的结构、命名方法、性质、制法及其代表物。
2 能够运用诱导效应、共轭效应解释硝基使苯环上氯原子的亲核取代活性增加和使酚羟基的酸性增强的原因。
3、掌握胺的结构、分类、命名和氮原子的杂化状态;了解胺的物理性质;重点掌握胺的化学性质;掌握通过官能团相互转变制备胺的方法以及伯胺的特殊制法;了解苯胺、二甲胺、乙二胺和已二胺的性质、工业制法和用途。
4、了解季铵盐和季铵碱的性质以及季铵碱的热消除规律(Hofmann规则)。
5、掌握重氮盐的性质以及它们在有机合成上的应用。
6、了解偶氮化合物的结构和颜色的关系,以及染料的显色原理。
重点:1、胺的碱性及其影响因素。
2、硝基对邻、对位上取代基的影响。
3、胺的制法:硝基物还原、醛酮还原胺化、Hoffmann降级、Gabriel法合成。
4、胺的化性:碱性,烷基化,酰基化,磺酰化,与HNO2作用,氧化,芳环上的取代反应。
5、重氮盐的制备及其在合成上应用。
重氮盐的放氮反应、偶联反应。
6、N-H的伸缩振动吸收:3300-3600cm-1,伯胺出双峰,仲胺出单峰,叔胺不出峰。
7、腈和丙烯腈的制法、性质及应用。
难点:1、胺的酰基化,磺酰化(Hinsber反应),胺与亚硝酸的反应及其应用。
2、重氮盐的制备及其在合成上应用。
教学组织教学方法:课堂教学采用多媒体教学,以ppt为主。
习题课采用黑板教学与学生讨论相结合的方式。
作业:P526一(1~6)、三(2、6)、四(1、3)、五、六(1、3)、七、八、十、十一(2选做、3、7除外)、十六、十七、十八参考书目文献:1、张黯主编,有机化学教程下册,北京:高等教育出版社,1990.580~6022、邢其毅等著,基础有机化学(第二版) 下册,北京:高等教育出版社,1994. 635~668,720~7563、徐寿昌编,有机化学(第二版) ,北京:高等教育出版社,1993,360~399 5、袁履冰主编,有机化学,北京:高等教育出版社,1999, 339~367授课小结授课情况正常。
第十五章 有机含氮化合物15.1 芳香族硝基化合物芳环上的一个或多个氢原子被硝基取代后的化合物为芳香族硝基化合物。
例如:NO 2CH 33)2NO 2NO 2CH 32O 2N2-硝基-4-异丙基甲苯2,4,6-三硝基甲苯2-硝基萘(TNT)键长测定表明,硝基中两个氮氧键长相同,负电荷平均分布在两个氧原子上。
硝基的构造可表示如下:NO O -NONO O -NO -O 或或15.1.1 芳香族硝基化合物的制法芳香族硝基化合物一般采用直接硝化法制备。
例如:+ HNO 324。
NO 2+ H 2O重要中间体,常用溶剂,缓和氧化剂CH 3CH 3H 3CCH 3CH 3H 3CNO 2HNO 33ClClNO 2Cl2Cl2NO 2324。
324130 C。
+15.1.2 芳香族硝基化合物的物理性质μ大,极性大,b.p 高,有苦杏仁味,有毒性,不溶于水,多硝基物易爆炸,但某些多硝基物有类似于天然麝香的香气,被称为硝基麝香,约占目前世界上商品化人造麝香的50%,其中葵子麝香是硝基麝香中用量最大的品种。
CH 3NO 2O 2NC(CH 3)3OCH 3CH 3COCH 3O 2N CH 3NO 2(CH 3)3CCH 3NO 2O 2N (CH 3)3CNO 2CH 3葵子麝香酮麝香二甲苯麝香长期接触芳香族硝基化合物会引进中毒,因为大多数芳香族硝基化合物能使血红蛋白变性。
15.1.3 芳香族硝基化合物的波谱性质在红外光谱中硝基化合物最典型的特征吸收峰为硝基中N-O 键的对称和反对称吸收,其次为碳-氮键的伸缩振动吸收:特征峰 ~1540 ~1350 ~870 2 ν2 ν例:硝基苯的红外光谱。
(高四P482)15.1.4 芳香族硝基化合物的化学性质 (1) 还原硝基化合物被还原的最终产物是胺。
还原剂、介质不同时,还原产物不同。
NO 2NONHOHNH2硝基苯亚硝基苯N -羟基苯胺苯胺[H][H][H][H] :LiAlH 4 , H 2/Cu , H 2/Pt , Fe+HCl , SnCl 2+HCl... ...例:NO 2NH 2H ,Cu o新工艺,清洁工艺苯胺重要的染料、药物中间体NH 2NO 22NHCOCH 3NHCOCH 325NH 2NH 2Fe+HCl+ Fe 3O 4“铁泥”NO 2NH 2对硝基苯胺对苯二胺讨论:①还原剂:H 2-Cu :产率高,质量纯度高,无“铁泥”污染,中性条件下进行,不破坏对酸或碱敏感的基团。
Fe+HCl :操作简单,实验室较为常用。
酸性条件下进行,不适于还原带有对酸或碱敏感的基团的化合物。
SnCl 2+HCl :特别适用于还原芳环有易被还原羰基的反应物:CHO NO 2CHO NO 2SnCl 2 , 浓HCl②反应介质:酸性介质:彻底还原,生成苯胺;中性介质:单分子还原,得N -羟基苯胺; 碱性介质:双分子还原,得到一系列产物。
2NO 2N=N +O -NH-NHNH 2偶氮苯氢化偶氮苯苯胺③选择性还原:NO 2NO 2(NH 4)2SNH 2NO 2or NH 4HS (NH 4)2S 2 Na 2S 2、、、Fe+HClNH 2NH 2OH NO 2NO 2O 2N225OHNH 2NO 2O 2NOHNO 22OHNH 22Na 2S, NH 4Cl o(2) 芳环上的亲电取代反应(“三化”)为什么是“三化”而不是“四化”?-NO 2是第二类定位基,使苯环钝化!所以,硝基苯不能发生付氏反应!NO 2NO 2NO 2324。
2NO 2Br NO 2。
24。
NO 2NO 2SO 3H特点:①反应温度均高于苯;②新引入基团上硝基的间位。
(3) 芳环的亲核取代反应芳环上连有硝基时,不易进行亲电取代反应,但可发生亲核取代反应。
例如:NO 2O 2NONaO 2N1. 5%NaOH ,季铵盐100 CoNO 22ClNO 22OH2o(1) Na CO , H O, 100 CNO 2NO 2OCH 3NO 2NO 2NHPh~80%180 Co芳环上的亲核取代反应在有机合成上应用有限,不如亲电取代反应那样应用广泛。
(4) 硝基对其邻、对位取代基的影响a. 对酚羟基酸性的影响时,酸性大增。
例如:pKa 10 7.15 4.0 0.25 原因:-NO 2的引入,使苯氧负离子的负电荷得到有效的分散。
当酚羟基与硝基处于间位时,酚的酸性增加并不十分明显:化合物OH OHNO2NO2OHOHO2NpKa 10 7.22 8.39 7.15原因:当硝基与羟基处于邻、对位时,既有诱导效应,又有共轭效应;当硝基与羟基处于间位时,只有诱导效应,没有共轭效应。
(b) 对羧酸酸性的影响当苯甲酸的苯环引入硝基后,与酚类似,其酸性增大。
且硝基处于羧基的邻、对位时更加显著:化合物COOH COOHNO2NO2COOHCOOHO2NNO2COOHO2NpKa 4.20 2.17 3.49 3.43 2.83 (c) 对卤原子活泼性的影响以下列水解反应为例:Ar-Cl Ar-OH水解ArCl 氯苯4-硝基氯苯2,4-二硝基氯苯2,4,6-三硝基氯苯反应条件NaOH,360℃20Mpa,铜催化剂Na2CO3/130℃Na2CO3/100℃Na2CO3/35℃反应条件苛刻反应条件温和以上的实验表明,若卤素原子的邻、对位有硝基等强吸电子基时,水解反应容易进行。
原因:硝基的引入有利于碱或亲核试剂的进攻。
15.2胺NH3(氨)分子中的氢原子被R-或Ar-取代后的衍生物叫做胺。
胺类广泛存在于生物界,如许多生物碱具有生理或药理作用。
例如:CHOHCHCH33CH3CH2OHH麻黄碱阿托品15.2.1 胺的分类和命名分类:① RNH 2 脂肪胺;ArNH 2 芳香胺;② RNH 2 伯胺、1°胺;R 2NH 仲胺、2°胺;R 3N 叔胺、3°胺;R 4N +X - 季铵盐,R 4N +OH - 季铵碱。
注意:伯、仲、叔胺与伯、仲、叔醇的涵义不同。
例:(CH 3)3C -OH 叔醇;(CH 3)3C -NH 2 伯胺;③ RNH 2 一元胺, H 2NRNH 2 二元胺 命名:① 习惯命名法:适用于简单胺。
CH 3NH 2(CH 3CH 2)2NH(HOCH 2CH 2)3NNH 2甲胺二乙胺苯胺三乙醇胺② 系统命名法:适用于复杂胺。
CH 3-CH-CH 2-CH-CH 2-CH 3CH 3NH 2CH 3-CH-CH 2-CH-N-CH 2-CH 3CH 3CH 3CH 2-CH 32-甲基-4-氨基己烷2-甲基-4-(二乙氨基)戊烷(-NH 2 氨基,-NHR 、-NR 2 取代氨基,=NH 亚胺基,)15.2.2 胺的结构NH 3(氨)分子中氮原子采取不等性sp 3杂化 ; 有机胺分子中氮原子也是采取不等性sp 3杂化。
CH 3H H 3H 3CH 3键长:键角:键角:键长:C-N 0.147nmC-N-C 108。
C-N 0.147nmN-H 0.101nm。
C-N-H 112.9H-N-H 105.9。
甲胺三甲胺由于下列转化所需的活化能较低(约25kJ/mol),简单的手性胺不能分离得到其中某一个对映体:CH 3C 2H 53C 2HCH 3C 2H H但手性的季铵盐却可被拆分:C 6H 5C 2H 5CH 32CH=CH 2+C 6H 5C 2H 5CH 3CH 2=CHCH 2+15.2.3 胺的制法 (1) 氨或胺的烃基化3RN +H 3 X -32 + NH 4X烷基化剂2 + RXR 2N +H 2 X-亲核试剂3R 24XR 3N + RXR 4N + X -该反应的产物是RNH 2、R 2NH 、R 3N 、R 4NX 等的混合物,需分离精制。
醇也可用作烷基化剂:CH 3 OH + H NH 2CH 3NH 2 + H 2O3)2NHAl 2O 3,23,3(CH 3)3N该产物仍是一混合物,以二甲胺和三甲胺为主。
(2) 腈和酰胺的还原腈经催化加氢得到伯胺:CH 2CN + H 2苯乙腈苄腈苯乙胺2- 苯乙胺CH 2CH 2NH 2NC(CH 2)4CNH 2NCH 2(CH 2)4CH 2NH 2己二腈己二胺制尼龙-66的原料酰胺用氢化铝锂还原得伯、仲、叔胺:4H 2ON-C-CH 3CH 3O2-CH 3CH 3N-甲基-N-乙酰苯胺N-甲基-N-乙基苯胺(91%)工业上由高级脂肪酸经酰胺制备有重要用途的高级脂肪伯胺的方法:C 15H 31C 15H 31NH 2OC 15H 31C N C 15H 31CH 2NH 23- H 2O- H 2O2(3) 醛和酮的还原氨化C=O CHNH 2+ NH 3260 C,P。