第五章 金属的钝化
- 格式:ppt
- 大小:224.00 KB
- 文档页数:24




钝化钝化的定义使金属表面转化为不易被氧化的状态,而延缓金属的腐蚀速度的方法。
一种活性金属或合金,其中化学活性大大降低,而成为贵金属状态的现象,叫钝化。
金属由于介质的作用生成的腐蚀产物如果具有致密的结构,形成了一层薄膜(往往是看不见的),紧密覆盖在金属的表面,则改变了金属的表面状态,使金属的电极电位大大向正方向跃变,而成为耐蚀的钝态。
如Fe→Fe++时标准电位为-0.44V,钝化后跃变到+0.5~1V,而显示出耐腐蚀的贵金属性能,这层薄膜就叫钝化膜。
金属的钝化也可能是自发的过程(如在金属的表面生成一层难溶解的化合物,即氧化物膜)。
在工业上是用钝化剂(主要是氧化剂)对金属进行钝化处理,形成一层保护膜。
钝化的机理我们知道,铁、铝在稀HN O3或稀H2SO4中能很快溶解,但在浓H NO3或浓H2SO4中溶解现象几乎完全停止了,碳钢通常很容易生锈,若在钢中加入适量的Ni、Cr,就成为不锈钢了。
金属或合金受一些因素影响,化学稳定性明显增强的现象,称为钝化。
由某些钝化剂(化学药品)所引起的金属钝化现象,称为化学钝化。
如浓H NO3、浓H2SO4、HClO3、K2C r2O7、KMnO4等氧化剂都可使金属钝化。
金属钝化后,其电极电势向正方向移动,使其失去了原有的特性,如钝化了的铁在铜盐中不能将铜置换出。
此外,用电化学方法也可使金属钝化,如将Fe置于H2S O4溶液中作为阳极,用外加电流使阳极极化,采用一定仪器使铁电位升高一定程度,Fe就钝化了。
由阳极极化引起的金属钝化现象,叫阳极钝化或电化学钝化。
金属处于钝化状态能保护金属防止腐蚀,但有时为了保证金属能正常参与反应而溶解,又必须防止钝化,如电镀和化学电源等。




金属的钝化有的金属(或合金)由于受某些氧化剂作用后其表面状况发生了改变,使金属(或合金)的化学活动性大大降低,耐腐蚀性大大增强,这种现象称为金属的钝化。
例如:Fe可与稀HNO3反应而溶解,但是,如果把Fe浸在密度大于1.25 g/cm3的浓HNO3中,铁却钝化而不溶。
Fe在浓HNO3中钝化后,不仅在稀HNO3中也不能再溶解,而且不能从铜盐(如CuSO4)溶液中置换出铜。
不仅铁,其它多种金属也可以发生钝化。
例如:Cr、Ni、Co、Mo、Al、Ta、Nb和W 等,其中最易钝化的金属是Cr、Mo、Al、Ni。
不仅硝酸,其它强氧化剂如浓H2SO4、氯酸、碘酸、重铬酸钾、高锰酸钾等,都可以使某些金属钝化,甚至空气中的氧气也能使有的金属(如Al、Cr等)钝化。
有许多因素能破坏钝化状态,或者阻止金属钝态生成。
将溶液加热或加入活性离子如Cl—、Br—、I—等和还原性气体如H2(特别在加热时)都能使钝态金属活化。
为什么金属会发生钝化现象?现在大多认为金属的钝化是由于金属跟介质作用而生成了一层极薄的肉眼看不见的保护膜的结果。
这层薄膜最经常的是金属的氧化物。
如铁与浓HNO3作用,铁表面被氧化成结构较复杂,组成为Fe8O11的氧化物。
这层氧化膜厚度是30×10-10~40×10-10m ,化学性质很不活泼,将Fe表面和介质完全隔绝,从而使铁处于钝态。
某些金属的钝化也可由阳极氧化来实现。
阳极氧化是将金属制件作阳极利用电解法使其表面上形成氧化物薄膜的过程。
像Al、Mg、Cu、钢等制件都可用此法钝化。
为了提高某些金属的抗蚀性能(有时同时增加美观),可采用化学方法或阳极氧化方法,使金属钝化。
金属的钝化在机械制造,仪器制造、武器、飞机及某些金属日常用品的制造中,以在某些金属制件表面生成防锈层或同时还有装饰性的覆盖层而广泛地被采用。
选自《中学生化学报》作者:阿元林、梁冬梅。
金属的钝化在现代工业生产中,我们常常会遇到金属钝化现象。
一些较活泼的金属,在某些特定的环境介质中,会呈现惰性状态。
如金属的电极电位因外加阳极电流或局部阳极电流而向正方向移动,当超过一定数值后,金属的溶解速度反而剧烈地减小了,铁和不锈钢在硫酸中进行阳极极化时便观察到此现象。
金属阳极溶解过程中的这种“反常”现象称为金属的钝化过程。
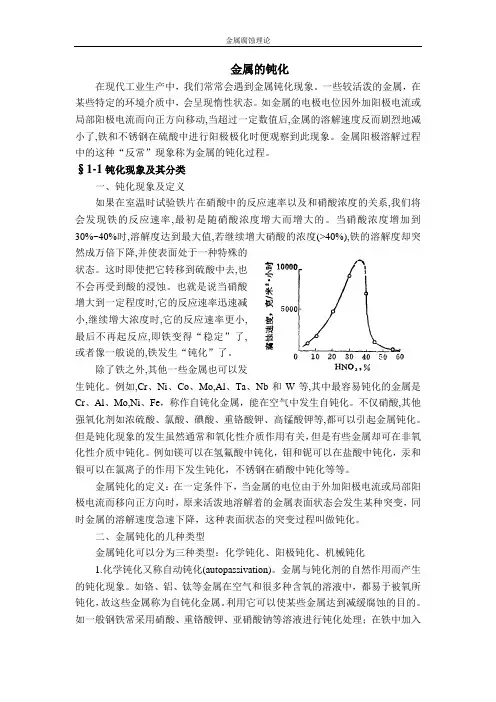
§1-1钝化现象及其分类一、钝化现象及定义如果在室温时试验铁片在硝酸中的反应速率以及和硝酸浓度的关系,我们将会发现铁的反应速率,最初是随硝酸浓度增大而增大的。
当硝酸浓度增加到30%~40%时,溶解度达到最大值,若继续增大硝酸的浓度(>40%),铁的溶解度却突然成万倍下降,并使表面处于一种特殊的状态。
这时即使把它转移到硫酸中去,也不会再受到酸的浸蚀。
也就是说当硝酸增大到一定程度时,它的反应速率迅速减小,继续增大浓度时,它的反应速率更小,最后不再起反应,即铁变得“稳定”了,或者像一般说的,铁发生“钝化”了。
除了铁之外,其他一些金属也可以发生钝化。
例如,Cr、Ni、Co、Mo,Al、Ta、Nb和W等,其中最容易钝化的金属是Cr、Al、Mo,Ni、Fe,称作自钝化金属,能在空气中发生自钝化。
不仅硝酸,其他强氧化剂如浓硫酸、氯酸、碘酸、重铬酸钾、高锰酸钾等,都可以引起金属钝化。
但是钝化现象的发生虽然通常和氧化性介质作用有关,但是有些金属却可在非氧化性介质中钝化。
例如镁可以在氢氟酸中钝化,钼和铌可以在盐酸中钝化,汞和银可以在氯离子的作用下发生钝化,不锈钢在硝酸中钝化等等。
金属钝化的定义:在一定条件下,当金属的电位由于外加阳极电流或局部阳极电流而移向正方向时,原来活泼地溶解着的金属表面状态会发生某种突变,同时金属的溶解速度急速下降,这种表面状态的突变过程叫做钝化。
二、金属钝化的几种类型金属钝化可以分为三种类型:化学钝化、阳极钝化、机械钝化1.化学钝化又称自动钝化(autopassivation)。

第5章金属的钝化铁、铝等金属在稀HNO3或稀H2SO4中能很快腐蚀,但是在浓HNO3或浓H2SO4中腐蚀现象几乎完全停止。
1836年斯柯比(Schobein)称金属在浓HNO3或浓H2SO4中获得的耐蚀状态为钝态。
从此,人们对金属的钝化进行了广泛的研究。
现今钝化在控制金属腐蚀和提高金属材料的耐蚀性方面占有十分重要的地位。
经钝化的铁重新放入稀HNO3中也不会再溶解,因为铁处于钝态。
金属或合金受一些因素影响,化学稳定性明显增强的现象,称为金属的钝化(Passivation of metals)。
由某些钝化剂(氧化剂)所引起的金属钝化,称为化学钝化。
如浓HNO3、浓H2SO4、HClO3、K2Cr2O7、KMnO4和O2等氧化剂都可使金属钝化。
此外,用电化学方法也可使金属钝化,如将铁置于H2SO4溶液中作为阳极,用外加的直流电使铁的电位升高到一定数值(即阳极极化),也能使铁的表面生成钝化膜。
由阳极极化引起的金属钝化现象,叫电化学钝化或阳极钝化。
研究钝化现象有很大的实际意义。
金属处于钝化状态能显著降低金属的自溶解和阳极溶解速度,保护金属防止腐蚀,但有时为了保证金属能正常参与反应而溶解,又必须防止钝化,如化学电源中电极的钝化常常带来有害的后果,使最大输出电流密度以及活性物质的利用率降低。
所以,长期以来,对钝化现象的研究受到很大的重视。
5.1 金属的钝化现象5.1.1 金属钝化的两种方式—化学钝化与电化学钝化1.化学钝化如果把一块铁片放在HNO3中,并考察铁片的溶解速度与HNO3浓度的关系(如图5.1所示),可以发现铁在稀硝酸中剧烈地溶解,并且铁的溶解速度随着HNO3浓度的增大而迅速增大。
当HNO3的浓度增加到30~40%时,铁的腐蚀速度达到最大值,若继续增加HNO3浓度超过40%,则铁的溶解速度就突然下降到原来的的1/4000,这一现象称为钝化。
如果继续增大HNO3浓度到90%以上,腐蚀速度又有较快的上升(在95%HNO3中铁的腐蚀速度约为90%HNO3中的10倍),这一现象称为过钝化。

金属钝化百科名片金属表面状态变化所引起的金属电化学行为使它具有贵金属的某些特征(低的腐蚀速率、正的电极电势)的过程。
若这种变化因金属与介质自然作用产生,称为化学钝化或自钝化;若该变化由金属通过电化学阳极极化引起,称为阳极钝化。
另有一类由于金属表面状态变化引起其腐蚀速率降低,但电极电势并不正移的钝化(如铅在硫酸中表面覆盖盐层引起腐蚀速率降低),称为机械钝化。
金属钝化后所处的状态称为钝态。
钝态金属所具有的性质称为钝性(或称惰性)。
钝化现象如果在室温时测试铁片在硝酸中的反应速率以及和硝酸浓度的关系,我们会发现铁的反应速率最初是随着硝酸浓度的增大而增大。
当增大到一定浓度时,它的反应速率迅速减小,继续增大硝酸的浓度时,它的反应速率更小,最后不再起反应。
此时我们就说铁变得“稳定”了,也就是铁发生“钝化”了。
不仅铁发生钝化,其他金属也可以发生钝化,如Cr(铬)、Ni (镍)、Co(钴)、Mo(钼)、Al(铝)、Ta(钽)、Nb(铌)和W(钨)等,其中最容易钝化的金属是Cr(铬)、Mo(钼)、Al(铝)、Ni(镍)、Fe(铁)。
不仅浓硝酸可以使金属发生钝化,其他强氧化剂如浓硫酸、(高)氯酸、(氢)碘酸、重铬酸钾、高锰酸钾酸性溶液等都可以引起金属的钝化。
在个别情况下,少数金属能在非氧化剂介质中钝化,如镁在HF(氢氟酸)中钝化,钼和铌在HCl(盐酸)中钝化,不锈钢在硝酸中钝化。
钝化的金属具有的特性一般来说,钝化后的金属在改变钝化的条件后,仍然在相当程度上保持钝化状态[1]。
如:铁在浓硝酸中钝化后,不仅在稀硝酸中保持稳定,而且在水蒸气及其他介质中也能保持稳定;钝化后的铁不能把硝酸铜中的铜置换出铜。
金属钝化的方法1.将金属浸在浓硝酸、浓硫酸等介质里钝化;2.把金属作为电极(阳极),通过电流使它发生氧化,当电流密度达到一定程度时,金属就能被钝化。
金属钝化的机理现在大都认为,金属钝化时由于金属和介质作用,生成一层极薄的肉眼所看不见的保护膜。