2019全国高中生化学竞赛(初赛)试卷及答案
- 格式:doc
- 大小:1019.16 KB
- 文档页数:7

.2019年全国高中学生化学竞赛试题答案及评分标准第1题(5分)二战期间日本是在战场上唯一大量使用毒气弹的国家,战争结束日军撤退时,在我国秘密地遗弃了大量未使用过的毒气弹,芥子气是其中一种毒气。
芥子气的分子式为(ClCH2CH2)2S。
人接触低浓度芥子气并不会立即感受痛苦,然而,嗅觉不能感受的极低浓度芥子气已能对人造成伤害,而且,伤害是慢慢发展的。
1-1用系统命名法命名芥子气。
2-氯乙硫醚或2-氯乙烷硫化物(1分)1-2芥子气可用两种方法制备。
其一是ClCH2CH2OH与Na2S反应,反应产物之一接着与氯化氢反应;其二是CH2=CH2与S2Cl2反应,反应物的摩尔比为2 : 1。
写出化学方程式。
2ClCH2CH2OH + Na2S = (HOCH2CH2)2S + 2NaCl (1分)(HOCH2CH2)2S + 2HCl = (ClCH2CH2)2S + 2H2O (1分)2CH2=CH2 + S2Cl2 = (ClCH2CH2)2S + S (1分)1-3用碱液可以解毒。
写出反应式。
(ClCH2CH2)2S + 2OH-= (HOCH2CH2)2S + 2Cl-(1分)用NaOH代替OH-也可。
方程式必须配平才能得分。
第2题(7分)50年前,Watson和Crick因发现DNA双螺旋而获得诺贝尔化学奖。
DNA 的中文化学名称是:脱氧核糖核酸;DNA是由如下三种基本组分构成的:脱氧核糖(基)、磷酸(基)和碱基;DNA中的遗传基因是以碱基的排列顺序存储的;DNA双链之间的主要作用力是氢键。
给出DNA双螺旋结构在现代科技中应用的一个实例:基因重组或基因工程、转基因作物、人类全基因图谱……。
(每空1分;无“基”字得分相同。
)第3题(5分)在正确选项上圈圈。
3-1下列化学键中碳的正电性最强的是A. C-FB.C-OC.C-SiD. C-Cl3-2电子构型为[Xe]4f145d76s2的元素是A. 稀有气体B.过渡元素C.主族元素D. 稀土元素3-3下列离子中最外层电子数为8的是A. Ga3+B. Ti4+C. Cu+D. Li+第4题(8分)在30o C以下,将过氧化氢加到硼酸和氢氧化钠的混合溶液中,析出一种无色晶体X。

评分通则:1.凡要求计算的,没有计算过程,即使结果正确也不得分。
2有效数字错误,扣0.5分,但每大题只扣1次。
3单位不写或表达错误,扣0.5分,但每大题只扣1次。
4只要求1个答案、而给出多个答案,其中有错误的,不得分。
5方程式不配平不得分。
6不包括在此标准答案的0.5分的题,可由评分组讨论决定是否给分。
第1题 (20分)1-1 Lewis 酸和Lewis 碱可以形成酸碱复合物。
根据下列两个反应式判断反应中所涉及Lewis酸的酸性强弱,并由强到弱排序。
F 4Si -N(CH 3)3 + BF 3 → F 3B -N(CH 3)3 + SiF 4 ;F 3B -N(CH 3)3 + BCl 3 → Cl 3B -N(CH 3)3 + BF 3BCl 3 > BF 3 > SiF 4 顺序错误不给分 (2分) 1-2 (1) 分别画出BF 3和N(CH 3)3的分子构型,指出中心原子的杂化轨道类型。
BFFF分子构型为平面三角形,不画成平面形不给分 (0.5分)sp 2(0.5分)H 3C33分子构型为三角锥形, 不画成三角锥形不给分 (0.5分)sp 3(0.5分)(2) 分别画出F 3B -N(CH 3)3 和F 4Si -N(CH 3)3的分子构型,并指出分子中Si 和B 的杂化轨道类型。
CH 3H 3C H 3CFB FF B :sp 3 (1分)+ (1分)CH 3H 3C H 3CFSi FFFSi ,sp 3d (1分)+ (1分)1-3 将BCl 3分别通入吡啶和水中,会发生两种不同类型的反应。
写出这两种反应的化学方程式。
BCl 3 + 3H 2O = B(OH)3+ 3HCl 不配平不给分 (1分) BCl 3 + C 5H 5N = Cl 3B-NC 5H 5或BCl 3 +N=Cl 3N(1分)1-4 BeCl 2是共价分子,可以以单体、二聚体和多聚体形式存在。
分别画出它们的结构简式,并指出Be 的杂化轨道类型。

2Mg 24.31Al 26.98Si 28.09S 32.079Cl 35.45Ca 40.08Sc 44.96T i4 7V 50.94Cr 52.00Fe55.85 Co58.93N i 5 8Cu 63.55Ga 69.72Ge 72.61 Se 478.96Br 79.90Sr Nb Mo Ru Rh87.6288.9192.9195.94101.1 102.9Ag 107.9In SnTe114.8118.7 <■‘127.6126.9Ba 137.3La — LuTa 180.9 W 183.8 Os 190.2 Ir 192.2Au 197.0Tl 204.4Fb 207.2Fo [210At [2102019年全国高中学生化学竞赛(安徽赛区)初赛试题题号-一一二二二-三四总分得分题号 答案 题号 答案Be 141516元素周期表10 11 12 13222324259.01210.8112.0116.0019.006 8 45 7 1718192021一、本题包括25小题,每小题2分,共50分。
每小题有1个或2个选项符合 题意,若该题只有1个选项符合题意,多选或错选均不得分。
若该题有 2个选生的植物、农作物等富含纤维素、半纤维素和木质素的物质为原料,采用生物热解液化技术而产生的新能源。
F 列有关说法错误的是 A 、 生物质油是一种有机化合物 B 、 这一类能源属于可再生能源C 、 禾U 用生物质能就是间接利用太阳能D 、 生物质油提炼技术中只要利用的是化学变化 2.—块铜板被等分成两块,Cu(a)和Cu(b);锤打Cu(a), Cu(b)不动。
再由Cu(a)、Cu(b)及CuS04溶液组成电池:Cu(a)|CuSO 4(cmol/L)|Cu(b),测得电动势 E > 0,因为 Cu(a)的 A . AS> 0, AH= 0 B . AS> 0, AH<= 0C . ASX 0, AH= 0D . A Sc 0, AH < 03•空间实验室“天宫一号”的供电系统中有再生氢氧燃料电池(RFC ), RFC 是一种将水电解技术与氢氧燃料电池技术相结合的可充电电池。
2019年高中化学竞赛初选考题胡征善一、写化学方程式[(1)和(4)题写离子方程式](10分)(1)已知:φ°(Ni3+/Ni2+)>φ°(Cl2/Cl—)。
则Ni2O3溶于盐酸(2)在Pd(PPh3)4和Ag2O的共同作用下,五氟苯硼酸C6F5B(OH)2与碘苯反应生成碘化银和联苯类化合物(用结构简式表示)(3)四氢硼钠是有机化学中一种特效还原剂。
遇水剧烈反应生成一种气体和盐(4)白磷P4有剧毒,硫酸铜溶液可解毒,反应生成很难溶解的Cu3P和磷酸(5)NaBH4与氯化镍(摩尔比2︰1)在水溶液中反应,可得到两种硼化物:硼化镍和硼酸(摩尔比1︰3)二、(8分)某金属氯化物的浓溶液A呈黄褐色,加水稀释过程中溶液颜色逐渐变成绿色,最后变为蓝色溶液B。
向B(aq)中加入NaOH(aq)生成蓝色沉淀C。
在C 中加入浓氨水,生成深蓝色溶液D。
向D的浓溶液中通入SO2,会析出白色沉淀E,E中Cu、S、N原子个数比为1︰1︰1。
结构分析显示E呈反磁性,其晶体中有呈三角锥型和正四面体型的物种。
E与足量10mol·dm—3的硫酸混合微热,生成沉淀F、气体G和溶液H。
(1)写出A~H的化学式。
(2)写出D与SO2的微酸性溶液反应的离子方程式。
(3)写出E与10 mol·dm—3的硫酸反应的离子方程式。
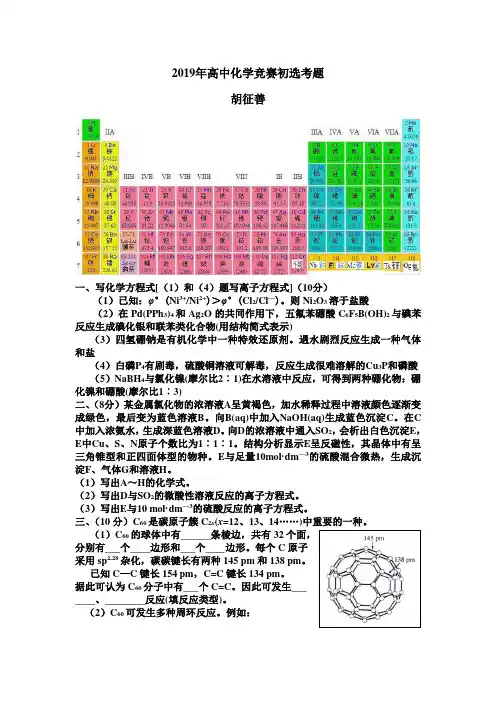
三、(10分)C60是碳原子簇C2x(x=12、13、14……)中重要的一种。
的球体中有______条棱边,共有32个面,(1)C分别有___个____边形和___个____边形。
每个C原子采用sp2.28杂化,碳碳键长有两种145 pm和138 pm。
已知C—C键长154 pm,C=C键长134 pm。
据此可认为C60分子中有___个C=C。
因此可发生_______、________反应(填反应类型)。
(2)C60可发生多种周环反应。
例如:①在甲苯中与Br—CH(COOEt)2反应生成,则Br—CH(COOEt)2在反应中形成的中间体是_______________________。

2019年全国中学生化学竞赛初赛试题一、(6分)物质M是一种日常生活中不可缺少的调味品.已知C可在D中燃烧发出苍白色火焰.M与其他物质的转化关系如图甲所示(部分产物已略去):(1)(1分)写出用惰性电极电解M溶液的离子方程式。
(2)(1分)若A是一种酸性氧化物,且可用于制造玻璃,则G的化学式是。
(3)(1分)若A是一种常见金属单质,且A与B溶液能够反应,则将过量的F溶液逐滴加入E溶液,边加边振荡,所看到的实验现象是(4)(1分)若A是一种盐,A溶液与B溶液混合产生白色絮状沉淀且瞬间变为灰绿色,最后变成红褐色的E,则由A转化成E的离子方程式是。
(5)(2分)若A是一种溶液,只可能含有H+,NH4+,Mg2+,Fe3+,Al3+,CO32-,SO42-中的某些离子,当向该溶液中加入B溶液时发现生成沉淀的物质的量随B溶液的体积发生变化如图乙所示.由此可知,该溶液中肯定含有的离子:,其浓度之比为。
二、(8分)有五种摩尔质量均为44g/mol的化合物甲、乙、丙、丁、戊,均由短周期元素组成.对甲的捕获在降低温室气体排放中具有重要的作用.乙为烃,等物质的量的乙与丁充分燃烧产物为甲与水,且生成水的质量前者是后者的2倍,丙在一定条件下分解获得两种单质,两单质放电时反应生成A,A遇空气变成红棕色气体B.戊是一种极不稳定的物质,在1180℃以下不存在.科学家用质谱仪在工业制硅的反应产物中证实了其存在。
(1)(2分)丁的分子式,甲的电子式。
(2)(1分)若生成戊的反应中氧化产物与还原产物为同一物质,写出生成戊的化学方程式。
(3)(1分)把铁和铜混和物放入一定量B通入水后形成的稀溶液中,反应后过滤,滤出的固体物质投入盐酸中无气体放出,则滤液中一定含有的溶质是。
(4)(2分)将0.2mol乙完全燃烧后生成的气体全部缓慢通入300mL某浓度的NaOH溶液中,气体完全被吸收,溶液中NaOH无剩余,则NaOH溶液的浓度为。
(若有定值则写具体数值,无定值则写范围).(5)(2分)将等物质的量A、B的混合物溶于NaOH溶液中得到只含有一种溶质的溶液,此溶质的化学式为,计简单实验方案证明溶液中含有此溶质。

全国中学生化学竞赛(安徽赛区)初赛试题注意:考试时间2.5小时,满分150分。
请在答题卡上答题,允许使用非编程计算器。
一、本题包括15小题,每小题2分,共30分。
每小题仅有1个选项符合题意。
1.某水溶液含0.5mol·L-1的Na+,1.0 mol·L-1的Mg2+和NO3-减乘,则NO3-的浓度应为A.1.5 mol·L-1B.2.0mol·L-1C.2.5 mol·L-1D.3.0 mol·L-12.SO2是大气中的有害气体,但在生物体内存在SO2生成系统。
内源性SO2在心血管生理和病理调节中起重要作用,表明SO2可能是又一种新型气体信号分子。
下列对大气中SO2的有关说法,错误的是A.可用碘量法检测其含量B.O的氧化数为负﹣lC.只含有极性键D.是酸雨的来源之一3.化学与生活密切相关。
下列说法正确的是A.PM2.5是指粒径大于2.5m的可吸人悬浮颗粒物B.开发全降解CO2塑料,可缓解日益严重的白色污染C.燃煤中加入CaO可以减少酸雨的形成及温室气体的排放D.可燃冰是我国目前推广使用的清洁燃料4.中国科学院科研团队研究表明,在常温常压和可见光下,基于LDH(一种固体催化剂)合成NH3的原理示意图如右。
下列说法错误的是A.该过程将太阳能转化为化学能B.该过程中,涉及极性键和非极性键的断裂与生成C.氧化剂与还原剂的物质的量之比为3:1D.原料气N2可通过分离液态空气获得5.监测SO2含量是否达到排放标准的反应原理可以表示为:SO2+H2O2+BaCl2=BaSO4↓+2HCl。
N A表示阿伏加德罗常数的值,下列说法正确的是A.17gH2O2中含有非极性键数目为0.5N AB.0.1molBaCl2晶体中所含微粒总数为0.1 N AC.25℃时,pH=1的HCl溶液中含有H+的数目为0.1 N AD.生成2.33gBaSO4沉淀时,转移电子数目为0.0l N A6.在ClO3-几何构型中,O—Cl—O的键角应为减A.109.5°B.小于109.5°C.大于109.5°D.120°7.当甲基胺在过量氧气中完全燃烧时,1.00mol甲基胺消耗氧气的物质的量为A.2.25molB.2.50molC.3.00molD.4.50mol8.我国在CO2催化加氢制取汽油方面取得突破性进展,CO2转化过程示意图如下:下列说法正确的是A.反应①的产物中含有水B.反应②属于加成反应C.汽油主要是C5和C11的烃类混合物D.图中a的名称是2-甲基戊烷9.下列实验操作、实验现象和实验结论均正确的是选项实验操作’实验现象实验结论A向待测溶液中先滴加几滴氯水,然后滴加KSCN溶液溶液变红待测溶液中含有Fe2+B 向KMnO4酸性溶液中滴加乙二酸溶液褪色乙二酸具有还原性C 向AgNO3溶液中滴加过量氨水得到澄清溶液Ag+与NH3·H2O能大量共存D向10mL0.1mol·L-1Na2S溶液中滴入2mL0.1mol·L-1ZnSO4溶液,再加入0.1mol·L-1CuSO4溶液开始有白色沉淀生成;后有黑色沉淀生成K sp(CuS)<K sp(ZnS) 10.一定条件下进行反应:COCl2(g)Cl2(g)+CO(g),向2.0 L恒容密闭容器中充入1.0 mol t/s 0 2 4 6 8n(Cl2)/mol 0 0.30 0.39 0.40 0.40 下列说法正确的是A.保持其他条件不变,升高温度,平衡时c(Cl2)=0.22 mol·L-1,则反应的ΔH<0B.若在2L恒容绝热(与外界没有热量交换)密闭容器进行该反应,化学平衡常数不变C.保持其他条件不变,起始向容器中充入1.2molCOCl2、0.60molCl2和0.60molCO,反应达到平衡前的速率:υ(正)>υ(逆)D.保持其他条件不变,起始向容器中充入1.0molCl2和0.8molCO,达到平衡时,Cl2的转化率小于60%11.短周期元素W、X、Y、Z的原子序数依次增大,四种元素的原子最外层电子数总和为17。
言简意赅,远见卓识,望君采纳,谢谢!删除水印可,编辑页眉,选中水印,点击删除。
中国化学会第31 届全国高中学生化学竞赛(省级赛区)试卷估分用答案( 2017 年 8 月 27 日 9:00 ~ 12:00 )题号 1 2 3 4 5 6 7 8 9 10 总分 满分 101012101012613107100得分评卷人·竞赛时间 3 小时。
迟到超过半小时者不能进考场。
开始考试后 1 小时内不得离场。
时间到,把试卷(背面朝上)放在桌面上,立即起立撤离考场。
·试卷装订成册,不得拆散。
所有解答必须写在指定的方框内,不得用铅笔填写。
草稿纸在最后一页。
不得持有任何其他纸张。
·姓名、报名号和所属学校必须写在首页左侧指定位置,写在其他地方者按废卷论处。
·允许使用非编程计算器以及直尺等文具。
H 相对原子质量He 1.008 4.003Li Be B C N O F Ne 6.941 9.012 10.81 12.01 14.01 16.00 19.00 20.18 Na Mg Al Si P S Cl Ar 22.99 24.31 26.98 28.09 30.97 32.07 35.45 39.95 K Ca Sc Ti V Cr Mn Fe Co Ni Cu Zn Ga Ge As Se Br Kr 39.10 40.08 44.96 47.88 50.94 52.00 54.94 55.85 58.93 58.69 63.55 65.41 69.72 72.61 74.92 78.96 79.90 83.80 Rb Sr Y Zr Nb Mo Tc Ru Rh Pd Ag Cd In Sn Sb Te I Xe 85.47 87.62 88.91 91.22 92.91 95.94 [98] 101.1 102.9 106.4 107.9 112.4 114.8 118.7 121.8 127.6 126.9 131.3 Cs Ba La - Hf Ta W Re Os Ir Pt Au Hg Tl Pb Bi Po At Rn 132.9 137.3 Lu 178.5 180.9 183.8 186.2 190.2 192.2 195.1 197.0 200.6 204.4 207.2 209.0 [210] [210] [222] Fr Ra Ac - Rf Db Sg BhHs Mt Ds Rg Cn Uut Uuq Uup Uuh Uus Uuo[223] [226] LaLa Ce Pr Nd Pm Sm Eu Gd Tb Dy Ho Er Tm Yb LuAcThPaUNpPuAmCmBkCfEsFmMdNoLr第 1 题( 10 分)根据条件书写化学反应方程式。

全国高中化学竞赛初赛试题(考试时间 3 小时,满分150 分)H元素周期表He 1.008 4.003 Li Be B C N O F Ne 6.9419.01210.8112.0114.0116.0019.008 Na Mg Al Si P S Cl Ar 22.9924.3126.9828.0930.9732.0735.4539.95 K Ca Sc Ti V Cr Mn Fe Co Ni Cu Zn Ga Ge As Se Br Kr 39.1040.0844.9647.8850.9452.0054.9455.8558.9358.6963.5565.3969.7272.6174.9278.9679.9083.80 Rb Sr Y Zr Nb Mo Tc Ru Rh Pd Ag Cd In Sn Sb Te I Xe 85.4787.6288.9191.2292.9195.94[98]101.1102.9106.4107.9112.4114.8118.7121.8127.6126.9131.3Cs BaLa- Lu Hf Ta W Re Os Ir Pt Au Hg Tl Pb Bi Po At Rn132.9137.3178.5180.9183.8186.2190.2192.2195.1197.06420[210][210][222] Fr Ra Ac - La[223][226]注意:答案必须写在答题卷上,写在试题卷上无效。
......................一、本题包括25 小题,每小题 2 分,共50 分。
每小题有 1 个或 2 个选项符合题意。
若该题只有 1 个选项合题意,多选或错选均不得分。
若该题有 2 个选项合题意,选对 1 个得 1 分,选对 2 个得 2 分;选错 1 个,该题不得分。
⒈我国有些煤矿的坑道中具有丰富的可燃性气体。
目前已建成利用坑道气的发电厂,这样既充分利用了能源,又保证了煤矿的安全生产,坑道中的可燃性气体是A.H 2B.COC.CH 4D. CH 4和 CO 的混合气体⒉ A 是烷烃, B 是单烯烃, B 分子中的碳原子数比 A 分子中多。

全国高中学生化学竞赛(初赛)试题与答案全国高中学生化学竞赛(初赛)试题与答案1.1999年是人造元素丰收年,一年间得到第114、116和118号三个新元素。
按已知的原子结构规律,118号元素应是第周期第族元素,它的单质在常温常压下最可能呈现的状态是(气、液、固选一填入)态。
近日传闻俄国合成了第166号元素,若已知原子结构规律不变,该元素应是第周期第族元素。
(5分)答案】七;零;气;八;VIA(5分,每个填空得1分)2.今年是XXX(Le Chatelier1850-1936)诞生150周年。
请用勒沙特列原理解释如下生活中的常见现象:打开冰镇啤酒瓶把啤酒倒入玻璃杯,杯中立即泛起大量泡沫。
(6分)答案】1)啤酒瓶中二氧化碳气体与啤酒中溶解的二氧化碳达到平衡:CO2(气)CO2(溶液),打开啤酒瓶,二氧化碳气体的压力下降。
根据勒沙特列原理,平衡向放出二氧化碳气体的方向移动,以减弱气体压力下降对平衡的影响。
2)温度是保持平衡的条件,玻璃杯的温度比冰镇啤酒的温度高,根据勒沙特列原理,平衡应向减弱温度升高的方向移动,即应向吸热方向移动,从溶液中放出二氧化碳气体是吸热的,因而,应从溶液中放出二氧化碳气体。
注:压力和温度各3分,不与勒沙特列原理挂钩不给分。
3.1999年合成了一种新化合物,本题用X为代号。
用现代物理方法测得X的相对分子质量为64;X含碳93.8%,含氢6.2%;X分子中有3种化学情况分歧的氢原子和4种化学情况分歧的碳原子;X份子中同时存在C—C、C=C和C≡C三种键,并发觉其C=C键比寻常的C=C短。
1.X的分子式是____(2分)2.请画出X的可能布局。
(4分)答案】1.C5H42.如右右上图注:只有一种可能布局;重键位置必须正确,而键角和平面结构则不必要求。
右上图是用Chemsketch程序制作的立体结构图,图形未画出重键,仅供参考,不是答案。
4.空想的宏观单一晶体呈规则的多面体外形。
多面体的面叫晶面。
2019年10月19日 9:00-12:00● 竞赛时间3小时。
迟到超过半小时者不能进考场。
开始考试后1小时内不得离场。
时间到,把试卷(背面朝上)放在桌面上,立即起立撤离考场。
● 试卷装订成册,不得拆散。
所有解答必须写在指定的方框内,不得用铅笔填写。
草稿纸在最后一页。
不得持有任何其他纸张。
● 姓名、报名号和所属学校必须写在首页左侧指定位置,写在其他地方者按废卷论处。
●允许使用非编程计算器以及直尺等文具。
1.008Zr Nb Mo T c RuRh Pd Ag Cd In S n S b Te I Hf Ta W Re OsIr Pt Au Hg Tl Pb Bi Po At Ac-Lr HLi BeB C N O F Na MgAl S i P Cl S K Ca S c Ti V Cr Mn Fe Co Ni Cu Zn G a G e As S e BrRbCs Fr S r Ba RaY LaLu -6.9419.01222.9924.3139.1040.0885.4787.62132.9137.3[223][226]44.9647.8850.9452.0054.9455.8558.9363.5558.6965.3910.8126.9869.7212.0128.0972.61114.8204.4118.7207.2112.4200.6107.9197.0106.4195.1102.9192.2101.1190.298.91186.295.94183.992.91180.991.22178.588.9114.0116.0019.0030.9774.92121.8209.032.0778.96127.6[210][210][210]126.979.9035.454.00320.1839.9583.80131.3[222]HeNe Ar Kr Xe Rn相对原子质量RfDb Sg Bh Hs Mt第1题(8分)X 是碘一氧系中研究得最多的稳定化合物,白色粉状固体,分解温度573K ,相对分子质量334。

2019年全国高中学生化学竞赛预赛试题(四川赛区)
题号 1 2 3 4 5 6 7 8 9 10 11 总计
满分9 10 8 7 8 8 10 10 10 10 10 100
得分
评卷人
本试卷共8页,11个大题,满分100分。
竞赛时间3小时。
迟到超过30分钟者不能进考场。
开始考试后1小时内不得离场。
时间到,把试卷(背面朝上)放在桌面上,立即起立撤离考场。
试卷装订成册,不得拆散。
所有解答必须写在指定的直线上或方框内,不得用铅笔填写。
草稿纸在最后一页。
不得持有任何其他纸张。
姓名、报名号和所属学校必须写在首页左侧指定位置,写在其他地方者按废卷论。
允许使用非编程计算器以及直尺等文具。
第1题(9分)有一化合物X,其水溶液为浅绿色,可发生如下的转化关系(部分反应物、生成
物从略)。
其中B、D、E、F均为无色气体,W、K为常见的金属单质,C为难溶于水的红褐色固体。
在混合液中加入BaCl2溶液可生成不溶于稀盐酸的白色沉淀,H和W反应可放出大量的热。
请回答下列问题:
1-1 B气体的检验方法为。
1-2 电解混合液时能产生O2的阳极反应式为。
1-3 按要求写出上述转化关系中有关反应的化学方程式:。
2019年全国高中学生化学竞赛(省级赛区)试题第一题(9 分)用α 粒子撞击铋-209 合成了砹-211。
所得样品中砹-211 的浓度<10-8mol/L ,砹-211 同位素半衰期较长,足以用它来研究砹的化学性质。
1 .写出合成砹的核反应方程式。
2.已知室温下用CCl4萃取I2的分配系数为c I2(CCl4)/c I2(H2O)=84,预计用CCl4萃取AtI 的分配系数c AtI(CCl4)/c AtI(H2O)84(填>,<或=);理由是。
3.已知I2+I-I3-的平衡常数K=800,可推断AtI +I -AtI 2-的平衡常数K 800(填>,<或=);依据是。
4.在AtI 中加入I2和I-的混合溶液,滴加AgNO3溶液,发现所得沉淀中只有AgI 而没有共沉淀的AgAt (如果有AgAt ,必然会被共沉淀),然而在上述产物中加入Pb(IO3)2却发现有砹的共沉淀。
写出有关化学方程式,解释上述实验现象。
5.已知室温下ICH 2COOH 的pK a=3.12,由此可推断AtCH 2COOH 的pK a 3.12;理由是。
第二题(12 分)为纪念1905 年爱因斯坦连续发表 6 篇论文导致物理学大变革100 周年,今年被定为国际物理年。
本题涉及的“热电效应”机理也是爱因斯坦首先阐释的,即他提出的被后人称为“爱因斯坦振荡器”的独立振荡原子与温度关系的模型。
1 .左上图是热电效应之一的图解。
给出图中所有英文单词(或词组)及物理学符号200 字(包括标点符号等)的说明文。
2.右上图是化学家合成的能实现热电效应的一种晶体的晶胞模型。
图中的大原子是稀土原子,如镧;小原子是周期系第五主族元素,如锑;中等大小的原子是周期系VIII 族元素,如铁。
按如上结构图写出这种热电晶体的化学式。
给出计算过程。
提示:晶胞的6个面的原子数相同。
设晶体中锑的氧化态为-1,镧的氧化态为+3,问:铁的平均氧化态多大?第三题(10 分)等摩尔的丙酮和过氧化氢混合,在盐酸催化下生成白色粉末A 和水,反应进行完全,产物分子总数是反应物分子总数的2/3。
第33届中国化学奥林匹克(初赛)试题解析2019年9月7日上午9:00至12:00,第33届中国化学奥林匹克(初赛)在全国30个省、自治区、直辖市同时举行,约有7万名高中生参加。
相比于往年,本届初赛试题对知识储备的要求有所降低,但对计算熟练度、思维灵活度和答题准确度的要求没有放松。
这是一件好事:化学的奥林匹克本就不应是“刷书”的奥林匹克,不应是“死记硬背”的奥林匹克;只喜欢画六边形与平行六面体,讨厌计算和推理,也不算真正学好了化学。
近年来,越来越多的同学(及部分老师)偏爱刷书、刷题,刷完基础教材刷高级教材,刷完高级教材刷专著,刷完中文书刷外文书,都刷完还不过瘾,还要去刷一级文献来“押题”,这种做法实在是舍本逐末,甚至是缘木求鱼了。
走马观花,囫囵吞枣,到头来才发现最基本的知识点掌握得不牢固,在高手过招时疏漏大意失了分数,反而怪罪题目故意“挖坑”,实在令人叹惋。
我们鼓励同学们好读书,读好书,但把书“读好”才是最重要的。
鉴于此,本文除了延续前文撰写的三个角度——“从同学角度出发的思路分析,从试题角度出发的考点分析,从科学角度出发的知识拓展”之外,行文中更加强调“明辨基础概念,防范解题漏洞”,希望同学们有所收获。
另一方面,如何在竞赛题目取材上做到严谨与趣味的平衡、经典与前沿的平衡,在树立中国化学奥林匹克思维高杆的同时,及时反映中国化学工作日新月异的进展,或许也是值得思考的。
第1题题目(10分)简要回答问题。
1-1利用不同的催化剂,乙烯催化氧化可选择性地生成不同产物。
产物A可使石灰水变浑浊。
写出与A相对分子质量相等的其他所有产物的分子式和结构简式。
1-2化合物CsAuCl3呈抗磁性。
每个Cs+周围有12个Cl−离子,每个Cl−离子周围有5个金属离子。
金离子处在Cl−围成的配位中心(也是对称中心)。
写出该化合物中Au的氧化态及其对应的配位几何构型。
1-3 2019年1月,嫦娥四号成功在月球着陆。
探测器上的五星红旗由一类特殊的聚酰亚胺制成。
2019年上海市高中生化学竞赛初赛试题及答案详解可能用到的相对原子质量(原子量):H-1 C-12 N-14 O-16 Na-23一、选择题(每小题只有一个正确答案)1. 我国科技创新成果斐然。
下列成果中获得诺贝尔奖的是A. 培育超级杂交水稻B. 发现抗疟疾新药青蒿素C. 人工合成结晶牛胰岛素D. 发明联合制碱法【答案】B【解析】【详解】A.袁隆平培育超级杂交水稻,无获得诺贝尔奖,A错误;B.屠呦呦发现抗疟疾新药青蒿素,获得2015年度诺贝尔医学奖,B正确;C.人工合成结晶牛胰岛素,是世界上第一个人工合成的蛋白质,没有获得诺贝尔奖,C错误;D.侯德榜发明联合制碱法,没有获得诺贝尔奖,D错误;答案选B。
2. 做好垃圾分类,推动城市绿色发展。
下列生活垃圾投放正确的是选项 A B C D 生活垃圾充电电池中药残渣花生壳易拉罐垃圾分类标识A. AB. BC. CD. D【答案】C【解析】【详解】A.电池中含多种金属,属于重金属污染,应为有害垃圾,A错误;B.中药残渣属于易腐生活废弃物,是厨余垃圾,也是湿垃圾,B错误;C.花生壳属于易腐的生活废弃物,是厨余垃圾,也是湿垃圾,C正确;D.易拉罐为金属材质,可以回收利用,属于可回收垃圾,D错误;答案选C 。
3. 《周易》对“革”卦卦象的解释中提到:“泽中有火”,描绘了沼泽水面上发生的燃烧现象。
“泽中有火”主要可能因为沼泽底部有机物发酵产生了 A. 甲烷 B. 乙烯C. 二氧化碳D. 氮气【答案】A 【解析】【详解】沼泽水面上发生的燃烧现象,则对应可燃性气体,可将该现象类比于沼气、天然气的燃烧,故该处是因为沼泽底部有机物发酵产生了甲烷气体,答案为A 。
4. 将金属钠投入足量水中,关于此过程说法错误的是 A. 破坏了金属键 B. 破坏了极性共价键 C. 生成了离子键 D. 生成了非极性共价键 【答案】C 【解析】【详解】A .将金属钠投入足量水中,发生反应生成氢氧化钠和氢气,金属钠的金属键被破坏,A 正确; B .将金属钠投入足量水中,破坏了水分子中的极性共价键,B 正确;C .将金属钠投入足量水中,发生反应生成氢氧化钠和氢气,氢氧化钠为强电解质,在水溶液中完全电离,因此并没生成离子键,故C 错误;D .将金属钠投入足量水中,发生反应生成氢氧化钠和氢气,氢气含非极性共价键,形成了非极性共价键,D 正确; 答案选C 。
全国高中学生化学竞赛初赛试题考试时间:二小时半一、(8分)单质和硝酸混合(1)反应生成相应硝酸盐的单质是、。
(2)反应生成最高价氧化物或含氧酸的单质是、。
(3)呈钝态的单质是、。
(4)不发生反应的单质是、。
二、(6分)酸雨主要是燃烧含硫燃料时释放二氧化硫造成的。
现每隔一定时间测定某份雨水样品的pH值。
测试时间(小时)0 1 2 4 8雨水的pH 4.73 4.62 4.56 4.55 4.55请说明在测定的时间里,雨水样品pH变小的原因。
三、(8分)为降低硫的氧化物对空气的污染,可把氧化钙或碳酸钙和含硫的煤混合后燃烧(这种方法叫做“钙基固硫”)。
请写出钙基固硫的反应方程式。
请从反应热角度讨论用氧化钙或碳酸钙的区别。
四、(1分)以无机物态存在于土壤中的磷,多半是和钙、铝、铁结合的难溶磷酸盐。
磷酸钙在酸性条件下溶解度增大,使磷的肥效增强;加入土壤中的磷酸钙久后则转变为磷酸铝、磷酸铁,导致磷的肥效降低。
请解释并回答下列问题。
(1)磷酸铝在酸性条件下其溶解量(和在近中性条件下的相比)(填入增大、持平或减小。
不同),在碱性条件下其溶解量。
因为:(2)磷酸铁在碱性条件下其溶解量。
因为:(3)作为磷肥,磷酸铁的肥效不高,但在水田中,其肥效往往明显增高。
因为:。
五、(4分)已知四种无机化合物在水中、液氮中的溶解度(克溶质/100克溶剂)为:写出上述几种化合物在水溶液和液氨溶液中发生复分解反应的方向六、(10分)从某些方面看,氨和水相当,NH4+和H3O+(常简写为H+)相当,NH2-和OH-相当,NH2-(有时还包括N3-)和O2-相当。
(1)已知在液氨中能发生下列二个反应NH4Cl+KNH2=KCl+2NH22NH4I+PbNH=PhI2+3NH3请写出能在水溶液中发生的与上二反应相当的反应方程式。
(2)完成并配平下列反应方程式(M为金属):M+NH3→MO+NH4Cl→M(NH2)2→七、(12分)已知:20(原子量;Ca,40.0;O,16.0;C,12.0;H,1.01)请用计算说明,当持续把二氧化碳(压强为0.982巴,下同)通入饱和石灰水,开始生成的白色沉淀会否完全“消失”?在多次实验中出现了下列现象,请解释。
2019年全国⾼中学⽣化学竞赛(江苏赛区)预赛试题含详细答案及指导在化竞的学习过程中,掌握国初核⼼知识点、明确⼀条合理的学习路径⾄关重要。
化竞知识庞杂,不少学化竞的同学对于⾃⼰应该学什么,或先学什么后学什么摸不清头脑,甚⾄有些同学临近考前了,还在问这个知识点国初考不考,要不要学。
因为对国初核⼼知识点不够了解,并且没有⼀条清晰合理的学习路径,⾛了不少冤枉路。
温馨提醒:在开始学习国初知识之前,同学们需先研读全国⾼中学⽣化学(奥林匹克)竞赛基本要求(2008年4⽉版⼤纲),了解国初考试对知识点的要求。
以下为分模块需掌握的知识点:化学基本原理1.现代化学⼊门:宏观⼿段对物质的分类,原⼦的发现,测量,有效数字,化学计量,化学反应的质量关系2.原⼦结构:原⼦结构模型,原⼦轨道,电⼦排布,元素周期表,元素周期律3.成键&离⼦键:化学键,电负性,键的极性,离⼦,离⼦晶体结构4.共价键理论&分⼦结构:共价键,键能,Lewis结构,⼋隅体规则,价键理论,VSEPR理论,杂化轨道,分⼦轨道理论5.⽓体:⽓体的温度和压强,理想⽓体定律,Dalton分压定律,Henry定律6.液体和固体:分⼦间作⽤⼒,液态,⾦属和⾦属键,晶体结构初步7.溶液的性质:溶液的组成,溶解度,相似相溶,蒸⽓压,熔沸点,胶体8.化学热⼒学:焓,Hess定律,标准⽣成热,键能,熵,热⼒学第⼆定律,⾃发过程,⾃由能,⾃由能和平衡,Gibbs-Helmholtz⽅程及应⽤9.化学平衡:平衡条件,平衡常数,化学平衡的移动10.溶液中的平衡:酸碱平衡,沉淀溶解平衡,氧化还原平衡&电化学,配位平衡&配位结构初步11.化学动⼒学初步&核化学:反应速率,速率⽅程,反应机理,催化剂,放射性衰变,放射性的应⽤与防护,同位素,核裂变和核聚变有机化学1.有机结构基础:基本概念,成键和结构,有机酸碱理论2.烷烃、环烷烃、构象:烷烃、环烷烃、构象3.⽴体化学:对映异构、⾮对映异构、顺反异构、构象异构4.烷烃、⾃由基取代反应:⾃由基、⾃由基反应、烷烃的⾃由基反应5.卤代烃、亲核取代反应:卤代烃、碳正离⼦,SN1,SN26.消除反应:E1, E2, Substitution Vs Elimination7.醇、醚:醇、硫醇、醚、环氧8.烯、炔的加成反应:构对⽐;亲电、⾃由基、亲核加成9.烯、炔:氧化、还原、聚合反应10.醛、酮:羰基、亲核加成、α,β-不饱和醛酮的加成、氧化、还原、wittig反应11.羧酸、羧酸衍⽣物、胺:羧酸、羧酸衍⽣物、胺、卡宾12.缩合反应:烯醇、烷基化反应、与羰基反应13.共轭、芳⾹性:共轭体系、分⼦轨道理论、芳⾹性14.共振、芳环的取代反应:共振论、芳环亲电取代、芳环亲核取代15.周环反应:前线轨道、经典周环反应机理举例16.重排反应:经典重排反应机理举例17.有机波谱分析:IR、MS、NMR在有机产物和中间体结构表征中的综合应⽤。
2019年高一化学竞赛试卷(考试时间:2小时;满分:150分)注意:1. 将答案写在答题卷上,写在试卷上无效,考试结束只上交答题卷。
2. 考生开始答题前,请先将答题卷上密封线内的项目填写完整。
第Ⅰ卷(选择题,共78分)一、选择题(本题包括10个小题,每小题3分,共30分;每小题只有一个选项符合题意。
) 1. 下列说法准确的是A.明矾水解时产生具有吸附性的胶体粒子,能够用于饮用水的杀菌消毒 B.通入过多的空气,能够使燃料充分燃烧,同时提升热量的利用率C.道尔顿、汤姆生、卢瑟福、玻尔等科学家的研究持续更新人们对原子结构的理解 D.水泥、玻璃、青花瓷、红宝石、玛瑙、分子筛都属于硅酸盐工业产品 2. 下列化学用语表述准确的是 A.NaCl的电子式:B.S2―的离子结构示意图: D.质子数为53、中子数为78的碘原子:131 53IC.次氯酸的结构式:H-Cl-O A.SiO2与干冰的晶体结构相似3.我国科学家制得了SiO2超分子纳米管,微观结构如图。
下列叙述准确的是 B.SiO2耐腐蚀,不与任何酸反应 C.SiO2属于酸性氧化物D.光纤主要成分是SiO2,具有导电性 4.下列说法准确的是A.高炉炼铁中焦炭直接还原化合态的铁B.钠是一种具有强还原性的金属,可用于冶炼钛、锆、铌等金属C.元素分析仪是一种可用于确定化学反应速率的比色分析仪器D.12C可用于考古断代B.制备S2Cl2的反应是化合反应,不是氧化还原反应C.S2Cl2遇水反应的化学方程式为:2S2Cl2+2H2O=3S↓+SO2↑+4HCl D.S2Br2与S2Cl2结构相似,沸点:S2Br20有体积可变(活塞与容器之间的摩擦力忽略不计)的密闭容器如图所示,现将3molNH3和2molCO2通入容器中,移动活塞至体积V为3L,用铆钉固定在A、B点。
发生合成尿素的总反应如下:CO2(g) + 2NH3(g)CO(NH2)2(S) + H2O(g)第6 / 8页Ⅱ. 室温下,0.1mol·L的二元酸H2A溶液中,溶液体系可能存在的含A微粒(H2A、HA-、A2-)所占物质的量分数(δ)随pH变化的关系如图所示,请回答下列问题。
全国高中学生化学竞赛(省级赛区)试卷
●竞赛时间3小时。
迟到超过30分钟者不能进考场。
开始考试后1小时内不得离场。
时
间到,把试卷(背面前上)放在桌面上,立即起立撤离考场。
●试卷装订成册,不得拆散。
所有解答必须写在站定的方框内,不得用铅笔填写。
草稿
纸在最后一页。
不得持有任何其他纸张。
●姓名、报名号和所属学校必须写在首页左侧指定位置,写在其他地方者按废卷论。
允许使用非编程计算器以及直尺等文具
第1题(7分)
1-1 向硫酸锌水溶液中滴加适当浓度的氨水至过量,发生两步主要反应。
简述实验现象并写出两步主要反应的离子方程式。
无色溶液产生白色沉淀,后逐渐溶解
(1分,如只写白色沉淀溶解不扣分,未表明白色,扣0.5分)(1)Zn2++2NH3+2H2O=Zn(OH)2↓+2NH4+(1分)
写成如下形式均给分:Zn2++2NH3·H2O=Zn(OH)2↓+2NH4+
[Zn(H2O)6]2++2NH3·H2O=Zn(OH)2↓+2NH4+ +6H2O
[Zn(H2O)6]2++2NH3=Zn(OH)2↓+2NH4+ +2H2O (2)Zn(OH)2 + 2NH4+ +2NH3 = [Zn(NH3)4]2+ +2H2O
如写成Zn(OH)2+4NH3= [Zn(NH3)4]2++2OH—也对,如产物写成[Zn(NH3)6]2+扣0.5分,因主要产物是[Zn(NH3)4]2+
1-2 化合物[Cu(Pydc)(amp)] ·3H2O]的组成为C11H14CuN4O7,热重分析曲线表明,该化合物受热分解发生两步失重,第一个失重峰在200~250℃,失重的质量分数为15.2%。
第二个失重峰在400~500℃,失重后的固态残渣质量为原化合物质量的20.0%。
Pydc 和amp是含有芳环的有机配体。
通过计算回答:
(1)第一步失重失去的组分。
水分子或H2O 3个水分子或3H2O C11H14CuN4O7的式量约377.8,失去3个水分子,失重质量分数理论值为14.3%。
1分
(2)第二步失重后的固态残渣是什么,解释理由。
CuO或Cu2O的混合物(2分)
理由:CuO、Cu2O及C11H14CuN4O7的式量分别为79.55、143.1和377.8。
若残渣为CuO,则失重质量分数为79.55/377.8=21.1%;若残渣为Cu2O,则质量分数为143.1/(377.8×2)=18.9%,实验值为20%介于两者之间,故残渣是两者的混合物。
(1分)只答CuO或只答Cu2O,只得1分。
答CuO和Cu混合物,计算正确,理由表述清晰,也可得3分。
虽然计算正确,但物质在题设条件下不存在(如乙炔铜、氢化铜等),也可得1分(计算分)。
第2题(7分)A和X是两种常见的非金属元素,其核外电子数之和为22,价电子数之和为10。
在一定条件下可生成AX、AX3(常见的Lewis酸)、A2X4和A4X4,反应如下:A(s) + 3/2X2(g) AX3(g)
Hg,放电
AX3(g) AX(g) +2X(g)
2Hg +2X(g) Hg2X2(g)
AX(g) +AX3(g) A2X4(g)
4 AX(g) A4X4(s)
2-1 指出A和X各是什么元素。
1。