第八章 理想气体的热力学要点
- 格式:ppt
- 大小:1.38 MB
- 文档页数:25

理想气体与热力学理想气体的状态方程与热力学定律理想气体是热力学研究中的一个重要概念,它假设气体分子之间没有相互作用,体积可以忽略不计。
理想气体的状态方程和热力学定律则是描述理想气体特性的公式和规律。
本文将从理想气体的状态方程和热力学定律两个方面介绍理想气体的基本性质。
一、理想气体的状态方程理想气体的状态方程,即描述气体状态的基本方程,也被称为理想气体定律。
根据气体分子动理论以及实验结果,理想气体状态方程可以写为:PV = nRT其中P表示气体的压强,V表示气体所占的体积,n为气体的物质量(以摩尔为单位),R为气体常量,T表示气体的温度(以开尔文为单位)。
此方程被称为理想气体状态方程或理想气体定律,它描述了理想气体在各种温度、压强和体积条件下的状态。
二、热力学定律除了理想气体的状态方程,热力学还有一些定律用于描述理想气体的特性。
1. Boyle定律Boyle定律也被称为气体的压强-体积定律。
它的表述为:在恒温下,理想气体的压强与其所占的体积成反比。
数学表达式为:P1V1 = P2V2其中P1和V1表示气体的初始压强和体积,P2和V2表示气体的最终压强和体积。
2. Charles定律Charles定律也被称为气体的温度-体积定律。
它的表述为:在恒压下,理想气体的体积与其温度成正比。
数学表达式为:V1/T1 = V2/T2其中V1和T1表示气体的初始体积和温度,V2和T2表示气体的最终体积和温度。
3. Gay-Lussac定律Gay-Lussac定律也被称为气体的压强-温度定律。
它的表述为:在恒容下,理想气体的压强与其温度成正比。
数学表达式为:P1/T1 = P2/T2其中P1和T1表示气体的初始压强和温度,P2和T2表示气体的最终压强和温度。
三、理想气体状态方程的推导理想气体状态方程可以通过分析而来。
考虑到气体分子的运动和碰撞,可以将气体分子的平均动能和压强联系起来。
根据动理论,气体分子的平均动能可以写为:(1/2)mv² = (3/2)kT其中m表示气体分子的质量,v表示气体分子的速度,k为玻尔兹曼常数,T为气体的温度。


理想气体的热力学热力学是研究物质内部能量转化和传递规律的科学,而理想气体是热力学研究中最为简单和重要的模型之一。
理想气体的热力学性质由状态方程、内能、焓、熵等基本参数来描述,下面将对理想气体的热力学行为进行详细讨论。
一、状态方程理想气体的状态方程可以表示为PV = nRT,其中P为气体压强,V为气体体积,n为气体的摩尔数,R为气体常数,T为气体的绝对温度。
根据理想气体的状态方程,我们可以推导出很多其他重要的热力学参数。
二、内能理想气体的内能只与温度有关,与体积和压强无关。
根据理想气体的内能公式,我们可以得出内能U和温度T之间的关系,即U = (3/2)nRT。
内能是描述理想气体热力学性质的重要参数之一。
三、焓理想气体的焓是在恒压条件下的热力学函数,表示了单位质量或单位摩尔气体在恒压过程中的能量变化。
理想气体的焓变化可以表示为ΔH = ΔU + PΔV,其中ΔH为焓的变化,ΔU为内能的变化,P为气体的压强,ΔV为气体的体积变化量。
四、熵理想气体的熵是描述系统无序程度的量,也可以理解为能量的分散程度。
根据热力学第二定律,一个孤立系统内部的熵不会减少,而理想气体在绝热膨胀或绝热压缩时熵是恒定的。
理想气体的熵变化可以表示为ΔS = nCvln(T2/T1)或ΔS = nCpln(T2/T1),其中Cv为定容热容,Cp为定压热容。
综上所述,理想气体的热力学性质是热力学研究中的重要内容,通过对理想气体的状态方程、内能、焓、熵等参数的分析,可以更深入地理解气体在不同条件下的热力学行为。
理想气体模型的简单性和适用性使其成为理论研究和工程应用中不可或缺的重要工具。
希望本文的介绍能够帮助读者更好地理解理想气体的热力学特性。

第八章热力学定律本章学习提要1.理解热力学第一定律,知道热力学第一定律反映了系统内能的变化和系统通过做功及传热过程与外界交换的能量之间的关系。
初步会用热力学第一定律分析理想气体的一些过程,以及生活和生产中的实际问题。
2.知道热力学第二定律的表述。
知道熵是描写系统无序程度的物理量。
热力学的两个基本定律是能量守恒定律和热力学第一定律。
热力学第二定律表述了热力学过程的不可逆性,即孤立系统自发地朝着热力学平衡方向——最大熵状态——演化。
这两个定律都是通过对自然界和生活、生产实际的观察、思考、分析、实验而得到的,这也是我们学习这两条基本定律应采取的方法。
人类的进步是与对蕴藏在物质内部能量的认识和利用密切相关的。
热力学定律为更好地设计和制造热机、更好地开发和利用能源指明了方向。
随着生产和科学实践的发展,人们逐步领悟到有效利用能源的意义,懂得遵循科学规律的重要性,从而更自觉地抵制违背科学规律的行为。
A 热力学第一定律一、学习要求理解热力学第一定律。
初步会用热力学第一定律分析理想气体的一些过程,以及生活和生产中的实际问题。
我们应聚焦于热力学第一定律的构建过程,理解它既包括内能的转换,也遵循能量守恒定律。
这一定律是通过对自然界以及生活和生产实际的深入观察、思考、分析和实验而得出的自然界中最基本、最普遍的定律之一。
通过学习热力学第一定律,我们能体会到它在科学史上的重要地位,并感受到它对技术进步和社会发展的巨大影响。
二、要点辨析1.热力学第一定律的含义和表式热力学第一定律涉及到能量的转化和能量守恒两个方面。
内能是物质内部大量微观粒子无序热运动所具有的能量形式。
一个物质系统的内能变化是由它与外部环境进行能量交换的结果,而这种能量交换可以通过两种方式实现:做功和热传递。
热力学第一定律揭示了系统内能变化(ΔU)与系统与外部环境交换的功(W)和热量(Q)之间的定量关系。
ΔU=Q+W。
2.应用热力学第一定律解题时,要注意各物理量正、负号的含义当热力学第一定律表示为ΔU=Q+W时,ΔU为正值,表示系统内能增加;负值表示系统内能减小。
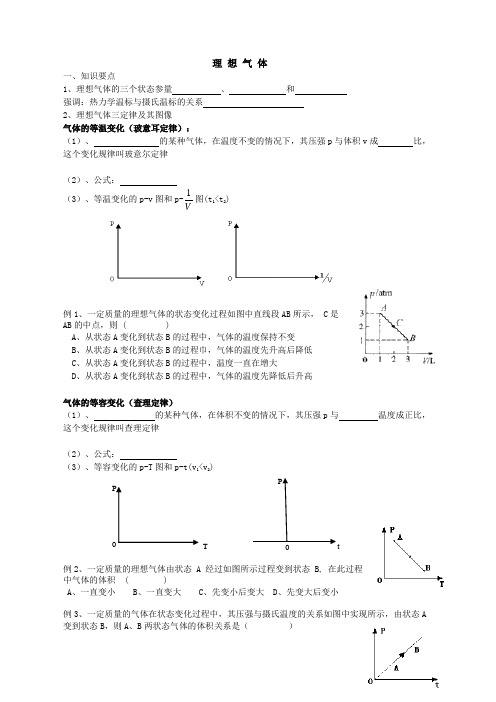
理 想 气 体 一、知识要点1、理想气体的三个状态参量 、 和 强调:热力学温标与摄氏温标的关系2、理想气体三定律及其图像气体的等温变化(玻意耳定律):(1)、 的某种气体,在温度不变的情况下,其压强p 与体积v 成 比,这个变化规律叫玻意尔定律(2)、公式: (3)、等温变化的p-v 图和p-V1图(t 1<t 2)例1、一定质量的理想气体的状态变化过程如图中直线段AB 所示, C 是AB 的中点,则 ( )A 、从状态A 变化到状态B 的过程中,气体的温度保持不变B 、从状态A 变化到状态B 的过程巾,气体的温度先升高后降低C 、从状态A 变化到状态B 的过程中,温度一直在增大D 、从状态A 变化到状态B 的过程中,气体的温度先降低后升高气体的等容变化(查理定律)(1)、 的某种气体,在体积不变的情况下,其压强p 与 温度成正比,这个变化规律叫查理定律(2)、公式:(3)、等容变化的p-T 图和p-t(v 1<v 2)例2、一定质量的理想气体由状态 A 经过如图所示过程变到状态 B, 在此过程中气体的体积 ( )A 、一直变小B 、一直变大C 、先变小后变大D 、先变大后变小例3、一定质量的气体在状态变化过程中,其压强与摄氏温度的关系如图中实现所示,由状态A 变到状态B ,则A 、B 两状态气体的体积关系是( )PtPTA 、V A >VB ; B 、V A <V B ;C 、V A =V B ;D 、无法判断 气体的等压变化(盖-吕萨克定律)(1)、 的某种气体,在压强不变的情况下,其体积V 与 温度成正比,这个变化规律叫盖-吕萨克定律(2)、公式:(3)、等容变化的V-T 图和V-t(P 1<P 2)例4、如图所示,一定质量的理想气体经历ab 、bc 、cd 、da 四个过程,下列说法中错误的是 ( )A 、ab 过程中气体压强不变B 、bc 过程中气体压强减小C 、cd 过程中气体压强不变D 、da 过程中气体压强增大例5、一定质量的气体,当它的压强不变时,气体温度从1000C 升高到2000C ,它的体积( ) A .增大到原来的2倍 B .增大到原来的100/273倍 C .增大到原来的473/373倍D .缩小到原来的1/2 3、理想气体状态方程(1)、在 温度、 压强下都遵从气体实验定律的气体叫做理想气体,当温度 ,压强 ,实际气体可当成理想气体来处理。
