晶胞计算专题均摊法
- 格式:ppt
- 大小:1.92 MB
- 文档页数:28
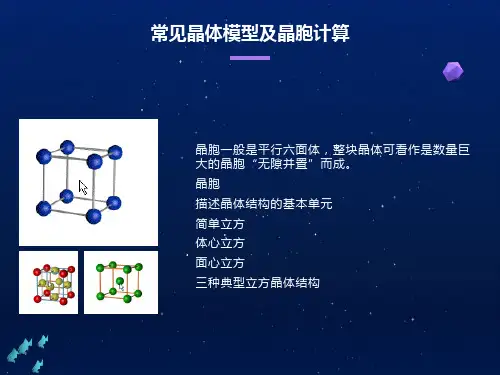

晶胞中微粒数的计算方法——均摊法晶胞中粒子个数的计算,其重要问题是正确分析晶胞中任意位置上的一个粒子被几个晶胞所共有。
1.平行六面体------长方体(正方体)晶胞中不同位置的粒子对晶胞的贡献:顶 ----1/8 棱----1/4 面----1/2 心----12.六方晶胞:在六方体顶点的微粒为6个晶胞共有,在面心的为2个晶胞共有,在体内的微粒全属于该晶胞。
3.非平行六面体---非长方体(正方体)晶体中粒子视具体情况而定。
如石墨晶胞每一层内碳原子排成六边形,其顶点(1个碳原子)被三个六边形共有,每个六边形占该粒子的1/3。
【练习】1.石墨晶体的层状结构,层内为平面正六边形结构(如图),试回答下列问题:(1)图中平均每个正六边形占有C 原子数为____个、占有的碳碳键数为____个。
碳原子数目与碳碳化学键数目之比为_______。
2.根据下列结构示意图,判断下列说法中不正确的是( )A .在NaCl 晶体中,距Na+最近的多个C l -构成正八面体B .在CaF 2晶体中,每个晶胞平均占有4个Ca 2+C .在金刚石晶体中,碳原子与碳碳键数之比为1:2D .该气态团簇分子的分子式为EF 或FE3.最近发现一种由钛(Ti)原子和碳原子构成的气态团簇分子,分子模型如图所示,其中白球表示钛原子,黑球表示碳原子,则它的化学式为( )A.TiCB.1314Ti CC.47Ti CD.1413Ti C4.在高温超导领域中,有一种化合物叫钙钛矿,其晶体结构中有代表性的最小单位结构如图所示试回答:(1)在该晶体中每个钛离子周围与它最近且相等距离的钛离子有多少个?(2)在该晶体中氧、钙、钛的粒子个数化是多少?5、如图是CsCl 晶体的晶胞(晶体中最小的重复单元)已知晶体中2个最近的Cs+核间距离为acm ,氯化铯的相对分子质量为M ,NA 为阿佛加德罗常数,则CsCl 晶体的密度为()A 、8M/a3NAB 、a3M/8NAC 、M/a3NAD 、a3M/NA6.现有四种晶体,其离子排列方式如图所示,其中化学式不属AB 型的是( )A B C D7、磁光存储的研究是Williams 等在1957年使Mn 和Bi 形成的晶体薄膜磁化并用光读取之后开始的。

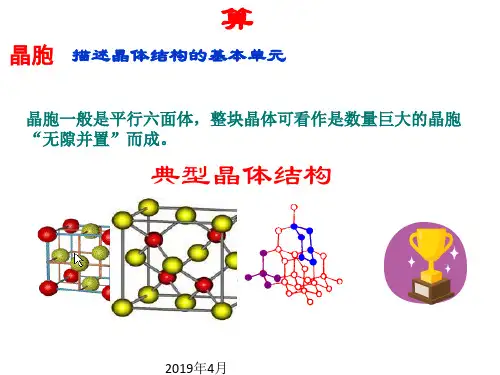

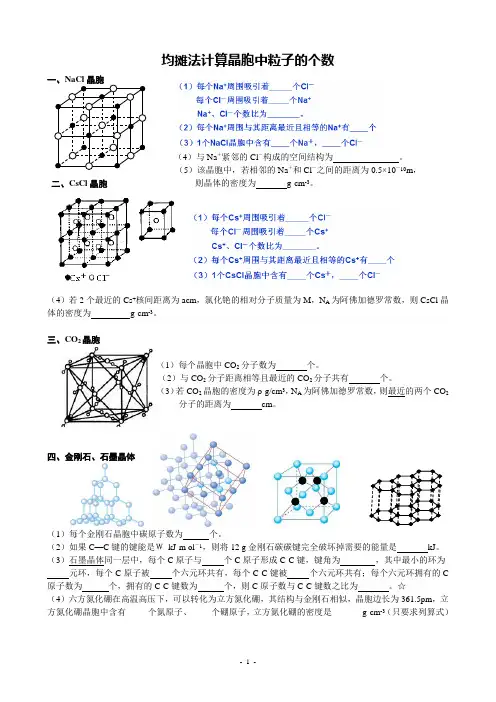
均摊法计算晶胞中粒子的个数一、NaCl晶胞(4)与Na+紧邻的Cl-构成的空间结构为。
(5)该晶胞中,若相邻的Na+和Cl-之间的距离为0.5×10-10m,二、CsCl晶胞则晶体的密度为g·cm-3。
(4)若2个最近的Cs+核间距离为acm,氯化铯的相对分子质量为M,N A为阿佛加德罗常数,则CsCl晶体的密度为g·cm-3。
三、CO2晶胞(1)每个晶胞中CO2分子数为个。
(2)与CO2分子距离相等且最近的CO2分子共有个。
(3)若CO2晶胞的密度为 g/cm3,N A为阿佛加德罗常数,则最近的两个CO2分子的距离为cm。
四、金刚石、石墨晶体(1)每个金刚石晶胞中碳原子数为个。
(2)如果C—C键的键能是WkJ·m ol-1,则将12 g金刚石碳碳键完全破坏掉需要的能量是kJ。
(3)石墨晶体同一层中,每个C原子与个C原子形成C-C键,键角为,其中最小的环为元环,每个C原子被个六元环共有,每个C-C键被个六元环共有;每个六元环拥有的C 原子数为个,拥有的C-C键数为个,则C原子数与C-C键数之比为。
☆(4)六方氮化硼在高温高压下,可以转化为立方氮化硼,其结构与金刚石相似,晶胞边长为361.5pm,立方氮化硼晶胞中含有_____个氮原子、_____个硼原子,立方氮化硼的密度是_______g·cm-3(只要求列算式)⊿六棱柱晶胞①处于顶点的微粒,同时为个晶胞所共有,每个晶胞占有该微粒的;②处于侧棱上的微粒,同时为个晶胞所共有,每个晶胞占有该微粒的;③处于底棱上的微粒,同时为个晶胞所共有,每个晶胞占有该微粒的;④处于面上的微粒,同时为个晶胞所共有,每个晶胞占有该微粒的;⑤处于晶胞内部的微粒,则完全属于该晶胞。
练1:2001年报道硼和镁形成的化合物刷新了金属化合物超导温度的最高记录。
右下图示意的是该化合物的晶体结构单元:镁原子间形成正六棱柱,且棱柱的上、下底面还各有一个镁原子;6个硼原子位于棱柱内。

正三棱柱晶胞均摊法的计算
正三棱柱晶胞均摊法是一种计算晶体结构中原子位置的方法。
在正三棱柱晶胞中,原子通常位于晶格点上,而且它们的位置相对较容易确定。
均摊法是通过考虑晶胞中原子的对称性来确定原子的位置。
首先,我们需要知道正三棱柱晶胞的结构特征。
正三棱柱晶胞有三个等边三角形的侧面和两个平行的正三角形底面。
在这种晶胞中,原子通常位于顶点和中心位置。
接下来,我们可以使用均摊法来计算原子的位置。
均摊法考虑了晶胞的对称性,以确定原子的位置。
具体步骤包括:
1. 确定晶胞中原子的类型和数量。
根据晶体的化学组成和晶胞的结构,确定晶胞中原子的种类和数量。
2. 考虑晶胞的对称性。
根据晶胞的对称性,确定原子可能的位置,并考虑原子之间的相互作用。
3. 计算原子的坐标。
根据晶胞的结构和原子的可能位置,计算
原子的坐标,通常使用笛卡尔坐标系或晶体学坐标系。
值得注意的是,均摊法是一种近似方法,它假设晶体中原子的
位置是均匀分布的。
在实际应用中,需要结合实验数据和理论模型
来确定原子的精确位置。
总之,正三棱柱晶胞均摊法的计算涉及确定晶胞中原子的位置,考虑晶胞的对称性,并计算原子的坐标。
这种方法在研究晶体结构
和性质时具有重要的应用。
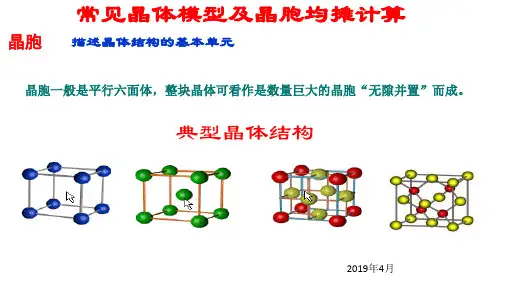


晶胞参数的估计之阳早格格创做1. 均摊法决定晶体的化教式给出晶体的—部分(称为晶胞)的图形,央供决定晶体的化教式:常常采与均摊法.均摊法犹如下准则,以NaCl的晶胞为例:①处于顶面的粒子,共时为8个晶胞所公有,所以,每个粒子只分摊1/8给该晶胞.②处于棱上的粒子,共时为4个晶胞所公有,所以,每个粒子只分摊1/4给该晶胞.③处于里上的粒子,共时为2个晶胞所公有,所以,每个粒子只分摊1/2给该晶胞.④处于晶胞里里的粒子,则实足属于该晶胞.由此算出正在NaCl的晶胞中:含数:含数:故NaCl晶体中,战数目之比为1∶1.2. 晶胞参数的估计根据(1)ρ= m/V(2)V=a3例.(1)化教课本中图示了NaCl晶体结构,它背三维空间蔓延得到完好晶体.NiO(氧化镍)晶体的结构与NaCl 相共,Ni2+与最临近O2-的核间距离为a×10-8cm,估计NiO晶体的稀度(已知NiO的摩我品量为74.7g/mol).(2)天然战绝大部分人为造备的晶体皆存留百般缺陷,比圆正在某氧化镍晶体中便存留如图所示的缺陷:一个Ni2+空缺,另有二个Ni2+被二个Ni3+所与代.其截止晶体仍呈电中性,但是化合物中Ni战O的比值却爆收了变更.某氧化镍样品组成Ni0.97O,试估计该晶体中Ni3+ 与Ni2+的离子个数之比.[训练]1. 由钾战氧组成的某种离子晶体中含钾的品量分数为78/126,其阳离子惟有过氧离子(O22-)战超氧离子(O2-)二种.正在此晶体中,过氧离子战超氧离子的物量的量之比为A. 2︰1B. 1︰1C. 1︰2D. 1︰32.食盐晶体如左图所示.正在晶体中,表示Na+,表示Cl.已知食盐的稀度为 g / cm3,NaCl摩我品量M g / mol,阿伏加德罗常数为N,则正在食盐晶体里Na+战Cl 的间距约莫是A cmB cmA cm D cm3.某物量的晶体中,含A、B、C三种元素,其排列办法如左图所示(其中前后二里心上的B本子没有克没有及绘出),晶体中A、B、C的本子个数比依次为 ( )A.1:3:1 B.2:3:1C.2:2:1 D.1:3:34.如左图所示,是一种晶体的晶胞,该离子晶体的化教式为()A.ABC B.ABC3 C.AB2C3 D.AB3C35.晶体具备准则的几许形状,晶体中最基础的沉复单位称为晶胞.NaCl晶体结构如左图所示.已知FexO晶体晶胞结构为NaCl 型,由于晶体缺陷,x值小于1.测知FexO晶体稀度为5.73g/cm3,晶胞边少为4.28×10-10m.⑴FexO中x值(透彻至0.01)为___________.⑵晶体中的Fe分别为Fe2+、Fe3+,正在Fe2+战Fe3+的总数中,Fe2+所占分数(用小数表示,透彻至0.001)为___________.⑶此晶体化教式为____________.⑷与某个Fe2+(或者Fe3+)距离迩来且等距离的O2-围成的空间几许构型形状是__________.⑸正在晶体中,铁元素的离子间最短距离为__________m.6.如图,曲线接面处的圆圈为NaCl晶体中离子或者离子所处的位子.那二种离子正在空间3个互相笔曲的目标上皆是等距离排列的.(1)请将其中代表离子的圆圈涂乌(没有必思量体积大小),以完毕NaCl晶体结构示企图.(2)晶体中,正在每个离子的周围与它最靠近的且距离相等的公有_________个.(3)晶体中每一个沉复的结构单元喊晶胞.正在NaCl晶胞中正六里体的顶面上、里上、棱上的或者Cl-为该晶胞与其相邻的晶胞所公有,一个晶胞中Cl-离子的个数等于_____________,即(挖估计式)___________;离子的个数等于___________,即(挖估计式)___________.(4)设NaCl的摩我品量为,食盐晶体的稀度为,阿伏加德罗常数为.食盐晶体中二个距离迩来的钠离子核心间的距离为___________cm.。

晶胞及其相关计算(答案在最后)1.掌握均摊法计算的一般方法,能根据晶胞中微粒的位置计算晶胞的化学式。
2.掌握晶体密度与晶胞参数计算的一般步骤。
考点一晶胞中微粒数的计算方法——均摊法1.晶胞(1)概念:描述晶体结构的基本单元。
(2)晶体中晶胞的排列——无隙并置①无隙:相邻晶胞之间没有任何间隙。
②并置:所有晶胞平行排列、取向相同。
感悟:2.晶胞中微粒数的计算方法——均摊法(1)长方体(包括立方体)晶胞中不同位置的粒子数的计算如某个粒子为N个晶胞所共有,则该粒子有1N属于这个晶胞。
中学中常见的晶胞为立方晶胞,立方晶胞中微粒数的计算方法如图1。
(2)非长方体晶胞在六棱柱(如图2)中,顶角上的原子有16属于此晶胞,面上的原子有12属于此晶胞,因此六棱柱中镁原子个数为12×16+2×12=3,硼原子个数为6。
【师说·助学】计算晶胞中微粒数的关键:确定一个粒子为几个晶胞所共有。
3.晶胞微粒配位数的计算(1)晶体中原子(或分子)的配位数若晶体微粒为同种原子或同种分子,则某原子(或分子)的配位数指的是距该原子(或分子)最接近且等距离的原子(或分子)的数目,常见晶胞的配位数如下:简单立方:面心立方:体心立方:配位数为6配位数为12配位数为8(2)离子晶体的配位数指一个离子周围最接近且等距离的异种电性离子的数目。
以NaCl晶体为例①找一个与其他粒子连接情况最清晰的粒子,如上图中心的黑球(Cl-)。
②数一下与该粒子周围距离最近的粒子数,如上图标数字的面心白球(Na+),确定Cl-的配位数为6,同样方法可确定Na+的配位数也为6。
【教考衔接】典例1[2023·湖南卷,11A]科学家合成了一种高温超导材料,其晶胞结构如图所示。
该晶体最简化学式为________。
典例2[2023·辽宁卷,14改编]晶体结构的缺陷美与对称美同样受关注。
某富锂超离子导体的晶胞是立方体(图1),进行镁离子取代及卤素共掺杂后,可获得高性能固体电解质材料(图2),判断下列说法是否正确。
2020届高三化学二轮复习物质结构与性质重点问题晶胞及组成微粒计算知识梳理1.晶胞中微粒数目的计算方法——均摊法2.晶胞求算(2)晶体微粒与M、ρ之间的关系若1个晶胞中含有x个微粒,则1 mol晶胞中含有x mol微粒,其质量为xM g(M为微粒的相对原子质量);又1个晶胞的质量为ρa3 g(a3为晶胞的体积,a为晶胞边长或微粒间距离),则1 mol晶胞的质量为ρa3N A g,因此有xM=ρa3N A。
3.金属晶体空间利用率的计算方法空间利用率=球体积晶胞体积×100%,球体积为金属原子的总体积。
例如简单立方堆积晶胞如图所示,原子的半径为r,立方体的棱长为2r,则V球=43πr3,V晶胞=(2r)3=8r3,空间利用率=V球V晶胞×100%=43πr38r3×100%≈52%。
强化训练1、如图是甲、乙、丙三种晶体的晶胞,则甲晶体中x 与y 的个数比是________,乙中a 与b 的个数比是________,丙中一个晶胞中有________个c 离子和________个d 离子。
答案 2∶1 1∶1 4 4解析 甲中N (x)∶N (y)=1∶(4×18)=2∶1;乙中N (a)∶N (b)=1∶(8×18)=1∶1;丙中N (c)=12×14+1=4,N (d)=8×18+6×12=4。
2、如图是由Q 、R 、G 三种元素组成的一种高温超导体的晶胞结构,其中R 为+2价,G 为-2价,则Q 的化合价为________。
答案 +3解析 R :8×18+1=2G :8×14+8×14+4×12+2=8Q :8×14+2=4R 、G 、Q 的个数之比为1∶4∶2,则其化学式为RQ 2G 4。
由于R 为+2价,G 为-2价,所以Q 为+3价。
3.下图为离子晶体立体构型示意图:(●阳离子,○阴离子)以M 代表阳离子,以N 表示阴离子,写出各离子晶体的组成表达式:A________、B________、C________。