大黄素的提取分离和鉴定
- 格式:doc
- 大小:31.00 KB
- 文档页数:4

实验5-1大黄中蒽醌的提取分离与鉴定一、实验目的:1、了解一个天然药物中含有的主要有效成分并对其进行提取分离。
2、掌握植物中活性成分的化学检测方法,并进行初步的鉴定工作。
二、实验原理:大黄是一味天然草药,具有泻下通便之效果。
其主要活性成份是大黄素与蒽醌类物质,其中瑞贝洛Ⅱ(rustbelineⅡ)、大黄素(emodin)、芦丁(rutin)等,在医学上有广泛的应用。
大黄素与蒽醌类物质在自然状态下大多处于质子化状态,存在于与水相较弱的有机溶剂中。
为了获得高品质的大黄素与蒽醌类物质,需要对有机溶剂进行筛选,筛选出适宜的溶剂并对大黄中的主要成分进行提取与分离工作。
三、实验步骤:A. 大黄中蒽醌的提取分离1、将粉末大黄紫锥子取 1g 加入圆底烧瓶中,加入 15 mL 95% 乙醇溶液,加热回流30分钟。
2、冷却后用干净的滤纸分离上清液用热水冲涤保持颜色相同(保留水冲涤液备用)。
3、将去溶剂后的渣用 10 mL 苯醇溶解,并过滤写滤液保存,不断冲涤干净渣质。
4、将 2mL 苯醇滤液分离于干净的离心管中,在室温下慢慢加入正硫酸,足量使呈酸性.,加入 5 mL 甲醇,蒸去溶剂后,注 1mL 50%氨水,筛过活性炭或过硅酸钠脱除杂物,使溶液呈现深黄色液体。
5、以上溶液在 20ml 分液漏斗中加入 20-25 mL 丙酮,振荡混合,分离两层液体,取下蒸馏收干(可以置于干燥器或开放场地自然干燥,当感觉无水分或连续称量两次称量值一致时即可)6、将干燥沉淀取少量溶解于绝对丙酮中成特邻醌的溶液。
7、分别进行下列试验来分离纯特邻醌:(1)纯特邻醌呈现红色;(2)用极少量生石灰进行检测,呈现橙色。
B. 大黄中大黄素含量的色谱定量测定色谱图谱图峰形面积法进行测定。
1、用同上操作,按“ A ”-“ E ”方法操作,取所得特邻醌溶液 1-5 mL 再加入丙酮使其溶解(溶液的浓度以能出现三个吸光峰为适宜,可调配NaOH溶液调节pH 值,使吸光峰相对集中于三个波长摆荡之一)。


中药制剂中大黄素提取工艺的进展摘要:本实验主要详细介绍了大黄素的几种常见的提取工艺,论述了提取工艺的进展,大黄素常见的提取方法有反相高效液相色谱法,葡聚糖凝胶分子筛及重结晶法,超声波-微波协同萃提取测定大黄素含量且获得较为满意的结果,实验证明该方法分离能力强、干扰少,具有广泛的应用性。
1 常用的大黄素提取方法1.1方法一:准确称取烘至恒重的本品粉末5 g,加硫酸液(2.5ml/1)30 ml,加热回流2h,冷却,加氯仿50ml,水浴回流1h,分取氯仿层,酸液再加氯仿40ml,继续回流,冷却后分取氯仿层,合并氯仿层,水洗三次,回收氯仿,残渣加甲醇溶解定容至5ml[1]。
1.2方法二:(双相水解提取法)精密称取样品粉末5g,加入60m1氯仿浓度为2.5M硫酸溶液,水浴回流4h,转至分液漏斗中静置,分出氯仿层再用氯仿60、50、40m1,萃取酸水层,合并回收氯仿液,残渣加甲醇溶解、定容至5m1,[1]1.3方法三:准确称取烘至干燥恒重的本品粉末5g,置圆底烧瓶内,加甲醇40m1,加热回流提取1h,过滤,滤液蒸干,残渣加2.5M硫酸液10m1,沸水浴中水解30 min,放冷后用乙醚萃取三次(20m1,15m1,15m1分取乙醚层,合并,回收乙醚,残渣加甲醇溶解、定容至5ml)。
将三种方法制得的样品液10m1点于同一块薄层板上,展开后观察。
[1]2 超声波-微波协同萃提取将萃取物先用硅胶层析板点样,初步确定萃取效果。
展开剂为石油醚∶乙酸乙酯∶甲酸= 15∶ 5∶ 1的上层清夜。
然后将萃取物样品测试条件进行HPLC分析,萃取液中保留时间为8.288 min 的峰和对照品中大黄素(保留时间8.354 min)的出峰时间基本一致,且峰型对称,结合薄层层析分析结果可确定该组分为大黄素[2]。
实验表明,超声波功率内置为50W的仪器条件下,影响超声波-微波协同萃取大黄素的因素依次为: 乙醇浓度、提取时间、乙醇用量、微波功率。

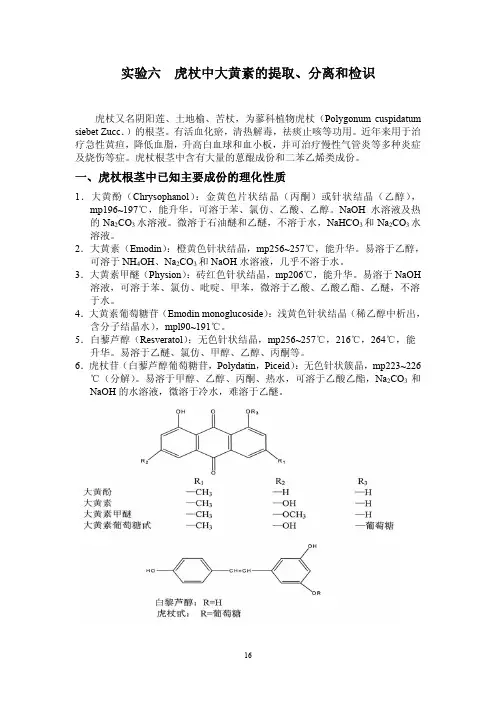
实验六虎杖中大黄素的提取、分离和检识虎杖又名阴阳莲、土地榆、苦杖,为蓼科植物虎杖(Polygonum cuspidatum siebet Zucc.)的根茎。
有活血化瘀,清热解毒,祛痰止咳等功用。
近年来用于治疗急性黄疸,降低血脂,升高白血球和血小板,并可治疗慢性气管炎等多种炎症及烧伤等症。
虎杖根茎中含有大量的蒽醌成份和二苯乙烯类成份。
一、虎杖根茎中已知主要成份的理化性质1.大黄酚(Chrysophanol):金黄色片状结晶(丙酮)或针状结晶(乙醇),mp196~197℃,能升华。
可溶于苯、氯仿、乙酸、乙醇。
NaOH水溶液及热的Na2CO3水溶液。
微溶于石油醚和乙醚,不溶于水,NaHCO3和Na2CO3水溶液。
2.大黄素(Emodin):橙黄色针状结晶,mp256~257℃,能升华。
易溶于乙醇,可溶于NH4OH、Na2CO3和NaOH水溶液,几乎不溶于水。
3.大黄素甲醚(Physion):砖红色针状结晶,mp206℃,能升华。
易溶于NaOH 溶液,可溶于苯、氯仿、吡啶、甲苯,微溶于乙酸、乙酸乙酯、乙醚,不溶于水。
4.大黄素葡萄糖苷(Emodin monoglucoside):浅黄色针状结晶(稀乙醇中析出,含分子结晶水),mpl90~191℃。
5.白藜芦醇(Resveratol):无色针状结晶,mp256~257℃,216℃,264℃,能升华。
易溶于乙醚、氯仿、甲醇、乙醇、丙酮等。
6.虎杖苷(白藜芦醇葡萄糖苷,Polydatin,Piceid):无色针状簇晶,mp223~226 ℃(分解)。
易溶于甲醇、乙醇、丙酮、热水,可溶于乙酸乙酯,Na2CO3和NaOH的水溶液,微溶于冷水,难溶于乙醚。
二、目的要求1.掌握从虎杖中提取羟基蒽醌类成份的方法。
2.熟悉用硅胶柱层析方法分离混合羟基蒽醌类成份的一般操作技术。
3.熟悉羟基蒽醌类化合物的主要检识反应。
三、实验原理本实验是根据游离蒽醌类成份能溶于含水氯仿的性质,先将原料的浓酸溶液湿润后,加入含水氯仿进行回流提取,在回流过程中即可将结合态的蒽醌(苷类)类成份水解成为游离蒽醌,这样就可连同原存在的游离态蒽醌成份,一并被含水氯仿提取出来。

大黄的提取分离的实验报告大黄的提取分离的实验报告引言:大黄,又称黄连木,是一种常见的中草药,具有清热泻火、解毒等功效。
其中的有效成分主要为大黄素,因此提取和分离大黄素成为研究的重点之一。
本实验旨在通过提取分离的方法,获得纯度较高的大黄素。
实验步骤:1. 材料准备:准备好干燥的大黄根,乙醇、水、醋酸等溶剂。
2. 粉碎大黄根:将大黄根研磨成粉末状,以增加提取效果。
3. 提取溶剂的选择:根据大黄素的溶解性,选择适合的溶剂。
在本实验中,选用乙醇为主要溶剂。
4. 提取:将粉碎后的大黄根与乙醇混合,放置一段时间,利用乙醇的溶解性,将大黄素从大黄根中提取出来。
5. 过滤:将提取液过滤,去除大黄根的残渣。
6. 浓缩:将过滤后的提取液进行浓缩,以减少体积,提高大黄素的浓度。
7. 结晶:将浓缩后的提取液进行结晶,通过控制温度和溶剂的浓度,使大黄素结晶出来。
8. 分离:将结晶后的大黄素与溶剂进行分离,得到纯度较高的大黄素。
实验结果:经过以上步骤,成功从大黄根中提取分离出了纯度较高的大黄素。
通过对提取液的浓缩和结晶,得到了结晶良好的大黄素晶体。
通过分离过程,成功去除了其他杂质,获得了纯度较高的大黄素。
实验讨论:1. 提取溶剂的选择:乙醇是一种常用的提取溶剂,对大黄素具有较好的溶解性。
但是在实际操作中,也可以根据实验需要选择其他溶剂进行提取。
2. 结晶条件的控制:结晶是将溶液中的溶质转化为晶体的过程。
在本实验中,通过控制温度和溶剂浓度,成功得到了结晶良好的大黄素晶体。
温度和溶剂浓度的选择对结晶的效果有重要影响,需要根据实际情况进行调整。
3. 分离的重要性:分离是提取分离过程中不可或缺的一步,通过分离可以去除杂质,提高目标物的纯度。
在本实验中,通过分离过程,成功去除了大黄根中的其他成分,获得了纯度较高的大黄素。
实验结论:通过本实验的提取分离过程,成功获得了纯度较高的大黄素。
实验结果表明,提取溶剂的选择、结晶条件的控制以及分离的重要性对于提高大黄素的纯度具有重要意义。



大黄中大黄素的提取、分离和鉴定一、实验目的与要求1.熟悉蒽醌类成分的提取分离方法。
2.掌握PH梯度提取法的原理和操作技术。
3.学习用硅胶柱色谱法分离精制大黄素。
4.学习羟基恩醌类化合物的鉴定方法。
二、实验方法(一)、基本原理大黄中羟基葸醌类化合物多数以苷的形式存在,故先用稀硫酸溶液把蒽醌苷水解成苷元,利用游离葸醌可溶于热氯仿的性质,用氯仿将它们提取出来。
由于各羟基葸醌结构上的不同所表现的酸性不同,用pH梯度萃取法分离它们;大黄酚和大黄素甲醚酸性相近,利用其极性的差别,用柱色谱分离之。
(二)操作步骤实验步骤实验操作实验现象和结果总羟基蒽醌苷元的提取1 称取大黄粉3.5g,用滤纸包裹,置索氏提取器中,圆底烧瓶中加入乙醚150ml,回流提取2h,得乙醚提取液。
乙醚提取液为黄色澄清溶液。
2 点板,展开,展开剂为石油醚-乙酸乙酯(7:3)。
硅胶板上可见四个斑点,从上往下依次为黄色斑点、橙色斑点、黄色斑点、黄色斑点。
pH梯度萃取分离1 大黄酸的分离和提纯:将提取液用5%NaHCO₃振荡提取数次,分出水层,重复提取数次后合并水层提取液,用盐酸酸化至pH3,得黄色沉淀。
抽滤,水洗沉淀,再用丙酮洗,干燥后待测。
水层提取液为呈紫红色。
盐酸酸化时有大量气泡生成。
酸化后得到黄色沉淀。
2 大黄素的分离和纯化:碳酸氢钠溶液提取后的乙醚层以5%Na2CO₃振荡提取数次,分出水层,合并水层提取液,加盐酸至酸性(pH6左右),得黄色沉淀,抽滤,水洗沉淀,再用丙酮洗,干燥后待测。
水层提取液呈红色。
盐酸酸化后得到黄色沉淀。
3 芦荟大黄素的分离和提纯:碳酸钠溶液提取后的乙醚层,用0.25%NaOH振荡提取数次,合并水层提取液,加盐酸至pH约为6,得橙色沉淀。
抽滤,水洗沉淀,干燥后待测。
水层提取液层红色。
盐酸酸化后得到橙色沉淀。
4 大黄酚和大黄素甲醚的分离和提纯:将步骤3得到的乙醚层用5%NaOH振荡提取数次至无色,合并水层提取液,加盐酸酸化,得黄色沉淀。

大黄中蒽醌类化合物的提取分离和鉴定
大黄(Rhizoma Rhei)是一种常用中药,主要含有蒽醌类化合物,如大黄素、大黄酚、大黄酸等。
提取、分离和鉴定大黄中的蒽醌类化合物的常用方法如下:
1. 提取:将大黄粉末与适量的乙醇或乙醚等有机溶剂进行浸泡提取,较常用的是乙醚提取。
在恒温搅拌的条件下,将大黄与乙醚按一定比例混合30分钟以上,然后进行过滤,过滤液即为提取液。
2. 分离:提取液中含有大黄中的多种化合物,其中包括蒽醌类化合物。
为了分离和纯化蒽醌类化合物,通常采用柱层析、薄层层析等技术。
柱层析是将提取液通过填料(如硅胶、活性炭等)柱进行洗脱,根据化合物在柱上的亲疏性和相互间作用力的差异,逐步分离目标化合物。
薄层层析则是将提取液涂抹在硅胶或其他载体上的薄层,再通过浸泡,将化合物分离开。
3. 鉴定:分离到目标化合物后,可以通过理化性质和光谱分析进行鉴定。
常用的鉴定方法有红外光谱(IR)、质谱(MS)和核磁共振(NMR)等。
红外光谱可以用于确定化合物的官能团,质谱可以用于分析分子的质量和结构信息,核磁共振则可以提供化合物的详细结构信息。
以上是大黄中蒽醌类化合物的提取、分离和鉴定的常用方法,通过这些方法可以对大黄中的蒽醌类化合物进行有效地提取、分离和鉴定。

大黄药材含量测定方法一、背景介绍大黄是一种中药原料,广泛应用于中医临床和民间传统医药。
大黄常用于清热泻火、通便利肠等疾病的治疗。
大黄中的主要有效成分是大黄素,其含量水平是影响其药效的一个重要指标。
准确地测定大黄中大黄素含量非常重要。
下面我们将介绍10种关于大黄药材含量测定方法的详细描述。
二、主要测定方法1. 高效液相色谱法(HPLC)HPLC是一种常用的大黄素含量测定方法。
该方法具有准确、快速、灵敏度高、重复性好等优点。
HPLC方法要求使用高品质的设备,例如高速离心机,从而获得准确的分离和定量数据。
2. 紫外分光光度法(UV)UV法是一种常用的大黄素含量测定方法。
该法无须特殊试剂,分析成本低廉。
但该方法受杂质干扰大,精密度差,显色反应不稳定等因素的影响,因此使用前应先去除大黄中的杂质。
3. 燃烧法燃烧法是大黄素中含量测定的一种传统方法。
该方法常用于水分及灰分含量的测定,并且操作简单,使用方便。
该方法的主要限制是无法区分大黄素与其他化合物,因此需要与其他方法结合使用。
4. 比色法比色法是大黄素含量测定的另一种常用方法。
使用比色法可以直接测量大黄素的吸光度,从而得出含量。
该方法的限制是对其他化合物不敏感,因此只能测定大黄中的大黄素含量。
5. 红外光谱法红外光谱法是一种非常灵敏和准确的大黄素含量测定方法。
该方法可以检测大黄素的特征峰,从而获得准确的含量数据。
使用该方法需要使用高品质的光谱仪,同时精确控制样品的温度和物质状态,以避免实验中的误差。
6. 气相色谱法气相色谱法是一种常用的大黄素含量测定方法。
该方法可以通过大黄素在气相中的相对分离和挥发率来推断其含量。
该方法需要使用高品质的气相色谱仪,从而获得准确的分离和定量数据。
7. HPLC-质谱法HPLC-质谱法是一种非常灵敏和准确的大黄素含量测定方法。
该方法能够对大黄素进行鉴定和测定,避免假阳性和假阴性结果,提高测定的准确性。
使用该方法需要使用高品质的质谱仪和高效液相色谱仪。
大黄中大黄素的提取一:前言(1)熟悉蒽醌类成分的提取分离方法(2)掌握PH梯度提取法的原理和操作技术(3)掌握蒽醌类化合物鉴定方法(4)了解液液萃取法分离混合物的实验方法关键词:大黄素 PH梯度提取法乙醚大黄为蓼科植物,味苦,性寒,具有泻热通肠、凉血解毒、逐瘀通经等功效。
其主要有效成分为大黄素、芦荟大黄素、大黄素甲醚等蒽醌类化合物 ,其中大部分为结合的蒽醌,少量为游离的蒽醌。
结合的蒽醌类化合物由于其苷元具有酚羟基,故呈弱酸性,能溶于水、乙醇、碳酸氢钠溶液,但在有机溶剂中的溶解度很小。
游离的蒽醌易溶于氯仿、乙醚等有机溶剂而不溶于水。
其中,大黄酸具有羧基,酸性最强;大黄素具有β-酚羟基,酸性第二;芦荟大黄素连有羟甲基,酸性第三;大黄素甲醚和和大黄酚的酸性最弱。
根据以上化合物的酸度差异,可用碱性强弱不同的溶液进行梯度萃取分离。
值由大到小分别为大黄酚和大黄素甲醚、本实验主要用薄层层析法分离纯化大黄素,其Rf大黄素、芦荟大黄素、大黄酸。
大黄酸:黄色针状结晶mp.321—322℃(升华),不溶于水,能溶于吡啶、碳酸氢钠水溶液,微溶于乙醇、苯、氯仿、乙醚和石油醚。
大黄素:橙黄色针状结晶,mp.256—257℃(乙醇或冰醋酸),能升华。
其溶解度如下:四氯化碳0.01%、氯仿0.07%、二硫化碳0.009%、乙醚0.14%、苯0.041%。
易溶于乙醇,可溶于稀氨水、碳酸钠水溶液,几乎不溶于水。
大黄酸 R1=H R2=COOH大黄素 R1=CH3R2=OH芦荟大黄素 R1=CH2OH R2=H大黄素甲醚 R1=CH3R2=OCH3大黄酚 R1=CH3R2=H二:实验试剂与仪器试剂:大黄粗粉、20%硫酸溶液、5%碳酸氢钠溶液、5%碳酸钠溶液、10%盐酸溶液、乙醚仪器:回流装置一套、蒸发皿、烧杯、试管、梨形分液漏斗、水浴锅、电热套、抽滤瓶、铁架台、真空泵等三:实验过程具体操作步骤:1.游离蒽醌的提取称取大黄粗粉30g,加20%H2SO4水溶液150mL,加热1小时,放冷,抽滤,同时滤饼水洗至近中性(除去H2SO4),于70℃干燥后,置回流装置中,加入乙酸乙酯300 mL回流提取1小时,得到乙酸乙酯提取液。
大黄中大黄素的提取、分离与鉴定一、实验目的(1)熟悉蒽醌类成分的提取分离方法(2)掌握PH梯度提取法的原理和操作技术(3)掌握蒽醌类化合物鉴定方法(4)了解液液萃取法分离混合物的实验方法二、实验原理大黄为蓼科植物,味苦,性寒,具有泻热通肠、凉血解毒、逐瘀通经等功效。
其主要有效成分为大黄素、芦荟大黄素、大黄素甲醚等蒽醌类化合物,其中大部分为结合的蒽醌,少量为游离的蒽醌。
结合的蒽醌类化合物由于其苷元具有酚羟基,故呈弱酸性,能溶于水、乙醇、碳酸氢钠溶液,但在有机溶剂中的溶解度很小。
游离的蒽醌易溶于氯仿、乙醚等有机溶剂而不溶于水。
其中,大黄酸具有羧基,酸性最强;大黄素具有β-酚羟基,酸性第二;芦荟大黄素连有羟甲基,酸性第三;大黄素甲醚和和大黄酚的酸性最弱。
根据以上化合物的酸度差异,可用碱性强弱不同的溶液进行梯度萃取分离。
【1】本实验主要用薄层层析法分离纯化大黄素,其R f值由大到小分别为大黄酚和大黄素甲醚、大黄素、芦荟大黄素、大黄酸。
【2】大黄酸:黄色针状结晶mp.321—322℃(升华),不溶于水,能溶于吡啶、碳酸氢钠水溶液,微溶于乙醇、苯、氯仿、乙醚和石油醚。
大黄素:橙黄色针状结晶,mp.256—257℃(乙醇或冰醋酸),能升华。
其溶解度如下:四氯化碳0.01%、氯仿0.07%、二硫化碳0.009%、乙醚0.14%、苯0.041%。
易溶于乙醇,可溶于稀氨水、碳酸钠水溶液,几乎不溶于水。
【3】大黄酸R1=H R2=COOH大黄素R1=CH3R2=OH芦荟大黄素R1=CH2OH R2=H大黄素甲醚R1=CH3R2=OCH3大黄酚R1=CH3R2=H三、实验器材试药:大黄粗粉、20%硫酸溶液、5%碳酸氢钠溶液、5%碳酸钠溶液、盐酸、丙酮、乙酸乙酯、硅胶CMC-Na板、石油醚、大黄素标准品等仪器:回流装置一套、烧杯、层析槽、试管、梨形分液漏斗、水浴锅、电热套、旋转蒸发仪循环水式多用真空泵、抽滤瓶、铁架台等四、实验内容大黄素的提取、分离流程图大黄粗粉30g【4】20%H2SO4150ml加热1h,抽滤、干燥滤饼乙酸乙酯回流提取1h乙酸乙酯层5%NaHCO3萃取水层(紫红色)乙酸乙酯层5%Na2CO3水层(红色)乙酸乙酯层(弃掉)HCl黄色沉淀(粗品)水洗至中性,丙酮溶解,分离纯化大黄素结晶具体操作步骤:1.游离蒽醌的提取称取大黄粗粉30g,加20%H2SO4水溶液150mL,加热1小时,放冷,抽滤,同时滤饼水洗至近中性(除去H2SO4),于70℃干燥后,置回流装置中,加入乙酸乙酯300mL回流提取1小时,得到乙酸乙酯提取液。
大黄中大黄素的提取分离
大黄酸R1=H R2=COOH
大黄素R1=CH3R2=OH
芦荟大黄素R1=CH2OH R2=H
大黄素甲醚R1=CH3R2=OCH3
大黄酚R1=CH3R2=H
黄色沉淀(粗品)
水洗至中性,丙酮溶解,分离纯化大黄素结晶
解释:
1.大黄中羟基蒽醌类化合物多数以苷的形式存在,故先用稀硫酸溶液把蒽醌苷水解成苷元,利用游离蒽醌可溶于乙醚的性质,用乙醚将它们提取出来。
2.由于各羟基蒽醌结构上的不同所表现的酸性不同,用pH梯度萃取法分离它们。
大黄酸具有羧基,酸性最强;大黄素具有β-酚羟基,酸性第二;芦荟大黄素连有羟甲基,酸性第三;大黄素甲醚和和大黄酚的酸性最弱。
根据以上化合物的酸度差异,可用碱性强弱不同的溶液进行梯度萃取分离。
【1】徐选明,刘新大黄中大黄素提取工艺的优化中国中医药信息杂志2004,11,5
【2】李乃明,丁宙大黄素的分离和结构鉴定广州医学院学报1985,13,3 【3】朱庆玲,李瑞和大黄中大黄素的提取工艺研究时珍国医国药2006,17,3。
大黄素的提取分离和鉴定(实验方案)
一、药物简介
【英文名称】:Emodin
【大黄素别名】:朱砂莲甲素
【化学名】:1'3'8-三羟基-6-甲基蒽醌
【分子式】:C15H10O5
【分子量】:
【结构式】:
【植物来源】:为蓼科植物虎杖的干燥根茎和根。
掌叶大黄的根茎。
【物理性质】:橙黄色长针状结晶(丙酮中结晶为橙色,甲醇中结晶为黄色),熔点256℃~257℃。
具有蒽醌的特殊反应。
几乎不溶于水,溶于乙醇及碱溶液。
【药理药效】:大黄素可用作泻药,虽有泻下活性,但由于体内易被氧化破坏,实际上泻下作用很弱,如与糖结合成苷类,则可发挥泻下作用。
大黄素国内专业生产商西安融升生物目前表示大黄素-1-O-β-D-葡萄糖苷和大黄素-8-O-β-D-葡萄糖苷者是大黄素与葡萄糖结合的苷,二者只是结合的位置不同,同时存在于大黄中。
另有抗菌、止咳、抗肿瘤、降血压等作用。
二、实验目的
1.掌握大黄素的提取原理及方法。
2.熟练掌握大黄素提取实验方法操作。
3.了解大黄素的不同提取方法。
三、实验原理
游离的蒽醌易溶于氯仿、乙醚等有机溶剂而不溶于水。
其中,大黄酸具有羧基,酸性最强;大黄素具有β-酚羟基,酸性第二;芦荟大黄素连有羟甲基,酸性第三;大黄素甲醚和和大
黄酚的酸性最弱。
根据以上化合物的酸度差异,可用碱性强弱不同的溶液进行梯度萃取分离。
本实验主要用薄层层析法分离纯化大黄素,其Rf值由大到小分别为大黄酚和大黄素甲醚、大黄素、芦荟大黄素、大黄酸。
大黄酸:黄色针状结晶
—322℃(升华),不溶于水,能溶于吡啶、碳酸氢钠水溶液,微溶于乙醇、苯、氯仿、乙醚和石油醚。
大黄素:橙黄色针状结晶,—257℃(乙醇或冰醋酸),能升华。
其溶解度如下:四氯化碳%、氯仿%、二硫化碳%、乙醚%、苯%。
易溶于乙醇,可溶于稀氨水、碳酸钠水溶液,几乎不溶于水。
四、仪器及试剂
试剂:大黄粗粉、90%乙醇、25%硫酸溶液、5%碳酸氢钠溶液、5%碳酸钠溶液、盐酸、丙酮、乙酸乙酯、硅胶CMC-Na板、石油醚、冰醋酸、大黄素标准品等
仪器:回流装置一套、烧杯、层析槽、试管、梨形分液漏斗、水浴锅、电热套、旋转蒸发仪、循环水式多用真空泵、抽滤瓶等。
五、实验内容
1、大黄素提取分离流程图
大黄粗粉30g
加8倍量的90%乙醇240ml
于500ml的圆底烧瓶中。
回流2次,温度80℃,时间1h
合并滤液,滤液浓缩至50ml 加入25%硫酸140ml,沸水浴中回流5min
乙酸乙酯萃取
乙酸乙酯层
5% Na2CO3
水层(红色)乙酸乙酯层
盐酸
黄色沉淀(粗品)
水洗至中性,丙酮溶解,分离纯化
大黄素结晶
具体步骤:
a.游离蒽醌的提取
搭好回流装置取大黄30g,加8倍量的90%乙醇240ml于500ml的圆底烧瓶中回流2次,温度80℃,时间1h,合并滤液滤液浓缩至50ml(旋蒸仪)加入25%硫酸140ml沸水浴中回流5min 倾出水解液,用乙酸乙酯萃取两次(100ml),合并提取液。
梯度萃取分离
将乙酸乙酯提取液加入分液漏斗中,用5% NaHCO3水溶液萃取三次,(经观察乙酸乙酯层颜色变浅及无气泡产生为止)。
经5% NaHCO3水溶液萃取后的乙酸乙酯层,继以5% Na2CO3水溶液萃取三次,乙酸乙酯层经薄层检查(标准大作对照),得知已提尽大黄素后,合并三次Na2CO3萃取液,并用5%HCl酸化,得大黄素沉淀。
(注意:加酸时应缓慢加入,以防酸液溢出)。
2、大黄素的精制
过滤大黄素沉淀,水洗沉淀物至洗出液呈中性,用适量丙酮溶解,用自备薄层色谱分离纯化大黄素。
薄层层析板上橙色层为大黄素,将其刮下溶于丙酮中。
用旋转蒸发仪浓缩丙酮溶液,得到大黄素结晶。
3、大黄素的薄层色谱检识
薄层板:硅胶CMC-Na板
样品液:自制大黄素溶液
对照品:标准大黄素溶液
展开剂:石油醚-乙酸乙酯-冰醋酸(15:2::1)
显色:观察斑点颜色及计算Rf值
4、注易事项
(1)游离蒽醌的提取要控制温度,不宜太高
(2)PH梯度萃取分离时,要检查是否萃取完全
(3)注意碱液浓度及萃取时的静置时间对实验结果的影响。
六、讨论
1.蒽醌类化合物的含量测定有哪些方法各有什么优缺点
答:含量测定方法有比色法、薄层扫描法、高效液相色谱法、及重现性较差。
薄层扫描相对简单,在一块板能处理许多样品,但因其为封闭系统,受外界影响较大,导致其测定的结果的重现性较差。
高效液相色谱法需要解决好样品的前处理问题,则比较准确、可行。
高效毛细管电泳法虽然有许多的优点,但它一直处于被研究和改进的阶段,技术上不是很成熟。