初中化学物质转化关系图
- 格式:doc
- 大小:267.50 KB
- 文档页数:6

一、中考初中化学推断题1.如图表示某些物质间转化关系。
A为暗紫色固体,X、F为液体且组成元素相同,X具有消毒杀菌作用,E为产生温室效应的常见气体,Y是一种金属。
请回答下列问题:(1)X的化学式为_____,Y的化学式为_____。
(2)写出反应①的化学方程式:_____。
(3)④的化学反应基本类型是_____。
(4)我们家乡大庆家用燃气的主要成分是甲烷,当燃气灶的火焰呈现黄色或橙色、锅底出现黑色时,说明_____,燃气发生不完全燃烧。
【答案】H2O2 Cu 2KMnO4K2MnO4+MnO2+O2↑化合反应有炭黑生成【解析】【分析】甲烷和B可以点燃生成E、F,所以B是氧气,A为暗紫黑色,所以A是高锰酸钾,高锰酸钾在加热的条件下生成锰酸钾和二氧化锰和氧气,所以D是锰酸钾,甲烷和氧气在点燃的条件下生成二氧化碳和水,所以C是二氧化锰,X、F为液体且组成元素相同,X具有消毒杀菌作用,所以X是过氧化氢,F是水,过氧化氢在二氧化锰做催化剂的条件下生成水和氧气,E为产生温室效应的常见气体,Y是一种金属,所以E是二氧化碳,Y是铜;铜和氧气和二氧化碳生锈得到绿色的碱式碳酸铜,碱式碳酸铜在加热的条件下生成氧化铜和二氧化碳和水,经过验证,推导正确。
【详解】(1)所以X的化学式为H2O2,Y的化学式为Cu,故填:H2O2、Cu;(2)反应①是高锰酸钾在加热的条件下生成锰酸钾、二氧化锰和氧气,化学方程式为:2KMnO4ΔK2MnO4+MnO2+O2↑,故填:2KMnO4ΔK2MnO4+MnO2+O2↑;(3)反应④是铜、氧气、水和二氧化碳反应生成碱式碳酸铜,化学反应基本类型是:化合反应,故填:化合反应;(4)家用燃气的主要成分是甲烷,当燃气灶的火焰呈现黄色或橙色、锅底出现黑色时,说明有炭黑生成,燃气发生不完全燃烧,故填:有炭黑生成。
【点睛】推断题的突破点在一些物质的特殊用途如作消毒剂,特殊的组成如常温下反应物与生成物都是液体且组成元素相同,特殊的物质颜色如暗紫色的高锰酸钾等。

浙教版中考科学一轮复习物质的推断与转化化学物质之间的相互转化、物质的推断一、选择题1.(2023·湖北宜昌·中考真题)如图所示,“—”表示相连的两种物质能发生反应,“→”表示一种物质能转化成另一种物质,部分反应物、生成物及反应条件未标出。
下列说法与图示关系不符..的是A .甲不能是碱B .丙不能是单质C .甲乙可以都是氧化物D .甲乙丙可以是不同类别的物质2.(2023·湖南岳阳·中考真题)甲、乙、丙是初中化学常见的三种物质, 他们之间的转化关系如图所示(“→”表示反应可一步实现,部分物质和反应条件略去)。
下列推断正确的是A .若甲是H 2O ,则乙可能是CaCl 2B .若甲是CO 2,则丙可能是H 2C .若甲转化为乙是置换反应,则乙转化为丙不可能也是置换反应D .若甲转化为乙是复分解反应,则乙转化为丙不可能也是复分解反应3.(2023·陕西·中考真题)下图是初中四种常见物质之间的常见反应关系图,图中“——”表示相连的两种物质能反应,“→”表示两端的物质通过一步反应能转化。
下列说法不正确...的是A .X 一定是()2Ca OHB .Y 可能是钠盐C .X 与Y 不可能都是盐D .X 与Y 反应能生成NaOH4.(2023·贵州·中考真题)通过化学变化创造物质是化学学科的特征。
甲、乙、丙、丁的转化关系如图所示。
(“→”表示能一步实现反应,部分物质和反应条件已略去),下列说法中错误的是A .若甲为2H ,则丁可以是Fe 或2H OB .若甲为2H ,则丁→甲不可以是复分解反应C .若甲为2CO ,则丙可以是水D .若甲为NaOH ,则丙可以是()33Fe NO5.(2022·江苏徐州·中考真题)A~E是初中化学中的常见物质且都含有一种相同元素,它们之间的一步反应转化关系如图所示(部分反应物、生成物未标出)。
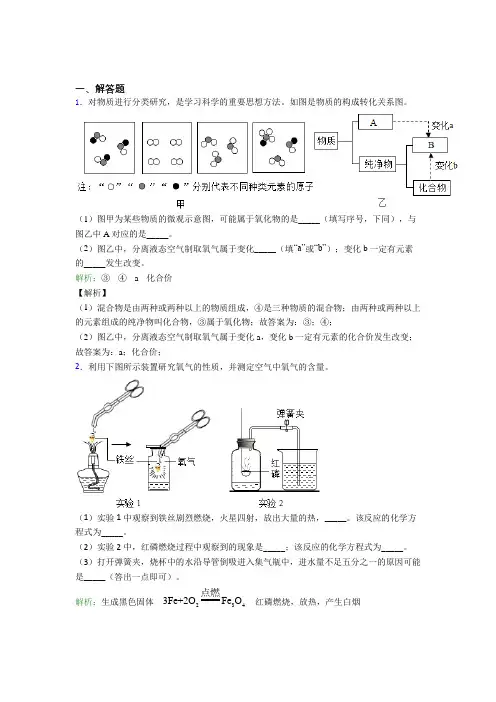
一、解答题1.对物质进行分类研究,是学习科学的重要思想方法。
如图是物质的构成转化关系图。
(1)图甲为某些物质的微观示意图,可能属于氧化物的是_____(填写序号,下同),与图乙中A 对应的是_____。
(2)图乙中,分离液态空气制取氧气属于变化_____(填“a”或“b”);变化b 一定有元素的_____发生改变。
解析:③ ④ a 化合价【解析】(1)混合物是由两种或两种以上的物质组成,④是三种物质的混合物;由两种或两种以上的元素组成的纯净物叫化合物,③属于氧化物;故答案为:③;④;(2)图乙中,分离液态空气制取氧气属于变化a ,变化b 一定有元素的化合价发生改变;故答案为:a ;化合价;2.利用下图所示装置研究氧气的性质,并测定空气中氧气的含量。
(1)实验1中观察到铁丝剧烈燃烧,火星四射,放出大量的热,_____。
该反应的化学方程式为_____。
(2)实验2中,红磷燃烧过程中观察到的现象是_____;该反应的化学方程式为_____。
(3)打开弹簧夹,烧杯中的水沿导管倒吸进入集气瓶中,进水量不足五分之一的原因可能是_____(答出一点即可)。
解析:生成黑色固体 2343Fe+2O Fe O 点燃 红磷燃烧,放热,产生白烟2254P+5O 2P O 点燃 气密性不好(合理即可)(1) 铁丝剧烈燃烧,火星四射,放出大量的热,生成黑色固体。
铁与氧气反应生成四氧化三铁,化学方程式为:2343Fe+2O Fe O 点燃(2) 红磷燃烧,放热,产生白烟;白磷燃烧生成五氧化二磷,化学方程式为:2254P+5O 2P O 点燃。
(3) 气密性不好会导致水进入集气瓶体积偏小,测量结果偏小(合理即可)。
3.写出下列反应的文字表达式(1)加热氯酸钾和二氧化锰的混合物制氧气: __(2)硫在氧气中燃烧: _ (3)铁丝在氧气中燃烧: _(4)过氧化氢制氧气: _上述反应中,反应(2)、(3)属于化学反应基本类型中的 反应;反应(1)、(4)属于化学反应基本类型中的 反应。
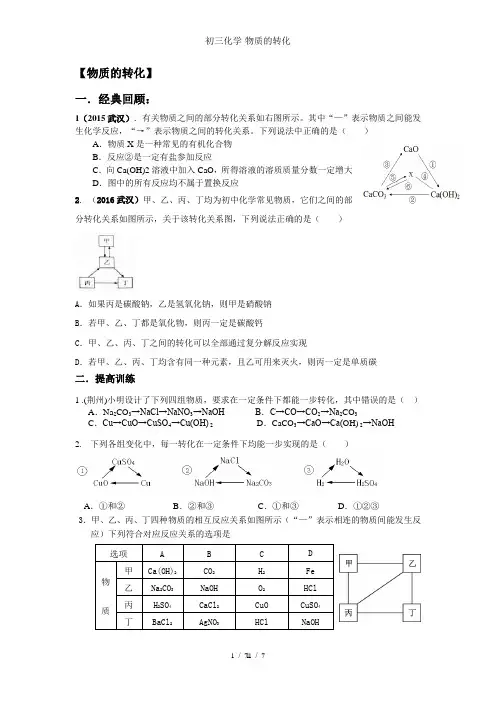
【物质的转化】一.经典回顾:1(2015武汉).有关物质之间的部分转化关系如右图所示。
其中“—”表示物质之间能发生化学反应,“→”表示物质之间的转化关系。
下列说法中正确的是( )A .物质X 是一种常见的有机化合物B .反应②是一定有盐参加反应C .向Ca(OH)2溶液中加入CaO ,所得溶液的溶质质量分数一定增大D .图中的所有反应均不属于置换反应2. (2016武汉)甲、乙、丙、丁均为初中化学常见物质,它们之间的部分转化关系如图所示,关于该转化关系图,下列说法正确的是( )A .如果丙是碳酸钠,乙是氢氧化钠,则甲是硝酸钠B .若甲、乙、丁都是氧化物,则丙一定是碳酸钙C .甲、乙、丙、丁之间的转化可以全部通过复分解反应实现D .若甲、乙、丙、丁均含有同一种元素,且乙可用来灭火,则丙一定是单质碳二.提高训练1 .(荆州)小明设计了下列四组物质,要求在一定条件下都能一步转化,其中错误的是( )A .Na 2CO 3→NaCl→NaNO 3→NaOHB .C→CO→CO 2→Na 2CO 3C .Cu→CuO→CuSO 4→Cu(OH) 2D .CaCO 3→CaO→Ca(OH) 2→NaOH2. 下列各组变化中,每一转化在一定条件下均能一步实现的是( )A .①和②B .②和③C .①和③D .①②③3.甲、乙、丙、丁四种物质的相互反应关系如图所示(“—”表示相连的物质间能发生反应)下列符合对应反应关系的选项是选项A B C D 物质 甲Ca(OH)2 CO 2 H 2 Fe 乙 Na 2CO 3 NaOH O 2 HCl 丙H 2SO 4 CaCl 2 CuO CuSO 4 丁 BaCl 2 AgNO 3 HCl NaOH4.甲乙丙丁四种物质的转化关系如图所示。
下列说法正确的是A.若丙为沉淀,则甲、乙中一定有一种物质是碱B.若丙为气体,则甲、乙中一定有单质C.若丁为水,则该反应一定是复分解反应D.若甲、丁为单质,则该反应一定是置换反应5(双选题).现有铁、氧化铁、稀盐酸、氢氧化钙溶液、碳酸钠溶液五种物质.存在如图所示的相互反应和转化关系。

一、初中化学物质的转化关系1、氧气、氧化物、酸、氢气、水H2OKMnO4↘↓↑↗CO、CO2↗SO2H2SO4H2O2→→P2O5+ Mg Al Zn Fe→ H2→H2O ↘MgO HClKClO3↗↓↘Al2O3 Fe3O42、碳与碳的化合物3、氢氧化钠、碳酸钠、氯化钠+ CO2↗ Na2SO4 → BaSO4↓(白)NaOH → Na2CO3 → CaCO3↓(白)(变质)↘ NaCl → AgCl↓(白)4、含钙化合物的关系:↙↗―――――――↘↖CaCO3→CaO→Ca(OH)2→CaCl2↖CO2↙5、氧化钡、氢氧化钡与硫酸钡1 / 32 /3 ↗BaCl 2 → BaSO 4↓(白)BaO → Ba(OH)2 ↗↘ + CuS O 4↘Cu(OH)2↓(蓝)6、硫酸铜、碳酸氢钙、碳酸氢钠、碳酸氢铵CuO ↗ CO 2↙ ↘ Ca(HCO 3)2 → CaCO 3→CaOCuSO 4.5H 2O →CuSO 4→ Cu ↘ H 2O↗Na 2CO 3 ↗ NH 3 → NH 3.H 2O NaHCO 3 →CO 2 NH 4HCO 3 → H 2O↘H 2O → H 2CO 3 ↘ CO 2 → H 2CO 37、铝、镁、锌、铁、铜及其化合物↗ZnSO 4↖ ↗ AlCl 3↖Zn → ZnO Al → Al 2O 3 ↘ZnCl 2↙ ↘Al 2(SO 4)3↙Fe Al↗MgCl 2↖ ↙﹉﹉﹉﹉↗ CuCl 2↘↖Mg → MgO Cu ←→CuO Cu(OH)2 ↘MgSO 4↙ ↖____↘ CuSO 4↗↙ Fe Al↙ FeCl 3 ↖ C CO H 2 Mg Al ↗FeSO 4Fe(OH)3 Fe 2O 3 ←――――→ Fe↖Fe 2(SO 4)3↙ O 2 H 2O ↘ FeCl 2 8、常见物质的相互转化关系(即注明必要的反应物、反应条件)CO 2 CO C 或O 2 O 2 H 2O H 2O 2Al 2O 3 AlCl 3 Al CuO CuSO 4 Cu ⑴ ⑵ ⑶ ⑷ MgO MgSO 4 Mg Cu H 2 Fe CaO Ca(OH)2 CaCO 3 CaCl 2 Ca(OH)2CaCO 3 ⑸ ⑹ ⑺ ⑻CaCO3Na2CO3CO2CO2NaOHNa2CO3CO2O2H2ONaOH NH4ClNH3⑼⑽⑾⑿3 / 3。



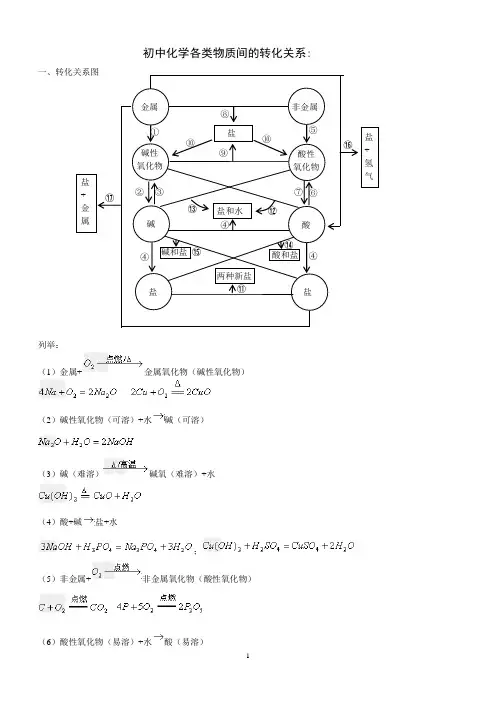
初中化学各类物质间的转化关系:
一、转化关系图
列举: (1)金属+
金属氧化物(碱性氧化物)
(2)碱性氧化物(可溶)+水
碱(可溶)
(3)碱(难溶)
碱氧(难溶)+水
(4)酸+碱
盐+水
;
(5)非金属+
非金属氧化物(酸性氧化物)
(6)酸性氧化物(易溶)+水
酸(易溶)
①
金属 非金属
碱性 氧化物 酸性 氧化物 盐 碱
盐和水 酸
盐
盐
两种新盐
碱和盐 酸和盐 盐+氢 气
盐
+ 金
属
②
③
④
④
④
⑤ ⑥
⑦ ⑧ ⑨
⑩
⑪
⑩
⑫
⑬
⑭
⑮
⑯
⑰
(7)酸(易挥发/难溶)酸氧+水(易挥发/难溶)
从纵向来看,金属碱性氧化物碱盐,其中金属元素相同。
非金属酸性氧化物酸(含氧酸)盐,其中非金属元素相同。
横向:
(8)金属+非金属(无氧酸)盐
(9)碱氧+酸氧(含氧酸)盐
(10)含氧酸盐碱氧+酸氧
(11)盐+盐两种新盐
交叉:
(12)酸+碱氧盐+水
(13)碱+酸氧盐+水
(14)酸+盐新酸+新盐
;
(15)碱+盐新碱+新盐
(16)金属+酸盐+
(17)金属+盐新盐+新金属
(18)金属+盐新盐+新金属
(置换反应)。

第2节 单质、氧化物、酸、碱、盐相互转化规律知识回顾各物质都具有一定的性质,同时各物质之间都相互联系,即有一定的相互转化规律。
1.金属(1)与氧气反应生成金属氧化物。
如:MgO O Mg 222点燃+;CuO O Cu 222∆+(2)活泼金属与酸反应生成盐和氢气。
如:↑+==+2442H FeSO SO H Fe ;↑+==+222H MgCI HCI Mg 金属与盐溶液反应生成新盐和新金属。
如:44FeSO Cu CuSO Fe +==+;Ag NO Cu Cu AgNO 2)(2233+==+。
2.非金属(1)与氧气反应生成非金属氧化物。
如:O H O H 22222点燃+;22SO O S 点燃+(2)与金属反应生成无氧酸盐。
NaCI CI Na 222点燃+;FeS S Fe ∆+3.碱性氧化物(1)与水反应生成碱。
如:22)(OH Ca O H CaO ==+。
(2)与酸反应生成盐和水。
如:O H SO Fe SO H O Fe 234242323)(3+==+(3)与酸性氧化物反应生成含氧酸盐。
如:32CaSiO SiO CaO 高温+4.酸性氧化物(1)与水反应生成酸。
如:3222CO H O H CO ==+。
(2)与碱反应生成盐和水。
如:O H CaCO OH Ca CO 2322)(+↓==+(3)与碱性氧化物反应生成含氧酸盐。
如:32CaSiO SiO CaO 高温+5.酸(1)与活泼金属反应生成盐和氢气。
如:↑+==+2442H ZnSO SO H Zn(2)与碱性氧化物反应生成盐和水。
如:O H FeCI HCI O Fe 2332326+==+。
(3)与碱反应生成盐和水。
如:4224222SO Na O H NaOH SO H +==+(4)与某些盐反应生成新盐和新酸。
如:33HNO AgCI AgNO HCI +↓==+6.碱(1)与酸性氧化物反应生成盐和水。
如: O H SO Na SO NaOH 2+==+(2)与酸反应生成盐和水。

饱和溶液和不饱和溶液的概念①饱和溶液:在一定温度下,在一定量的溶剂里,不能再溶解某种溶质的溶液,叫做这种溶质的饱和溶液②不饱和溶液:在一定温度下,在一定量的溶剂里,还能再继续溶解某种溶质的溶液,叫做这种溶质的不饱和溶液判断一种溶液是否是饱和溶液要注意:①在一定温度下。
②在一定量的溶剂里。
因为温度改变或溶剂量改变都会把饱和溶液变成不饱和溶液,也就是说饱和溶液与不饱和溶液在一定条件下可以互相转化,③被溶解的物质,即溶质能否继续溶解,若能继续溶解则为不饱和溶液,若不能继续溶解则为饱和溶液。
④某一种物质的饱和溶液是对该物质而言,但对其他物质则不是饱和溶液。
如20℃时,NaCl的饱和溶液不能再溶解NaCl了,但还能继续溶解KNO3,即此溶液对于NaCl来说是饱和溶液,但对KNO3来说则是不饱和溶液。
饱和溶液与不饱和溶液的相互转化方法:(1)对于大多数固体:在一定量的水中溶解的最大量随温度升高而增大饱和溶液不饱和溶液(2)对于Ca(OH)2:在一定量的水中溶解的最大量随温度升高而减少饱和石灰水不饱和石灰水概念的理解:(1)溶液的饱和与不饱和跟温度和溶质的量的多少有关系。
因此在谈饱和溶液与不饱和溶液时,一定要强调“在一定温度下”和“一定量的溶剂里”,否则就无意义。
(2)一种溶质的饱和溶液仍然可以溶解其他溶质。
如氯化钠的饱和溶液中仍可溶解蔗糖。
(3)有些物质能与水以任意比例互溶,不能形成饱和溶液,如:酒精没有饱和溶液。
饱和溶液和不饱和溶液的相互转化:一般,对饱和溶液与不饱和溶液相互转化过程中溶液组成的分析:①饱和溶液不饱和溶液(或不饱和溶液饱和溶液。
不发生结晶的前提下)溶液中溶质、溶剂、溶液的质量不变,溶质质量分数不变。
②不饱和溶液饱和溶液溶液的溶剂质量不变,溶质、溶液、溶质质量分数均增大。
③不饱和溶液饱和溶液(不发生结晶的前提下)溶质质量不变,溶剂、溶液质量变小,溶质质量分数变大。
④饱和溶液不饱和溶液溶剂、溶液质量增大,溶质质量不变,溶质质量分数变小判断溶液是否饱和的方法:①观察法:当溶液底部有剩余溶质存在,且溶质的量不再减少时,表明溶液已饱和。
物质的分类和转化规律一.物质的转化规律:1.金属+氧==金属氧化物2.金属氧化物+还原剂=金属+非金属氧化物①CuO+H2== 现象:,H2还原优点是反应生成物之一是,且产物较纯净。
②CuO+CO== (CO有剧毒,实验时一定)③2CuO+C;现象:(虽然C的还原能力强于H2,但固体还原剂与氧化物的充分接触程度没有固体与气体还原剂充分,自然反应温度就比H2要高,最好使用酒精喷灯或加罩的酒精灯。
C要稍微过量。
)④2Fe2O3+3C;⑤Fe2O3+3CO;(加热时一定要持续高温)⑥Fe2O3+3H2 ;现象:3.金属氧化物+水==碱4.碱==金属氧化物+水5.非金属+氧==非金属氧化物①氢气在空气中燃烧:2H2+O2现象:相关知识点: (1)氢气是一种常见的还原剂; (2)点燃前,一定要检验它的纯度否则会爆炸。
②红磷在空气中燃烧:4P+5O2现象:相关知识点: (1)烟是固体小颗粒;雾是液体小颗粒. (2)测量氧气在空气中的体积分数。
(3)可做烟雾弹。
③硫粉在空气中燃烧: S+O2现象:在空气中是发出微弱的火焰,在氧气中是发出明亮的火焰. 有强烈气味。
相关知识点:(1)反应后的产物可用紫色的石蕊试液来检验(紫色变成红色);(2)SO2污染空气,要用溶液进行尾气处理。
(3)SO2是气体,所以测量氧气在空气中的体积分数,若将水改为溶液,也可以测量氧气在空气中的体积分数。
④碳在氧气中充分燃烧:C+O2现象:在空气中是发出 ,在氧气中是发出。
相关知识点:反应后的产物可用来进行检验.⑤碳在氧气中不充分燃烧:2C+O26.非金属氧化物 + 活泼金属 == 非金属+金属氧化物①金属钠与水反应:2Na+2H2O== ,现象:浮(钠块浮在水面上)、游(钠块在水面上无规则游动)、熔(钠块熔化为小球)、响(发出嘶嘶的响声)、红(使滴入酚酞试液的溶液变红)②金属镁与CO2反应:2Mg+CO22MgO+C 现象:发出白光,有白色粉末(MgO)生成,有黑色固体(C)生成,同时放出大量的热。
[难点聚焦]单质、氧化物、酸、碱、盐之间的转化关系[难点聚焦]单质、氧化物、酸、碱、盐之间的转化关系盐和金属金属非金属碱性氧化物酸性氧化物碱酸盐盐盐(无氧酸盐)盐(含氧酸盐)盐和水碱和盐酸和盐两种新盐盐和氢气+酸+碱(16)(1)+O2(7)(17)+O2(4)(17)(8)(2)+H2O-H2O(3)(11)(12)(5)+H2O-H2O(6)(15)(9)(14)(13)(10)物、酸、碱、盐五大类,但对于书写化学方程式来说,将物质分为七类更好:金属、非金属、碱性氧化物、酸性氧化物、酸、碱、盐。
一般把它叫做“八圈图”(如上图)。
物质间的相互关系也是物质间的反应规律,必须牢牢掌握!2.发掘“八圈图”的内涵。
⑴表示物质间的纵横衍变关系,如从金属或非金属如何衍变成盐;⑵表示15个基本反应规律(9条连线和6个箭头);⑶表示物质的性质(除了跟指示剂反应这一性质在图中无法表示外,图中酸没有打箭头的4根线表示的是酸的性质,其余类推!);⑷表示物质(特别是盐)的制法;15个反应中至少有10个与盐有关,俗称“十大成盐”规律!3.使用“八圈图”的注意事项。
⑴各类物质的相互关系图并非无所不含,有以下一些规律未能体现:H2、C、CO还原CuO或Fe2O3;CuSO4转化为胆矾晶体;碳酸(氢)盐的分解;酸式盐与正盐的转换规律等。
⑵复分解反应规律的条件:可溶的反应物,能生成沉淀、气体或水。
⑶置换反应规律的条件:金属活动顺序强换弱。
判断金属与酸反应时:金属必须排在H前面;酸不可用硝酸、浓硫酸。
判断金属与盐反应时:必须同时满足“排在前面的金属;可溶性盐”。
例题:小梅同学学习了单质、氧化物、酸、碱、盐性质后,发现许多不同类别的物质反应时能生产盐,于是她构建了下图所示的知识网络图。
铜及其化合物在工业上有重要的应用。
借助网络图回答:(1)写出用酸和碱生产硫酸铜的化学方程式:。
(2)请你把图中①②处补充完整,要求不能与图中已有信息重复。
中考知识点(四)——物质间的转化与推断一、初中化学物质间转化网络关系图1.以碳、氧元素为中心的各物质的转化C CH4CuOFe3O4(1) (2) (5) H2CO3 (23) (21) (20)(22)(6) (7)2(8) (9) (17)(10) (11) Na2CO3 (14) (15) (16)(18)CaCO3 H2O2 CO物质之间转化关系的化学方程式:(1)2C + O2点燃 2CO(2)C + O2点燃 CO2 C + 2CuO 高温 2Cu + CO2↑ 3C+2Fe2O高温4Fe+3CO2↑(3)2CO + O2点燃 2CO2 3CO+Fe2O高温2Fe+3CO2 CO + CuO △ Cu + CO2(4)CO2 + C 高温 2CO(5)CH4+ 2O2点燃 CO2+ 2H2O(6)CO2 + H2O = H2CO3(7)H2CO3 = H2O + CO2↑(8)CO2 + 2NaOH = Na2CO₃ + H2O(9)Na2CO3 + H2SO4 = Na2SO4 + H₂O + CO₂↑ Na2CO3 + 2HCl = 2NaCl + H₂O + CO₂↑(10)CaCO3 + 2HCl = CaCl₂ + H₂O + CO₂↑ CaCO3 高温CaO + CO2↑(11)CO2 + Ca(OH)2 = CaCO3↓+ 2H2O(12)2H2O通电2H2↑+ O2↑(13)2H2 + O2点燃 2H2O 3H2 + Fe2O3高温 2Fe + 3H2O H2 + CuO 加热 Cu + H2O(14)2H2O2 MnO2 2H2O + O2↑(15)2H2O2 MnO2 2H2O + O2↑(16)O2 + 2C 点燃 2CO(17)CO 2 + C 高温 2CO(18)2CO + O 2 点燃 2CO 2(19)O 2 + C 点燃 CO 2(20)2O 2 + 3Fe 点燃 Fe 3O 4(21)O 2 + 2Cu △ 2CuO(22)Fe 2O 3 + 3CO 高温 2Fe + 3CO 2(23)CuO + H 2 加热 Cu + H 2O CuO + H 2SO 4 = CuSO 4 + H 2O2.以钙、铁元素为中心的各物质的转化CaCO 3 FeCl 3 Fe 3O 4(1) (2) (3) (14) (13) (12) (7) CaCl ₂ (6) CaO Fe(OH)FeCl 2(5) (4) (15) (16) (11) (9) Ca(OH)2 FeSO 4物质之间转化关系的化学方程式:(1)CaCO 3 + 2HCl = CaCl ₂ + H ₂O + CO ₂↑(2)CaCl 2 + Na 2CO 3 = CaCO 3↓+ 2NaCl CaCl 2 + K 2CO 3 = CaCO 3↓+ 2KCl(3)CaCO 3 高温CaO + CO 2↑(4)CaO + H 2O = Ca(OH)2(5)Ca(OH)2 + 2HCl = CaCl 2 + 2H 2O Ca(OH)2 + MgCl 2 = Mg(OH)2↓+ CaCl 2(6)Ca(OH)2 +CO 2=CaCO ₃↓+ 2H 2O Ca(OH)2 + Na 2CO 3 = CaCO 3↓+ 2NaOH Ca(OH)2 + K 2CO 3= CaCO 3↓+ 2KOH(7)3Fe + 2O 2 点燃 Fe 3O 4(8)Fe + 2HCl = FeCl 2 + H 2↑ Fe + CuCl 2 = FeCl 2 + Cu(9)Fe + H 2SO 4 = FeSO 4 + H 2↑ Fe + CuSO 4 = FeSO 4 + Cu(10)Fe 2O 3 + 3CO 高温 2Fe + 3CO 2 Fe 2O 3 + 3H 2 高温 2Fe + 3H 2O(11)Fe 2O 3 + 3H 2SO 4 = Fe 2(SO 4)3 + 3H 2O(12)Fe 2O 3 + 6HCl = 2FeCl 3 + 3H 2O(13)Fe(OH)3 + 3HCl = FeCl 3 + 3H 2O(14)FeCl 3 + 3NaOH = Fe(OH)3↓+ 3NaCl 2FeCl 3 + 3Ca(OH)2 = 2Fe(OH)3↓+ 3CaCl 2(15)2Fe(OH)3 + 3H 2SO 4 = Fe 2(SO 4)3 + 6H 2O(16)Fe 2(SO 4)3 + 6NaOH = 2Fe(OH)3↓+ 3Na 2SO 4 Fe 2(SO 4)3 + 3Ca(OH)2 = 2Fe(OH)3↓+3CaSO 43.以酸和碱为中心的知识网络酸碱指示剂CO2(2) (3) (4) (6) (7)Fe2O3 NaOH Na2CO3 H2SO4物质之间反应的化学方程式:(1)Fe + 2HCl = FeCl2 + H2↑(2)Fe2O3 + 6HCl = 2FeCl3 + 3H2O(3)HCl + NaOH = NaCl + H₂O(4)2HCl + Na2CO3 = 2NaCl + H₂O + CO₂↑(5)2HCl + Ca(OH)2 = CaCl2 + 2H2O(6)Ca(OH)2 + Na2CO3 = CaCO3↓ + 2NaOH(7)H2SO4 + Ca(OH)2 = CaSO4+ 2H2O(8)Ca(OH)2 + CO2 = CaCO3↓ + 2H2O4.以几种盐为中心的各物质的转化4 FeSO4物质之间转化关系的化学方程式:(1)CaCO3 + 2HCl = CaCl₂ + H₂O + CO₂↑ CaCO3 高温CaO + CO2↑(2)Na2CO3 + CaCl2 = CaCO3↓+ 2NaCl Na2CO3 + Ca(OH)2 = CaCO3↓ + 2NaOH (3)Na2CO3 + 2HCl= 2NaCl + H₂O + CO₂↑ Na2CO3 + H2SO4 = Na2SO4 + H₂O + CO₂↑(4)Na2CO3 + 2HCl= 2NaCl + H₂O + CO₂↑ Na2CO3 + CaCl2 = CaCO3↓+ 2NaCl(5)NaCl+ AgNO3 = AgCl↓ + NaNO3(6)AgNO3 + NaCl = AgCl↓ + NaNO3 AgNO3 + HCl = AgCl↓ + HNO3(7)BaCl2+ 2AgNO3 = 2AgCl↓ + Ba(NO3)2(8)BaCl2 + H2SO4 = BaSO4↓ + 2HCl BaCl2 + Na2SO4 =BaSO4↓ + 2NaCl(9)CuSO4 + Ba(OH)2 = Cu(OH)2↓+ BaSO4↓ CuSO4 + BaCl2 = CuCl2 + BaSO4↓(10)CuSO4 + Fe = FeSO4 + Cu(11)CuSO4 + 2NaOH = Cu(OH)2↓+ Na2SO4 CuSO4 + Ca(OH)2 = Cu(OH)2↓+ CaSO4二、推断突破口1.物质的颜色(1)固体物质的颜色白色固体:无水CuSO4、Mg0、P2O5、Ca0、Ca(OH)2、NaOH、 NaCl、Na2CO3等红色固体:Cu、Fe2O3等暗红色固体:红磷等绿色固体:Cu2(OH)2C03等淡黄色固体:S等黑色固体:C(木炭粉)、Cu0、MnO2、Fe3O4、Fe(粉)等紫黑色固体:KMnO4等(2)沉淀的颜色(七种常见沉淀)白色:BaSO4、AgCl、CaCO3、BaCO3、Mg(OH)2蓝色:Cu(OH)2红褐色:Fe(OH)3(3)溶液的颜色蓝色溶液:含Cu2+的溶液,如CuSO4溶液黄色溶液:含Fe3+的溶液,如FeCl3溶液浅绿色溶液:含Fe2+的溶液,如FeSO4溶液紫色溶液:KMnO4溶液、紫色石蕊试液(4)火焰的颜色淡蓝色火焰:CH4、H2、S在空气中燃烧发出淡蓝色火焰蓝色火焰:C0在空气中燃烧发出蓝色火焰蓝紫色火焰:S在纯氧中燃烧发出蓝紫色火焰2.物质的气味(1)有刺激性气味的气体:HCl、SO2、NH3等(2)无色无味的气体:O2、H2、N2、CO2、CH4、CO(剧毒)3.特殊反应条件(1)点燃:一般有O2参加反应(2)高温:主要有4个化学反应3CO+Fe2O高温2Fe+3CO2 CaCO3 高温CaO+CO2↑ CO2+C 高温 2CO C+2CuO高温2Cu+CO2↑(3)通电:主要有3个化学反应2H2O通电2H2↑+O2↑ 2Al2O通电4Al+3O2↑(4)催化剂:主要有2个反应2KCl + 3O2↑2H2O2 MnO22H2O+O2↑ 2KClO3MnO₂∆4.化学之最(1)地壳中含量最多的金属元素——铝(2)地壳中含量最多的非金属元素——氧(3)空气中含量最多的物质——氮气(4)最简单的有机物——CH4(5)相对分子质量最小的氧化物——水(6)相同条件下密度最小的气体——氢气(7)相对原子质量最小的原子——氢(8)组成化合物种类最多的元素——碳(9)日常生活中应用最广泛的金属——铁(10)最早使用的金属——铜5.反应的特征现象化学反应的特征现象有:“带火星的木条复燃”、“火星四射”、“澄清石灰水变浑浊”、“物质溶于水温度升高或降低”、“无水硫酸铜变蓝”等模拟预测1. A、B、C是三种初中阶段常见的三种物质,它们之间的反应及转化关系如图所示,(箭头表示转化,横线表示反应),已知B与另外两种物质的元素种类均不相同。
专题3 八圈图及物质的转化1一、单质、氧化物、酸、碱、盐的相互反应1、金属+氧气→碱性氧化物如:2、碱性氧化物+水→可溶性碱(不溶性碱除外)如:3、不容性碱→碱性氧化物(可溶性碱除外)+水如:4、酸+盐→盐+水5、非金属+ O2→酸性氧化物(H2燃烧、C不完全燃烧等除外)如:6、酸性氧化物+水→含氧酸(二氧化硅除外)如:7、含氧酸→酸性氧化物+水如:8、金属+非金属(除O2、H2外)→无氧酸盐如:9、碱性氧化物+酸性氧化物→含氧酸盐如:10、不容性盐→碱性氧化物+酸性氧化物如:11、盐1+盐2→盐3+盐412、碱性氧化物+酸→盐+水13、酸性氧化物+碱→盐+水14、酸+盐→新酸+新盐15、碱+盐→新碱+新盐16、金属+酸→盐+ H217、金属+盐溶液→新金属+新盐溶液1、一定条件下,下列物质的转化均可一步实现的是()A.CaCl2→CaCO3→Ca(OH)2 B. AgNO3→Fe(NO3)2→Zn(NO3)2C. NaNO3→NaOH→Na2CO3D. Fe2O3→FeSO4→Fe(OH)32、下列物质间的转化,在一定条件下均能一步实现的是①C→CO→CO2 ②Cu→CuO→CuSO4 ③Na2CO3→NaCl→NaNO3 ④CaCO3→CaO→Ca(OH)2 A.①②③B.①③④C.①②④ D.①②③④3、下列物之间的转化,能通过一步反应实现的是( )①C2H5OH→CO2②CaO→Ca(OH)2③H2O2→H2O④HNO3→HCl⑤Fe3O4→Fe A.①②③④ B.①②③⑤ C.①③④⑤ D.②③④⑤4、下列物质间的每一转化不能..都通过一步反应实现的是()A.CuO→Cu→CuO B.NaOH→H2O→NaOH C.O2→Fe3O4→O2D.Fe→FeCl2→Fe5、下列物质间的每一转化不能都通过一步反应实现的是()A.Ca→CaO→CaCl2B.NaOH→Na2CO3→NaClC.O2→CuO→Cu(OH)2D.C→CO2→Na2CO36、下列转化能一步完成的()① CH4→CO2 ②HNO3→HCl ③CaO→Ca(OH)2 ④Ba(OH)2→NaOH ⑤C→CuA.①③④⑤ B.②③④⑤ C.①②④⑤ D.①②③④7、下列转化能一步完成的是()①CaCO3→CO2②HCl→NaCl③CaO→Ca(OH)2④Ca(OH)2→NaOH⑤CuO→Cu.A.①②③④⑤B.②③④⑤C.①②④⑤D.①②③④8、下列转化能一步完成的是()①Ba(OH)2→NaOH②CuO→Cu(OH)2 ③HNO3→HCl④SO2→Na2SO3.A.①④ B.②③ C.③④ D.只有④9、下列物质之间的转化能够实现的是()10、下列物质间的转化关系正确的是()A.①②B.②③ C.①③ D.①②③【类型2】1、现有Fe、CuO、MgCl2、Ca(OH)2、稀H2SO4等五种物质,在常温下它们两两相互发生的化学反应有()A.7个B.6个C.5个D.4个2、现有氧化铁、稀硫酸、氢氧化钠溶液、氯化钡溶液和碳酸钾溶液五种物质,在常温下它们两两相互发生的化学反应有()A.4个B.5个C.6个D.7个3、现有Zn、Fe2O3、MgCl2、Cu(OH)2、稀H2SO4等五种物质,在常温下它们两两相互发生的化学反应有()A.3个B.4个C.5个D.6个4、对于化学反应X + Na2CO3 == 2Y+ CaCO3↓的分析错误的是()A.该反应属于复分解反应B.Y中一定含有钠元素C.X一定是熟石灰D.X中阴离子化合价是—1价5、对于复分解反应:X+2NaOH2Y+Cu(OH)2↓,下列分析中正确的是()A.X一定是CuCl2B.相对分子质量大小:X>Y C.Y可能是H2O D.Y可能是Na2SO4【类型3】1、下列各组变化中,每一转化在一定条件下均能一步实现的是()A.①和② B.②和③ C.①和③ D.①②③2、下列各组物质间通过一步反应就能实现如图所示的转化,则甲、乙、丙可能分别是()A.NaOH、NaCl、NaNO3B.CO、CO2、H2 CO3C.CaO、Ca(OH)2、CaCO3D.H2O2、H2O、O23、(2013•徐州一模)下列各组中物质间的转化不都是通过一步反应实现的是()4、下列各组物质间通过一步反应就能实现如右图转化,则甲、乙、丙可能是()A.KOH KCl KNO3B.CuO CuCl2Cu(OH)2C.C CO2COD.H2O2H2O O25、(2014·宿迁)下列物质的三角转化关系中都能按箭头方向一步实现的是( )A.① B.①② C.①②③ D.②③6、下列各组转化中,一定条件下均能一步实现的组合是()A.①②B.②③C.①③D.①②③专题3 八圈图及物质的转化2【类型3】7、下列有关说法正确的是( ) A .实现CO CO 2的相互转化,都只有一种途径B .Al 可以实现单质氧化物碱C .实现C CO 的转化,都利用了碳的可燃性D .实现H 2OO 2相互转化,化学反应的基本类型不同8、比较归纳是化学学习中常用的一种方法.以下是C 、CH 4、CO 三种物质转化为CO 2的转化关系,即:①C→CO 2②CH 4→CO 2③CO→CO 2,对它们的比较归纳正确的是( )A .三种转化发生的都是化合反应B .三种物质都只能跟氧气反应转化为二氧化碳C .三种物质都可以在点燃条件下转化为二氧化碳D .三种转化所有的生成物在常温下都是气体 9、(2014黄冈市)已知甲、乙、丙、丁是初中化学中的四种常见物质,丁是甲与乙、乙与丙反应的生成物之一(反应条件均已略去),转化关系如图:(1)常温下,若乙为红色粉末,甲为黑色粉末,则丙的化学式是______,甲与乙反应的化学方程式为______。