实验二十四第一过渡系元素二铁钴镍
- 格式:ppt
- 大小:2.59 MB
- 文档页数:19
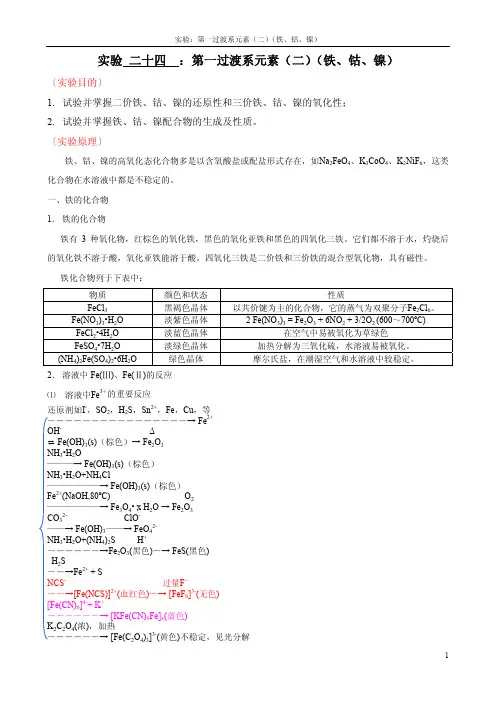
实验二十四:第一过渡系元素(二)(铁、钴、镍)〔实验目的〕1.试验并掌握二价铁、钴、镍的还原性和三价铁、钴、镍的氧化性;2.试验并掌握铁、钴、镍配合物的生成及性质。
〔实验原理〕铁、钴、镍的高氧化态化合物多是以含氧酸盐或配盐形式存在,如Na2FeO4、K3CoO4、K2NiF6,这类化合物在水溶液中都是不稳定的。
一、铁的化合物1.铁的化合物铁有3种氧化物,红棕色的氧化铁,黑色的氧化亚铁和黑色的四氧化三铁。
它们都不溶于水,灼烧后的氧化铁不溶于酸,氧化亚铁能溶于酸。
四氧化三铁是二价铁和三价铁的混合型氧化物,具有磁性。
铁化合物列于下表中:物质颜色和状态性质FeCl3黑褐色晶体以共价键为主的化合物,它的蒸气为双聚分子Fe2Cl6。
Fe(NO3)3 = Fe2O3 + 6NO2 + 3/2O2 (600~700ºC) Fe(NO3)3•H2O 淡紫色晶体 2FeCl2•4H2O 淡蓝色晶体在空气中易被氧化为草绿色FeSO4•7H2O 淡绿色晶体加热分解为三氧化硫,水溶液易被氧化。
(NH4)2Fe(SO4)2•6H2O 绿色晶体摩尔氏盐,在潮湿空气和水溶液中较稳定。
2.溶液中Fe(Ⅲ)、Fe(Ⅱ)的反应⑴溶液中Fe3+的重要反应还原剂如I-,SO2,H2S,Sn2+,Fe,Cu,等――――――――――――――――→ Fe2+OH-Δ⇌ Fe(OH)3(s)(棕色)→ Fe2O3NH3•H2O———→ Fe(OH)3(s)(棕色)NH3•H2O+NH4Cl——————→ Fe(OH)3(s)(棕色)Fe2+(NaOH,80ºC) O2——————→ Fe3O4• x H2O → Fe2O3CO32-ClO-——→ Fe(OH)3——→ FeO42-NH3•H2O+(NH4)2S H+――――――→Fe2O3(黑色)―→ FeS(黑色)H2S――→Fe2+ + SNCS-过量F-――→[Fe(NCS)]2+(血红色)―→ [FeF6]3-(无色)[Fe(CN)6]4-+ K+――――――→ [KFe(CN)6Fe]x(蓝色)K2C2O4(浓),加热――――――→ [Fe(C2O4)3]3-(黄色)不稳定,见光分解⑵溶液中Fe2+的重要反应氧化剂如Cr2O72-,浓HNO3等―――――――――――→ Fe3+OH-O2⇌ Fe(OH)2(s)(纯白色)→Fe(OH)3(s)(棕色)NH3•H2O――→ Fe(OH)2(s)(纯白色)NH3•H2O+NH4Cl――――――→无沉淀CO32-H2O + CO2 O2――→ FeCO3(白色)――→ Fe(HCO3)2―→Fe(OH)3(s)(NH4)2S―――→ FeS(黑色)NO――→[Fe(NO)( H2O)5]2+( 棕色)H2O2 +过量F-―――――→ [FeF6]3-(无色)NCS-――→无溶液、无颜色CN-过量CN-Cl2―→Fe(CN)2(s) (白色) ――→[Fe(CN)6]4-――→[Fe(CN)6]3-[Fe(CN)6]3-+ K+――――――→ [KFe(CN)6Fe]x(蓝色)二、钴的化合物1. 钴的化合物钴的氧化物与铁的氧化物类似,为暗褐色的Co2O3•xH2O和灰绿色的CoO。

d区金属元素(铬、锰、铁、钴、镍)一、实验目的1. 试验并掌握铬、锰主要氧化态化合物的重要性质及各氧化态之间相互转化的条件。
2. 试验并掌握二价铁、钴、镍的还原性和三价铁、钴、镍的氧化性。
3. 试验并掌握铁、钴、镍的配合物的生成及性质。
二、实验原理位于周期表中第四周期的Sc~Ni称为第一过渡系元素,第一过渡系元素铬、锰、铁、钴、镍是最常见的重要元素。
铬为周期表中ⅥB族元素,最常见的是+3和+6氧化态的化合物。
+3价铬盐容易水解,其氢氧化物呈两性,碱性溶液中的 +3价氧化态铬以CrO2-形式存在,易被强氧化剂如Na2O2或H2O2氧化为黄色的铬酸盐。
2 CrO2- +3 H2O2 + 2 OH-CrO42- +4 H2O常见+6价氧化态的铬化合物是铬酸盐和重铬酸盐,它们的水溶液中存在着下列平衡:2 CrO42- + 2 H+Cr2O72- + H2O除了加酸、加碱条件下可使上述平衡发生移动外,向Cr2O72-溶液中加入Ba2+、Ag+、Pb2+离子时,根据平衡移动规则,可得到铬酸盐沉淀。
2 Ba2+ + Cr2O72- + H2O BaCrO4↓(柠橙黄色) + 2 H+4 Ag+ + Cr2O72- + H2O Ag2CrO4↓(砖红色) + 2 H+2 Pb2+ + Cr2O72- + H2O PbCrO4↓(铬黄色) + 2 H+重铬酸盐是强氧化剂,易被还原成+3价铬(Cr3+溶液为绿色或蓝色)。
锰为周期表ⅦB族元素,最常见的是+2、+4、+7氧化态的化合物。
+2价态锰化合物在碱性介质中形成Mn(OH)2。
Mn(OH)2为白色碱性氢氧化物,溶于酸及酸性盐溶液中,在空气中易被氧化,逐渐变成棕色MnO2的水合物[MnO(OH)2]。
4 Mn(OH)2 + O MnO(OH)2(褐色) + 2 H2O+2价态锰化合物在酸性介质中比较稳定,与强氧化剂(如NaBiO3、PbO2、S2O82-等)作用时,可生成紫红色MnO4-离子,这个反应常用来鉴别Mn2+。

第一过渡元素实验报告第一过渡元素实验报告引言:过渡元素是化学中一类重要的元素,它们的特性和性质对于我们理解化学反应和物质变化起着关键的作用。
本实验旨在通过实际操作和观察,探究第一过渡元素的一些性质和反应。
实验材料与方法:1. 实验材料:- 铜片- 锌片- 镁片- 铁片- 镍片- 铬片- 锰片- 钛片- 锂片- 钾片- 盐酸- 硫酸- 纸巾- 试管- 火柴2. 实验方法:1) 将实验材料准备齐全,并按照实验步骤依次进行实验。
2) 将每种过渡元素片放入不同的试管中,注意标记。
3) 分别将盐酸和硫酸倒入不同的试管中,观察反应情况。
4) 使用火柴点燃每种过渡元素片,观察燃烧现象。
实验结果与讨论:1. 盐酸和硫酸反应:在盐酸中,铜片发生了气泡的产生,同时溶液颜色变为浅蓝色。
而锌片、镁片和铁片则产生了更多的气泡,且溶液颜色变为无色。
这表明铜和锌、镁、铁之间具有不同的反应性,铜的反应性较低。
在硫酸中,铜片同样发生了气泡的产生,但溶液颜色变为深蓝色。
而锌片、镁片和铁片则产生了更多的气泡,且溶液颜色变为无色。
这表明铜和锌、镁、铁之间在硫酸中的反应性也存在差异,但与盐酸反应性的差异不同。
2. 燃烧现象:铜片在点燃后迅速燃烧,产生了明亮的火焰和黑色的氧化铜。
锌片、镁片和铁片也发生了燃烧,但火焰较铜片暗淡,且产生了不同颜色的氧化物。
这表明不同过渡元素在燃烧时产生的反应产物和火焰特性也存在差异。
结论:通过本实验,我们观察到了第一过渡元素的一些性质和反应。
在盐酸和硫酸中,铜与锌、镁、铁之间的反应性不同,且硫酸中的反应性差异与盐酸有所不同。
此外,不同过渡元素在燃烧时产生的反应产物和火焰特性也存在差异。
这些观察结果与过渡元素的电子结构和周期表上的位置密切相关。
过渡元素具有不完全填充的d轨道,因此它们的化学性质与其他元素有所不同。
其反应性和燃烧特性的差异可以归因于元素之间的电子转移和氧化还原反应。
本实验只涉及了第一过渡元素的一些基本性质和反应,对于进一步研究和理解过渡元素的化学行为仍有待深入探索。

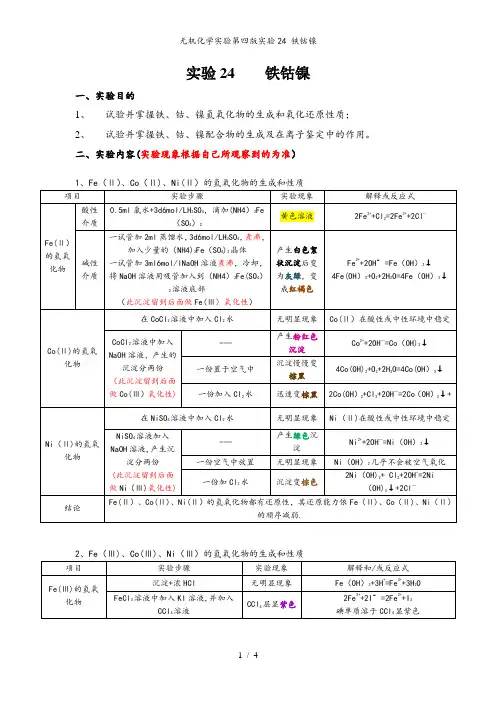
实验24 铁钴镍一、实验目的1、试验并掌握铁、钴、镍氢氧化物的生成和氧化还原性质;2、试验并掌握铁、钴、镍配合物的生成及在离子鉴定中的作用。
二、实验内容(实验现象根据自己所观察到的为准)三、实验讨论(从自己实验操作展开)四、实验思考题和习题1。
实验步骤(2)要求整个实验不能带入空气到溶液中,为什么?Fe(Ⅱ)易被氧化,如若带入了空气,可能不能观察到颜色的转化过程。
2.根据实验现象总结+2价的铁、钴、镍化合物的还原性和+3价的铁钴镍化合物氧化性的变化规律。
Fe(Ⅱ)、Co(Ⅱ)、Ni(Ⅱ)的氢氧化物都有还原性,其还原能力依Fe(Ⅱ)、Co(Ⅱ)、Ni(Ⅱ)的顺序减弱。
Fe(Ⅲ)、Co(Ⅲ)、Ni(Ⅲ)在酸性介质中的氧化能力依Fe(Ⅲ)、Co(Ⅲ)、Ni(Ⅲ)的顺序增加。
3。
比较钴镍氨配合物的氧化还原性相对大小及溶液稳定性。
钴盐和镍盐生成碱式盐溶于过量的氨水生成氨配合物,Co(Ⅱ)氨配合物易氧化转化成 Co(Ⅲ)氨配合物。
即镍盐更稳定.4。
为什么制取+3价的钴镍氢氧化物要用+2价为原料在碱性条件下进行氧化,而不+3价直接制取?首先,作为最高价氧化值,Co3+、Ni3+氧化性比较不稳定,易变成其它价态,故不用采用+3价直接氧化得到。
其次,而Co(OH)2、Ni(OH)2两性,在碱性条件下易被氧化成+3价氢氧化物。
5。
如何分离混合液中的?Fe3+、Cr3+、Ni2+ ?6.总结Fe(Ⅱ、Ⅲ)、Co(Ⅱ、Ⅲ)、Ni(Ⅱ、Ⅲ)主要化合物性质。
Fe(Ⅱ)、Co(Ⅱ)、Ni(Ⅱ)具有强的还原性,都易形成配合物,且Co的配合物极易被氧化,它们的氢氧化物也易被氧化;Fe(Ⅲ)、Co(Ⅲ)、Ni(Ⅲ)具有强的氧化性,也易生成配合物。
7。
(此题面字太多,不好打得,请谅解)A:(NH4)2Fe (SO4)2B:(NH4)2Fe (SO4)2溶液C:Fe(OH)2D:NH3E:I2F:Fe3+G:KFe[Fe(CN)6]H:BaSO4这些方程式都是简单的,都可以轻易写出,在此我不一一写出了。

实验24 第一过渡系元素(铬、锰、铁、钴、镍)一、实验目的掌握铬、锰主要氧化态的化合物的重要性质及各氧化态之间相互转化的条件。
掌握铁、钴、镍的氢氧化物及配合物的生成和性质。
掌握铁盐的性质。
学习Fe2+、、Fe3+和Ni2+的鉴定方法。
二、实验前应思考的问题1.转化反应须在何种介质(酸性或碱性)中进行?为什么?2.从电势值和还原剂被氧化后产物的颜色考虑,选择哪些还原剂为宜?如果选择亚硝酸钠溶液可以吗?3.转化反应须在何种介质中进行?为什么?4.从电势值和氧化剂被还原后产物的颜色考虑,应选择哪些氧化剂?3%H2O2溶液可用否?三、实验用品仪器:试管、台秤、沙浴皿、蒸发皿、试管、离心试管、烧杯、玻璃棒、滴管、点滴板、酒精灯固体药品:二氧化锰、亚硫酸钠、高锰酸钾、FeSO4·7H2O、KCl、NH4Cl液体药品:H2SO4(浓,1 mol·L-1),H2O2(3%)、NaOH(40%,6 mol·L-1,2 mol·L-1,0.1 mol·L-1),CuCl2(0.2 mol·L-1)、HCl(浓,6 mol·L-1,2 mol·L-1,0.1 mol·L-1)、H2SO4(2 mol·L-1)、HAc(2 mol·L-1)、NH3·H2O(浓)、K2SO4·Cr2(SO4)3·24H2O(0.2 mol·L-1)、NH3·H2O(2 mol·L-1)、K2Cr2O7(0.1 mol·L-1)、FeSO4(0.5 mol·L-1)、K2CrO4(0.1 mol·L-1)、AgNO3(0.1 mol·L-1)、BaCl2(0.1 mol·L-1)、Pb(NO3)2(0.1 mol·L-1)、MnSO4(0.2 mol·L-1,0.5 mol·L-1)、NH4C1(2 mol·L-1 )、NaClO(稀)、H2S(饱和)、Na2S(0.1 mol·L-1、0.5 mol·L-1),KMnO4(0.1 mol·L-1)、Na2SO3(0.1 mol·L-1)、K4[Fe(CN)6] (0.1 mol·L-1)、K3[Fe(CN)6] (0.1 mol·L-1)、CoCl2(0.1 mol·L-1)、NiSO4(0.1 mol·L-1)、FeCl3(0.1 mol·L-1)、KI(0.1 mol·L-1)、Na2CO3(0.1 mol·L-1)、KMnO4(0.1 mol·L-1)MnSO4(0.1 mol·L-1)、CrCl3(0.1 mol·L-1)、NH4F(1 mol·L-1)、NH4Cl(1 mol·L-1)、KSCN(0.1 mol·L-1、25%)、Pb(Ac)2(0.5 mol·L-1)、KNO2(饱和)溴水、淀粉溶液、二乙酰二肟(1%)、H2O2(3%)、滤纸、淀粉KI试纸、邻菲罗啉、戊醇材料:pH试纸、沸石四、实验内容1 铬的化合物的重要性质⑴铬(Ⅵ)的氧化性Cr2O72-转变为Cr3+。
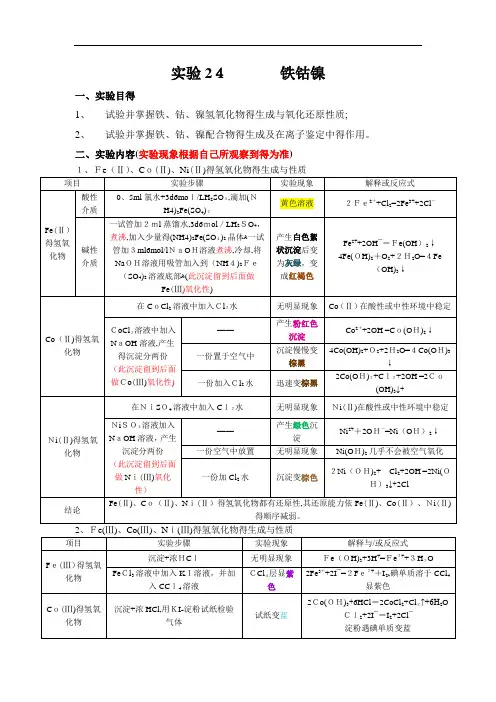
实验24铁钴镍一、实验目得1、试验并掌握铁、钴、镍氢氧化物得生成与氧化还原性质;2、试验并掌握铁、钴、镍配合物得生成及在离子鉴定中得作用。
二、实验内容(实验现象根据自己所观察到得为准)三、实验讨论(从自己实验操作展开) 四、实验思考题与习题1、实验步骤(2)要求整个实验不能带入空气到溶液中,为什么?F e(Ⅱ)易被氧化,如若带入了空气,可能不能观察到颜色得转化过程。
2.根据实验现象总结+2价得铁、钴、镍化合物得还原性与+3价得铁钴镍化合物氧化性得变化规律。
Fe (Ⅱ)、Co (Ⅱ)、Ni(Ⅱ)得氢氧化物都有还原性,其还原能力依Fe (Ⅱ)、Co (Ⅱ)、Ni (Ⅱ)得顺序减弱。
Fe(Ⅲ)、Co(Ⅲ)、Ni (Ⅲ)在酸性介质中得氧化能力依Fe(Ⅲ)、Co(Ⅲ)、Ni(Ⅲ)得顺序增加。
3、比较钴镍氨配合物得氧化还原性相对大小及溶液稳定性。
钴盐与镍盐生成碱式盐溶于过量得氨水生成氨配合物,Co(Ⅱ)氨配合物易氧化转化成 Co (Ⅲ)氨配合物。
即镍盐更稳定。
4、为什么制取+3价得钴镍氢氧化物要用+2价为原料在碱性条件下进行氧化,而不+3价直接制取?首先,作为最高价氧化值,Co 3+、Ni 3+氧化性比较不稳定,易变成其它价态,故不用采用+3价直接氧化得到。
其次,而C o(OH)2、Ni(OH)2两性,在碱性条件下易被氧化成+3价氢氧化物。
53+3+2+ﻩ6.配合物极易被氧化,它们得氢氧化物也易被氧化;Fe(Ⅲ)、Co(Ⅲ)、Ni(Ⅲ)具有强得氧化性,也易生成配合物。
7、(此题面字太多,不好打得,请谅解)A:(NH4)2Fe (SO4)2B:(NH4)2Fe(SO4)2溶液C:Fe(OH)2D:NH3E:I2F:Fe3+G:KFe[Fe(CN)6]H:BaSO4这些方程式都就是简单得,都可以轻易写出,在此我不一一写出了。

第一过渡元素二铁钴镍实验报告一、引言二铁钴镍合金是一种重要的金属材料,具有高强度、高韧性、高温稳定性等优点,被广泛应用于航空、航天、汽车等领域。
本实验旨在制备二铁钴镍合金,并研究过渡元素对合金性能的影响。
二、实验方法1.实验材料:铁、钴、镍粉末。
2.实验设备:熔融法制备设备、高温炉、电子显微镜、扫描电子显微镜等。
3.实验步骤:(1)将铁、钴、镍粉末按一定比例混合均匀。
(2)将混合粉末放入熔融法制备设备中,在氩气氛围下进行熔融处理,保持温度为1650℃,时间为2h,使其充分熔融混合。
(3)将熔融合金放入高温炉中,在氩气氛围下进行加热处理,升温速度为5℃/min,将温度升至1000℃保持10h,随后降温处理。
(4)用电子显微镜和扫描电子显微镜对制备的二铁钴镍合金进行形貌和组织结构分析。
三、实验结果经过制备和分析,得到的二铁钴镍合金的形貌和组织结构如下:1.形貌分析:合金表面呈灰黑色,略带光泽,无氧化现象,颗粒较细。
2.组织结构分析:经电子显微镜观察,发现合金中含有大量的球形和棒状的晶粒,晶粒大小约为1-10μm。
通过扫描电子显微镜,发现晶界清晰,无明显的孔洞、裂纹等缺陷。
四、实验分析二铁钴镍合金是由铁、钴、镍三种金属元素组成,其中铁为主要成分,钴和镍是过渡元素。
过渡元素的添加对合金的性能有重要的影响。
实验结果表明,制备的二铁钴镍合金表面光泽度高,无氧化现象,晶粒分布均匀,晶界清晰。
这表明合金制备工艺优良,达到了预期的效果。
钴和镍的添加可以提高二铁钴镍合金的热稳定性和耐腐蚀性,同时对其力学性能和磁性能也有影响。
在合金中添加适量的过渡元素,可以调节晶粒尺寸、组织结构和晶格畸变等因素,从而优化合金的性能。
五、结论本实验成功制备了二铁钴镍合金,并对其形貌和组织结构进行了分析。
实验结果表明,过渡元素的添加可以调节合金的性能,优化其力学性能和磁性能等。
通过本实验的研究,对二铁钴镍合金的制备和性能分析有了更加深入的认识,为进一步研究和应用该材料奠定了基础。


无机化学实验第四版实验24铁钴镍(总4页)--本页仅作为文档封面,使用时请直接删除即可----内页可以根据需求调整合适字体及大小--实验24 铁钴镍一、实验目的1、试验并掌握铁、钴、镍氢氧化物的生成和氧化还原性质;2、试验并掌握铁、钴、镍配合物的生成及在离子鉴定中的作用。
二、实验内容(实验现象根据自己所观察到的为准)三、实验讨论(从自己实验操作展开)四、实验思考题和习题1.实验步骤(2)要求整个实验不能带入空气到溶液中,为什么?Fe(Ⅱ)易被氧化,如若带入了空气,可能不能观察到颜色的转化过程。
2.根据实验现象总结+2价的铁、钴、镍化合物的还原性和+3价的铁钴镍化合物氧化性的变化规律。
Fe(Ⅱ)、Co(Ⅱ)、Ni(Ⅱ)的氢氧化物都有还原性,其还原能力依Fe(Ⅱ)、Co(Ⅱ)、Ni(Ⅱ)的顺序减弱。
Fe(Ⅲ)、Co(Ⅲ)、Ni(Ⅲ)在酸性介质中的氧化能力依Fe(Ⅲ)、Co(Ⅲ)、Ni(Ⅲ)的顺序增加。
3.比较钴镍氨配合物的氧化还原性相对大小及溶液稳定性。
钴盐和镍盐生成碱式盐溶于过量的氨水生成氨配合物,Co(Ⅱ)氨配合物易氧化转化成 Co(Ⅲ)氨配合物。
即镍盐更稳定。
4.为什么制取+3价的钴镍氢氧化物要用+2价为原料在碱性条件下进行氧化,而不+3价直接制取?首先,作为最高价氧化值,Co3+、Ni3+氧化性比较不稳定,易变成其它价态,故不用采用+3价直接氧化得到。
其次,而Co(OH)2、Ni(OH)2两性,在碱性条件下易被氧化成+3价氢氧化物。
5.如何分离混合液中的?Fe3+、Cr3+2+6.总结Fe(Ⅱ、Ⅲ)、Co(Ⅱ、Ⅲ)、Ni(Ⅱ、Ⅲ)主要化合物性质。
Fe(Ⅱ)、Co(Ⅱ)、Ni(Ⅱ)具有强的还原性,都易形成配合物,且Co的配合物极易被氧化,它们的氢氧化物也易被氧化;Fe(Ⅲ)、Co(Ⅲ)、Ni(Ⅲ)具有强的氧化性,也易生成配合物。
7.(此题面字太多,不好打得,请谅解)A:(NH4)2Fe (SO4)2B:(NH4)2Fe (SO4)2溶液C:Fe(OH)2D:NH3E:I2F:Fe3+G:KFe[Fe(CN)6]H:BaSO4这些方程式都是简单的,都可以轻易写出,在此我不一一写出了。

第过渡系元素实验报告一、实验目的本次实验旨在深入研究第过渡系元素的物理性质、化学性质以及它们在不同反应中的表现,通过实验操作和观察,增强对第过渡系元素特性的理解和掌握。
二、实验原理第过渡系元素包括钛(Ti)、钒(V)、铬(Cr)、锰(Mn)、铁(Fe)、钴(Co)、镍(Ni)、铜(Cu)和锌(Zn)。
这些元素在电子构型、氧化态和化学性质上具有一定的规律性和特殊性。
例如,钛具有较强的耐腐蚀性,常用于航空航天领域;钒在钢铁工业中可提高钢材的强度;铬能形成多种氧化态,其化合物在电镀和颜料制造中有广泛应用;锰在催化剂和电池材料中起着重要作用;铁是生物体必需的元素,也是钢铁生产的主要原料;钴常用于催化剂和电池;镍在不锈钢制造中不可或缺;铜具有良好的导电性和导热性;锌则在防腐和电池制造方面有重要用途。
在化学反应中,这些元素的氧化还原性质、配合物形成能力以及与不同试剂的反应特性是研究的重点。
三、实验仪器与试剂(一)实验仪器电子天平、容量瓶、移液管、酸式滴定管、碱式滴定管、锥形瓶、烧杯、玻璃棒、酒精灯、蒸发皿、坩埚、铁架台、石棉网、pH 计等。
(二)实验试剂钛(IV)盐溶液、钒(V)盐溶液、铬(III)盐溶液、铬(VI)盐溶液、锰(II)盐溶液、铁(II)盐溶液、铁(III)盐溶液、钴(II)盐溶液、镍(II)盐溶液、铜(II)盐溶液、锌(II)盐溶液、硫酸、盐酸、硝酸、氢氧化钠溶液、氨水、氯化铵溶液、过氧化氢溶液、碘化钾溶液、硫氰酸钾溶液、高锰酸钾溶液、重铬酸钾溶液等。
四、实验步骤(一)钛(Ti)的实验1、取少量钛(IV)盐溶液,加入氢氧化钠溶液,观察沉淀的生成及颜色。
2、向上述沉淀中加入过量的盐酸,观察沉淀的溶解情况。
(二)钒(V)的实验1、取适量钒(V)盐溶液,加入硫酸酸化,然后滴加高锰酸钾溶液,观察溶液颜色的变化。
2、向钒(V)盐溶液中加入氢氧化钠溶液,调节 pH 值,观察沉淀的生成和颜色。
(三)铬(Cr)的实验1、铬(III)的性质取少量铬(III)盐溶液,加入氢氧化钠溶液,观察沉淀的生成及颜色。
第1篇一、实验目的本次实验旨在通过一系列化学反应和物理实验,研究铁、钴、镍三种金属的性质,包括它们的还原性、氧化性、配合物生成以及磁性等。
通过对比实验结果,加深对这三种金属化学性质的理解。
二、实验原理1. 还原性:在还原反应中,金属原子失去电子,氧化态降低。
铁、钴、镍在酸性或碱性介质中表现出不同的还原性。
2. 氧化性:在氧化反应中,金属原子获得电子,氧化态升高。
铁、钴、镍的三价离子具有氧化性。
3. 配合物生成:金属离子与配体形成配合物,配体提供孤对电子与金属离子配位。
4. 磁性:铁、钴、镍为铁磁性材料,其磁性能受温度、磁场等因素影响。
三、实验内容1. 还原性实验(1)铁(II)的还原性:在酸性介质中,铁(II)具有还原性,可还原溴水中的溴离子。
实验结果显示,加入(NH4)2Fe(SO4)2溶液后,溶液颜色由黄色变为棕色,说明铁(II)具有还原性。
(2)钴(II)和镍(II)的还原性:在酸性介质中,钴(II)和镍(II)的还原性较弱,氯水不能将它们氧化。
实验结果显示,加入氯水后,溶液颜色无变化,说明钴(II)和镍(II)的还原性较弱。
2. 氧化性实验(1)三价铁的氧化性:在碱性介质中,三价铁具有氧化性,可将亚铁离子氧化为铁离子。
实验结果显示,加入氯水后,溶液颜色由浅绿色变为棕色,说明三价铁具有氧化性。
(2)三价钴和三价镍的氧化性:在碱性介质中,三价钴和三价镍具有氧化性,可被还原为二价离子。
实验结果显示,加入NaOH溶液后,溶液颜色由浅绿色变为蓝绿色,说明三价钴具有氧化性;加入氯水后,溶液颜色由蓝绿色变为棕色,说明三价钴具有氧化性。
3. 配合物生成实验(1)铁(II)配合物:在氨水存在下,铁(II)难以形成稳定的氨配合物。
实验结果显示,加入氨水后,溶液中出现白色沉淀,说明铁(II)难以形成稳定的氨配合物。
(2)钴(II)和镍(II)配合物:在氨水存在下,钴(II)和镍(II)可形成稳定的氨配合物。
实验结果显示,加入氨水后,溶液颜色由浅绿色变为深蓝色,说明钴(II)和镍(II)与氨形成了稳定的配合物。
过渡元素实验报告过渡元素实验报告引言:过渡元素是化学中的一类重要元素,它们的特性在化学反应和物质性质中起着关键作用。
本次实验旨在通过对过渡元素进行一系列实验,探索它们的性质和应用。
实验一:钴的催化作用钴是一种重要的过渡元素,具有良好的催化性能。
我们通过将钴粉加入氢氧化钠溶液中,观察其对过氧化氢的催化作用。
实验结果显示,加入钴粉后,过氧化氢迅速分解,产生氧气气泡。
这表明钴具有催化剂的作用,能够加速氧化反应的进行。
这一性质使得钴在工业上广泛应用于催化剂的制备。
实验二:铁的氧化反应铁是一种常见的过渡元素,在氧气存在下容易发生氧化反应。
我们将铁片暴露在空气中,观察其表面是否会出现锈迹。
实验结果显示,经过一段时间后,铁片表面出现了红棕色的锈迹。
这是由于铁与氧气反应生成了氧化铁。
这一反应对于铁的腐蚀有着重要的意义,并且在工程材料的选择中需要考虑到铁的抗氧化性。
实验三:镍的电化学性质镍是一种广泛应用于电池中的过渡元素。
我们通过将镍丝浸泡在硫酸镍溶液中,观察其在电解质中的电化学性质。
实验结果显示,镍丝在电解质中发生了氧化反应,同时释放出电子。
这表明镍具有良好的电导性和电化学稳定性,适合用于电池的制备。
实验四:铬的颜色变化铬是一种过渡元素,具有多种氧化态。
我们通过在硫酸铬溶液中加入不同浓度的硫酸,观察其颜色的变化。
实验结果显示,当硫酸浓度较低时,溶液呈现出绿色;而当硫酸浓度较高时,溶液呈现出橙红色。
这是由于铬在不同氧化态下具有不同的颜色。
这一性质使得铬在化妆品和染料工业中有着广泛的应用。
结论:通过本次实验,我们对过渡元素的性质和应用有了更深入的了解。
钴具有良好的催化性能,铁容易发生氧化反应,镍适合用于电池制备,而铬在不同氧化态下呈现不同的颜色。
这些性质和应用使得过渡元素在化学和工业领域中具有重要的地位。
通过进一步的研究和实验,我们可以进一步挖掘过渡元素的潜力,为科学和技术的发展做出更大的贡献。
第一过度系元素实验报告
实验目的:
1. 通过电热直接还原法制备第一过渡系元素钨。
2. 通过物理方法分离纯钨。
实验原理:
钨加热至高温时,可以被还原成钨粉末。
这是因为钨金属的氧化还原平衡是比较倾向于氧化态的,但是在高温下可以大幅度地增加还原产物的热力学稳定性,使得钨可以被还原成钨粉末。
实验步骤:
1. 准备物品:纯的钨三氧化物、使用纵向电炉的直径足够大、电子天平、研钵、亚硝酸钠、树脂盆,水槽、铁钳、过滤棉。
2. 秤出约1克的钨三氧化物,用研钵将它细磨,至于研钵上有很少或没有粉末剩余。
3. 将粉末放置于树脂盆的底部上。
4. 在电子天平上称出0.2-0.4克的亚硝酸钠,加入足够的水后,将其倒在树脂盆中的钨三氧化物粉末上。
5. 铁钳将树脂盆放入选定的直径足够大的电子天平中,接通电源进行实验(注意使用保护设备)。
6. 实验结束,将剩余的亚硝酸钠溶液倒入水槽中进行处理;将树脂盆从电子天平中取出,拿出滤纸过滤,并将粉末收集起来,就得到了纯钨。
实验结果:
通过以上实验步骤,我们制备了高纯度的钨粉末,并成功地完成了第一过度系元素的制备实验。
在这个实验中要注意实验前需要准备好实验所需的物品,以确保实验能够成功进行,同时在实验中需要注意安全问题,以避免做实验期间发生意外事件。
结论:
借助电热直接还原法制备第一过渡系元素钨,可以成功地制备出高纯度的钨粉末,这说明这种方法是非常可行的,同时为研究及应用钨提供了更加广阔的空间。
实验第一过渡系元素(II)(铁,钴,镍)一、实验目的与要求:1.掌握二价铁,钴,镍的还原性和氧化性。
2.掌握铁,钴,镍配合物的生成及性质。
二、教学重点与难点:掌握二价铁,钴,镍的还原性和氧化性;掌握铁,钴,镍配合物的生成及性质。
三、教学方法与手段:讲授法;演示法四、教学课时: 4课时五、课的类型:实验课六、教学内容:[实验内容]:一、铁(II)、钴(II)、镍(II)的化合物的还原性1、铁(II)的还原性(1)酸性介质:往盛有0.5ml氯水的试管中加入3滴6 mol.L-1H2SO4溶液,然后滴加(NH4)2Fe(SO4)2溶液,观察现象,写出反应式:2Fe2+ + Cl2 === 2Fe3++ 2Cl-Fe3++nSCN-====[Fe(SCN)n]3-n(血红色)说明:Fe2+被氧化为Fe3+的现象不明显(淡绿色 黄棕色),可用KSCN检验Fe3+。
亚铁盐一般用硫酸亚铁铵,它稳定,不易分解,为防万一还需要加硫酸。
(2)碱性介质:在一试管中放入2ml蒸馏水和3滴6mol.L-1H2SO4溶液煮沸,以赶尽溶于其中的空气,然后溶于少量硫酸亚铁铵晶体。
在另一试管中加入3ml 6mol.L-1NaOH溶液煮沸。
冷却后,用一长滴管吸收NaOH溶液,插入(NH4)2Fe(SO4)2溶液到底部,慢慢挤出NaOH,观察产物颜色和状态。
Fe2++2OH- ====Fe(OH)2(为纯白色沉淀)4Fe(OH)2+O2+2H2O====4Fe(OH)3 (红褐色)说明:为了得到纯净的白色氢氧化亚铁沉淀,将溶液加热以赶净溶解在其中的氧气。
放置一段时间白色沉淀变为灰绿色,至实验结束也没有变为红褐色。
【现象:沉淀由白变成灰绿色再变成红棕色】2、钴(II)的还原性(1)、往盛有CoCl2溶液的试管中加入氯水,观察有何变化两者不反应.2Co2++Cl2+2H+ 不反应说明:在酸性溶液中,Co2+比较稳定,不易被氧化。
(2)、在盛有1ml CoCl2溶液的试管中滴入稀NaOH溶液(注:),观察沉淀的生成。
一、实验目的1. 了解铁系元素的基本性质和特点。
2. 掌握铁系元素在化学实验中的应用。
3. 通过实验,加深对铁系元素的认识。
二、实验原理铁系元素是指铁、钴、镍这三种性质相似的元素,它们在周期表中分别位于8族、9族及10族(合称B族)之首,位于6个铂族元素上方。
铁系元素的电子壳层最外层都有两个电子,但第二外层的电子数不同,分别为6、7、8。
由于它们具有相近的原子半径,因此它们的性质也会很相似。
铁系元素的一大特征为其单质在常温下表现出铁磁性。
三、实验材料与仪器1. 实验材料:铁、钴、镍单质,盐酸,硫酸,氢氧化钠,硫酸铜溶液,硫酸亚铁溶液,硫酸钴溶液,硫酸镍溶液,氯化铁溶液,氯化钴溶液,氯化镍溶液等。
2. 实验仪器:烧杯,试管,酒精灯,铁架台,滴定管,移液管,玻璃棒,滤纸等。
四、实验步骤1. 铁的实验(1)取一定量的铁片,用砂纸打磨表面,观察其颜色和硬度。
(2)将铁片放入盐酸中,观察铁片表面产生的气泡,记录反应速率。
(3)取一定量的硫酸亚铁溶液,加入氢氧化钠溶液,观察沉淀的形成。
(4)将硫酸亚铁溶液与硫酸铜溶液混合,观察颜色变化。
2. 钴的实验(1)取一定量的钴片,用砂纸打磨表面,观察其颜色和硬度。
(2)将钴片放入盐酸中,观察铁片表面产生的气泡,记录反应速率。
(3)取一定量的硫酸钴溶液,加入氢氧化钠溶液,观察沉淀的形成。
(4)将硫酸钴溶液与硫酸铜溶液混合,观察颜色变化。
3. 镍的实验(1)取一定量的镍片,用砂纸打磨表面,观察其颜色和硬度。
(2)将镍片放入盐酸中,观察铁片表面产生的气泡,记录反应速率。
(3)取一定量的硫酸镍溶液,加入氢氧化钠溶液,观察沉淀的形成。
(4)将硫酸镍溶液与硫酸铜溶液混合,观察颜色变化。
五、实验结果与分析1. 铁的实验(1)铁片表面呈现银白色,硬度较高。
(2)铁片与盐酸反应产生气泡,反应速率较快。
(3)硫酸亚铁溶液与氢氧化钠溶液反应生成白色沉淀。
(4)硫酸亚铁溶液与硫酸铜溶液混合后,溶液颜色变为浅绿色。