CO中低温变换数据
- 格式:xlsx
- 大小:31.25 KB
- 文档页数:4

一氧化碳的低温变换CO变换的工艺流程主要由原料气组成来决定的,同时还与催化剂、变换反应器的结构,以及气体的净化要求有关。
目前低温变换主要是串接在中温变换催化剂后作为一氧化碳深度变换的。
而入口一氧化碳含量5%-8% , 最高使用温度不超过300℃。
中变串低变流程一般采用两种方法,一是中变炉外加低变炉, 另一种为变换炉中一二层用中变触媒, 三层使用低温触媒。
两种方法都使系统出口一氧化碳含量降至1%左右, 起到稳定生产、增产节能之效果。
1.中(高)变-底变串联流程采用此流程一般与甲烷化脱除少量碳氧化物相配合。
这类流程先通过中(高)温变换将大量CO变换达到3%左右后,再用低温变换使一氧化碳含量降低到0.3%-0.5%,。
为了进一步降低出口气中CO含量,也有在低变后面串联一个低变的流程。
当CO含量较高时,变换气一般选择在炉外串低变;而一氧化碳含量较低时,可选择在炉内串低变。
中串低流程中要主要两个问题,一是要提高低变催化剂的抗毒性,防止低变催化剂过早失活;二是要注意中变催化剂的过度还原,因为与单一的中变流程相比,中串低特别是中低低流程的反应汽气比下降,中变催化剂容易过度还原,引起催化剂失活、阻力增大及使用寿命缩短。
2.全低变流程中(高)变-低变串联流程操作繁琐,设备增加,特别是特殊材料阀门的选用给管理带来了许多不便。
使用全低变变换催化剂代替原Fe-Cr系中变催化剂,在低温下完成变换即可克服以上两种工艺的缺点,又能达到理想的目的。
全低变工艺采用宽温区的钴钼系耐硫变换催化剂,主要有下列优点。
(1)催化剂的起始活性温度低,变换炉入口温度及床层热点温度低于中变炉入口及热点温度100-200℃。
这样,就降低了床层阻力,缩小了气体体积约20%,从而提高了变换炉的生产能力。
(2)变换系统处于较低的温度范围内操作,在满足出口变换气中CO含量的前提下,可以降低入炉蒸汽量,使全低变流程的蒸汽消耗降低。
使用全低变变换催化剂代替原。


一氧化碳低温变换工艺及应用陈劲松(湖北省化学研究所,湖北武汉430074)1前言众所周知,一氧化碳变换反应是放热反应,反应温度愈低愈利于反应进行,也就愈利于节汽、节能、提高设备能力。
因此降低催化剂的活性温度成为变换催化剂科技工作者的奋斗目标。
自1912年Fe—Cr变换催化剂问世以来,催化剂的性能日益完善,低温活性也愈来愈好,随之而来的变换工艺也取得了长足的进步,特别是Co—Mo耐硫变换催化剂的开发成功给变换工艺带来了一场革命,利用该催化剂我国80年代成功开发了部分低温变换工艺即中变串低变工艺,取得明显的经济效益。
在此基础上又继续开发了中变串双低变(中低低),中变串三低变(中低低低)工艺和全部使用Co—Mo系变换催化剂的全低变工艺,显然,从中变一中串低一中低低一中低低低一全低变,其节能效果也越来越好。
2 Co—Mo耐硫变换催化剂的性能钴钼系变换催化剂是当今耐硫变换催化剂的主体,萝:组分为1%~5%CoO,8%~15%MoO。
/7/A1。
0。
常见的工业产品有美国UCI公司的C25—2-02;丹麦Tops忙公司的SSK;德国BASF 公司的K8—1l等,我国也有近20家催化剂厂生产,国家牌号只有三个,即上海化工研究院的B301,湖北省化学研究所的B302Q、B303Q。
2.1催化剂的制备及硫化Co—Mo系耐硫宽温变换催化剂的制备已有很多专利文献报道,一般都用硝酸钴、钼酸铵的氨溶液浸渍活性氧化铝而成,这种类型的催化剂的组分大体相同,其活性高低、抗低硫性、抗毒性取决于表面活性中心结构,即与其制备工艺和硫化方法密切相关。
催化剂以盐类或氧化物形态提供,在使用时要用硫化氢或CS:进行活化即硫化。
将其转化为硫化物才具有活性,这一过程称为硫化,其主要反·】84·应为:CoO+H2S=CoS+H20 △Ho一一13.6 kJ/toolM003+2H2S十H2一MoS2+3Hz0 △H。
=一48.1 kJ/mol 我们对这类催化剂的硫化方法及硫化剂进行了研究,常用的硫化剂有:(1)二硫化碳硫化,向系统添an--硫化碳;(2)采用高硫煤或人造高硫煤造气以提高煤气中的硫化氢含量;(3)固体硫化剂(我所发明专利)硫化,固体硫化剂在煤气的作用下产生硫化氢。
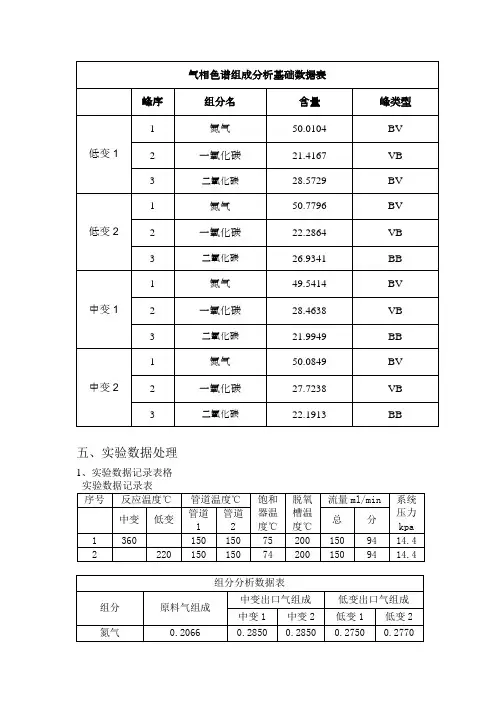
五、实验数据处理1、实验数据记录表格一氧化碳0.1377 0.1410 0.1390 0.1020 0.1070 氢气0.3099 0.4770 0.4780 0.4950 0.4920 二氧化碳0.0344 0.0960 0.0980 0.1270 0.1230 水0.3113 0.0000 0.0000 0.0000 0.0000计算实例:以中变1、低变1为例:中变1:T1=633.15K;低变1:T2=493.15K。
(1)求中、低变反应的平衡常数由:得到:中变1的平衡常数:Kp1=18.857 ;低变1的平衡常数:Kp2=157.326。
(2)求汽气比有记录的饱和平均温度:74.5℃,由:,式中:A=7.9846,B=1678.95,C=228.97。
计算得出:Ph2o=283.21mmHg,式中:Pa=760 mmHg、Pg=150 mmHg计算得出汽气比:R=283.21760+150−283.21=0.452(3)求CO变换率CO变化率计算公式:得:中变1的变化率:α1=0.0590.2∗(1+0.141)=0.259、同理得:低变变换率:α2=0.2−0.1020.2∗(1+0.2)=0.408(4)由于式中fi(pi)与α有关,但是本次试验不能连续积分,所以可采用数值计分方法:在α[0,0.123]的范围内任选五个值做数值积分,同时由公式得:i f(Pi)=0.5p coy co2-0.5y(1-co2y H2yKp1*coy H2oyP=760+150760´101.3=121.3Kpa通过查资料可得:本实验中采用的是普通型的转子流量计,所以直接按照不锈钢的材质来修正总分的流量,具体修正如下:总流量的修正:分流量的修正:因为:,所以:s m =i m 14åiy =28´0.2+2´0.45+44´0.05+28´0.3=17.1ir=P i M RT =101325*17.1*0.0018.314*293.15=0.710kg /3m s V =d V ´=150´=202.43ml /minfV=f 1V ´=94´=125.87ml /min1P 1V 1T=2P 2V 2T所以:(5)转子流量计计量的分流需要换算,换算公式为:所以:而1atm,20℃下,V 分=94ml/min在低变反应器中,,计算后列表如下,在在α[0,0.408]的范围内任选五个值做数值积分,同时由公1V =2P sV 1T 2T 1P=(760+150)*202.43*273.15760*293.15=225.85ml /min01V =1V (1+1R )=225.85´(1+0.452)=327.93ml /min =19.68l /h T 1K=01V CO0y 22.4d a ifi (Pi )=19.68´0.137722.40aò´0.064753(18.069+26.6869+45.6274+24.7708+14.0517)=4.70´-310(mol *-1h *-0.5kpa*-1g )lCO 2,dy=0.096lCO ,dy=0.141lH 2,dy=0.477l N 2,dy=0.285s m =i m 14åli ,dy=28´0.147+2´0.474+44´0.092+28´0.287=17.148s 0m =i m 14åli ,d y=28´0.141+2´0.477+44´0.096+28´0.285=17.106s ,d 'V =1P s V 2T s0m1T 2P sm=760´633.15´17.106´125.87910´293.15´17.148=226.49ml /mins V =s ,d 'V ´11-(h 2o0y-h 2o0y´a 1)=226.49´11-(0.3113-0.259´0.1377)=312.67ml /min02V =0V s -V =226.49-312.67´273.15663.15=97.70ml /min =5.862l /h i f (Pi )=0.5p H 200.2yco H 20.2y y co 2-0.5y (1-co 2y H 2y Kp 2*co y H 2oy )在辛普森积分法计算可得:反应速率常数单位:六、结果与讨论本次试验是采用不同温度不同催化剂下进行的一氧化碳的中低温变换反应,反应温度分别为220℃和360℃,从上述结果中可以看出,一氧化碳中变1,2的反应速率常数差值很少,所以可以看出来本次试验还是较准确的;一氧化碳在低温下铜基上的转化率更高,说明铜作为催化剂对于一氧化碳变换反应而言,其转化率更好,且需要的温度更低,故在一氧化碳中低温串联变换反应中可以采用更多的铜基催化剂,同时可以适当增加串联反应釜的数量,以使一氧化碳的反应速率达到最大值,实现工艺上产物产量的最大化。


实验十二 一氧化碳中温—低温串联变换反应实验一.实验目的一氧化碳变换反应是石油化工与合成氨生产中的重要过程,现代大型合成氨装置中一氧化碳的转化与净化采用中温—低温串联变换加甲烷化工艺。
本实验模拟中温—低温串联变换反应过程,不仅具有工艺类专业实验的典型特点,而且体现了本专业生产领域内的先进技术。
通过用直流流动法同时测定铜基与铁基催化剂的相对活性,并通过讨论与思考,要求达到:1.复习多相催化反应有关知识,初步接触工艺设计思想。
2.掌握气固相催化反应动力学实验研究方法及催化剂活性的评比方法。
3.获得两种催化剂上变换反应的速率常数k T 与活化能E 。
二.实验原理一氧化碳变换反应为CO+H 2O==CO 2+H 2反应必须在催化剂存在的条件下进行。
中温变换采用铁基催化剂,反应温度为350~500℃,低温变换采用铜基催化剂,反应温度为220~320℃。
设反应前气体混合物中各个组分干基摩尔分率为d CO y ,0、d CO y ,02、d H y ,02、d N y ,02;初始汽化比为R 0;反应后气体混合物中各组分干基摩尔分率为d CO y ,、d CO y ,2、d H y ,2、dN y ,2,一氧化碳的变换率为 )1()1(,0,0,,,0,,0,222d CO d CO d CO d CO d CO d CO d CO d CO y y y y y y y y --=+-=α (1)根据研究,铁基催化剂上一氧化碳中温变换反应本征动力学方程可表示为: )1(2222125.01OH CO P H CO CO CO T CO CO p p K p p p p k dW dN dW dN r -==-=-)(,)()1(15.0121h g mol p f k p p k i T CO CO T ∙=-=-β (2)铜基催化剂上一氧化碳低温变换反应本征动力学方程可表示为: )(,)()1(22.05.02.0222222hg mol p f k p p p p k r i T H CO O H CO T ∙=-=--β (3) 式中:r i ——反应速率,)(h g m ol ∙;i T k ——反应速率常数,)(hg m ol ∙; CO N 、2CO N ——一氧化碳、二氧化碳的摩尔流量,)(h g m ol ∙; W ——催化剂量(g );p i ——各组分的分压;K p ——以分压表示的平衡常数 )]218.2100604.1106218.0ln 3026.21102.02185(3026.2exp[273-⨯-⨯+-⨯=--T T T T K P (4) T ——反应温度,(K )。

一氧化碳变换概述一氧化碳的变换是指煤气借助于催化剂的作用,在一定温度下,与水蒸气反应,一氧化碳生成二氧化碳和氢气的过程。
通过变换反应既除去了煤气中的一氧化碳,又得到了制取甲醇的有效气体氢气。
因此,变化工段既是转化工序,又是净化工序。
前工段来的煤气中,一氧化碳含量高,通过变换反应以后,要求达到工艺气体中的CO/H2约为2.05~2.1的关系,以满足甲醇合成的要求。
一氧化碳变换反应是在催化剂存在的条件下进行的,是一个典型的气固相催化反应。
60年代以前,变换催化剂普遍采用Fe-Gr催化剂,使用温度范围为350~550℃,60年代以后,开发了钴钼加氢转化催化剂和氧化锌脱硫剂,这种催化剂的操作温度为200~280℃,为了区别这两种操作温度不同的变换过程,习惯上将前者称为“中温变换”,后者称为“低温变换”。
按照回收热量的方法不同,变换又可分为激冷流程和废锅流程,冷激流程中,冷激后的粗原料气已被水蒸气饱和,在未经冷却和脱硫情况下直接进行变换,因此,两种流程按照工艺条件的不同选用不同的催化剂,激冷流程采用Co-Mo耐硫变换催化剂,废锅流程采用Fe-Cr 变换催化剂。
第一节变换反应原理变换过程为含有C、H、O三种元素的CO和H2O共存的系统,在CO变换的催化反应过程中,除了主要反应CO+H2O=CO2+H2以外,在某种条件下会发生CO分解等其他副反应,分别如下:2CO=C+CO22CO+2H2=CH4+CO2CO+3H2=CH4+H2OCO2+4H2=CH4+2H2O这些副反应都消耗了原料气中的有效气体,生成有害的游离碳及无用的甲烷,避免副反应的最好方法就是使用选择性好的变换催化剂。
一、变换反应的热效应一氧化碳变换反应是一个放热反应,CO+H2O=CO2+H2+41kJ/gmol反应的热效应视H2O的状态而定,若为液态水,则是微吸热反应,若是水蒸气,则为放热反应。
变换反应的反应热随温度的升高而降低,具体反应热列表如下:表1 CO+H2O=CO2+H2的反应热压力对变换反应的反应热影响较小,一般不做考虑。

国内外高职院校招生制度对比研究2014年9月国务院发布《关于深化考试招生制度改革的实施意见》,其中指出,到2020年,基本建立中国特色的现代教育考试招生制度,形成分类考试、综合评价、多元录取的考试招生模式。
这一意见的提出,将招生考试改革又一次推到了大众面前,引发了广泛的讨论。
与此同时,美国、德国、加拿大等发达国家的招生制度也在不断地发展和完善,我们在思考自身的同时,也可以比较各国的招生制度,通过分析研究促进我国教育招生制度的改革。
标签:高职院校;招生制度改革;国内外对比高校招生制度改革一直是一个热门话题,高校招生制度的优劣直接影响了整个教育体系,高职院校作为高校的一部分,在招生制度的改革中也起着举足轻重的作用。
近年来,高职院校的招生制度随着我国高考制度的改革也一直在调整着,无论从招生方式、考试内容还是管理办法方面,都进行了很大的改革。
一、我国高职院校招生制度的改革及现行招生制度1.我国招生制度的历史沿革我国古代选拔人才的方式可以追溯到秦朝以前的“世卿世禄”制度,直到隋唐年间,随着改革的深入,形成了比较完善的科举制,科举制又经过历次改革,一直沿用到清朝灭亡,但是这些制度主要都是古代为统治者选拔人才服务的,古代的学校数量稀少,学生大都是家境宽裕以及有一定文化程度的,这也体现了当时考试制度的缺失。
直到新中国成立后,我国才逐步建立起了全国统一的招生制度,虽然有一定的弊端,但是当时国家亟须人才,统一的招生考试的确在一定时间内为国家解决了一部分困难。
后来由于“文化大革命”影响,高考制度暂停了一段时间,直到1976年才正式恢复,恢复后的高校仍然主要是通过高考的形式选拔学生,但是高考的内容一直有小的变动,比如英语课程的加入等。
到了21世纪,随着学校数量的增多,考生生源的扩大,不同省份学校、生源的差异越来越明显,部分省份对高考试卷采用自主命题的方式,其他省份还是沿用全国高考卷。
2003年,教育部开始推行自主招生,结束了此前高校只能在每年同一时间通过高考选拔学生的历史,这次改革可以说是比较大的改变,也有很深远的影响。



co在各温度下的与标准生成热的差值理论说明1. 引言1.1 概述本文旨在研究CO在不同温度下的生成热差值,并通过理论分析来解释其变化规律。
CO作为一种常见的有机化合物,其生成热是许多化学反应中的关键参数之一。
了解CO生成热随温度变化的规律可以帮助我们更好地理解和控制相关化学反应。
1.2 文章结构本文包括引言、正文、实验方法、结果与讨论以及结论等部分。
首先,在引言部分简要概述文章内容和目标,并介绍文章结构。
然后,通过正文部分对CO的标准生成热以及温度对其生成热的影响进行理论说明。
接下来,详细描述实验方法,包括实验条件设置、数据采集与处理等内容。
然后,通过结果与讨论部分分析温度变化下CO生成热的趋势,以及温度对CO生成热差值的影响,并讨论可能存在的误差来源及排除方法。
最后,在结论部分总结主要研究结果,并展望未来进一步的研究方向。
1.3 目的本文旨在深入探讨CO在不同温度下生成热与标准生成热的差值,并解释其背后的物理化学原理。
通过实验方法的优化和结果分析,为进一步研究和应用CO相关反应提供参考和基础。
2. 正文:2.1 理论背景在研究CO在不同温度下的生成热差值之前,我们需要了解一些理论背景知识。
CO是一种常见的一氧化碳气体,它的生成热是指在标准状态下,1摩尔CO气体生成时释放的热量。
通常以kcal/mol或kJ/mol为单位来表示。
2.2 CO的标准生成热根据化学平衡定律,标准生成热可以通过测量反应中物质的焓变来确定。
对于CO的生成反应,可以简化为以下方程式:C(s) + 0.5O2(g) →CO(g)根据这个方程式,我们可以计算出CO的标准生成焓变ΔH°。
通过实验测定输入和输出系统的能量变化,我们可以确定反应过程中吸收或释放的能量量,并进而计算出ΔH°。
2.3 温度对CO生成热的影响温度是一个重要因素,它会对化学反应速率和平衡位置产生影响。
对于CO的生成反应来说,温度变化也会导致其生成热发生改变。
第二章粗原料气制取一、固体燃料气化法名词解释:煤气化:使煤与气化剂作用,进行各种化学反应,把煤炭转变为燃料用煤气或合成用煤气。
加氮空气;水蒸汽和空气同时加入,空气的加入增加了气体中N的含量,用来调节原料气中氢氮比,制得合格煤气标准煤:含碳量为84%的煤(每千克标准煤的热值为7000千卡)1.煤气化有几种工业方法?各有什么特点?蓄热法:将空气和水蒸气分别送入煤层,也称间歇式制气法富氧空气气化法:用富氧空气或纯氧代替空气进行煤气化外热法: 利用其他廉价高温热源来为煤气化提供热能,尚未达到工业化阶段2.气化炉有哪些床层类型,描述各自的特点?工业用煤气化炉有几种类型?固定床:气体从颗粒间的缝隙中穿过,颗粒保持静止流化床:增大气速,颗粒开始全部悬浮于气流中,而且床层的高度随气速的增大而升高气流床:气流速度增大至某一极限值时,悬浮于气流中的颗粒被气流带出间歇式气化炉、鲁奇炉、温克勒炉、K-T炉、德士古炉3.煤的气化剂有哪些?用不同气化剂进行煤气化,气体产物各是什么?空气和水蒸气空气煤气(N2、CO)、水煤气(H2、CO)、混合煤气、半水煤气4.固定床煤气化炉燃料层如何分区?各区进行什么过程?干燥区:使新入煤炉中的水分蒸发干馏区:煤开始热解,逸出以烃类为主的挥发分,而燃料本身开始碳化气化区:煤气化的主要反应在气化区进行灰渣区:灰渣于该区域出炉5.固定床气化炉燃料最下层是什麽区?其有何作用?灰渣区可预热从底部进入的气化剂并保持不因过热而变形6.间歇式制半水煤气的工作循环是什么?为什么?循环时间如何分配?工业上将自上一次开始送入空气至下一次再送入空气为止,称为一个循环。
每个循环有五个阶段,吹风阶段、蒸汽一次上吹、蒸汽下吹、蒸汽二次上吹、空气吹净7.什麽是加氮空气?其作用为何?使用中应注意什麽事项?水蒸汽和空气同时加入,空气的加入增加了气体中N的含量。
用来调节原料气中氢氮比,制得合格煤气使炉温下降慢调节合成氨气体成分,严格控制氮含量,以免引起事故8.德士古炉废热如何回收?直接激冷法、间接冷却法、间接冷却和直接淬冷9.画出间歇式煤气化、德士古炉及谢尔废热锅炉连续气化工艺制备合成氨流程,为什么后两者流程有差别?P70P72二、一氧化碳变换1、名词解释:高温变换:CO在320~350℃变换,使CO含量低于3%。
制氢低温变换催化剂的性质和使用经过中温变换反应后,出口气体中CO含量一般为3~4%,再经过低温变换,出口气中CO可降低倒0.2~0.4%,从而提高装置的产氢率。
低温变换所用的催化剂称为低温变换催化剂,简称低变催化剂。
我国的低变催化剂主要有两大系列,分别是铜锌铬系和铜锌铝系。
生产方法也硝酸法发展到络合法。
1.1催化剂的物化性质1.1.1铜基低变催化剂的化学组成至1989年底止,我国已有6种铜基低变催化剂经过部级鉴定统一命名,列为国家正式产品,其型号及化学组成见下表5-14。
表5-14 国产低变催化剂的型号用化学组成±3.5 ±3.5 ±2 1505000 产我国大、中、小型制氢低变催化剂已全部实现国产化。
1.1.2铜基低变催化剂主要组分的作用1.Cu的作用金属铜微晶是低变催化剂的活性组分。
催化剂制造厂通常只供应氧化态产品,用户必须先将催化剂还原,使CuO变为Cu。
Cu对某些气体的化学吸附性质见表5-15。
表5-15 Cu对某些气体的化学吸附活性T,℃N2H2CO2COC2H4C2H2O2说明-183~ 0 –––+ + + + +表示有吸附作用–表示无吸附作用可知,在变换气体中,Cu对N2、、H2、CO2没有化学吸附活性,Cu对CO具有化学吸附作用。
低变催化剂中的铜微晶愈小,其比表面愈大,则活性中心愈多,其活性也愈高。
由下面左图可知:催化剂的活性随铜微晶的变小而增加,两者大致呈线性关系。
铜微晶大小和铜表面以及活性的关系见右图。
铜晶粒愈小其表面能愈高,在操作温度下会迅速向表面能低的大晶粒转变,亦即通常所说催化剂向热稳定态转移的“半熔”或“烧熔”。
将50~150Å铜微晶在200℃左右的还原性气体中处理6个月,烧结后其最小微晶也成为大于1000×10-10m的晶粒;若在相同气体、相同时间将温度调为300℃,其最小晶粒也大于10000×10-10m,可见温度愈高、愈易烧结。