消毒灭菌效果检测方法.
- 格式:doc
- 大小:18.00 KB
- 文档页数:4


消毒灭菌效果监测标准
介绍
本文档旨在规定消毒灭菌效果监测的标准,以确保消毒操作的有效性和安全性。
监测方法
1.化学指示剂监测:
使用化学指示剂对消毒操作进行监测。
根据指示剂的颜色变化判断消毒效果,确保达到预定的消毒水平。
2.生物指示剂监测:
采用生物指示剂对消毒操作进行监测。
将生物指示剂暴露于消毒环境中,根据指示剂的生长情况判断消毒效果。
必要时,进行培养和检测以确认消毒效果。
3.物理监测:
使用物理监测设备对消毒操作进行监测。
如温度计、压力计等,确保消毒操作中的物理参数符合标准要求。
监测标准
1.化学指示剂监测标准:
指示剂变色范围和时间应符合相关行业标准。
变色结果应清晰可见,且与标准色标一致。
2.生物指示剂监测标准:
生物指示剂的生长情况应符合相关行业标准。
生长情况的判断应基于定量评价方法。
3.物理监测标准:
物理参数应符合相关行业标准。
监测设备的准确性和可靠性应符合相关要求。
结论
本文档规定了消毒灭菌效果监测的标准,包括化学指示剂监测、生物指示剂监测和物理监测三种方法。
确保消毒操作的有效性和安
全性,保护人们的健康与安全。
注:以上内容仅供参考,请根据实际情况进行处理。

实验室消毒灭菌效果监测一、消毒灭菌效果监测(一)压力蒸汽灭菌效果监测1.化学监测法(1)化学指示剂监测方法:将既能指示蒸汽温度,又能指示温度持续时间的化学指示剂放入大包和难以消毒部位的物品包中央,经一个灭菌周期后,取出指示剂,根据其颜色及性状的改变判断是否达到灭菌条件。
(2)化学指示胶带监测法:将化学指示胶带粘贴于每一待灭菌物品包外,经一个灭菌周期后,观察其颜色的改变,以指示是否经过灭菌处理。
对预真空和脉动真空压力蒸汽灭菌,应进行B-D 试验。
结果判定:检测时,所放置的指示卡/管、胶带的性状或颜色均变至规定的条件,判为灭菌合格;若其中之一未达到规定的条件,则灭菌过程不合格。
2.物理监测法应每年用温度压力检测仪检测温度、压力和时间等参数,检测仪探头放置于最难灭菌部位。
3.生物监测法生物指示物为嗜热脂肪杆菌(ATCC7953或SSIK31株)芽孢。
试验用培养基为溴甲酚紫葡萄糖蛋白胨水培养基。
检测方法:将两个嗜热脂肪杆菌芽孢菌片分别装入灭菌小纸袋内或使用自含式生物指示剂,置于标准试验包中心部位。
分别在下排气压力蒸汽灭菌器灭菌柜室内,排气口上方放置一个标准试验包;预真空和脉动真空压力蒸汽灭菌器灭菌柜室内,排气口上方放置一个标准测试包;手提压力蒸汽灭菌器用带有指示菌的小型测试包,放于手提压力蒸汽灭菌器底部。
经一个灭菌周期后,取出标准试验包,无菌取出指示菌片,投入溴甲酚紫葡萄糖蛋白胨水培养基中,经56℃培养7d(自含式生物指示物按说明书执行),观察培养基颜色变化。
同时设阴性对照和阳性对照。
结果判定:每个试验组和阴性对照组指示菌片接种的溴甲酚紫蛋白胨水培养基都不变色,阳性对照组由紫色变为黄色时,判定为灭菌合格;否则灭菌不合格。
(二)干热灭菌效果监测方法1.化学监测法(1)检测方法:将既能指示温度又能指示温度持续时间的化学指示剂3~5个分别放入待灭菌的物品中,并置于灭菌器最难达到灭菌的部位。
经一个灭菌周期后,取出化学指示剂,据其颜色及性状的改变判断是否达到灭菌条件。

消毒灭菌监测方法(一)消毒灭菌监测方法首先,我们需要了解什么是消毒和灭菌。
消毒是指在无菌条件下利用物理或化学方法使表面或环境减少病原菌数量,达到预防、控制疾病的目的。
而灭菌是指在单位时间内,使细菌、病毒、真菌、孢子等微生物完全死亡的过程。
灭菌是比消毒效果更高的一种处理方法。
为了保证医学、实验室等场所的卫生,必须实施并监测消毒灭菌过程的有效性。
下面分别介绍几种用来监测消毒灭菌效果的方法。
1.生物指示器法生物指示器是一种人工制备的微生物反应器,它含有一定数量的微生物孢子。
用于验证常规消毒灭菌过程中是否有效,其使用范围涵盖几乎所有消毒灭菌方法。
生物指示器的检测流程简单,但需要长时间培养,且非常敏感,造成误差较小。
因此,生物指示器法是一种最可靠的监测方法。
2.物理化学指示器法物理化学指示器法是一种通过颜色或温度来展示消毒灭菌效果的方法。
它可以很快地重复使用并且检测结果可以在即时展示。
物理化学指示器法对于某些情况下的操作效果有一定的参考价值,但是并不能完全保证消毒灭菌效果。
3.系统监控法系统监控法是通过记录实验室、手术室、病房等场所每次消毒灭菌过程的温度、时间、浓度、玻璃器皿的摆放和使用等信息来监测消毒灭菌效果。
系统监控法的优点是可以帮助操作人员发现过程中可能存在的问题并及时调整,同时也规范化了操作过程。
总之,消毒灭菌效果的监测是非常重要的,它有助于减少病原体的繁衍和消除医疗场所的交叉感染。
使用合适的监测方法,可以确保消毒灭菌效果的正确性,并且保障人们的生命安全。

一、手和皮肤黏膜消毒效果监测1、采样时间:在消毒后立即采样。
2、采样方法(1) 手的采样:被检人五指并拢,用浸有含相应中和剂的无菌洗脱液的棉拭子在双手指屈面从指根到指端往返涂擦 2 次(一只手涂擦面积约 30cm2),并随之转动采样棉拭子,剪去操作者手接触部位,将棉拭子投入 10ml 含相应中和剂的无菌洗脱液试管内,立即送检。
(2) 皮肤粘膜采样:用 5cm×5cm 的标准灭菌规格板,放在被检皮肤处,用浸有含相应中和剂的无菌洗脱液的棉拭子 1 支,在规格板内横竖往返均匀涂擦各 5 次,并随之转动棉拭子,剪去手接触部位后,将棉拭子投入 10ml 含相应中和剂的无菌洗脱液的试管内,立即送检。
不规则的粘膜皮肤处可用棉拭子直接涂擦采样。
3、检测方法(1) 细菌总数检测:将采样管在混匀器上振荡20s或用力振打 80 次,用无菌吸管吸取 1.0ml 待检样品接种于灭菌平皿,每一样本接种2个平皿,内加入已溶化的45℃~48℃的营养琼脂 15ml~18ml,边倾注边摇匀,待琼脂凝固,置 36℃±1℃温箱培养 48h,计数菌落数。
采样结果计算方法:平板上菌落数 ×稀释倍数细菌总数(cfu/cm2)=────────────────采样面积(cm2)(2) 致病菌检测:致病菌的检测依据污染情况进行相应指标检测的原则执行。
4、结果判定(1) 消毒洗手Ⅰ、Ⅱ类区域工作人员:细菌总数≤5cfu/cm2,并未检出金黄色葡萄球菌、大肠杆菌、铜绿假单孢菌为消毒合格。
Ⅲ类区域工作人员:细菌总数≤10cfu/cm2,并未检出金黄色葡萄球菌、大肠杆菌为消毒合格。
Ⅳ类区域工作人员:细菌总数≤15cfu/cm2,并未检出金黄色葡萄球菌、大肠杆菌为消毒合格。
母婴同室、婴儿室、新生儿室及儿科病房的工作人员手上,不得检出沙门菌、大肠杆菌、溶血性链球菌、金黄色葡萄球菌为消毒合格。
(2)皮肤黏膜:参照手的卫生学标准执行。

消毒、灭菌效果监测的方法
实验室必须对消毒、灭菌效果定期进行监测。
灭菌合格率必须达到100%,不合格的物品不得离开实验室。
一、使用中的消毒剂、灭菌剂,应进行生物和化学监测。
生物监测:消毒剂每季度一次,细菌含量必须<100cfu/mL,不得检出致病微生物。
灭菌剂每月一次,不得检出任何微生物。
化学监测:应根据消毒、灭菌剂的性能定期监测,含氯制剂、过氧乙酸等应每日监测,对戊二醛的监测应每周不少于一次。
消毒灭菌物品的监测:应定期对消毒、灭菌物品进行随机抽检,消毒物品不得检出致病性微生物,灭菌物品不得检出任何微生物。
二、高压蒸汽灭菌效果监测。
高压蒸汽灭菌应进行工艺监测、化学监测和生物监测。
工艺监测应每锅进行,并详细记录。
化学监测应每包进行,对于高危险性物品需进行中心部位的化学监测。
预真空压力灭菌器每天灭菌前进行B-D试验,生物监测应每月进行,新灭菌器使用前必须先进行生物监测,合格后方可使用。
三、紫外线消毒效果监测
紫外线消毒应进行灯管照射强度监测和生物监测。
灯管照射强度监测每半年进行一次,不得低于70μw/cm2。
新使用的灯管也要进行监测,不得低于100μw/cm2
生物监测必要时进行,要求经消毒后的物品或空气中的自然菌应减少90.00%以上,人工染菌杀灭率应达到99.90%。
四、环境监测
环境监测包括对空气、仪器设备、物体表面和工作人员手的监测。
在怀疑有实验室污染时应进行环境监测。
监测方法和卫生标准见《医院消毒卫生标准》(GB15982-2012)。
第1 页/共 1 页。

消毒器械灭菌效果评估方法消毒器械灭菌效果评估方法1.引言消毒器械灭菌效果评估是确保医疗设备在使用过程中能够有效杀灭病原微生物的重要环节。
正确评估消毒器械的灭菌效果,可以保障患者和医护人员的安全。
本文将介绍一些常用的消毒器械灭菌效果评估方法,并探讨其优缺点。
2.微生物负荷测试微生物负荷测试是评估消毒器械灭菌效果的重要手段之一。
它通过在器械表面涂布一定数量的模拟微生物,再进行消毒处理,最后测试处理后是否有残留的活菌。
常用的微生物负荷测试方法包括菌落计数法和生物指示器法。
2.1 菌落计数法菌落计数法是通过采集处理前后的器械表面菌落,进行培养和计数来评估灭菌效果的方法。
它可以对细菌、真菌和病毒进行检测。
该方法操作简便,结果可靠,但需要较长时间进行培养和计数,对专业实验室要求较高。
2.2 生物指示器法生物指示器法使用含有标准数量的抵抗力较强的微生物,如肉毒杆菌孢子或芽孢杆菌,来评估灭菌效果。
利用这些生物指示器在消毒过程中生存或灭活的情况,可以判断消毒器械是否达到预期的灭菌效果。
生物指示器法结果准确可靠,但操作复杂,需要专业人员进行操作。
3.化学指标检测除了微生物负荷测试,还可以通过检测器械消毒过程中的化学指标,如消毒剂浓度和pH值等来评估灭菌效果。
3.1 消毒剂浓度检测消毒剂浓度对消毒器械的灭菌效果起着至关重要的作用。
通过检测消毒剂的浓度,可以确保消毒剂在达到一定浓度的情况下才能有效杀灭微生物。
检测方法有比色法、电化学法和光谱法等。
这种方法操作简便,结果快速,但需要专门的仪器设备支持。
3.2 pH值检测pH值也是评估灭菌效果的重要指标之一。
不同的消毒剂对应不同的pH值范围,只有在特定的pH条件下,消毒剂的灭菌效果才能得到保证。
通过检测消毒过程中的pH值,可以判断消毒器械是否处于合适的灭菌环境中。
pH值检测方法简单易行,可用通用pH试纸进行测试。
4.灭菌效果验证灭菌效果验证是评估消毒器械灭菌效果非常重要的一环。

消毒与灭菌效果的评价方法与标准第一篇压力蒸汽灭菌效果评价方法与标准1主题内容与适用范围本方法规定了压力蒸汽灭菌技术标准及其评价灭菌效果的检测方法。
本方法适用于对压力蒸汽灭菌设备灭菌效果的评价。
2试剂本标准所用试剂,凡未说明规格者,均为分析纯(AR),水为蒸馏水。
2.1蛋白胨。
2.2葡萄糖。
2.3溴甲酚紫酒精溶液:取溴甲酚紫2.0g,溶于100mL95%乙醇中。
2.4溴甲酚紫蛋白胨水培养基配制:蛋白胨10.0g,葡萄糖5.0g,溶于1000mL蒸馏水中,调pH值至7.0~7.2,然后再加2%溴甲酚紫酒精溶液0.6mL,摇匀后,按5 mL/管,分装包口,置压力蒸汽灭菌器中,于115℃灭菌40min后备用。
3指示菌嗜热脂肪杆菌芽胞(ATCC 7953或SSI K31)菌片,含菌量为5×105~5×106cfu/片,1 21℃下,杀灭90%微生物所需时间D121值为1.3~1.9min,杀灭时间(KT值)为≤19m in,存活时间(ST值)为≥3.9min。
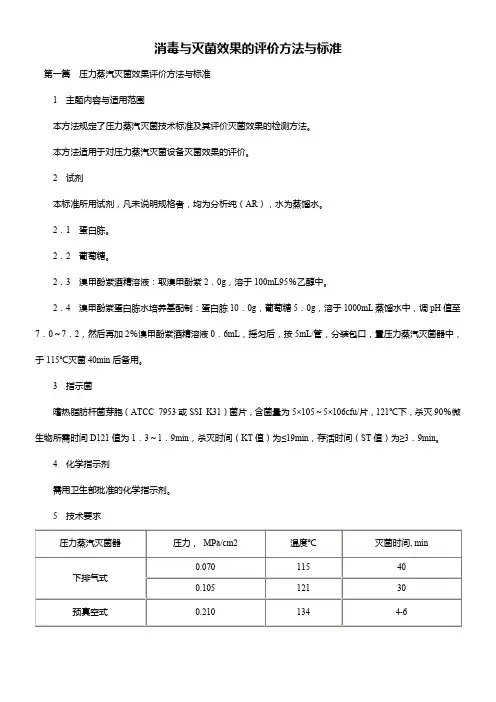
4化学指示剂需用卫生部批准的化学指示剂。
5技术要求国家技术监督局1995-12-15批准1996-07-01实施6检测方法6.1生物学指标(用作压力蒸汽灭菌设备灭菌效果的依据)。
6.1.1将嗜热脂肪杆菌芽胞菌片两个分别放入灭菌小纸袋内,置于标准试验包中心部位。
6.1.2灭菌柜室内,上、中层中央和排气口处各放置一个标准试验包(由3件平纹长袖手术衣,4块小手术巾,2块中手术巾,1块大手术巾,30块10cm×10cm、8层纱布敷料包裹成25cm×30cm×30cm大小)。
手提压力蒸汽灭菌器用通气贮物盒(22cm×13cm×6cm)代替标准试验包,盒内盛满中试管,指示菌片放于中心部位两只灭菌试管内(试管口用灭菌牛皮纸包封),将盒平放于手提压力蒸汽灭菌器底部。
6.1.3经一个灭菌周期后,在无菌条件下,取出标准试验包或通气贮物盒中的指示菌片,投入溴甲酚紫葡萄糖蛋白胨水培养基中,56℃培养48h,观察培养基颜色变化。
消毒与灭菌效果的评价方法与标准第一篇压力蒸汽灭菌效果评价方法与标准1主题内容与适用范围本方法规定了压力蒸汽灭菌技术标准及其评价灭菌效果的检测方法。
本方法适用于对压力蒸汽灭菌设备灭菌效果的评价。
2试剂本标准所用试剂,凡未说明规格者,均为分析纯(AR),水为蒸馏水。
2.1蛋白胨。
2.2葡萄糖。
2.3溴甲酚紫酒精溶液:取溴甲酚紫2.0g,溶于100mL95%乙醇中。
2.4溴甲酚紫蛋白胨水培养基配制:蛋白胨10.0g,葡萄糖5.0g,溶于1000mL蒸馏水中,调pH值至7.0~7.2,然后再加2%溴甲酚紫酒精溶液0.6mL,摇匀后,按5mL/管,分装包口,置压力蒸汽灭菌器中,于115℃灭菌40min后备用。
3指示菌嗜热脂肪杆菌芽胞(ATCC 7953或SSI K31)菌片,含菌量为5×105~5×106cfu/片,121℃下,杀灭90%微生物所需时间D121值为1.3~1.9min,杀灭时间(KT值)为≤19min,存活时间(ST值)为≥3.9min。
4化学指示剂需用卫生部批准的化学指示剂。
5技术要求国家技术监督局1995-12-15批准1996-07-01实施6检测方法6.1生物学指标(用作压力蒸汽灭菌设备灭菌效果的依据)。
6.1.1将嗜热脂肪杆菌芽胞菌片两个分别放入灭菌小纸袋内,置于标准试验包中心部位。
6.1.2灭菌柜室内,上、中层中央和排气口处各放置一个标准试验包(由3件平纹长袖手术衣,4块小手术巾,2块中手术巾,1块大手术巾,30块10cm×10cm、8层纱布敷料包裹成25cm×30cm×30cm大小)。
手提压力蒸汽灭菌器用通气贮物盒(22cm×13cm×6cm)代替标准试验包,盒内盛满中试管,指示菌片放于中心部位两只灭菌试管内(试管口用灭菌牛皮纸包封),将盒平放于手提压力蒸汽灭菌器底部。
6.1.3经一个灭菌周期后,在无菌条件下,取出标准试验包或通气贮物盒中的指示菌片,投入溴甲酚紫葡萄糖蛋白胨水培养基中,56℃培养48h,观察培养基颜色变化。

消毒灭菌效果监测方法概述本文档旨在介绍消毒灭菌效果监测的基本方法。
消毒灭菌是确保环境和物品卫生的重要措施,对于防止病原菌的传播具有重要意义。
监测消毒灭菌效果可以评估消毒措施的有效性,并采取必要的补救措施。
本文将介绍常用的消毒灭菌效果监测方法。
方法一:物理监测物理监测方法主要通过测量温度和时间来评估消毒灭菌过程的有效性。
常见的物理监测方法包括:1.温度计监测:使用合适的温度计测量消毒过程中的温度,确保温度达到杀菌要求。
2.时间监测:记录消毒过程中的持续时间,确保达到所需的时间要求。
物理监测方法简单易行,但无法评估外部如热量分布或物体形状对杀菌效果的影响。
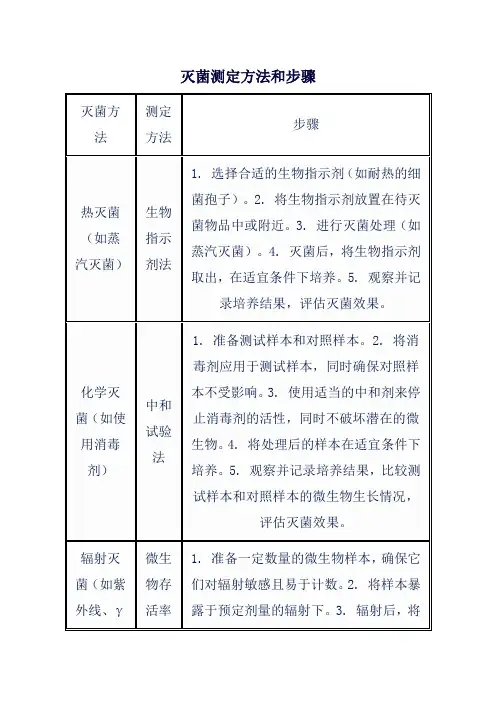
方法二:生物监测生物监测方法通过使用生物指示物质来评估消毒灭菌过程的有效性。
常见的生物监测方法包括:1.生物指示器法:使用含有特定微生物的指示器,如脱氢酶、芽孢等,将其置于消毒过程中进行监测。
监测完成后,对指示器进行培养和检测,判断是否有生物生长,以评估灭菌效果。
2.菌落计数法:通过培养并计数消毒前后的菌落数来评估灭菌效果。
消毒后菌落数显著减少或完全消失即可认为消毒灭菌效果良好。
生物监测方法能够直接评估杀菌的效果,但需要更专业的设备和实验操作,并需更长时间进行结果分析。
方法三:化学监测化学监测方法通过测量化学物质的浓度来评估消毒灭菌过程的有效性。
常见的化学监测方法包括:1.酶监测法:通过测量消毒剂残留物的酶活性来判断消毒过程中杀菌剂的效果。
2.指示剂监测:使用化学指示剂,如指示纸或试纸,来测定消毒结果。
指示剂的颜色变化可以间接反映杀菌效果。
化学监测方法简便易行,并能够快速获得结果,但只能提供相对的指数,无法直接评估消毒灭菌的效果。
结论消毒灭菌效果的监测是确保消毒措施有效性的重要手段。
根据需要和实际情况选择适合的监测方法,综合使用不同的监测方法可以更全面地评估消毒灭菌效果。
在实施消毒灭菌过程中,还需注意操作规范,确保消毒设备的正确运行和消毒剂的正确使用,以提高消毒灭菌效果。
消毒器械灭菌效果评价方法消毒与灭菌是医疗卫生领域不可或缺的重要环节。
其中,消毒主要用于去除病原菌、病毒和真菌等微生物,而灭菌则是彻底杀死微生物。
消毒器械的灭菌效果评价方法则是医疗卫生行业常见的问题,本文将介绍其评价方法。
1.微生物学检验法微生物学检验法是评价消毒器械灭菌效果的一种传统方法。
方法是将一定数量的标准菌落放置于消毒器械内,经过特定的灭菌程序后检测存活微生物的数量。
这种方法具有可重复性、精确性高等优点。
但是这种方法对检测人员的技能水平要求高,需要在一定的实验室环境下进行,同时检测过程耗费时间较长。
2. 物化指标检测法物化指标检测法是消毒器械灭菌效果评价的一种较为常见的方法,其中化学物理检测比较常见。
例如,可以检测器械表面温度、压力、湿度等一系列物理指标变化。
这种方法能够对灭菌过程进行准确监控,同时便于快速得到结果。
不过需要注意的是,实验室内部温度、湿度等环境因素的影响可能使得物理指标变化不够准确。
3. 生物指标检测法生物指标检测法是目前较为广泛应用的方法之一,其标准是符合美国国家PDA(Parenteral Drug Association)协会制定的规范。
该方法考察灭菌器将经验证的保存量完全杀死的可生长孢子,主要关注消毒器械内的菌落数量。
生物指标检测法实验操作过程简单,结果可靠,能够检验消毒器械内的真实灭菌效果。
4. 过程指标检测法过程指标检测法是对于消毒器械灭菌过程监测的一种方法。
这种方法能够根据不同的灭菌要求设定相应的指标,例如时间、温度、压力等。
通过对灭菌过程中各项参数的监控,能够准确评估消毒器械灭菌效果。
此种方法的实施方便,操作简单,不需要在实验室内进行,灵活性较高,经济实惠。
总之,以上介绍的消毒器械灭菌效果评价方法各有优缺点。
应根据具体情况来选择其中的一种或几种方法进行评估。
同时,为了保证评价效果的准确性,评估过程中,需要严格按照评价标准进行操作,同时采用多维度检测方法为摆脱灭菌失败的情况提供多重保障。
医院消毒灭菌效果监测标准操作规程医院消毒是预防医院内感染的重要措施之一,消毒效果的监测是评价其消毒设备运转是否正常、消毒药剂是否有效、消毒方法是否合理、消毒效果是否达标的唯一手段。
为规范消毒效果监测,特制定医院消毒灭菌效果监测的标准操作规程。
一、空气消毒效果的监测1、监测频次:每季进行。
2、采样⑴采样时间:空气消毒后4小时内、手术操作前。
⑵平板暴露法:暴露前先检查平板是否污染,是否有气泡及霉点。
将普通营养琼脂平板(直径为 9cm)放在室内各采样点处,采样高度为距地面 1.5m,采样时将平板盖打开,斜扣放于平板旁,暴露5min,在放置、收取平皿时,手不能在暴露平皿的正上方移动。
⑶布点方法:室内面积≤30m2,设内、中、外对角线上的3点,内、外点布点部位距墙1M处;室内面积>30m2,设 4 角及中央共 5 点,4 角的布点部位距墙壁 1m 处。
图1 室内面积≤30m2布点图图2 室内面积>30m2的布点图3、注意事项⑴采样前,关好门、窗,在无人走动的情况下,静止10min 进行采样。
⑵平板摆放如取一条对角线,避免离门近的一条。
⑶工作人员不要靠近自动门,以免影响监测结果。
4、结果判定⑴非洁净手术部(室)、非洁净骨髓移植病房、产房、导管室、新生儿室、器官移植病房、烧伤病房、重症监护病房、血液病病区空气中的细菌菌落总数≤4cfu/15min·直径9cm平皿。
⑵儿科病房、母婴同室、妇产科检查室、人流室、治疗室、注射室、换药室、输血科、消毒供应中心、血液透析中心(室)、急诊室、化验室、各类普通病室、感染疾病科门诊及其病房空气中的细菌菌落总数≤4cfu/5min·直径9cm平皿。
二、手、物体表面消毒效果监测1、监测重点科室:手术室、产房、导管室、层流洁净病房、骨髓移植病房、器官移植病房、重症监护病房、新生儿室、母婴室、血液透析病房、烧伤病房、感染疾病科、口腔科、消毒供应中心等。
2、监测频次⑴重点科室物表每月监测,工作人员手每季度监测。
医院消毒供应中心清洗消毒及灭菌效果监测1、刖言医院消毒是预防医院内感染的重要措施之一,消毒效果的监测是评价消毒设备运转是否正常、消毒药剂是否有效,消毒方法是否合理、消毒效果是否达标的唯一手段,因而在医院消毒、灭菌工作中必不可少。
2、热力灭菌效果监测方法2.1压力蒸汽灭菌效果监测方法化学监测法:理想的化学指示剂是既能指示温度又能指示持续时间。
化学监测法又分为指示卡监测法、指示管监测法和指示胶带监测法。
其中指示胶带法主要用于程序监测,即指示是否经过灭菌处理,要求每个待灭菌物品包处都要粘贴。
指示卡和指示管主要用于待灭菌物品包内作为灭菌效果的参考,不一定要求每个包内都放。
对于预真空和脉动真空压力真汽灭菌,要求每天进行一次B-D试验。
监测方法:将指示物放入大包(不得大于标准包)内和难以消毒部位的物品包中央,经一个灭菌周期后,取出指示物,根据其颜色及性状的变化来判断是否达到灭菌条件。
结果判定:检测时,所放置的指示物颜色或性状均变至规定的条件,则判定为灭菌过程合格;若其中之一未达到规定的条件,则判定为灭菌过程不合格。
生物监测法:即用活的指示生物来监测灭菌过程是否合格的方法。
指示生物为耐热和嗜热脂肪杆菌芽抱(ATCC7953或SSIK31)菌片,含菌量为5.0X105~5.0X106cfu/片,在121℃±0.5℃条件下,D 值为 1.3〜1.9min, 杀灭时间(KT值)W19min,存活时间(ST值)为三3.9min。
监测方法:将两个菌片分别装入灭菌小纸袋内,置于标准包中心部位,或装入灭菌试管内,置于标准盒内。
将标准包放于下排气压力蒸汽灭菌器灭菌柜室内的排气口上方,或将标准盒放于手提式压力蒸汽灭菌器的底部。
经一个灭菌周期后,将标准包或标准盒拿回实验室,在无菌操作条件下,取出菌片投入臭甲酚紫卡芬糖蛋白胨水培养其中,经56℃± 1℃培养7d (自含式生物指示物按说明书执行),观察培养基颜色的变化。
消毒灭菌效果的监测制度
1压力蒸汽灭菌的监测:包括物理监测法(工艺监测)、化学监测、B—D测试和生物监测法。
1.1物理监测法(工艺监测):每锅监测,每次灭菌时必须连续监测并记录灭菌时的温度、压力、时间等灭菌参数。
1.2化学监测法:每包监测,高危险性物品同时包括包外灭菌化学指示胶带监测和包内灭菌化学批示卡监测。
1.2.1化学指示胶带的监测法:将合格的化学指示胶带粘贴于每一待灭菌包的包外,灭菌后观察其颜色和形状的改变,达到规定的要求为合格。
1.2.2化学指示卡的监测方法:将合格的化学指示卡放入待灭菌包最难灭菌的部位,灭菌后,在无菌包检查或使用前,打开无菌包时先取出指示卡,观察其颜色和形状的改变,达到规定的要求为合格。
1.3生物监测法:应每周一次,根据灭菌器的类型选择代表性的标准生物测试包或嗜热脂肪杆菌芽胞(ATCC7953或SSIK31株)的指示管放在标准测试包(有16条全棉手术巾每条41cm*66cm,每条手术巾的长边先折成3层,短边折成2层,然后叠放,做成23cm*23cm*15cm大小的测试包)内,然后放在灭菌器排气口的上方,满载(快速灭菌器空锅时)后灭菌,灭菌后将嗜热脂肪杆菌芽胞的指示管送微生物试验室进行微生物培养,监测样品按规定培养阴性为合格,并设阳性对照。
1.4 B-D试验:每日开始灭菌运行前应进行B-D测试。
消毒与灭菌效果的评价方法与标准消毒与灭菌是保障公共卫生和个人健康的重要手段,而评价其效果的方法与标准则是确保消毒与灭菌工作质量的关键。
本文将介绍消毒与灭菌效果的评价方法与标准,以期为相关工作提供参考和指导。
一、微生物浓度检测法。
微生物浓度检测法是一种常用的评价消毒与灭菌效果的方法。
通过取样检测被消毒或灭菌的物品或场所中的微生物浓度,可以客观地评价消毒与灭菌的效果。
通常采用培养基培养法或PCR法进行微生物浓度检测,其中培养基培养法具有操作简便、成本低廉的特点,而PCR法则能够快速准确地检测微生物的DNA,具有高灵敏度和特异性。
二、生物指示剂法。
生物指示剂法是一种直接评价灭菌效果的方法。
通过将含有高浓度孢子的生物指示剂置于被灭菌物品或场所中,再进行灭菌处理,最后检测生物指示剂的存活情况,可以评价灭菌效果。
生物指示剂法具有直接、准确的特点,能够客观地评价灭菌效果,是一种常用的灭菌效果评价方法。
三、化学指标法。
化学指标法是一种通过检测消毒剂残留量评价消毒效果的方法。
通过检测消毒剂在被消毒物品或场所中的残留量,可以客观地评价消毒效果。
常用的消毒剂残留检测方法包括高效液相色谱法、气相色谱法等,这些方法能够准确地检测各种消毒剂的残留量,为评价消毒效果提供了可靠的依据。
消毒与灭菌效果的评价标准主要包括国家标准、行业标准和企业标准。
国家标准是指国家制定的关于消毒与灭菌效果评价的标准,具有普适性和权威性;行业标准是指某个行业制定的关于消毒与灭菌效果评价的标准,具有针对性和实用性;企业标准是指某个企业制定的关于消毒与灭菌效果评价的标准,具有针对性和操作性。
这些评价标准为消毒与灭菌效果的评价提供了具体的指导和要求,有助于保障消毒与灭菌工作的质量。
在实际工作中,需要根据被消毒或灭菌物品的特点和使用要求,选择合适的评价方法和标准,并严格执行,以确保消毒与灭菌效果的可靠性和有效性。
同时,还应定期对消毒与灭菌效果进行评价,及时调整消毒与灭菌措施,确保工作质量和效果。
一、手和皮肤黏膜消毒效果监测
1、采样时间:在消毒后立即采样。
2、采样方法
(1) 手的采样:被检人五指并拢,用浸有含相应中和剂的无菌洗脱液的棉拭子在双手指屈面从指根到指端往返涂擦 2 次(一只手涂擦面积约 30cm2),并随之转动采样棉拭子,剪去操作者手接触部位,将棉拭子投入 10ml 含相应中和剂的无菌洗脱液试管内,立即送检。
(2) 皮肤粘膜采样:用 5cm×5cm 的标准灭菌规格板,放在被检皮肤处,用浸有含相应中和剂的无菌洗脱液的棉拭子 1 支,在规格板内横竖往返均匀涂擦各 5 次,并随之转动棉拭子,剪去手接触部位后,将棉拭子投入 10ml 含相应中和剂的无菌洗脱液的试管内,立即送检。
不规则的粘膜皮肤处可用棉拭子直接涂擦采样。
3、检测方法
(1) 细菌总数检测:将采样管在混匀器上振荡20s或用力振打 80 次,用无菌吸管吸取 1.0ml 待检样品接种于灭菌平皿,每一样本接种2个平皿,内加入已溶化的45℃~48℃的营养琼脂 15ml~18ml,边倾注边摇匀,待琼脂凝固,置 36℃±1℃温箱培养 48h,计数菌落数。
采样结果计算方法:
平板上菌落数 ×稀释倍数
细菌总数(cfu/cm2)=────────────────
采样面积(cm2)
(2) 致病菌检测:致病菌的检测依据污染情况进行相应指标检测的原则执行。
4、结果判定
(1) 消毒洗手
Ⅰ、Ⅱ类区域工作人员:细菌总数≤5cfu/cm2,并未检出金黄色葡萄球菌、大肠杆菌、铜绿假单孢菌为消毒合格。
Ⅲ类区域工作人员:细菌总数≤10cfu/cm2,并未检出金黄色葡萄球菌、大肠杆菌为消毒合格。
Ⅳ类区域工作人员:细菌总数≤15cfu/cm2,并未检出金黄色葡萄球菌、大肠杆菌为消毒合格。
母婴同室、婴儿室、新生儿室及儿科病房的工作人员手上,不得检出沙门菌、大肠杆菌、溶血性链球菌、金黄色葡萄球菌为消毒合格。
(2)皮肤黏膜:参照手的卫生学标准执行。
5、注意事项
皮肤粘膜采样处,若表面不足 5cm×5cm 可用相应面积的规格板采样。
二、物品和环境表面消毒效果的监测
1、采样时间:在消毒处理后进行采样。
2、采样方法:用 5cm×5cm 的标准灭菌规格板,放在被检物体表面,采样面积
≥100cm2,连续采样 4 个,用浸有含相应中和剂的无菌洗脱液的棉拭子 1 支,在规格板内横竖往返均匀涂擦各 5 次,并随之转棉拭子,剪去手接触部位后,将棉拭子投入 10ml含相应中和剂的无菌洗脱液试管内,立即送检。
门把手等不规则物体表面用棉拭子直接涂擦采样。
3、检测方法
(1) 细菌总数检测:检测方法将采样管在混匀器上振荡20s或用力振打 80 次,用无菌吸管吸取 1.0ml 待检样品接种于灭菌平皿,每一样本接种2个平皿,内加入已溶化的 45℃~48℃的营养琼脂 15ml~18ml,边倾注边摇匀,待琼脂凝固,置36℃±1℃温箱培养 48h,计数菌落数。
小型物体表面的结果计算,用 cfu/件表示。
(2) 致病菌检测:致病菌的检测依据污染情况进行相应指标检测的原则执行。
4、结果判定
Ⅰ、Ⅱ类区域:细菌总数≤5cfu/cm2,并未检出致病菌为消毒合格。
Ⅲ类区域细菌:总数≤10cfu/cm2,并未检出致病菌为消毒合格。
Ⅳ类区域细菌:总数≤15cfu/cm2,并未检出致病菌为消毒合格。
母婴同室、早产儿室、婴儿室、新生儿室及儿科病房的物体表面不得检出沙门菌。
5、注意事项
(1) 采样时间:在灭菌处理后,存放有效期内采样。
(2) 样本量及处理:按消毒技术规范3.17.5.2(1)执行。
三、空气消毒效果的监测
1、采样时间:在消毒处理后、操作前进行采样。
2、采样方法:平板暴露法
(1) 布点方法:室内面积≤30m2,设内、中、外对角线3点,内、外点布点部位距墙壁1M处;室内面积>30m2,设 4 角及中央 5 点,4 角的布点部位距墙壁 1m 处。
(2) 采样方法:将普通营养琼脂平板(直径为 9cm)放在室内各采样点处,采样高度为距地面 1.5m 采样时将平板盖打开,扣放于平板旁,暴露 5min,盖好立即送检。
3、检测方法:按照消毒技术规范2.1.3要求进行。
平板暴露法结果计算公式:
细菌总数(cfu/m3)=50000N/(A × T)
式中A为平板面积(cm2);T为平板暴露时间(min);N为平均菌落数(cfu)。
4、结果判定
Ⅰ类区域:细菌总数≤10cfu/m3(或0.2cfu/平板),未检出金黄色葡萄球菌、溶血性链球菌为消毒合格;
Ⅱ类区域:细菌总数≤200cfu/m3(或4cfu/平板),未检出金黄色葡萄球菌、溶血性链球菌为消毒合格;
Ⅲ类区域:细菌总数≤500cfu/m3(或10cfu/平板),未检出金黄色葡萄球菌、溶血性链球菌为消毒合格。
5、注意事项
采样前,关好门、窗,在无人走动的情况下,静止10min 进行采样。
四、医疗器械灭菌效果的监测
1、采样时间: 在灭菌处理后,存放有效期内采样。
2、无菌检验
无菌检验是指检查经灭菌的敷料、缝线、一次性使用的医疗用品、无菌器械以及适合于无菌间查的其它品种是否无菌的一种方法。
无菌检验应在洁净度为100级单向流空气区域内进行,应严格遵守无菌操作,避免微生物污染;对单向流空气区域及工作台面,必须进行洁净度验证。
(1)无菌检验前准备
1)洗脱液与培养基无菌性试验:无菌试验前 3d,于需-厌养培养基与霉菌培养基内各接种 1ml 洗脱液,分别置 30℃~35℃与 20℃~25℃培养 72h,应无菌生长。
2)阳性对照管菌液制备:
①在试验前一天取金黄色葡萄球菌[CMCC(B)26003]的普通琼脂斜面新鲜培养物,接种1环至需-厌氧培养基内,在 30℃~35℃培养 16h~18h 后,用0.9%无菌氯化钠溶液稀释至10 cfu/ml~100cfu/ml;
②取生孢梭菌[CMCC(B)64941]的需氧菌、厌氧菌培养基新鲜培养物1接种环种于相同培养基内,于30℃~35℃培养 18h~24h后,用0.9%无菌氯化钠溶液稀释至
10 cfu/ml~100cfu/ml;
③取白色念珠菌[CMCC(F)98001]真菌琼脂培养基斜面新鲜培养物1接种环种于相同培养基内,于20℃~25℃培养 24h后,用0.9%无菌氯化钠溶液稀释至
10cfu/ml~100cfu/ml。
(2)无菌操作: 取缝合针、针头、刀片等小件医疗器械5件直接浸入 6 管需-厌氧培养管(其中一管作阳性对照)与 4 管霉菌培养管。
培养基用量为 15ml/管。
1)取5付注射器,在 5ml 洗脱液中反复抽吸 5 次,洗下管内细菌,混和后接种需-厌养菌培养管(共 6 管,其中 1 管作阳性对照)与霉菌培养管(共 4 管)。
接种量:1ml注射器为 0.5ml,2ml注射器为 1ml,5ml~10ml 注射器为 2ml,20ml~50ml 注射器为 5ml,培养基用量:接种量为 2ml 以下为 15ml/管,接种量5ml为 40ml/管。
2)手术钳、镊子等大件医疗器械取 2 件用沾有无菌洗脱液的棉拭子反复涂抹采样,将棉拭子投入 5ml 无菌洗脱液中,将采样液混匀,接种于需-厌氧培养管(共6 管,其中 1 管作阳性对照)与霉菌培养基(共 4 管)。
接种量为 1ml/管,培养基用量为 15ml/管。
(3)培养:在待检样品的需-厌氧培养管中,接种预先准备的金黄色葡萄球菌阳性对照管液 1:1000 稀释 1ml,将需-厌氧培养管以及阳性与阴性对照管均于 30℃~35℃培养 5d,霉菌培养管与阴性对照管于 20℃~25℃培养 7d,培养期间逐日检查是否有菌生长,如加入供试品后培养基出现混浊或沉淀,经培养后不能从外观上判断时,可取培养液转种入另一支相同的培养基中或斜面培养基上,培养 48h ~72h 后,观察是否再现混浊或在斜面上有无菌落生长,并在转种的同
时,取培养液少量,涂片染色,用显微镜观察是否有菌生长。
(4)结果判定:阳性对照在 24h 内应有菌生长,阴性对照在培养期间应无菌生长,如需-厌氧菌及霉菌培养管内均为澄清或虽显混浊但经证明并非有菌生长,判为灭菌合格;如需-厌氧菌及霉菌培养管中任何1管显混浊并证实有菌生长,应重新取样,分别同法复试 2 次,除阳性对照外,其他各管均不得有菌生长,否则判为灭菌不合格。
3、注意事项
(1)送检时间不得超过 6h,若样品保存于 0℃~4℃,则不得超过24h。
(2)被采样本表面积<100cm2取全部表面;被采样本表面积≥100cm2,取
100cm2。
(3)若消毒因子为化学消毒剂,采样液中应加入相应中和剂。