第12章 醛和酮 亲核加成 共轭加成
- 格式:ppt
- 大小:1.86 MB
- 文档页数:93

醛和酮 亲核加成反应一、基本要求1.掌握醛酮的命名、结构、性质;醛酮的鉴别反应;不饱和醛酮的性质 2.熟悉亲核加成反应历程及其反应活性规律;醛酮的制备二、知识要点(一)醛酮的分类和命名(二)醛酮的结构:醛酮的官能团是羰基,所以要了解醛酮必须先了解羰基的结构。
C=O 双键中氧原子的电负性比碳原子大,所以π电子云的分布偏向氧原子,故羰基是极化的,氧原子上带部分负电荷,碳原子上带部分正电荷。
(三)醛酮的化学性质醛酮中的羰基由于π键的极化,使得氧原子上带部分负电荷,碳原子上带部分正电荷。
氧原子可以形成比较稳定的氧负离子,它较带正电荷的碳原子要稳定得多,因此反应中心是羰基中带正电荷的碳。
所以羰基易与亲核试剂进行加成反应(亲核加成反应)。
此外,受羰基的影响,与羰基直接相连的α-碳原子上的氢原子(α-H )较活泼,能发生一系列反应。
亲核加成反应和α-H 的反应是醛、酮的两类主要化学性质。
1.羰基上的亲核加成反应醛,酮亲核加成反应的影响因素:羰基碳上正电性的多少有关,羰基碳上所连的烃基结构有关,亲核试剂的亲核性大小有关。
(1)与含碳的亲核试剂的加成 ○1氰氢酸: ○2 炔化物COC O H C H O 121.8116.5。
sp 2杂化键键近平面三角形结构πσC C RO H H ( )δδ酸和亲电试剂进攻富电子的氧碱和亲核试剂进攻缺电子的碳涉及醛的反应 氧化反应( )αH 的反应羟醛缩合反应卤代反应C O C OH+ HCN CN 羟基睛α○3 有机金属化合物:(2)与含氮的亲核试剂的加成 ○11o 胺 ○2 2o 胺 ○3氨的多种衍生物:(3)与含硫的亲核试剂的加成-------亚硫酸氢钠产物α-羟基磺酸盐为白色结晶,不溶于饱和的亚硫酸氢钠溶液中,容易分离出来;与酸或碱共热,又可得原来的醛、酮。
故此反应可用以提纯醛、酮。
反应范围: 醛、甲基酮、八元环以下的脂环酮。
反应的应用:鉴别化合物,分离和提纯醛、酮。


有机化学基础知识点整理醛和酮的亲核加成反应有机化学基础知识点整理:醛和酮的亲核加成反应亲核加成反应是有机化学中常见的反应类型之一,醛和酮作为常见的碳酸酯化合物,也会参与到亲核加成反应当中。
本文将对醛和酮的亲核加成反应进行整理和归纳,以帮助读者更好地理解和掌握这一反应过程。
一、醛和酮的亲核加成反应基础概念亲核加成反应是指一个亲核试剂(如醇、胺等)的亲电中心攻击碳酰基(醛或酮)的羰基碳,形成一个新的共价键。
醛和酮的亲核加成反应一般可以分为醛酮亲核加成反应和酮酮亲核加成反应两类。
二、醛酮亲核加成反应1. 醛酮与缩合试剂的反应醛酮与缩合试剂(如水合肼和氨等)反应时,会经历酮缩反应,生成相应的醇和胺。
2. 醛酮与氰基试剂的反应醛酮与氰基试剂(如氢氰酸和氰化物等)反应时,会生成相应的羟基腈和氨基腈。
3. 醛酮与硫醇试剂的反应醛酮与硫醇试剂(如氢硫酸和硫化钠等)反应时,会生成相应的硫醇和亚硫酸盐。
三、酮酮亲核加成反应1. 酮酮与亲核试剂的反应酮酮与亲核试剂(如胺、醇等)反应时,会经历亲核加成反应,生成相应的醇和胺。
2. 酮酮与腈试剂的反应酮酮与腈试剂(如氰化物和亚氨基甲酸酯等)反应时,会生成相应的羟基腈。
3. 酮酮与水试剂的反应酮酮与水试剂反应时,会经历水解反应,生成相应的醇。
四、醛和酮的亲核加成反应机理醛和酮的亲核加成反应机理主要涉及亲核试剂的亲电攻击和质子迁移等步骤。
在醛酮亲核加成反应中,亲核试剂的亲电攻击会使羰基碳中的空本电子对与亲核试剂的亲电中心形成共价键。
此后,质子迁移会重新确定醛或酮中的羰基碳骨架。
在酮酮亲核加成反应中,亲核试剂的亲电攻击同样会使羰基碳中的空本电子对与亲核试剂的亲电中心形成共价键。
在这种情况下,质子迁移通常不会发生,因为酮中存在两个相邻的碳酰基。
五、总结醛和酮的亲核加成反应是有机化学中重要而常见的反应类型。
理解和掌握醛和酮的亲核加成反应对于有机化学的学习至关重要。
本文对醛酮和酮酮亲核加成反应进行了整理和概述,为读者提供了一定的参考和指导。



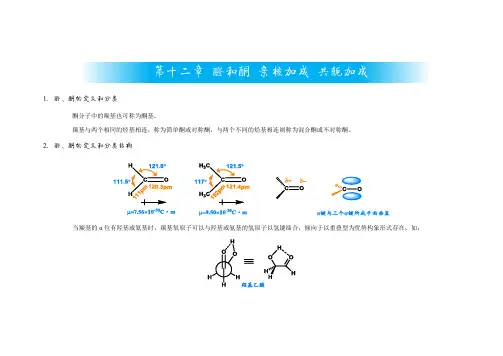
1. 醛、酮的定义和分类酮分子中的羰基也可称为酮基。
羰基与两个相同的烃基相连,称为简单酮或对称酮,与两个不同的烃基相连则称为混合酮或不对称酮。
2. 醛、酮的定义和分类结构当羰基的α位有羟基或氨基时,羰基氧原子可以与羟基或氨基的氢原子以氢键缔合,倾向于以重叠型为优势构象形式存在,如:第十二章 醛和酮 亲核加成 共轭加成3.醛、酮的物理性质由于羰基的偶极矩增加了分子间的吸引力,因此醛、酮的沸点比相应相对分子质量的烷烃高,但比醇低。
醛酮的氧原子可以与水形成氢键,因此低级醛酮能与水混溶(甲醛易溶于水,丙酮能与水以任意比例互溶,乙醛的溶解度为16g(100g H2O)-1)。
脂肪族醛酮相对密度小于1,芳香族醛酮相对密度大于1。
4.醛、酮的反应(1)羰基的亲核加成由于电子效应和空间位阻的原因,醛比酮表现的更活泼。
1)和含碳亲核试剂的加成①与有机金属化合物的加成此反应仅限于酮的烃基和格氏试剂的烃基都不太大,即空间位阻不很突出。
否则将发生两种“不正常”的反应:烯醇化反应及酮被还原。
烷基锂体积较小,因此当格氏试剂反应结果不好时,有时可以用烷基锂进行反应,会得到较好的结果,因此,格氏试剂与烷基锂可以相互补充。
当羰基与一个手性中心相连时,它与格氏试剂(也包括氢化铝锂等试剂)反应就是一个手性诱导反应。
亲核加成反应遵循Cram规则一,即:亲核试剂从空间位阻较小的一边进攻羰基碳原子。
为什么R与L取重叠型构象?因为这些试剂与羰基发生加成反应时,它们的金属部分须与羰基氧络合,因此羰基氧原子一端位阻增大,α碳上最大基团(L)与羰基处于反式,故R与L取重叠型构象为最有利于反应的构象。
②与HCN的加成丙酮与氢氰酸在氢氧化钠的水溶液中反应,生成丙酮羟腈,然后和甲醇在硫酸的作用下,即发生失水及腈的醇解反应,氰基变成甲氧酰基(-COOCH3):工业上就是利用这个反应步骤合成有机玻璃的。
碱性条件能加速该反应,这是由于氢氰酸是弱酸,其离解很少,[CN-]浓度很低,当加入NaOH时,碱与H+ 结合促使离解平衡右移,使亲核性的增大,但是碱性不能太强,因为最后还需要H+才能完成反应。
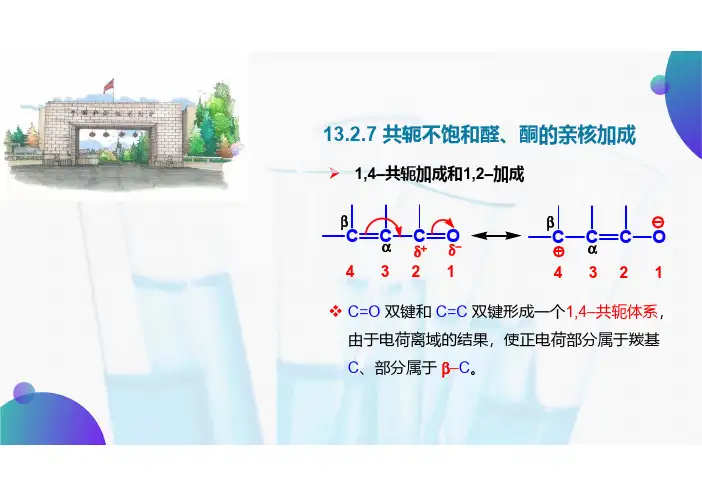
13.2.7 共轭不饱和醛、酮的亲核加成1,4–共轭加成和1,2–加成C=O 双键和C=C 双键形成一个1,4–共轭体系,由于电荷离域的结果,使正电荷部分属于羰基C 、部分属于β–C 。
CC C O δ−δ+βCCC Oβα4 3 2 1 4 3 2 1CC C O4 3 2 1α+ :Nu C C C ONu1,2-H+C C C OHNuC C C O HNuC C C ONu H烯醇式酮式:异构酸性条件下的1,4 –共轭加成反应机理:与水、胺、醇、硫醇等加成:CC C OC C C OHC C C OH烯醇式ZC C C OZH酮式Z:C C C OH H +4 3 2 1碱性条件下的1,4 –共轭加成反应机理:与有机金属化合物、CN –等加成:HOHC C C OHNu 烯醇式Nu C CC OH酮式-OHC C C OC C C ONu 4 3 2 1亲核加成是以1,4–加成为主,还是以1,2–加成为主?取决于:a)C=O 和C=C 上取代基空间位阻的相对大小——如果羰基上连有较大的基团,则以1,4–加成为主。
b)亲核试剂:Nuϴ的亲核性大小——亲核性强的:Nuϴ倾向于进攻C=O,进行1,2–加成。
α,β–不饱和醛酮发生加成反应时的选择规律:①HX、HCN、NH3及NH3的衍生物、ROH、RSH等(亲核性较弱)与α,β–不饱和醛酮的加成以1,4–共轭加成为主。
O+ RNH2OHNHR ONHR③R 2CuLi 、CdR 2(空间位阻大,亲核性相对较弱)与α,β–不饱和醛酮反应,以1,4–加成为主。
②RLi 与α,β–不饱和醛酮反应时以1,2–亲核加成为主。
PhPhO+ PhLiPhPh OH PhH 2OO+ (CH 3)2CuLiOH 2OCH 3etherPhHO1,2-加成,100%21,2-加成,100%(E)-3-苯基-2-丁烯醛PhPh OHPhOH(E)-3-phenylacrylaldehyded)RMgX 与α,β–不饱和醛加成时,以1,2–亲核加成为主;而与α,β–不饱和酮反应,则视反应物的空间结构(羰基C 原子上的基团大小和格氏试剂烃基大小)而定,空间位阻小的地方易发生反应。

有机化学基础知识点整理醛和酮的亲核加成和还原反应机理有机化学基础知识点整理醛和酮的亲核加成和还原反应机理一、引言有机化学是研究碳元素和碳以及其他元素之间的化学反应的学科。
在有机化学中,醛和酮是常见的官能团,其具有亲核加成和还原反应机理。
本文将对醛和酮的亲核加成和还原反应机理进行整理。
二、醛和酮的亲核加成反应1. 亲核加成反应定义亲核加成反应是指亲核试剂中的亲核试剂从反应中代替醛或酮中的部分或全部官能团的过程。
该反应常见的亲核试剂有:醇、胺、氨等。
2. 亲核加成反应机理(1)亲核试剂攻击羰基碳亲核试剂通过其自由电子对攻击醛或酮中的碳,形成一个五元环中的过渡态。
(2)五元环的形成亲核试剂中的亲核部分攻击羰基碳后,将剩余的电子通过共轭转向氧原子上,形成五元环中的过渡态。
(3)负电荷的转移氧原子上的负电荷转移到亲核试剂的负电荷上,亲核试剂离开后,得到最终产物。
三、醛和酮的还原反应1. 还原反应定义还原反应是指通过还原剂将醛或酮中的羰基还原成相应的醇。
常用的还原剂有:氢气、亚磷酸酯等。
2. 还原反应机理(1)氢化钠和水的生成还原剂与醛或酮中的羰基发生反应,生成相应的醇官能团。
(2)还原剂的失去电子还原剂通过失去电子的方式与醛或酮中的羰基发生反应,形成相应的醇官能团。
(3)中间物的形成中间物形成后,通过质子转移的方式,生成最终的醇产物。
四、示例以丙酮和甲醛为例,说明醛和酮的亲核加成和还原反应机理。
1. 丙酮的亲核加成反应以氯乙烷为亲核试剂,攻击丙酮中的碳,形成五元环过渡态。
氯离子离开后,得到丙酮和氯乙烷反应生成的产物。
2. 甲醛的还原反应以氢气和铜催化剂为还原剂,发生还原反应。
氢氧化钠作为碱催化剂。
甲醛经过还原反应后,得到甲醇作为最终产物。
五、结论本文对醛和酮的亲核加成和还原反应机理进行了整理。
醛和酮的亲核加成反应通过亲核试剂攻击羰基碳,形成五元环过程实现。
而醛和酮的还原反应则是通过还原剂将羰基还原成相应的醇官能团。
第12章醛和酮亲核加成共轭加成一、选择题1.下列化合物中,不能发生碘仿反应的是()。
[天津大学2000研]【答案】B【解析】若醛或酮分子中含有多个-Hα都可以被卤素取代,生成各种多α,则这些-H卤代物,若果含有三个-Hα,则可卤代生成三卤衍生物,所生成的三卤衍生物在碱性溶液中易分解为三卤甲烷(俗称卤仿),这就是卤仿反应。
故只有含有或能被次卤酸钠氧化而成CH3CO结构的化合物才能发生卤仿反应。
2.的主要产物是()。
[武汉大学2001研]【答案】A【解析】醛、酮分子中的α-H具有酸性。
在碱性条件下,碱先夺取α-H,生成烯醇负离子,卤素再对C=C加成,发生取代反应。
3.有一羰基化合物,分子式为C5H100,核磁共振谱只有两个单峰,其结构式是()。
[中国科学院-中国科学技术大学2003研]【答案】C【解析】该化合物的核磁共振谱只有两个单峰,说明分子中只有两种不等性氢原子且彼此间无偶合现象。
4.从库房领来的苯甲醛,瓶口常有一些白色固体,该固体为()。
[中国科学院-中国科学技术大学2003研]A.苯甲醛聚合物B.苯甲醛过氧化物C.苯甲醛与C02反应产物D.苯甲酸【答案】D【解析】苯甲醛易被空气氧化,生成苯甲酸。
5.下列化合物分别与HCN反应,()的活性最大。
[大连理工大学2004研]【答案】B【解析】羰基碳缺电子程度越高,其亲电性越强,越易发生亲核加成反应。
Cl为吸电子基,使羰基碳电子云密度减小。
6.指出下列反应中何者为主要产物?()[清华大学2000研]【答案】(A)【解析】从空间位阻较小的方向进攻羰基碳。
二、填空题1.。
[南京大学2001研]【答案】PhCH2OH【解析】无活泼α-H的醛在碱性条件下可发生Cannizzaro反应,有甲醛时,一般是甲醛被氧化,而另一醛被还原,发生“交错”的Cannizzaro反应。
2.。
[中国科学院-中国科学技术大学2001研]【答案】【解析】醛或酮与锌汞齐和浓盐酸一起加热,羰基被还原成亚甲基;醛或酮与氢化铝锂反应,羰基被还原为醇羟基。