有机化合物的吸收光谱及溶剂的影响
- 格式:pdf
- 大小:215.58 KB
- 文档页数:4


有机化合物的紫外吸收光谱及溶剂的影响
一.实验目的和要求
1.了解双光束紫外-可见分光光度计的仪器构造和使用。
2.学习紫外吸收光谱的绘制方法。
3.了解溶剂的性质对同一种物质的吸收光谱的影响。
二.实验原理
苯具有环状共轭体系,在紫外区有三个吸收谱带:E1带、E2带和B带,这些吸收带都是π→π*电子跃迁产生的。
当苯环上的氢被助色团取代后,苯的吸收光谱会发生变化:E2吸收带向长波方向移动,复杂的B吸收带变得简单化。
溶剂对紫外吸收光谱的吸收峰的波长、强度及形状都可能产生影响,这种现象被称为溶剂效应。
造成这种影响的原因是溶剂和溶质间形成氢键,也可能是由于溶剂的偶极作用使溶质的极性增强。
三.仪器与试剂
仪器:TU-1901双光束紫外-可见分光光度计,1 cm石英吸收池。
试剂:邻甲苯酚,HCl, NaOH,无水乙醇。
四.实验内容与步骤
1.溶剂性质对吸收光谱的影响
配制浓度为12.5 mg L-1的邻甲苯酚溶液,其溶剂分别为(a)无水乙醇;(b)0.1 mol L-1HCl;(c)0.1 mol L-1NaOH,
摇匀。
用1 cm石英吸收池,以相应的溶剂作参比,绘制各溶液在200-400 nm范围内的吸收光谱。
五.数据处理
1.记录各邻甲苯酚溶液的吸收光谱。
2.找出各邻甲苯酚溶液的吸收光谱的最大吸收波长,并与邻甲苯酚-无水乙醇溶液的吸收峰进行比较。
六.思考题
1.产生紫外光谱的电子跃迁有那些类型?2.影响紫外吸收光谱的因素有哪些?。

西昌学院仪器分析实验报告试验项目名称:苯的紫外吸收光谱的测绘及溶剂对紫外吸收光谱影响实验序号:02 指导教师:陶明学生姓名:封德军年级专业:化学学号:1004010026 日期:2012/6/7一、实验目的:1、了解不同极性的溶剂对有机化合物紫外吸收光谱的影响。
2、学习掌握TV—1901紫外—可见分光光度计的使用方法。
二、实验原理:1、具有不饱和结构的有机化合物特别是芳香族化合物在紫外区(200—400nm)有特征吸收,为鉴定有机化合物提供有效信息。
2、改变溶剂的极性,会对紫外—可见光谱产生影响,引起吸收带形状和吸收峰伴随苯环上取代基的不同而发生位移。
三、实验步骤:1、苯的吸收光谱的绘制:①在1cm的石英比色皿中加入2滴苯加盖用手温热底部;②在紫外可见分光光度计上用石英空白比色皿做参照,从220—360nm范围内扫描的光谱图③将光谱图保存2、溶剂性质对紫外吸收光谱的影响:①在三支25mL的容量瓶中各加入一滴丁酮,分别用水、乙醇氯仿稀释至刻度线、摇匀②将其依次加入石英比色皿中,分别用各自溶剂做参照,并在220——360nm 波长中扫描制的吸收光谱③对吸收光谱保存并求得最大吸收波长。
四、实验仪器及试剂①仪器:TV—1901紫外—可见分光光度计、25mL容量瓶、吸量管等。
②试剂:苯、乙醇、丁酮、等。
五、实验数据处理及见附页。
实验结果:1、在苯的吸收光谱中可以看出笨的最大吸收波长及苯的特征吸收峰2、在不同溶剂中丁酮的吸收光谱大致相同,但不同试剂时,最大吸收波长也在发生变化,从图中可以看出随着溶剂极性的增大最大吸收波长在增大。
六、思考题:、1、实验中不能用玻璃比色皿,因为玻璃会吸收紫外光;加盖是因为苯沸点低极易挥发。
2、εmax与待测溶液的浓度溶剂的极性有关。
3、不能用水代替,因为水的极性与其他溶剂不同。




实验九有机化合物的紫外吸收光谱及溶剂效应实验目的:(1)学习有机化合物结构与其紫外光谱之间的关系;(2)了解不同极性溶剂对有机化合物紫外吸收带位置、形状及强度的影响。
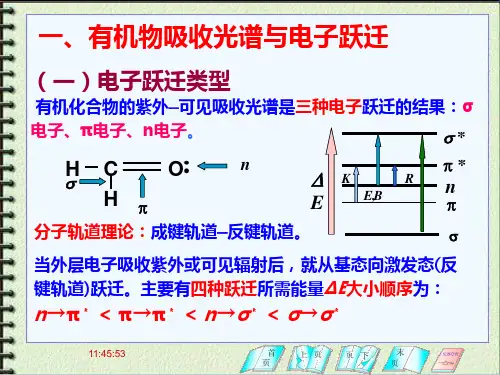
(3)学习紫外—可见分光光度计的使用方法实验原理:与紫外-可见吸收光谱有关的电子有三种,即形成单键的σ电子、形成双键的π电子以及未参与成键的n电子。
跃迁类型有:σ→σ*,n→σ* ,n→π*,π→π* 四种。
在以上几种跃迁中,只有π-π*和n-π*两种跃迁的能量小,相应波长出现在近紫外区甚至可见光区,且对光的吸收强烈,是我们研究的重点。
影响有机化合物紫外吸收光谱的因素有内因和外因两个方面。
内因是指有机物的结构,主要是共轭体系的电子结构。
随着共轭体系增大,吸收带向长波方向移动(称作红移),吸收强度增大。
紫外光谱中含有π键的不饱和基团称为生色团,如有C=C、C=O、NO2、苯环等。
含有生色团的化合物通常在紫外或可见光区域产生吸收带;含有杂原子的饱和基团称为助色团,如OH、NH2、OR、Cl等。
助色团本身在紫外及可见光区域不产生吸收带,但当其与生色团相连时,因形成n→π*共轭而使生色团的吸收带红移,吸收强度也有所增加。
影响有机化合物紫外吸收光谱的外因是指测定条件,如溶剂效应等。
所谓溶剂效应是指受溶剂的极性或酸碱性的影响,使溶质吸收峰的波长、强度以及形状发生不同程度的变化。
这是因为溶剂分子和溶质分子间可能形成氢键,或极性溶剂分子的偶极使溶质分子的极性增强,从而引起溶质分子能级的变化,使吸收带发生迁移。
例如异丙叉丙酮的溶剂的溶剂效应如表1所示。
随着溶剂极性的增加K带红移,而R带向短波方向移动(称作蓝移或紫移)。
这是因为在极性溶剂中π→π * 跃迁所需能量减小,吸收波长红移(向长波长方向移动)如图(a)所示;而n→π * 跃迁所需能量增大,吸收波长蓝移(向短波长方向移动),溶剂效应示意图如(b)所示。
图1 电子跃迁类型σπ *σ *nπ∆C*—C-△E n>△E p C=0 △E n>△E p图2溶剂极性效应(a)π→π * 跃迁(b)n→π * 跃迁B吸收带,在不同极性溶剂中,其强度和形状均受到影响、在非极性溶剂正庚烷中,可清晰看到苯酚B吸收带的精细结构,但在极性溶剂乙醇中,苯酚B吸收带的精细结构消失,仅存在一个宽的吸收峰,而且其吸收强度也明显减弱。

实验一有机化合物的紫外吸收光谱及溶剂性质对吸收光谱的影响一、实验目的:1、熟练紫外—可见分光光度计的操作。
2、学习利用紫外吸收光谱检查物质的纯度的原理和方法。
3、掌握溶剂极性对跃迁,跃迁的影响二、仪器与试剂1、仪器730型紫外—可见分光光度计,带盖石英吸收池1cm 2只。
2、试剂(1 苯、乙醇、正己烷、氯仿、丁酮。
(2 异亚丙基丙酮:分别用水、氯仿、正已烷配成浓度为0.4g/L溶液。
二、实验原理具有不饱和结构的有机化合物,如芳香族化合物,在紫外区(200~400nm有特征的吸收,为有机化合物的鉴定提供了有用的信息。
紫外吸收光谱定性的方法是比较未知物与已知纯样在相同条件下绘制的吸收光谱,或将绘制的未知物吸收光谱与标准谱图(如Sadtler紫外光谱图相比校,若两光谱图的和相同,表明它们是同一有机化合物。
极性溶剂对有机物的紫外吸收光谱的吸收峰波长、强度及形状有一定的影响。
溶剂极性增加,使跃迁产生的吸收带蓝移,而跃迁产生的吸收带红移。
影响有机化合物紫外吸收光谱的因素,有内因(分子内的共轭效应、位阻效应、助色效应等和外因(溶剂的极性、酸碱性等溶剂效应由于受到溶剂极性和酸碱性的影响,将使溶质的吸收峰的波长、强度以及形状发生不同程度的变化,这是因为溶剂分子和溶质分子之间可能形成氢键,使极性溶剂分子的偶极减弱,溶质分子的极性增强,因而在极性溶剂中跃迁所需的能量减小,吸收波长红移,而在极性溶剂中所需能量增大,吸收波长蓝移,由于物质的紫外吸收光谱是物质分子中生色团和助色团的贡献,也是物质整个分子的特征表现。
例如具有键电子的共轭双键化合物、芳香烃化合物等,在紫外光谱区都有强烈吸收,其摩尔吸光系数可达104~105数量级,这与饱和烃化物有明显的不同。
利用这一特性,可以很方便地检查纯饱和烃化物中是否含有共轭双键、芳香烃等化合物杂质。
三、实验步骤1、苯的吸收光谱的测绘在1cm的石英吸收池中,加入两滴苯,加盖,用手心温热吸收池底部片刻,在紫外分光光度计上,以空白石英吸收池为参比,从220~360nm范围内进行波长扫描,绘制吸收光谱。

1 有机化合物的紫外吸收光谱及溶剂性质对吸收光谱的影响一 实验原理具有不饱和结构的化合物,在紫外区(200~400nm )可能有特征吸收,为有机化合物的结构鉴定提供一定的信息。
紫外吸收光谱可用于某些物质的定性,定性的方法是比较未知物与已知纯物质在相同条件下的吸收光谱,如两物质的吸收光谱的形状一样,且λmax 和 κmax 相同,表明它们是同一物质。
溶剂的极性对有机化合物的吸收光谱的形状、λmax 和 κmax 有一定的影响。
溶剂极性增加,使*π→n 跃迁的吸收带蓝移,而*ππ→跃迁的吸收带红移。
二 仪器与试剂1 主要仪器 紫外吸收分光光度计1台(自己记录仪器的型号、名称和生产厂家);2 试剂 苯、乙醇、正己烷、丁酮、异亚丙基丙酮丙酮溶液:分别用水、乙醇和正己烷配制一定浓度的丙酮溶液,在λmax 的吸光度A 控制在1.5以内。
异亚丙基丙酮溶液:分别用水、乙醇和正己烷配制一定浓度的异亚丙基丙酮溶液浓度不同的2份,使在强吸收带的λmax 的吸光度A 控制在1.5以内,在弱吸收带的λmax 的吸光度A 控制0.5左右。
三 实验步骤1 苯的吸收光谱的绘制在1cm 的石英比色皿中滴入1滴苯,加盖,在紫外分光光度计上,用空白石英比色皿为参比,从200~400nm 范围内扫描吸收光谱曲线。
观察苯的E 2吸收带和B 吸收带(五指峰),并记录峰值的波长。
2 乙醇中微量苯的检测用1cm 的石英比色皿,以乙醇为参比,在200~300nm 范围内扫描乙醇试样的吸收光谱(乙醇试样在乙醇中加入微量的苯),并确定是否存在苯的E 2吸收带和B 吸收带?3 溶剂性质对紫外吸收光谱的影响(1)丙酮的吸收光谱:用1cm 的石英比色皿,以各自的溶剂为参比,在200~350nm 波长范围内,分别扫描丙酮在三种不同溶剂中的吸收曲线。
并把三条吸收曲线叠加在同一张图中,记录它们的λmax ,说明电子跃迁类型,并比较它们的变化,并解释原因。
(2)异亚丙基丙酮的吸收光谱:用1cm 的石英比色皿,以各自的溶剂为参比,在200~350nm 波长范围内,分别扫描异亚丙基丙酮在三种不同溶剂中的吸收曲线。

实验八 有机化合物紫外吸收光谱及溶剂对其吸收光谱的影响一、实验目的:1、学习并掌握紫外-可见分光光度计的使用;2、了解不同的助色团对苯的紫外吸收光谱的影响;3、观察pH 对苯酚的吸收光谱的影响。
二、实验原理:具有不饱和结构的有机化合物,特别是芳香族化合物,在近紫外区(200~400nm )有特征的吸收,给鉴定有机化合物提供了有用的信息。
苯有三个吸收带,它们都是由*ππ→跃迁引起的,E 1带:11max 180(60000)nm L cm mol λε--==⋅⋅,E 2带:11max 204(8000)nm L cm mol λε--==⋅⋅,两者都属于强吸收带。
B 带出现在230~270nm ,其11max 254(200)nm L cm mol λε--==⋅⋅ 。
在气态或非极性溶剂中,苯及其许多同系物的B 带有许多精细结构,这是振动跃迁在基态电子跃迁上叠加的结果。
在极性溶剂中,这些精细结构消失。
当苯环上有取代基时,苯的三个吸收带都将发生显著的变化,苯的B 带显著红移,并且吸收强度增大。
溶剂的极性对有机物的紫外吸收光谱有一定的影响。
当溶剂的极性由非极性改变到极性时,精细结构消失,吸收带变平滑。
显然,这是由于未成键电子对的溶剂化作用降低了n 轨道的能量使*π→n 跃迁产生的吸收带发生紫移,而*ππ→跃迁产生的吸收带则发生红移。
影响有机化合物的紫外吸收光谱的因素有:内因(共轭效应、空间位阻、助色效应)和外因(溶剂的极性和酸碱性)。
溶剂的极性和酸碱性不仅影响待测物质吸收波长的移动,还影响吸收峰吸收强度和它的形状。
本实验重点在了解不同的助色团对苯的紫外吸收光谱的影响和观察pH 对苯酚的吸收光谱的影响。
三、仪器:紫外-可见分光光度计,带盖石英比色皿(1.0cm )。
四、试剂:苯、环己烷、0.1mol/L HCl 、0.1mol/L NaOH 、苯的环己烷溶液(1:250)、甲苯的环己烷溶液(1:250)、苯酚的环己烷溶液(0.3g/L )、苯酚的水溶液(0.4 g/L )。
实验八有机化合物紫外吸收光谱及溶剂对其吸收光谱的影响引言有机化合物的紫外吸收光谱是研究有机化合物结构特性和分子间相互作用的重要手段之一、溶剂的选择和使用对实验结果具有重要影响。
本实验旨在通过研究有机化合物在不同溶剂中的紫外吸收光谱,探究溶剂对其吸收光谱的影响。
实验部分1.实验仪器及试剂(1)实验仪器:紫外可见光谱仪(2)实验试剂:有机化合物溶液,常用溶剂(如乙醇、甲醇、二甲基甲酰胺等)2.实验步骤(1)取不同溶剂制备一系列浓度相同的有机化合物溶液,浓度通常选择在10-5mol/L以内。
(2)将每种溶液倒入光化学池中,分别记录它们的吸收光谱。
(3)将有机化合物的吸收峰波长和吸收强度记录在实验报告中。
实验结果及分析根据实验步骤所得吸收光谱数据,整理结果如下表所示:溶剂,吸收峰波长(nm) ,吸收强度:-------:,:------------:,:-------:乙醇,200,0.8甲醇,210,0.6二甲基甲酰胺,220,0.5从表中可以看出,不同溶剂中有机化合物的吸收峰波长和吸收强度存在差异。
这是因为溶剂分子在溶液中与有机化合物分子之间存在相互作用,会导致有机化合物分子的电子结构改变,从而影响其紫外吸收光谱。
对于吸收峰波长的差异,可以解释为溶剂对有机化合物分子的极性影响。
溶剂分子与有机化合物分子之间的相互作用是通过静电作用、氢键作用、范德华力等相互作用来实现的。
当溶剂为乙醇时,其分子极性较大,能够与有机化合物分子形成较强的相互作用,从而使有机化合物分子的电子结构发生改变,吸收峰波长红移。
当溶剂为甲醇时,其分子极性较乙醇小,与有机化合物分子的相互作用较弱,吸收峰波长相对乙醇红移。
当溶剂为二甲基甲酰胺时,分子极性最小,与有机化合物分子的相互作用最弱,吸收峰波长相对甲醇红移。
对于吸收强度的差异,可以解释为溶剂对有机化合物分子的溶解度和聚集状态的影响。
溶剂的极性和极性与非极性成分的比例可以影响有机分子的相对溶解度和聚集状态。
实验三有机化合物的吸收光谱及溶剂效应一、实验目的1.了解紫外可见分光光度计的结构及使用方法。
2.了解苯及其衍生物的紫外吸收光谱及鉴定方法。
3.观察溶剂对吸收光谱的影响。
二、实验内容1.未知有机化合物的鉴定。
2.溶剂对紫外吸收光谱的影响。
三、实验原理、方法和手段紫外吸收光谱、红外光谱、核磁共振波谱和质谱是有机结构解析的四大工具,尽管紫外吸收光谱谱带数目少,缺少精细结构,光谱的特征不强,但它在有机化合物结构鉴定中仍是一种有用的辅助手段,特别对于芳香族化合物,由于它在紫外区的特征吸收,给鉴定提供了有用的信息。
芳香族化合物的紫外光谱的特点是具有由π→π*跃迁产生的3个特征吸收带。
例如,苯在184nm附近有一个强吸收带,ε=68000;在204nm处有一较弱的吸收带,ε=8800;在254nm附近(或230~270nm)有一个弱吸收带,ε=250。
当苯处在气态时,这个吸收带具有很好的精细结构。
当苯环上带有取代基时,则强烈地影响苯的3个特征吸收带。
利用紫外吸收光谱鉴定有机化合物的方法是在相同的条件下,比较未知物与已知纯化合物的吸收光谱,或将未知物的吸收光谱与标准谱图(例如Sadtler紫外光谱图)对比,如果两者的吸收光谱完全一致,则可认为是同一种化合物。
四、仪器与试剂(一)仪器:紫外—可见分光光度计;比色管(带塞):5mL 10支,10mL 3支;移液管:lmL 6支,0.1mL 2支。
(二)试剂:苯、乙醇、环己烷、正己烷、氯仿、丁酮、异亚丙基丙酮。
溶液:HCl(0.1mol·L-1),NaOH(0.1mo1·L-1),苯的环己烷溶液(1:250),甲苯的环己烷溶液(1:250),苯的环己烷溶液(0.3g·L-1),苯甲酸的环己烷溶液(0.8g·L-1),苯胺的环己烷溶液(1:3000),苯酚的水溶液(0.4g·L-1)。
异亚丙基丙酮分别用水、氯仿、正己烷配成浓度为0.4g·L-1溶液。
有机化合物的吸收光谱及溶剂的影响一、目的要求
1.学习有机化合物结构与其吸收光谱之间的关系。
2.了解溶剂的性质对吸收光谱的影响。
3.学习紫外-可见分光光度计的使用方法。
三、原理
1、紫外吸收光谱的产生
紫外吸收光谱法是由于物质吸收了一定波长的紫外光引起分子中价电子能级跃迁而形成的一种分析方法。
不同物质分子中电子类型、分布和结构不同,紫外光谱就不同,因此紫外光谱可用于定性和结构分析。
有机分子中有几种不同性质的价电子:形成单键的σ电子、形成双键的π电子以及氧、氮等杂原子所含的未成键的n电子。
可能产生的主要电子跃迁以及所需能量大小持续如下:
σ→σ*>n→σ*≥π→π*>n→π*
其中,σ→σ*、n→σ*和孤立双键的π→π*跃迁所需能量较大,吸收带波长较短,一般出现在远紫外区(10~200 nm),在普通的紫外可见分光光度计的检测范围(200~1000 nm)之外。
共轭效应所形成的大π键各能级间距离较近,使π→π*跃迁能量下降,吸收带向长波方向移动到仪器检测范围内。
所以紫外吸收光谱研究的重点是共轭体系中π→π*和与双键相连接的杂原子(C=O、C=N、S=O等)上未成键的孤对电子的n→π*跃迁的结果。
紫外吸收光谱是带状光谱,吸收带的位置用吸收强度最大处的波长,即最大吸收波长(λmax)表示,吸收带的强度用该波长处的摩尔吸收系数(кmax)表示。
分子中有些吸收带已被指认,其中由共轭体系中π→π*产生的吸收带称为K带,其特点是吸收强度大,кmax在104 L•mol-1•cm-1左右,λ
随着共轭体系中双键数增加而增大,在217~280 nm范max
围内变化;n→π*产生的吸收带称为R带,是弱吸收带,кmax<100 L•mol-1•cm-1;在芳香族化合物中,环状共轭体系的π→π*产生E
、E2和B三个
1
吸收带,其中E2和B带的吸收波长大于200 nm,能被仪器所检测。
2、溶剂对紫外吸收光谱的影响
影响紫外吸收光谱的外因是指测定条件,如溶剂效应等。
所谓溶剂
效应是指受溶剂极性或酸碱性的影响,使溶质吸收峰的波长、强度以及形状发生不同程度的发生变化。
因为溶剂分子和溶质分子间能够形成氢键、或极性分子的偶极使溶质分子的极性增强,从而引起溶质分子能级的变化,使吸收带发生迁移。
如异丙叉丙酮的溶剂效应如表3-1所示。
随着溶剂极性的增加K带红移,而R带蓝移。
这是因为在极性溶剂中
π→π*跃迁所需能量减小,如图3-1(a)所示;而n→π*跃迁所需能量增大,如图3-1(b)所示。
表 3-1 溶剂极性对异丙叉丙酮紫外吸收光谱的影响
溶剂
正己烷氯仿甲醇水吸收带位移
跃迁
π→π*230 nm238 nm237 nm243 nm红移
n→π*329 nm315 nm309 nm305 nm蓝移
图 3-1 溶剂极性效应
溶剂的极性不仅影响溶质吸收带的波长,而且还影响其吸收强度和形
状,如苯酚在非极性溶剂中,可清晰看到B吸收带的精细结构,而在极性溶剂中,B带的精细结构消失,仅出现一个宽的吸收峰,而且吸收强度也明显下降。
在许多芳香烃化合物中均有此现象。
由于存在溶剂效应,所以在记录有机化合物紫外吸收光谱时,应注明所用的溶剂,如、分别表示在乙醇中和在三氯甲烷中的最大吸收波长。
另外,由于有的溶剂本身在紫外光谱区也有一定的吸收波长范围,故在选用溶剂时,必须考虑它们的干扰。
表 3-2列举某些溶剂的波长极限,测定波长范围应大于波长极限或用纯溶剂作空白,才不致受到溶剂吸收的干扰。
表 3-2 某些溶剂吸收波长极限
溶剂波长极限/nm溶剂波长极限/nm
环己烷210乙醇215
正己烷210水190
正庚烷21096%硫酸210
乙醚220二氯甲烷233
甲醇210氯仿245
3、紫外光谱仪的结构
请查阅参考书,画出结构原理图
4、紫外吸收光谱的实验方法
略
三、仪器与试剂
仪器 UV757CRT型紫外-可见分光光度计;石英比色皿;100 mL容量瓶。
试剂异丙叉丙酮;苯酚;正己烷;乙醇;0.1 mol•L-1HCl;0.1 mol•L-1NaOH;。
8种待测试样:①苯酚中性水溶液,②苯酚酸性水溶液,③苯酚碱性水溶液,④苯酚正己烷溶液,⑤异丙叉丙酮乙醇溶液(高浓度),⑥异丙叉丙酮乙醇溶液(低浓度),⑦异丙叉丙酮正己烷溶液(高浓度),⑧异丙叉丙酮正己烷溶液(低浓度)
四、实验步骤
1.根据实验条件,将UV757CRT型仪器按操作步骤进行调节,若仪
器状态正常,即可测定上述8种试液的紫外吸收光谱。
2.用1 cm石英比色皿,以相应的溶剂为参比,测绘各溶液在
200~450 nm的吸收光谱。
3.异丙叉丙酮的K带(π→π*跃迁)和R带(n→π*跃迁)强度相差将近100倍,所以用低浓度溶液测定以获得K带的λmax;用高浓度溶液测定以获得R带的信息。
五、数据处理
结果分析:
1、比较分析酸度对苯酚吸收光谱的影响;
2、比较苯酚在极性溶剂和非极性溶剂中吸收光谱的差异;
3、在低浓度下比较溶剂对异丙叉丙酮π-π*跃迁的影响;
4、在高浓度下比较溶剂对异丙叉丙酮n-π*跃迁的影响。
六、注意事项
1.本实验所用试剂均应为光谱纯或经提纯处理。
2、石英比色皿每换一种溶液或溶剂必须清洗干净,并用被测溶液或参比液荡洗三次。
用完后必须清晰干净。
注意清洗时使用的溶剂要适当。
3、仪器状态是否正常一般可通过基线的平直度表示。
必要时还应检查溶剂的背景吸收是否合格。
4、吸收峰强度应适中。
如果测得的紫外吸收峰为平头峰或太小,可适当改变试液浓度。
七、思考题
1.当助色团或生色团与苯环相连时,紫外吸收光谱有哪些变化?
2.在异丙叉丙酮紫外吸收光谱图上有几个吸收峰?它们分别属于什么类型跃迁?如何区别它们?
3.举例说明极性溶剂对π→π*和n→π*跃迁的吸收峰产生的影响。
4.被测试液浓度太大或太小时,对测试结果将产生什么影响,应如何加以调节?
5.在本实验中是否可用去离子水代替各溶剂作参比溶剂,为什么?。