细菌内毒素检查常见异常结果分析
- 格式:pdf
- 大小:304.19 KB
- 文档页数:20

影响内毒素、G试验结果的一些常见因素
一、采血严格按照无菌要求采集,须用专门配套耗材,采血后及时送检。
二、黄疸、溶血、乳糜血会影响检测结果。
三、引起细菌内毒素假阳性原因是:使用某些抗生素类药物,如磺胺类、以细菌为原料加工成的药物。
四、引起G试验假阳性原因有:
1、应用纤维素膜进行血液透析患者;
2、某些纱布或其他医疗物品中含有葡聚糖;
3、某些品牌的静脉制剂(白蛋白、凝血因子、免疫球蛋白等)含有葡聚糖;
4、某些细菌败血病患者(尤其是链球菌败血症);
5、抗肿瘤药物(如香菇多糖、裂殖菌多糖等);
6、含有菌类食物。
五、隐球菌和接合菌不能检出。
六、内毒素检测的灵敏度大概为88%,特异性为90%;G试验的灵敏度为88%,特异性为85%。
七、一次检测结果不能成为确诊依据,须由临床医生根据检测结果并结合临床症状及其他检测结果综合分析。
八、G试验适用于深部真菌,浅部真菌在体内血液中含量并不增高。
九、尽管假阳性原因不清,需进行动态监测(1-3)-β-D葡聚糖的变化,可以降低假阳性的发生。
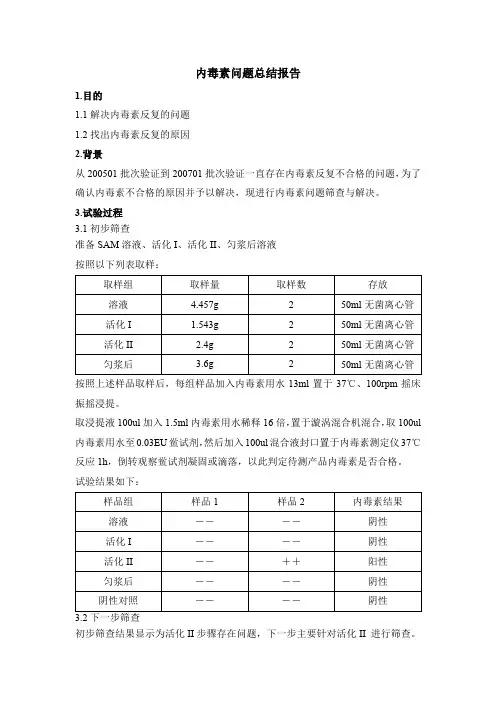
内毒素问题总结报告1.目的1.1解决内毒素反复的问题1.2找出内毒素反复的原因2.背景从200501批次验证到200701批次验证一直存在内毒素反复不合格的问题,为了确认内毒素不合格的原因并予以解决,现进行内毒素问题筛查与解决。
3.试验过程3.1初步筛查准备SAM溶液、活化I、活化II、匀浆后溶液按照以下列表取样:按照上述样品取样后,每组样品加入内毒素用水13ml置于37℃、100rpm摇床振摇浸提。
取浸提液100ul加入1.5ml内毒素用水稀释16倍,置于漩涡混合机混合,取100ul 内毒素用水至0.03EU鲎试剂,然后加入100ul混合液封口置于内毒素测定仪37℃反应1h,倒转观察鲎试剂凝固或滴落,以此判定待测产品内毒素是否合格。
试验结果如下:初步筛查结果显示为活化II步骤存在问题,下一步主要针对活化II 进行筛查。
准备活化II、溶液+CaCl2、溶液+EDC、清洗未匀浆、200501二楼冻干成品、200501三楼冻干成品样品,按照下表取样:按照上述样品取样后,每组样品加入内毒素用水13ml置于37℃、100rpm摇床振摇浸提。
取浸提液100ul加入1.5ml内毒素用水稀释16倍,置于漩涡混合机混合,取100ul 内毒素用水至0.03EU鲎试剂,然后加入100ul混合液封口置于内毒素测定仪37℃反应1h,倒转观察鲎试剂凝固或滴落,以此判定待测产品内毒素是否合格。
试验结果如下:根据当前两次筛查结果显示,可能在活化II阶段存在干扰,其他步段无法检出干扰因素,分别针对溶液加CaCl2、EDC进行筛查,结果显示均为阴性,因此结合文献推断可能是Ca2+和β-葡聚糖组合干扰。
当前阶段,可供选择的解决方案有:1.采用物理方法排除干扰因素2.采用试剂排除干扰因素3.增大稀释倍数,采用精度更高的鲎试剂4.采用抗增液,结合更高精度鲎试剂3.3物理方法排除干扰针对活化II溶液,采取离心、过滤的方法进行试验。
离心方案为取2.4g溶液在3000rpm离心10min,然后对上清液进行浸提、稀释、检测,结果发现3000rpm离心10min无明显分层现象,且上层呈阳性;过滤方案为取2.4g溶液使用0.22um和0.45um的过滤器进行过滤,对滤液进行浸提、稀释、检测,结果发现溶液使用过滤器容易堵塞过滤器且过滤效率慢,且检测滤液呈阳性。





凝胶法细菌内毒素检查中常遇的问题及解决方法陈邦树广西壮族自治区药品检验所广西南宁530021[摘要] 目的:探讨凝胶法细菌内毒素检查中常遇的问题及解决方法。
方法:对实际工作中遇到的一些具体问题进行多侧面的分析。
结果:对凝胶法细菌内毒素检查中常遇的问题进行分析并提出了解决方法。
结论:凝胶法细菌内毒素检查法影响因素较多,存在的问题仍需多方努力进行克服。
[关键词] 凝胶法环境内毒素鲎试剂问题Some commonly encountered problems and Solution methods on Gel-clot bacterial endotoxins testCHEN Bang-shu(Guangxi zhuang Autonomous Region Institute for Drug Control ,Nanning 530021)[Key words] Gel-clot; natural bacterial endotoxins; TAL; problems细菌内毒素检查法的优越性已为大多数质检人员所体会和认识。
但在实际工作中,也有一些问题使实验者感到困惑。
因此,作者认为有必要对这些问题提出并加以探讨,供大家参考。
1. 选择鲎试剂(TAL)的灵敏度值等于样品原液细菌内毒素限值进行试验是最佳方案吗?未必!选择TAL的灵敏度值等于样品原液细菌内毒素限值进行试验,无疑可节省对样品的稀释,但却不利于减少样品溶液对细菌内毒素试验干扰的可能性。
中国药典从1998年增补本[1] 开始的细菌内毒素检查法已增加了供试品阳性对照(PPC)管,如因样品溶液浓度较高而出现PPC管不凝的情况,会导致试验无效,结果“最佳方案”可能变成重试方案。
如今,国内TAL的制备技术得到了较大的发展,更高灵敏度(0.25 EU.ml -1 、0.125 EU.ml -1 、0.06 EU.ml -1 、0.03 EU.ml -1 )的TAL供应已不成问题。

常见干扰及消除湛江安度斯生物有限公司2016年7月实验助手APP授权发布BET干扰的普遍性!70%!•一项对人用药品与鲎试验相容性的研究证实了干扰的影响范围,在所研究的品种中仅30%的药品可以不经任何处理直接进行BET;有97%的干扰问题可以通过稀释供试品的方法去消除。
2干扰的表现•凝胶法ChP(2015年)规定无干扰条件:当溶液A和溶液D的所有平行管都为阴性,并且系列溶液C的结果符合鲎试剂灵敏度复核试验要求时,试验方为有效。
当系列溶液B的结果符合鲎试剂灵敏度复核试验要求时,认为供试品在该浓度下无干扰作用。
3干扰的类型•抑制–供试品含有的内毒素浓度≥2倍检测试剂的灵敏度,但检测结果仍为阴性,称之为假阴性。
•增强–供试品含有的内毒素浓度低于检测试剂灵敏度的1/2,但检测结果仍为阳性,称之为假阳性。
4光度法的判断?无干扰可接受范围:50%≤回收率≤200%抑制:回收率<50%增强:回收率>200%550%200%无干扰增强抑制鲎试剂内毒素 二价阳离子浓度不足聚集高渗透压酶、酶抑制剂LAL-RM 脂质体吸附洗涤剂表面活性剂pH值干扰的因素!pH值的影响鲎试剂中的酶需要在 pH值6~8的范围内才能正常反应,极端的pH环境影响酶的活性,造成抑制一般来说鲎试剂配方中都添加了缓冲剂以帮助样品的pH值的调节,但这不足以解决所有样品的pH问题测定以1:1为比例混合的样品稀释液+鲎试剂的pH值 以获得准确的pH值7解决有关pH的问题1•用BET水对供试品在允许的范围内进行稀释2•用缓冲液制备供试品3•用酸、碱或缓冲液来调节pH8二价阳离子浓度不足Mg2+离子是鲎试剂重要的辅因子,没有Mg2+离子,内毒素将无法激活鲎试剂的酶。
供试品中的螯合剂成分会螯合试剂中的二价阳离子(如Mg2+离子),造成抑制常见的螯合剂有:EDTA、柠檬酸钠、肝素钠、喹诺酮类药物等9解决二价阳离子浓度不足问题1•用BET水对供试品在允许的范围内进行稀释2•使用含Mg 2+或Ca 2+离子的稀释剂稀释样品,降低活性螯合剂含量3•注意过高的二价阳离子(如Ca 2+)浓度可能会带来抑制10高渗透压问题较高浓度的糖或者盐通常会抑制鲎试剂反应,如50%葡萄糖或5%氯化钠溶液。



BET常见异常
结果分析
湛江安度斯生物有限公司
2016年7月
实验助手APP授权发布
1
BET常见异常结果分析
凝胶法
灵敏度复核不符合规定
阳性对照阴性供试品阳性
对照阴性
阴性对照
阳性
供试品一
阳一阴
2
1.阴性对照为阳性
✓实验环境-有扬尘;
✓实验操作不规范-人为污染;
✓配套用品(移液管、反应管、吸头污染或没有完全除热原)
✓试剂性能-鲎试剂或水出问题
✓设备-恒温水浴,水滴进反应混合液中
3
2.阳性对照为阴性
✓标准内毒素溶液的制备是否准确;
✓试剂性能(内毒素标准品、鲎试剂和检查用水的质量和是否匹配);
✓配套用品(移液管、稀释管、反应管、吸头是否有干扰);
✓操作是否规范;
✓设备-恒温孵育的温度和时间是否合适;✓实验环境;
4
3.供试品阳性对照为阴性
阳性对照为阴性,供试品阳性对照为
阴性—参考实验结果出现异常的分析2) 阳性对照为阳性,供试品阳性对照为
阴性
✓供试品阳性对照溶液配制是否正确;
✓供试品有抑制干扰作用;
✓配套用品(稀释管、反应管、移液用
具是否有干扰);
✓其他
5
4.阴性对照正常,供试品为阳性
供试品内毒素含量不符合规定;
污染
✓配套用品(稀释管、反应管、刻度吸管、吸头);
✓试验操作、环境、试剂等
假阳性-增强干扰作用
•凝胶法中,没有对照项可以判断供试品是否存在增强作用。
6
4.阴性对照正常,供试品为阳性
假阳性
的判断
凝胶法
检测
配套稀释液抗增液
复溶鲎
试剂
特异性
鲎试剂
光度法
检测
分析内
毒素含
量
反应动
力学曲
线分析
7
5.同一供试品结果有时阳性,有时阴性
样品
✓供试品内毒素含量在1/2L左右;
✓供试品存在干扰
试剂-不同试剂,抗干扰能力不同
试验条件(环境、人员操作技能、恒温孵育温度和时间)
8
6.灵敏度复核不符合规定
参照案例分析(二)鲎试剂灵敏度复核不符合规定原因调查。
9
BET常见异常结果分析
光度法
标准曲线的线性不合格
变异系数大内毒素回收率
不合格
阴性对照不合
格
不正确的预设
Rt或OD值,
导致的异常结
果
10
1.线性不足
标准内毒素
•某个标准内毒素浓度制备误差•标准品旋涡混合不充分
•标准品储存不当或用具干扰试剂
•污染
•检测能力不足
仪器设置
•不正确的预设Rt/OD值
不正确的反应时间
•终点法
11
2.阴性对照不合格
配套用品激活(污染)鲎试剂
✓塑料吸头和吸管可激活或污染鲎试剂 反应试管或孔没有完全除内毒素
操作污染
✓细菌内毒素检查用水
✓鲎试剂
✓反应试管或孔受污染
试剂灵敏度不足或不合适的预设Rt/OD
12
3.变异系数偏大
气泡试剂
质量加样
误差
试管/
孔受
污染
移液
管/吸
头污
染
样品
沉淀
或悬
浮
内毒
素添
加的
量不
准确
13
4.回收率问题
标准内毒素溶液制备或加入不准确 试剂加入不准确
样品
✓内毒素浓度太高
✓抑制作用
✓增强作用
✓工艺、原辅料的改变
14
5.不正确的预设Rt或OD值,导致的异
常结果
预设Rt/OD值指光度变化值,是一个参考值,一般由鲎试剂生产厂家提供。
合适的预设Rt/OD值
✓标准曲线最低点浓度在设定时间内能达到预设
Rt/OD值
✓标准曲线最低点浓度在设定时间内反应时间和阴性对照有差异
✓标准曲线的相关系数|r| ≥ 0.980
预设Rt/OD值的取值范围越宽,鲎试剂的稳健性越好(安度斯光度法试剂的特征)
15
光度变化预设值的影响
预设OD值0.02
相关系数-0.9990
0.0024
供试品内毒素含量
(EU/ml)
回收率92.9%
50.50.050.00
5
16
光度变化预设值的影响
预设OD值0.05
相关系数-0.9984
<0.0038
供试品内毒素含量
(EU/ml)
回收率102.3%
50.50.050.00
5
17
光度变化预设值的影响
预设OD值0.1相关系数
-0.9985供试品内毒素含量(EU/ml)<0.0051回收率
?104.6%50.5
0.05
0.005
标准曲线最低点浓度OD值不达限18
安度斯光度法鲎试剂预设光度变化值
(建议)
表1:动态试管检测仪-405nm
仪器名称动态试管检测仪厂家莱伯金耐特
检测波长405nm
光度法试剂动态浊度法动态显色法
预设Rt值95%92%
表2:动态试管检测仪-660nm
仪器名称动态试管检测仪厂家莱伯金耐特
检测波长660nm
光度法试剂动态浊度法动态显色法
预设Rt值95%/
安度斯光度法鲎试剂预设光度变化值
(建议)
表3:ELx808IU酶标仪-405nm
仪器名称ELx808IU酶标仪厂家美国伯腾
检测波长405nm
光度法试剂动态浊度法动态显色法
预设OD值0.030.05
表4:FC/ET型酶标仪-405nm
仪器名称FC/ET型酶标仪厂家赛默飞世尔
检测波长405nm
光度法试剂动态浊度法动态显色法(微孔板法)
预设OD值/0.1
20。