(完整版)初三化学中考总复习专题一物质的共存、检验、鉴别和除杂
- 格式:doc
- 大小:93.01 KB
- 文档页数:10

【中考化学】2023届第一轮复习分类专题—物质的检验、鉴别、除杂及成分确定(基础篇)一、选择题1.化学与生活息息相关,人类的生活离不开化学。
生活中下列做法错误的是( )A .食品包装中充氮气防腐B .用过滤和蒸馏等方法净化水C .用灼烧方法区分棉纤维和合成纤维D .用硬水洗涤衣服有利于节约肥皂2.向溶液X 中加入氢氧化钠溶液,加热,产生的气体能使湿润的红色石蕊试纸变蓝。
则溶液X 中一定含有的微粒是A. Cl - B.C. Ca 2+D.23CO -4NH +3.除去下列物质中的少量杂质,所选除杂试剂及方法不正确的是选项物质杂质除杂试剂及方法A KCl MnO 2加水溶解、过滤、蒸发B H 2HCl 先通入氢氧化钠溶液,再通入浓硫酸C Cu CuO 加入过量的稀硫酸,过滤、洗涤、干燥D CO 2CO将气体点燃A. AB. BC. CD. D4.下列实验操作能达到目的的是选项实验目的实验操作A鉴别二氧化锰和木炭粉观察颜色B鉴别尿素[CO(NH2)2]和硝酸钾加碱混合研磨闻气味C除去硝酸钠溶液中的硫酸钠加入适量的硝酸钡溶液,过滤D除去氯化钾中的氯酸钾加适量的二氧化锰,加热A. AB. BC. CD. D5.下列实验设计不能达到实验目的的是选项实验目的试剂或方法A除去粗盐中难溶性杂质溶解、过滤、蒸发B验证铜与银的金属活动性稀盐酸C鉴别合成纤维和羊毛纤维灼烧闻气味D除去硫酸亚铁溶液中混有的少量硫酸铜加过量铁粉、过滤A. AB. BC. CD. D6.下列实验方案,能达到实验目的的是实验目的实验方案A检验集气瓶中CO2是否收集满将带火星的木条伸入集气瓶内B除去KCl溶液中混有的K2SO4滴加适量Ba(OH)2溶液后过滤C鉴别CH4、H2两种无色气体点燃气体,分别在火焰上方罩一个干燥的冷烧杯D鉴别稀盐酸和蒸馏水取样,分别滴加紫色石蕊溶液A. AB. BC. CD. D7.除去下列物质中混有的少量杂质,所选试剂和操作方法均正确的是选项物质杂质所选试剂和操作方法A KCl MnO ₂加入足量的水溶解,过滤,洗涤,干燥B O 2H 2O 通过氢氧化钠溶液C Cu Fe 加入过量的稀硫酸,过滤,洗涤,干燥DNaCl 溶液BaCl 2加入适量的稀硫酸,过滤A. AB. BC. CD. D8.某兴趣小组为探究“猪肝中的铁元素”,进行了以下实验:选用新鲜猪肝,如图操作I 将猪肝中的铁转化为铁离子,再用硫氰化钾溶液检验(硫氰化钾溶液遇铁离子变红色)。


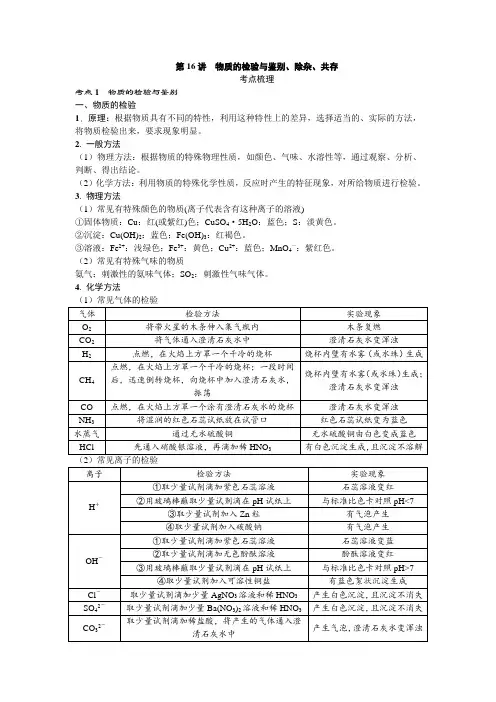
第16讲物质的检验与鉴别、除杂、共存考点梳理考点1 物质的检验与鉴别一、物质的检验1. 原理:根据物质具有不同的特性,利用这种特性上的差异,选择适当的、实际的方法,将物质检验出来,要求现象明显。
2. 一般方法(1)物理方法:根据物质的特殊物理性质,如颜色、气味、水溶性等,通过观察、分析、判断、得出结论。
(2)化学方法:利用物质的特殊化学性质,反应时产生的特征现象,对所给物质进行检验。
3. 物理方法(1)常见有特殊颜色的物质(离子代表含有这种离子的溶液)①固体物质:Cu:红(或紫红)色;CuSO4·5H2O:蓝色;S:淡黄色。
②沉淀:Cu(OH)2:蓝色;Fe(OH)3:红褐色。
③溶液:Fe2+:浅绿色;Fe3+:黄色;Cu2+:蓝色;MnO4—:紫红色。
(2)常见有特殊气味的物质氨气:刺激性的氨味气体;SO2:刺激性气味气体。
4. 化学方法(1)常见气体的检验1. 物质的鉴别原则:操作简单、试剂种类少、现象明显。
2. 物质鉴别的方法:应先简后繁,先用物理方法后用化学方法。
(1)物理方法:依据物质的特殊的物理性质(如颜色、状态、气味、溶解性、溶解时的吸放热现象)进行观察、分析、判断,得出结论。
(2)化学方法:依据物质间反应时所产生的特殊反应现象(如变色、放出气体、生成沉淀、放热等)进行鉴别。
3. 物质鉴别的形式(1)一种试剂鉴别:选择一种试剂,分别加入待测物质中,观察实验现象。
(2)多种试剂鉴别:选择多种试剂,依次加入待测物质中,会出现明显不同现象。
(3)无试剂鉴别:先利用物质物理性质不同或物质间的相互反应(包括与生成物反应)而产生不同现象把物质鉴别出来。
考点2 物质的除杂1. 除杂原则:不增、不减、易分(1)主不减:所选试剂不能与被提纯物质(主要成分)反应。
(2)杂不增:在除去杂质的同时,不能产生新的杂质。
(3)易分离:除杂后生成的产物的状态与被提纯物质的状态要不同,方便除去。
2. 除杂方法(1)气体的除杂方法一:将杂质气体通过物质吸收、反应除去,如氧气中的水蒸气可通过浓硫酸吸收除去、一氧化碳中的二氧化碳可通过氢氧化钠溶液吸收除去。





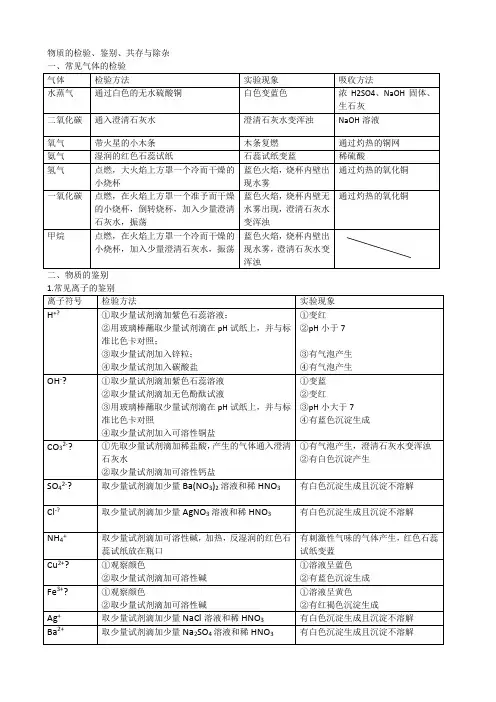

专题一物质的共存、检验、鉴别和除杂I .物质的共存(8年3考)针对训练1. (2013 长沙)下列各组物质分别加入到足量的水中,能得到无色透明溶液的是()A. KNO3、NaCl、HClB. FeCl 3、Na2SO4、KClC. CuSO4、H2SO4、NaClD. FeCl 2、KCl、NaOH2. (2016赤峰)某溶液中大量存在的离子仅有Nbt Ba2+和X离子,则X是()--+2-A. OH-B. Cl -C. K +D. SO42-3. (2016重庆A)某植物培养液中含有NHCI和CuSQ,下列物质在该培养液中能大量存在的是()A. NaOHB. BaCI 2C. KNO 3D. AgNO 34. (2017衡阳)下列离子在pH= 1的溶液中能大量共存,且为无色溶液的是()+2+--A. NH4+Ca2+CI-NO3-++-2-B. K +Na +CI -CO 32-3+2+--C. Fe 3+Mg 2+NO3-CI -D. Na+Ba 2+NO 3-OH-5. (2017 荆州)某溶液能使紫色石蕊溶液变蓝,下列各组离子在该溶液中能大量共存的是()2--2+-A. SO24-、NO-3、Ba2+、CI-2++-+B. Cu 2+、Na+、NO3-、K+C. K +、CO32-、NO3-、CI-D. H +、Ba2+、K+、NO3-6. (2017 南京)下列各组离子在水中能大量共存的是()2++--A. Cu 2+、Na+、CI -、OH-B. H +、K+、NO3-、SO42-C. Na +、NH4 、NO3-、OH-D. Ag +、Ba2+、NO3-、CI -7. (2017 滨州)小滨对某无色溶液所含溶质的记录,合理的是()A. HCI 、NaOH、Na2SO4B. KNO3、ZnCI2、FeCI3C. AgNO3、H2SO4、NaCID. NaOH、Na2CO3、NaCI8. (2016 巴中)下列各组离子在指定的溶液中能大量共存的一组是()A. 在硝酸铵溶液中:Na: Cu2: OHB. 在稀盐酸中:Ba2+> cO「、Zn2+C. 在氯化钠溶液中:K、C『、NOD. 在氢氧化钠溶液中:H、MgS C「n .物质的检验、鉴别(8年4考)针对训练【长沙真题精选】1. (2011 长沙)“家庭小实验”是利用家庭生活中常用的物质,进行化学实验探究的活动。
除杂、共存、鉴别、鉴定、推断题型解题技法总结知识要点:一、除杂题:1、解答除杂质一类的题目时,要注意三原则;三要领;五种常用的方法。
三原则:①不引入新杂质;②不减少被提纯物质的质量;③杂质便于分离。
三要领:①根据物理性质或化学性质的差异;②确定除杂质方法;③选择适宜试剂。
除杂质思路分析方法:(1)沉淀法:加入一种试剂将被除去的杂质变为沉淀,再用过滤法除去。
(2)化气法:加热或加入一种试剂将杂质变为气体逸出。
(3)置换法:利用置换反应的原理将杂质除去。
(4)转纯法:将被除去的杂质变为提纯的物质。
(5)吸收法:常用于气体的提纯。
在掌握了以上除杂质的原则、要领、方法后,解答题目时要审清题目要求,分析理顺思路且与题目要求吻合,才能准确解题。
2. 混合物的分离:(1)可溶性与难溶性物质的混合物——常用溶解、过滤、蒸发三步操作加以分离,分别得到纯净物。
如:粗盐的提纯;BaSO4和Na2SO4的混合物。
(2)两种物质均溶于水,但两种物质的溶解度一种随温度变化大,另一种变化不大时,可考虑——结晶法。
即冷却热饱和溶液的方法加以分离。
如:NaCl和KNO3的混合物。
(3)两种物质均溶于水时,可考虑用化学方法分离。
如BaCl2和NaCl的混合物。
可将混合物先溶于水,加入适量Na2CO3溶液,得到BaCO3和NaCl溶液。
BaCl2+ Na2CO3=BaCO3↓+2NaCl。
将沉淀过滤出,洗净后在沉淀中加入适量盐酸溶液,又得到BaCl2溶液,CO2逸出。
BaCO3+2HCl =BaCl2+H2O+CO2↑。
最后分别将NaCl溶液和BaCl2溶液蒸发,分别得到纯净的NaCl固体和BaCl2固体。
注意:用化学方法或用物理方法进行混合物分离时,要区别除杂质与分离物质的不同点是:除杂质时只要求把杂质除掉、保留原物质即可;而混合物分离是几种物质用一定的方法分开,原混合物中各成分都必须保留。
二、共存的问题(相互间不能发生复分解反应的离子间能共存)1、在溶液中不能共存的:a.能反应的酸碱盐、Mg2+、Al3+;Ag+与Cl-、CO32-、SO32-、S2-;Cu2+(蓝色)、Fe2+(浅绿色)、Fe3+(黄棕色)、MnO4-(紫色)。
物质的共存、检验、除杂和鉴别【教学目标】1.知识目标:掌握物质的鉴别、除杂,掌握物质的性质和以及之间反应才是解答本题之间的关键。
2.技能目标:分清楚物质的鉴别和除杂的区别,掌握不同类别的物质的鉴别和除杂的方法,学会分析和解决问题。
3.情感目标:掌握物质的性质才是解决本题的关键类型一物质的共存1.物质共存条件(1)组内物质均可溶(2)在同一溶液中,物质之间不发生化学反应,即构成物质的离子之间不会生成水,气体或沉淀。
2.常见不能共存的离子对三气一水八沉淀3.物质共存的隐含条件(1)溶液为中性(不显电性),即在同一组物质的离子中,同时含有阳离子和阴离子(2)“无色”条件型:在无色溶液中,下述溶液中的溶质不能存在。
色溶液:含铜离子溶液,如氯化铜,硫酸铜溶液等。
色溶液:含亚铁离子溶液,如氯化亚铁,硫酸亚铁溶液等。
色溶液:含铁离子的溶液,如氯化铁溶液,硫酸铁溶液紫红色溶液:高锰酸钾溶液。
(3)“酸碱性或pH”条件型:①酸性:溶液的pH<7,溶液中一定存在大量H+ ,则该溶液中一定不含能与H+反应的离子,如等。
②碱性:溶液的pH>7,溶液中一定存在大量的,则该溶液中一定不含能与该离子反应的离子,如等。
中考链接(2019十堰)1.在无色溶液中,下列各组物质能大量共存的是()A.氯化钠、氢氧化钙、稀盐酸B.硝酸钾、氯化铜、氢氧化钠C.硝酸钠、氢氧化钾、氯化钡D.碳酸氢钠、氯化钾、稀硫酸(2019遵义)2.下列各组离子能够在指定溶液中大量共存的一组是()A.在氯化钠溶液中:Zn2+、SO42-B.在稀盐酸中:Ag+、NO3-C.在硫酸钾溶液中:Ba2+、Cl-D.在硝酸铵溶液中:K+、OH-(2019百色)3.下列各组离子在溶液中一定能大量共存的是()A.Na+、Cu2+、NO3-、OH-B.Zn2+、K+、Cl-、SO42-C.Ba2+、H+、Cl-、OH-D.NH4+、K+、OH-、NO3-(2020德阳)4.有一包固体粉末可能含有NaOH、NaCl、CuCl2、Mg(0H)2、CaCO3中的一种或多种,为探究其成分,某同学取样进行了如图所示实验:(1)操作Ⅰ和操作Ⅱ相同,其名称是。
专题一物质的共存、检验、鉴别和除杂Ⅰ. 物质的共存(8年3考)针对训练1. (2013长沙)下列各组物质分别加入到足量的水中,能得到无色透明溶液的是()A. KNO3、NaCl、HClB. FeCl3、Na2SO4、KClC. CuSO4、H2SO4、NaClD. FeCl2、KCl、NaOH2. (2016赤峰)某溶液中大量存在的离子仅有NH+4、Ba2+和X离子,则X是()A. OH-B. Cl-C. K+D. SO2-43. (2016重庆A)某植物培养液中含有NH4Cl和CuSO4,下列物质在该培养液中能大量存在的是()A. NaOHB. BaCl2C. KNO3D. AgNO34. (2017衡阳)下列离子在pH=1的溶液中能大量共存,且为无色溶液的是()A. NH+4Ca2+Cl-NO-3B. K+Na+Cl-CO2-3C. Fe3+Mg2+NO-3Cl-D. Na+Ba2+NO-3OH-5. (2017荆州)某溶液能使紫色石蕊溶液变蓝,下列各组离子在该溶液中能大量共存的是()A. SO2-4、NO-3、Ba2+、Cl-B. Cu2+、Na+、NO-3、K+C. K+、CO2-3、NO-3、Cl-D. H+、Ba2+、K+、NO-36. (2017南京)下列各组离子在水中能大量共存的是()A. Cu2+、Na+、Cl-、OH-B. H+、K+、NO-3、SO2-4C. Na+、NH+4、NO-3、OH-D. Ag+、Ba2+、NO-3、Cl-7. (2017滨州)小滨对某无色溶液所含溶质的记录,合理的是()A. HCl、NaOH、Na2SO4B. KNO3、ZnCl2、FeCl3C. AgNO3、H2SO4、NaClD. NaOH、Na2CO3、NaCl8. (2016巴中)下列各组离子在指定的溶液中能大量共存的一组是()A.在硝酸铵溶液中:Na+、Cu2+、OH-B.在稀盐酸中:Ba2+、CO2-3、Zn2+C.在氯化钠溶液中:K+、Ca2+、NO-3D.在氢氧化钠溶液中:H+、Mg2+、Cl-Ⅱ.物质的检验、鉴别(8年4考)针对训练【长沙真题精选】1. (2011长沙)“家庭小实验”是利用家庭生活中常用的物质,进行化学实验探究的活动。
下列实验不能..用“家庭小实验”完成的是()A. 检验自来水是否含有氯离子B. 用闻气味的方法鉴别酒精和水C. 检验自来水是否为硬水D. 探究铁在潮湿的空气中是否生锈2. (2014长沙)鉴别下列物质使用的方法或试剂,正确的是()A. 氧气与氢气——闻气味B. 硫酸铜粉末与氯化钠固体——加水C. 稀硫酸与稀盐酸——滴加紫色石蕊溶液D. 二氧化碳气体与氯气——用燃着的木条3. (2017长沙)下列各组物质的溶液,不另加试剂就不能..鉴别出来的一组是()A. CuSO4NaOH KNO3B. FeCl3AgNO3NaNO3C. Na2CO3HCl BaCl2D. CaCl2K2CO3NaCl【好题精练】4. (2017北京)下列方法能区分氧气和二氧化碳两瓶气体的是()A. 闻气味B. 观察颜色C. 倒入适量氢氧化钠溶液D. 将燃着的木条伸入集气瓶中5. (2017成都)能用于鉴别氢氧化钠溶液和氢氧化钙溶液的物质是()A. HClB. KNO3C. K2CO3D. FeCl36. (2017株洲)只用一种试剂可以区分(NH4)2SO4、NH4Cl、K2SO4三种无色溶液,这种试剂是()A. AgNO3溶液B. Ba(OH)2溶液C. NaOH溶液D. 盐酸7. (2017南雅下学期一模改编)下列鉴别物质的方法中,切实可行的是()A. 用酚酞溶液鉴别NaCl溶液和盐酸B. 用水鉴别Na2CO3和CaCO3固体C. 用碳酸钠鉴别稀盐酸和稀硫酸D. 用酚酞溶液鉴别烧碱与纯碱8. (2017麓山一模)用括号内试剂不能一次性将组内物质鉴别出来的是()A. 固体:NaOH、NH4NO3、NaCl(水)B. 液体:稀盐酸、H2O、Ca(OH)2溶液(石蕊溶液)C. 固体:NaCl、CaCO3、KCl(水)D. 液体:Ba(NO3)2溶液、MgCl2溶液、K2CO3溶液(稀硫酸)9. (2017烟台改编)下列各组物质的溶液,不用其他试剂,只用观察和组内物质的溶液相互混合的方法,就能将它们一一鉴别出来的是()A. NaCl、BaCl2、CuSO4、KNO3B. Ba(NO3)2、NaCl、Na2SO4、HClC. NaOH、CuCl2、NaCl、KClD. HCl、Na2CO3、KCl、CaCl210. (2017哈尔滨)区分下列各组物质的两种方法都正确的是()12. (2017德州)下列四个实验方案设计不合理的是()鉴别的是()A. Na2SO4、BaCl2、KNO3、NaClB. NaOH、Na2SO4、FeCl3、BaCl2C. Na2SO4、Na2CO3、BaCl2、HClD. NaCl、AgNO3、NaNO3、HClⅢ. 物质的除杂(近8年仅2011年未考)针对训练【长沙真题精选】2. (2014长沙)除去下列物质中混有的少量杂质(括号内为杂质),所用方法正确的是()A. CO(CO2)——通过灼热的氧化铜B. NaCl(Na2SO4)——加入硝酸银溶液C. CaCO3固体(CaO固体)——高温煅烧D. FeSO4溶液(H2SO4)——加入铁粉【好题精练】3. (2017株洲)除去氯化钾溶液中混有的少量碳酸钾,最合理的方法是()A. 加入足量的氯化钡溶液,过滤B. 加入足量的稀盐酸,加热C. 加入足量的硝酸钡溶液,过滤D. 加入足量的稀硫酸,加热4. 下列各组括号内除杂质的试剂或方法错误的一组是()A. O2中混有少量的水蒸气(浓硫酸)B. CaO中混有CaCO3(高温煅烧)C. 铜粉中混有少量铁粉(稀硫酸,过滤)D. KCl溶液中混有少量MgCl2(适量NaOH溶液,过滤)5. (2017湘潭)要除去下列物质中的少量杂质(括号内物质为杂质),所选试剂不正确的是()A. NaOH(Na2CO3):盐酸B. CO2(O2):灼热的铜粉C. CO(CO2):氢氧化钠溶液D. O2(H2O):浓硫酸6. (2017广州改编)下列除杂所选用试剂与操作方法均正确的是()7. ),所用试剂及主要操作均合理的是()确的是()9. (2017麓山一模)下列关于物质的除杂所选用的试剂或方法错误的是()11. (2017南京改编)除去下列物质中混有的少量杂质(括号内为杂质),拟定的实验方案不可行的是()A. FeCl2溶液(CuCl2)——加入过量的铁粉,过滤B. KCl固体(KClO3)——加入少量的二氧化锰,并加热C. CuSO4溶液(H2SO4)——加入足量的氧化铜粉末,过滤D. NaCl溶液(MgCl2)——加入过量的氢氧化钠溶液,过滤,滤液中加稀盐酸至中性12. (2017遵义改编)除去下列物质中少量杂质(括号内为杂质)的方法,叙述正确的是()A. 一氧化碳(二氧化碳)——通过灼热的氧化铜B. 水(植物油)——加洗洁精,搅拌振荡C. Na2CO3(NaHCO3)固体——充分加热至固体质量不变D. NaCl溶液(CaCl2)——滴加适量K2CO3溶液、过滤参考答案及解析Ⅰ.物质的共存针对训练1. A【解析】A中的三种物质溶于水都能形成无色透明的溶液,相互之间不发生化学反应;B中FeCl3的水溶液呈黄色;C中CuSO4的水溶液呈蓝色;D中FeCl2的水溶液呈浅绿色,且FeCl2与NaOH不能共存。
2. B【解析】铵根离子和钡离子均属于阳离子,三种离子可大量共存,所以X离子一定是阴离子,C错误;铵根离子与氢氧根离子结合生成氨水,不能大量共存,A错误;氯离子与铵根离子、钡离子均不会结合生成沉淀、气体或水,可以大量共存,B正确;钡离子与硫酸根离子结合生成硫酸钡沉淀,不能大量共存,D错误。
3. C【解析】氯化铵、硫酸铜溶液均能与氢氧化钠反应,氢氧化钠不能在该培养液中能大量存在,A错误;硫酸铜溶液能与氯化钡反应产生BaSO4白色沉淀,氯化钡不能在该培养液中大量存在,B错误;氯化铵、硫酸铜溶液均不与硝酸钾反应,硝酸钾能在该培养液中大量存在,C正确;氯化铵溶液能与硝酸银反应产生AgCl白色沉淀,硝酸银不能在该培养液中大量存在,D错误。
4. A【解析】pH=1的溶液显酸性。
铵根离子、钙离子、氯离子、硝酸根离子、氢离子相互间不反应,可在酸性溶液中共存,且溶液为无色,A正确;酸性溶液中含有氢离子,碳酸根离子与氢离子不能共存,B错误;铁离子的溶液显黄色,C错误;氢氧根离子与氢离子结合生成水,二者不能共存,D错误。
5. C【解析】由题中信息溶液能使紫色石蕊变蓝,可知溶液显碱性,溶液中含有大量的OH-。
A组中硫酸根离子能与钡离子反应生成硫酸钡沉淀,所以这组离子在该溶液中不能大量共存,A错误;B中铜离子能与氢氧根离子反应生成氢氧化铜沉淀,所以B组离子不能在该溶液中大量共存,B错误;C组中各组离子间不会反应生成沉淀、水或气体,且不与OH-反应,所以C组离子可在该溶液中大量共存,C正确;D组中氢离子能与氢氧根离子反应生成水,所以D组离子不能在该溶液中大量共存,D错误。
6. B【解析】因为Cu2+与OH-能反应生成Cu(OH)2沉淀,所以Cu2+和OH-在水中不能大量共存,A错误;因为H+、K+、NO-3、SO2-4相互间都不能反应生成水、沉淀或,所以H+、K+、NO-3、SO2-4在水中能大量共存,B正确;因为NH+4与OH-能反应生成NH3·H2O,NH3·H2O不稳定,会进一步分解生成H2O和NH3气体,所以NH+4和OH-在水中不能大量共存,C错误;因为Ag+与Cl-能反应生成AgCl沉淀,所以Ag+和Cl-在水中不能大量共存,D错误。
故选B。
7. D【解析】HCl和NaOH反应生成H2O,不能共存,A错误;FeCl3呈黄色,B错误;AgNO3和NaCl能反应生成AgCl沉淀,不能共存,C错误。
故选D。
8. C【解析】针对训练【长沙真题精选】1. A【解析】检验Cl-要用到硝酸银溶液,但家里没有硝酸银溶液,A无法完成;酒精有特殊气味,水无气味,B可实现;区分自来水为硬水还是软水可用肥皂水,C可实现;要探究铁在潮湿的空气中是否生锈,可通过观察铁钉表面颜色的变化,D可实现。
2. B【解析】氧气和氢气都是无味的气体,不能通过闻气味的方法鉴别,A错误;硫酸铜粉末溶于水形成蓝色溶液,氯化钠固体溶于水形成无色溶液,B正确;稀硫酸和稀盐酸都是酸,都显酸性,因此滴加紫色石蕊溶液后,溶液都变为红色,C错误;二氧化碳气体和氯气都不支持燃烧,都会使燃着的木条熄灭,D错误。