九年级化学磷与氧气
- 格式:pdf
- 大小:1.36 MB
- 文档页数:10

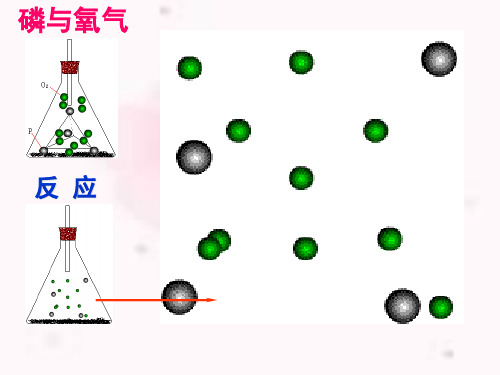
红磷在氧气中燃烧的现象
红磷在氧气中燃烧化学反应式:4P+5O2=2P2O5。
在氧气中燃烧现象:红磷在氧气中剧烈燃烧,发出白光,放出热量,生成大量的白烟。
在空气中燃烧现象:红磷在空气中燃烧会出现黄白色火焰,放热,有大量白烟。
产生了五氧化二磷,五氧化二磷颗粒飘在空气中就是现象的白烟。
红磷是紫红或略带棕色的无定形粉末,有光泽。
密度2.34g/cm3,加热升华,但在4300KPa压强下加热至590℃可熔融。
汽化后再凝华则得白磷。
难溶于水和CS2,乙醚、氨等,略溶于无水乙醇,无毒无气味,燃烧时产生白烟(注:白烟为五氧化二磷),烟有毒。
化学活动性比白磷差,不发光磷在常温下稳定,难与氧反应。
以还原性为主,80℃以上着火。
与卤素、硫反应时皆为还原剂。
用于生产安全火柴、有机磷农药、制磷青铜等。

红磷在氧气中燃烧的文字表达式红磷在氧气中燃烧的文字表达式为"P4 + 5O2 → 2P2O5"。
红磷是一种非金属元素,是磷的主要形态之一,具有很高的反应活性。
当红磷与氧气发生化学反应时,会产生磷酸盐,化学方程式为P4 + 5O2 → 2P2O5。
红磷是一种黄色或红色的物质,具有很高的活性。
在常温下,红磷相对较稳定,但当与氧气接触时,会发生剧烈的氧化反应。
这是因为红磷有很高的氧化性,而氧气则是一种强氧化剂,两者相遇时会发生激烈的化学反应。
当红磷与氧气充分接触时,红磷开始燃烧。
在燃烧过程中,红磷的分子结构发生变化,原子之间的键被打破,释放出大量的能量。
同时,氧气分子与红磷原子结合,形成了磷酸盐的化合物。
这个化合物被称为磷酸五氧化二磷,化学式为P2O5。
磷酸五氧化二磷是一种白色固体,具有很高的腐蚀性。
它在水中溶解后会形成磷酸,具有较强的酸性。
磷酸盐广泛应用于农业、医药、化工等领域,是一种重要的化学物质。
红磷在氧气中燃烧的反应释放出大量的能量,产生强烈的热和光。
因此,在实验室中进行红磷燃烧实验时,需要注意安全措施,避免火灾和爆炸等危险。
红磷的燃烧反应是一种氧化反应。
在氧气的作用下,红磷原子失去电子,形成正离子,氧气分子接受这些电子,形成负离子。
这种电子的转移过程导致了能量的释放,产生了热和光。
这个过程是不可逆的,一旦红磷开始燃烧,就无法逆转回原来的状态。
红磷在氧气中燃烧的过程是一个复杂的化学反应。
它涉及到原子之间的键的断裂和重新组合,以及电子的重新分配。
这个过程是在高温下进行的,需要提供足够的能量来启动反应。
一旦反应开始,它会自行维持,直到红磷完全燃尽或氧气耗尽。
红磷在氧气中燃烧的化学反应是一种放热反应,释放出大量的能量。
这个反应在自然界中不常见,但在实验室中可以通过适当的条件和控制来实现。
研究红磷燃烧的反应机制和能量释放过程,对理解化学反应的基本原理和能量转化有重要意义。
红磷在氧气中燃烧是一种高度放热的氧化反应。

白磷燃烧的化学方程式
白磷在空气中燃烧的化学方程式是4P+5O2=燃烧=2P2O5。
白磷在氧气中燃烧,生成白色的五氧化二磷。
白磷自燃和点燃只是反应条件有区别,但都是在燃烧状态下与氧气反应生成五氧化二磷。
扩展资料
白磷燃烧时的现象:4P+5O2=2P2O5,产生大量白烟,发光发出火焰,然后说放出热量,然后说生成白烟,最后留下白色固体(不管红磷还是白磷,空气中充分燃烧的主要产物都是五氧化二磷)。
白磷是白色或浅黄色半透明性固体。
质软,冷时性脆,见光色变深。
暴露空气中在暗处产生绿色磷光和白烟。
在湿空气中约40℃着火,在干燥空气中则稍高。
相对密度1.83(α型)、1.88(β型)。
熔点44.1℃(β型)。
白磷能直接与卤素、硫、金属等起作用,与硝酸生成磷酸,与氢氧化钠或氢氧化钾生成磷化氢及次磷酸钠。
应避免与氯酸钾、高锰酸钾、过氧化物及其他氧化物接触。
白磷化学性质
1、氧气充足燃烧:P4+5O2==2P2O5
2、氧气不充足燃烧:P4+3O2==2P2O3
3、臭氧制取:P4+2O2==P4O+O3。

红磷在氧气中燃烧的化学方程式
红磷在氧气中燃烧
化学方程式:4P+5O2点燃
=====2P2O5
文字表达式为:红磷+氧气点燃
=====五氧化二磷
【红磷燃烧的现象】
现象:产生大量的白烟,放出大量的热,生成一种白色固体
原因是:红磷和氧气反应生成了五氧化二磷颗粒,五氧化二磷是白色的固体。
【红磷燃烧的原理】
红磷燃烧的原理是氧化反应。
氧化反应是指物质与氧发生的化学反应,氧气在此过程中提供氧。
红磷燃烧也就是红磷和氧气的反应。
【红磷介绍】
磷位于元素周期表第15位,元素符号P,红磷是磷的同素异形体之一。
红磷是紫红或略带棕色的无定形粉末,有光泽。
密度2.34克/厘米3,加热升华,但在4300千帕压强下加热至590℃可熔融。
汽化后再凝华则得白磷。
化学活动性比白磷差,不发光
【五氧化二磷介绍】
五氧化二磷,化学式P2O5。
白色无定形粉末或六方晶体。
易吸湿。
360℃升华。
溶于水产生大量热并生成磷酸,相对密度2.39。
熔点569℃。
为酸性氧化物有腐蚀性,不可用手直接触摸或食用,也不可直接闻气味。
储存注意事项:储存于干燥清洁的仓间内。
相对湿度保持在75%以下。
远离火种、热源。
包装必须密封,切勿受潮。
应与易燃、可燃物,碱类等分开存放。
不可混储混运。

【化学知识点】红磷燃烧的现象和结论
红磷燃烧的现象是产生黄白色火焰,产生大量白烟,放出热量。
结论是空气中有氧气、氧气能助燃、红磷燃烧会产生大量白烟。
实验现象:红磷在氧气中燃烧会产生剧烈燃烧,并发出白光,放出热量,生成大量的
白烟。
燃烧的文字表达式:红磷+氧气—点燃→五氧化二磷。
化学方程式:4P+5O2=2P2O5。
产生物质:五氧化二磷。
实验现象:在空气中燃烧会出现黄白色火焰,放热,有大量白烟。
产生了五氧化二磷,五氧化二磷颗粒飘在空气中就是现象的白烟。
燃烧的文字表达式:红磷+氧气—点燃→五氧化二磷。
(这里需要解释的是:红磷在
空气中燃烧实质上是和氧气反应,故反应方程式中是氧气。
)
化学方程式:4P+5O2=2P2O5。
产生物质:五氧化二磷。
(1)剧烈程度不同。
红磷在氧气中是属于剧烈燃烧,而在空气中则不然,在空气中
燃烧的程度没有氧气中剧烈。
(2)颜色不同。
在氧气中的是白光,而在空气中是黄白色火焰。
(3)两种燃烧的过程中都属于放热现象,且都产生白烟,该白烟是五氧化二磷颗粒。
(1)所有燃烧或爆炸反应。
(2)酸碱中和反应。
(3)多数化合反应。
(4)活泼金属与水或酸生成H2的反应。
(5)很多氧化还原反应(但不能绝对化)。
如氢气、木炭或者一氧化碳还原氧化铜都
是典型的放热反应。
(6)NaOH或浓硫酸溶于水(注:这两点只是说会放热,但严格说起来并不算化学反应,考试时应注意)
感谢您的阅读,祝您生活愉快。
磷和氧气反应的化学方程嘿,朋友们!今天咱来聊聊磷和氧气反应的化学方程这个神奇的事儿。
你知道吗,这就像是一场微观世界里的奇妙派对呢!磷,这个小家伙,在化学世界里可是有着独特的魅力。
它就像一个活泼好动的小精灵,总是迫不及待地想要和其他小伙伴一起玩耍。
而氧气呢,就像是一个热情的伙伴,随时准备和磷来一场热烈的互动。
当磷和氧气相遇时,一场精彩的化学反应就开始啦!它们反应的化学方程式是:4P + 5O₂ = 2P₂O₅ 。
你看,这几个简单的符号和数字,背后可藏着大大的奥秘哦。
就好比在一个小小的化学舞台上,4个磷原子像是4个调皮的小舞者,它们手舞足蹈地冲向5个氧气分子,每个氧气分子就像两个紧紧相拥的好朋友。
它们一相遇,就像是点燃了一场欢乐的篝火晚会,瞬间释放出巨大的能量,然后华丽地转变成了2个五氧化二磷分子。
这些五氧化二磷分子就像是这场派对的新产物,带着全新的面貌和性质出现在我们眼前。
这个反应过程可有意思啦!磷在空气中燃烧的时候,会发出明亮的光,就像夜空中绽放的绚丽烟花,那光芒简直美极了!同时,还会伴随着大量的热释放出来,让你感觉仿佛能感受到它们之间热烈的情感交流。
这热量就像是它们兴奋的情绪,在空气中蔓延开来。
而且哦,这个反应在我们生活中也有不少应用呢。
比如说在火柴的制作中,磷就发挥了重要作用。
当我们划动火柴时,就是让磷和氧气快速反应,产生的热量和光让火柴点燃,就像点燃了我们生活中的小便利。
在一些工业生产中,这个反应也被用来制造相关的化学产品,为我们的生活和生产提供了很多帮助。
从微观的角度来看,磷原子和氧原子在反应中重新组合,形成了新的分子结构,就像是一群小伙伴重新排列组合,变成了一个全新的团队,展现出不同的能力和特点。
这也让我们感受到了化学世界的神奇和美妙,每一个原子都像是一个充满潜力的小宝藏,等待着我们去发现和探索它们的奥秘。
磷和氧气反应的化学方程不仅仅是几个符号的组合,它更是一场微观世界的奇妙盛宴,展示了化学的魅力和力量。
磷与氧气反应的化学方程式
水中磷是水体中一种重要的营养素和污染物,它的形态可以是溶解的食物素形式或可沉淀
的氢氧根酸根形式,它是鱼类和藻类的主要营养物,也是水体中的生物污染物之一。
因此,磷与氧气反应在水体中具有很重要的意义,它是水体生态系统中一个重要的营养物质来源。
磷是由一种具有特定结构的离子组成的,它可以形成一系列的氧化还原反应,并可以与氧
气反应形成特定的化合物,其化学方程式如下:
P + O2 ⇌ P2O5
该反应是一个可逆反应,在室温下该反应的反向反应速率要比正向反应速率快。
当磷与氧气反应时,会形成二酸磷,这是一种氧化物。
当发生气-液相反应时,二酸磷以液态的酸
溶液存在,在水体中可以被植物和生物吸收。
从磷的氧化还原性来看,它能够与水上的氧气反应,形成水溶性的二酸磷,从而形成水体
生态系统中的有效营养物,水质健康的同时,可以提供生物营养物质,促进水体生态系统
的平衡。
综上所述,磷与氧气反应是水体生态系统中一个重要的化学反应,它可以为水体提供营养物质,有效的改善水体的营养状况。
此外,该反应还可以控制水体的环境条件,维持水体
生态系统的稳定性和健康状态。
白磷在氧气燃烧的现象
白磷在氧气中燃烧会产生大量的白烟和光,同时生成五氧化二磷(P2O5)。
具体来说,白磷是一种高活性的化学物质,它在与氧气接触并达到一定温度时会发生剧烈的化学反应。
这个过程中,白磷迅速与氧气结合,释放出大量热量和光芒,生成白色的烟雾,这些烟雾实际上是微小的五氧化二磷颗粒。
此外,白磷燃烧的化学方程式可以表示为:4P + 5O2 → 2P2O5。
这个反应通常伴随着明亮的火光和浓烈的白烟,因此在实验室中进行这类实验时需要格外小心,采取适当的安全措施。
总的来说,白磷的燃烧是一个典型的氧化还原反应,它不仅展示了物质与氧气反应的典型现象,也是化学教学中常用的示例来说明燃烧反应和氧化还原反应的概念。