实验六叶绿体色素的质及叶绿素ab含量的测定
- 格式:ppt
- 大小:923.50 KB
- 文档页数:29

一、实验目的1. 了解叶绿素在植物光合作用中的作用。
2. 掌握叶绿素提取和测定的方法。
3. 通过实验,掌握分光光度法测定叶绿素含量的原理和操作步骤。
二、实验原理叶绿素是植物进行光合作用的重要色素,其含量直接影响植物的光合作用效率。
本实验采用分光光度法测定叶绿素含量,通过测定叶绿素a和叶绿素b的吸光度,计算出叶绿素的总含量。
分光光度法测定叶绿素含量的原理:叶绿素a和叶绿素b对光的吸收具有选择性,在一定波长范围内,其吸光度与叶绿素含量成正比。
通过测定特定波长下的吸光度,可以计算出叶绿素含量。
三、实验材料1. 新鲜植物叶片(如菠菜、生菜等)。
2. 95%乙醇溶液。
3. 0.1mol/L硫酸铜溶液。
4. 0.1mol/L氢氧化钠溶液。
5. 分光光度计。
6. 移液器。
7. 烧杯。
8. 试管。
9. 移液管。
四、实验步骤1. 准备实验材料:取适量新鲜植物叶片,洗净、擦干,剪成小块备用。
2. 叶绿素提取:取10g植物叶片,加入50mL 95%乙醇溶液,用研钵研磨至匀浆。
将匀浆转移到50mL容量瓶中,用95%乙醇溶液定容至刻度。
3. 吸光度测定:取适量叶绿素提取液,分别加入0.1mol/L硫酸铜溶液和0.1mol/L氢氧化钠溶液,配制成叶绿素a和叶绿素b溶液。
4. 标准曲线绘制:取一系列已知浓度的叶绿素a和叶绿素b标准溶液,分别测定其在特定波长下的吸光度,以吸光度为纵坐标,浓度对数值为横坐标,绘制标准曲线。
5. 样品测定:取适量叶绿素提取液,按照标准曲线绘制步骤,测定其吸光度。
6. 计算叶绿素含量:根据样品的吸光度,从标准曲线上查得对应的叶绿素a和叶绿素b浓度,计算叶绿素的总含量。
五、实验结果与分析1. 标准曲线绘制:绘制叶绿素a和叶绿素b的标准曲线,相关系数R²均大于0.99,表明标准曲线线性关系良好。
2. 样品测定:根据样品的吸光度,从标准曲线上查得叶绿素a和叶绿素b的浓度,计算叶绿素的总含量。
3. 结果分析:通过对不同植物叶片的叶绿素含量测定,可以发现不同植物叶片的叶绿素含量存在差异,这与植物的种类、生长环境等因素有关。
CONSTRUCTION节能环保一、叶绿素的概念叶绿素是一类与光合作用有关的最重要的色素。
光合作用是通过合成一些有机化合物将光能转变为化学能的过程。
叶绿素实际上存在于所有能营造光合作用的生物体,包括绿色植物、原核的蓝绿藻(蓝菌)和真核的藻类。
叶绿素从光中吸收能量,然后能量被用来将二氧化碳转变为碳水化合物。
叶绿素是植物进行光合作用的主要色素,是一类含脂的色素家族,位于类囊体膜。
叶绿素吸收大部分的红光和紫光但反射绿光,所以叶绿素呈现绿色,它在光合作用的光吸收中起核心作用。
叶绿素为镁卟啉化合物,包括叶绿素a、b、c、d、f 以及原叶绿素和细菌叶绿素等。
去镁叶绿素。
叶绿素有造血、提供维生素、解毒、抗病等多种用途。
二、实验材料和方法1、实验材料使用韭菜叶片作为实验材料,测定其叶绿素含量,样品购自菜市场,仪器使用SPECORD ®50PLUS 型双光束分光光度计、高速电动匀浆机和电子天平。
药品:无水乙醇、石油醚、聚四氯乙烯、蒸馏水、丙酮(80%)、叶绿素a 和叶绿素b 标准品;用具:锥形瓶、超声波水浴锅。
2、实验方法(1)叶绿素提取提取前先进行提取试剂的优化选择,使用乙醇、丙酮和石油醚、异辛烷、正庚烷配制成2∶3的混合溶液。
从中选择出提取叶绿素含量最高的配比溶剂进行最终提取。
叶绿素含量根据朗伯.比尔定律进行计算,叶绿素含量测定结果用mg/kg 表示,使用如下公式:w=(kxA 校正xV)/mxl,其中A 校正=A665-(A705+A625)/2,w 为样品中叶绿素含量单位为mg/kg;A665为最大吸收665nm 的吸收值;A705为705nm 附近峰谷的吸收值;A625为625nm 附近峰谷的吸收值;k 为吸光常数取值13;l 为光程,指石英杯的厚度,单位为cm;m 为试样质量数值,单位为g;V 是提取试剂的体积,单位是ml。
称量定量切碎韭菜样品放入锥形瓶内,加入乙醇和石油醚混合浸提液(2:3,以上结果证明该配比提取含量最高),使用聚四氟乙烯密封带将瓶口密封,避免混合液挥发。

实验名称:叶绿素a、叶绿素b含量测定一、实验目的:熟悉在未经分离的叶绿体色素中测定叶绿素a、叶绿素b的方法。
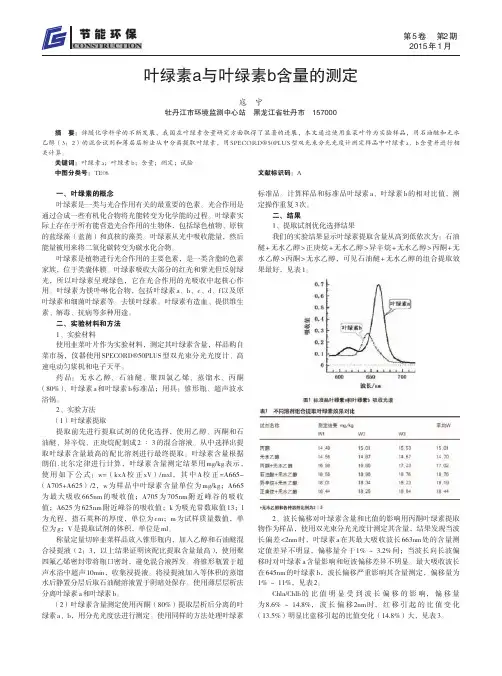
二、实验原理;根据叶绿体色素提取液对可见光的吸收,利用分光光度计在某一特定波长下测其吸光度,即可利用公式计算出提取液中各种色素的含量:Ca=13.95A665-6.88A649Cb=24.96A649-7.32 A665C T= Ca+ Cb=18.08 A649+6.63 A665三、仪器、试剂与材料:仪器:分光光度计、离心机、研钵;试剂:96%乙醇溶液、石英砂、CaCO3粉末;材料:菠菜叶片;四、实验步骤:1.取干净的菠菜叶片剪碎,分别混匀。
2.称取剪碎的样品0.2g,各2份,分别放入研钵中,加少量石英砂和CaCO3粉末、及2-3ml 96%乙醇溶液,研成匀浆,倒入离心管,再用96%乙醇溶液多次洗涤研钵,洗涤液也倒入离心管中。
3.将离心管放入离心机后取上述提取液放入比色皿中,以96%乙醇为对照,分别测定665nm、649nm处的吸光度值。
4.按公式计算提取液中叶绿素a、叶绿素b及叶绿素a+b的浓度。
五、实验结果及分析:1.研磨提取叶绿素是加入石英砂和CaCO3粉末各有什么作用?加入石英砂有助于研磨得更充分;加入CaCO3粉末可以保护叶绿素在研磨时不被破坏。
2.计算: A665(1)=0.399A A665(2)=1.237A 故A665=0.818AA649(1)=0.208A A649(2)=0.626A 故A649=0.417A 所以: Ca=13.95A665-6.88A649=8.542Cb=24.96A649-7.32 A665=4.421C T= Ca+ Cb=18.08 A649+6.63 A665=12.963。



叶绿素含量的测定实验报告一、实验目的1、掌握叶绿素含量测定的原理和方法。
2、学会使用分光光度计测定叶绿素的含量。
3、了解叶绿素在植物光合作用中的重要作用。
二、实验原理叶绿素是植物进行光合作用的重要色素,包括叶绿素 a 和叶绿素 b 两种类型。
叶绿素在特定波长的光下有吸收峰,利用分光光度计分别测定叶绿素提取液在 665nm 和 649nm 波长下的吸光度,根据朗伯比尔定律,可以计算出叶绿素 a 和叶绿素 b 的含量,进而得出叶绿素的总含量。
叶绿素 a 和叶绿素 b 在 665nm 和 649nm 波长下的吸光系数分别为8331 和 1675,在 649nm 波长下的吸光系数分别为 2454 和 4466。
三、实验材料与仪器1、实验材料新鲜的菠菜叶片。
2、实验仪器分光光度计、电子天平、研钵、漏斗、容量瓶、移液管、剪刀等。
3、实验试剂95%乙醇、石英砂、碳酸钙。
四、实验步骤1、材料准备选取新鲜的菠菜叶片,用剪刀剪碎,称取 05g 左右,放入研钵中。
2、研磨提取在研钵中加入少量石英砂和碳酸钙,以及 10ml 95%乙醇,充分研磨成匀浆。
3、过滤将研磨好的匀浆用漏斗过滤到 25ml 容量瓶中,用少量 95%乙醇冲洗研钵和漏斗,将滤液收集到容量瓶中,直至刻度线,摇匀。
4、吸光度测定以 95%乙醇作为空白对照,用分光光度计分别测定提取液在 665nm 和 649nm 波长下的吸光度,每个波长重复测定 3 次,取平均值。
五、实验结果与计算1、记录吸光度值665nm 波长下的吸光度平均值记为 A665,649nm 波长下的吸光度平均值记为 A649。
2、计算叶绿素含量叶绿素 a 的浓度(Ca,mg/L)= 1395×A665 688×A649叶绿素 b 的浓度(Cb,mg/L)= 2496×A649 732×A665叶绿素的总浓度(C,mg/L)= Ca + Cb叶绿素含量(mg/g)=(C×V)/(W×1000)其中,V 为提取液总体积(ml),W 为叶片鲜重(g)。



(完整版)叶绿体色素含量的测定编辑整理:尊敬的读者朋友们:这里是精品文档编辑中心,本文档内容是由我和我的同事精心编辑整理后发布的,发布之前我们对文中内容进行仔细校对,但是难免会有疏漏的地方,但是任然希望((完整版)叶绿体色素含量的测定)的内容能够给您的工作和学习带来便利。
同时也真诚的希望收到您的建议和反馈,这将是我们进步的源泉,前进的动力。
本文可编辑可修改,如果觉得对您有帮助请收藏以便随时查阅,最后祝您生活愉快业绩进步,以下为(完整版)叶绿体色素含量的测定的全部内容。
(完整版)叶绿体色素含量的测定编辑整理:张嬗雒老师尊敬的读者朋友们:这里是精品文档编辑中心,本文档内容是由我和我的同事精心编辑整理后发布到文库,发布之前我们对文中内容进行仔细校对,但是难免会有疏漏的地方,但是我们任然希望 (完整版)叶绿体色素含量的测定这篇文档能够给您的工作和学习带来便利。
同时我们也真诚的希望收到您的建议和反馈到下面的留言区,这将是我们进步的源泉,前进的动力。
本文可编辑可修改,如果觉得对您有帮助请下载收藏以便随时查阅,最后祝您生活愉快业绩进步,以下为〈(完整版)叶绿体色素含量的测定> 这篇文档的全部内容。
叶绿体色素含量的测定---—分光光度法中文摘要:本实验利用菠菜叶作为原料用80%的丙酮提取叶绿体色素,应用分光光度计在某一特定波长下所测定的吸光度,带入公式计算出色素溶液中各色素浓度。
英文摘要:In this experiment , we used spinach leaves as raw material and used 80% of acetone to extract pigments from them ,and apply spectrophotometer at a particular wavelength to determine absorbance, then take the absorbance into the formula to calculate concentration of each pigment。

实验14 叶绿素a 和b 含量的测定(分光光度法)一、目的学会Chla 、b 含量的测定方法,了解叶片中Chla 、b 的含量。
二、材料用具及仪器药品菠菜叶片、721分光光度计、天平、研钵、剪刀、容量瓶(25ml )、漏斗、滤纸、乙醇(95%)三、原理叶绿素a 、b 在波长方面的最大吸收峰位于665nm 和649nm ,同时在该波长时叶绿素a 、b 的比吸收系数K 为已知,我们即可以根据Lambert Beer 定律,列出浓度C 与光密度D 之间的关系式:D 665=83.31Ca+18.60C b (1)D 649=24.54Ca+44.24 C b (2)(1)(2)式中的D 665、D 649为叶绿素溶液在波长665nm 和649nm 时的光密度。
为叶绿素a 、b 的浓度、单位为每升克数。
82.04、9.27为叶绿素a 、b 在、在波长665nm 时的比吸收系数。
16.75、45.6为叶绿素a 、b 在、在波长649nm 时的比吸收系数。
解方程式(1)(2),则得 :C A =13.7 D 665—5.76 D 649 (3)C B =25.8 D 649—7.6 D 665 (4)G=C A +C B =6.10 D 665+20.04 D 649 (5)此时,G 为总叶绿素浓度,C A 、C B 为叶绿素a 、b 浓度,单位为每升毫克,利用上面(3)(4)(5)式,即可以计算叶绿素a 、b 及总叶绿素的总含量。
四、方法步骤1.称取0.1克新鲜叶片,剪碎,放在研钵中,加入乙醇10ml 共研磨成匀浆,再加5ml 乙醇,过滤,最后将滤液用乙醇定容到25ml 。
2.取一光径为1cm 的比色杯,注入上述的叶绿素乙醇溶液,另加乙醇注入另一同样规格的比色杯中,作为对照,在721分光光度计下分别以665nm 和649nm 波长测出该色素液的光密度。
计算结果:叶绿素a 含量(mg/g. FW )=2.01100025⨯⨯A C 叶绿素b 含量(mg/g.FW )=2.01100025⨯⨯B C 叶绿素总量(mg/g.FW )=2.01100025⨯⨯G五、实验报告计算所测植物材料的叶绿素含量。

叶绿素的提取及含量测定实验报告一、实验目的1、掌握叶绿素提取的原理和方法。
2、学会使用分光光度计测定叶绿素的含量。
3、了解叶绿素的性质和在植物光合作用中的重要作用。
二、实验原理叶绿素是植物进行光合作用的重要色素,包括叶绿素 a 和叶绿素 b两种类型。
叶绿素不溶于水,易溶于有机溶剂,如丙酮、乙醇等。
在提取过程中,利用有机溶剂将叶绿素从植物叶片中溶解出来。
叶绿素溶液在特定波长下有吸收峰,叶绿素 a 在 663nm 波长处,叶绿素 b 在 645nm 波长处。
根据朗伯比尔定律,吸光度与溶液中物质的浓度成正比。
通过测定提取液在这两个波长下的吸光度,并利用公式计算,可以得出叶绿素a 和叶绿素b 的含量,进而计算总叶绿素含量。
三、实验材料与仪器1、实验材料新鲜菠菜叶2、实验仪器电子天平、研钵、漏斗、玻璃棒、容量瓶(25ml、50ml)、分光光度计、移液管(1ml、2ml、5ml)、剪刀3、实验试剂丙酮、无水乙醇、石英砂、碳酸钙四、实验步骤1、材料准备选取新鲜的菠菜叶,洗净擦干,去除叶柄和中脉,剪碎备用。
2、叶绿素提取称取 2g 剪碎的菠菜叶放入研钵中,加入少量石英砂和碳酸钙,再加入 5ml 丙酮和 5ml 无水乙醇,充分研磨成匀浆。
用漏斗过滤,将滤液收集到 25ml 容量瓶中,并用少量丙酮和无水乙醇冲洗研钵和漏斗,将冲洗液也倒入容量瓶中,最后用丙酮和无水乙醇定容至刻度,摇匀。
3、吸光度测定以丙酮和无水乙醇的混合液为空白对照,用分光光度计分别测定叶绿素提取液在 663nm 和 645nm 波长下的吸光度。
每个波长重复测定 3 次,取平均值。
4、计算叶绿素含量根据以下公式计算叶绿素 a、叶绿素 b 和总叶绿素的含量(单位:mg/g):叶绿素 a 含量= 127×A663 269×A645叶绿素 b 含量= 229×A645 468×A663总叶绿素含量=叶绿素 a 含量+叶绿素 b 含量式中,A663 和 A645 分别为在 663nm 和 645nm 波长下的吸光度。
实验四、叶绿体色素的提取、分离及叶绿素a、b含量的测定刘家富(40508014)05生科(一)一、实验原理1.脂溶性叶绿体色素提取:可用乙醇、丙酮等有机溶剂提取。
2.分离:(1)叶绿体色素的分离<纸层析法>因吸附剂对不同物质的吸附力不同,当用适当的溶剂推动时,混合物中各种成分在两相(固定相和流动相)间具有不同的分配系数,所以移动速度不同,经过一定时间后,可将各种色素分开。
纸层析是以滤纸纤维为固定相,而以有机溶剂作为流动相。
由于样品中各物质有不同的分配系数,移动速度因此而不同,从而达到分离的目的。
(2)叶绿素与类胡萝卜素的分离<皂化反应>叶绿素是一种二羧酸——叶绿酸与甲醇和叶绿醇形成的复杂酯,故可与碱起皂化反应而生成醇与叶绿酸的盐,产生的盐能溶于水中,可用此法将叶绿素与类胡萝卜素分开。
3.叶绿素a、b含量的测定:根据朗伯—比尔定律,某有色溶液的吸光度A与其溶液浓度c和液层厚度L成正比,即:A=φCL(φ为吸光系数)因此,根据叶绿体色素提取液对可见光谱的吸收,利用分光光度计在某一特定波长下测定其吸光度,用公式即可计算出提取液中各色素含量。
测定663nm和645nm两个特定波长下的吸光度A,并根据叶绿素a、b在对应波长下的吸光系数即可求出叶绿素a、b含量。
其校正过的公式为:C a=12.7A663-2.69A645 Ca:叶绿素a浓度,mg/LC b=22.9A645-4.68A663 Cb:叶绿素b浓度,mg/LCT=Ca + Cb CT:叶绿素总浓度,mg/L二、仪器药品剪刀、漏斗、烧杯、分光光度计、分液漏斗、铁架台、移液管、吸耳球、试管、毛细管、平底大试管、石英砂、碳酸钙、丙酮、乙醚、四氯化碳、无水硫酸钠、30%KOH-甲醇溶液、天平、研钵、滤纸三、操作步骤1. 叶绿体色素的提取取去中脉叶片(2g左右),剪碎后加入少量石英砂、碳酸钙、纯丙酮5ml后放入研钵研磨成匀浆成深绿色提取液,之后用漏斗过滤。
实验14 叶绿素a 和b 含量的测定(分光光度法)一、目的学会Chla 、b 含量的测定方法,了解叶片中Chla 、b 的含量。
二、材料用具及仪器药品菠菜叶片、721分光光度计、天平、研钵、剪刀、容量瓶(25ml )、漏斗、滤纸、乙醇(95%)三、原理叶绿素a 、b 在波长方面的最大吸收峰位于665nm 和649nm ,同时在该波长时叶绿素a 、b 的比吸收系数K 为已知,我们即可以根据Lambert Beer 定律,列出浓度C 与光密度D 之间的关系式:D 665=83.31Ca+18.60C b (1)D 649=24.54Ca+44.24 C b (2)(1)(2)式中的D 665、D 649为叶绿素溶液在波长665nm 和649nm 时的光密度。
为叶绿素a 、b 的浓度、单位为每升克数。
82.04、9.27为叶绿素a 、b 在、在波长665nm 时的比吸收系数。
16.75、45.6为叶绿素a 、b 在、在波长649nm 时的比吸收系数。
解方程式(1)(2),则得 :C A =13.7 D 665—5.76 D 649 (3)C B =25.8 D 649—7.6 D 665 (4)G=C A +C B =6.10 D 665+20.04 D 649 (5)此时,G 为总叶绿素浓度,C A 、C B 为叶绿素a 、b 浓度,单位为每升毫克,利用上面(3)(4)(5)式,即可以计算叶绿素a 、b 及总叶绿素的总含量。
四、方法步骤1.称取0.1克新鲜叶片,剪碎,放在研钵中,加入乙醇10ml 共研磨成匀浆,再加5ml 乙醇,过滤,最后将滤液用乙醇定容到25ml 。
2.取一光径为1cm 的比色杯,注入上述的叶绿素乙醇溶液,另加乙醇注入另一同样规格的比色杯中,作为对照,在721分光光度计下分别以665nm 和649nm 波长测出该色素液的光密度。
计算结果:叶绿素a 含量(mg/g. FW )=2.01100025⨯⨯A C 叶绿素b 含量(mg/g.FW )=2.01100025⨯⨯B C 叶绿素总量(mg/g.FW )=2.01100025⨯⨯G五、实验报告计算所测植物材料的叶绿素含量。
叶绿素a、b含量测定【实验原理】如果混合液中的两个组分,它们的光谱吸收峰虽然有明显的差异,但吸收曲线彼此有些重叠,在这种情况下要分别测定两个组分,可根据Lambert-Beer定律,通过代数方法,计算一种组分由于另一种组分存在时对光密度的影响,最后分别得到两种组分的含量。
叶绿素a和b的吸收光谱曲线,叶绿素a的最大吸收峰在663nm,叶绿素b在645nm,吸收曲线彼此又有重叠。
根据Lambert-Beer定律,最大吸收光谱峰不同的两个组分的混合液,它们的浓度C与光密度OD之间有如下的关系:OD1=C a·k a1+C b·k b1(1)OD2=C a·k a2+C b·k b2(2)式中:C a为组分a的浓度,g/L;C b 为组分b的浓度,g/L;OD1为在波长λ1(即组分a的最大吸收峰波长)时,混合液的光密度OD值;OD2为在波长λ2(即组分b的最大吸收峰波长)时,混合液的光密度OD值;k a1为组分a的比吸收系数,即组分a当浓度为1g/L时,于波长λ1时的光密度OD值;k a2为组分a(浓度为1g/L),于波长λ2时的光密度OD值;k b1为组分b(浓度为1g/L),于波长λ1时的光密度OD值;k b2为组分b的比吸收系数,即组分b当浓度为1g/L时,于波长λ2时的光密度OD值;从文献中可以查到叶绿素a和b的80%丙酮溶液,当浓度为1g/L时,比吸收系数k值如下:波长(nm)叶绿素a叶绿素b66382.049.2764516.7545.60将表中数值代入上式(1)、(2),则得:OD663=82.04×C a+9.27×C bOD645=16.75×C a+45.60×C b经过整理之后,即得到下式:C a=0.0127 OD663-0.00269 OD645C b=0.0229 OD645-0.00468 OD663如果把C a,C b的浓度单位从原来的g/L改为mg/L,则上式可改写为下列形式:C a=12.7 OD663-2.69 OD645(3)C b=22.9 OD645-4.68 OD663(4)C T= C a+ C b=8.02 OD663+20.21 OD645(5)(5)式中C T为总叶绿素浓度,单位为mg/L。
试验汇报课程名称: 植物生理学试验(乙) 指导老师: 成绩: __________________试验名称: 叶绿体色素提取、 分离、 理化性质和叶绿素含量测定 试验类型:一、试验目和要求了解改良半叶法、 氧电极法测定光合作用和呼吸作用基础原理, 掌握红外线CO2分析仪法测定光合作用和呼吸作用, 蒸腾速率和气孔导度测定基础原理;掌握用LI-6400测定光合作用、 呼吸作用、 蒸腾速率和气孔导度方法, 测定光-光合响应曲线方法.二、 试验基础原理(一)改良半叶法测定光合作用(二)熟悉仪器基础结构, 及按装调试。
以榕树和蚕豆等植物为材料, 用LI-6400portable photosynthesis system 测定它们光合作用、 呼吸作用、 蒸腾速率和气孔导度及光-光合响应曲线, 经过比较分析其属于什么光合类型植物。
Principles for measuring photosynthesis and respiration 6CO 2+6H 2O 6(CH 2O)+6O 2一)测干重——改良半叶法: 同面积光暗叶片重量差。
使用三氯乙酸(TCA )涂抹在叶片叶柄处, 阻断叶片在进行光合作用时候向外输出营养物质。
测定为总光合作用量。
二)测放O2 ——氧电极法。
气相和液相。
氧电极原理: 氧电极是由嵌在有机玻璃上铂和银所组成, 以0.5mol/L KCl 为电解质, 电极头外覆盖一层聚乙烯或聚四氟乙烯薄膜, 其厚度在15~25μm 之间, 用“〇”形套膜环固定, 使电极与被测溶液隔离, 而溶解在溶液中氧仍能透过薄膜, 进入电极内。
较薄膜易透过氧, 所以对氧浓度改变响应时间短.三)红外线CO2分析仪法: CO2吸收4260nm 红外线,有封闭式: 单位时间内CO2下降量和开放式: 参比室和叶室CO2差值 本试验将采取开放式测得。
三、 试验材料与试剂1. 试验试剂: 三氯乙酸(TCA )2. 试验材料: 树叶、 菜豆四、试验器材与仪器天平、湿毛巾、烘箱、打孔器、游标卡尺、剪刀、 LI-6400 portable photosynthesis system五、试验操作方法和步骤(一)改良半叶法: 光照不少于1.5h, 注意测定打孔器内径(计算面积)。