两水相萃取蛋白质的相图制作实验
- 格式:pdf
- 大小:363.11 KB
- 文档页数:5



双水相萃取牛血清蛋白数据记录表1 PEG2000-硫酸铵双水相体系相图的制作表实验现象记录图1 取的三个成相比例的成相试管图图2 分别拍照的试管其中之一近图图3 余下两支试管图4 一个成相比例的试管取上下相溶液各1ml后加入双缩脲试剂图实验结果处理由标准曲线得吸光度和蛋白质浓度关系为y=0.2321x+0.0089(其中y代表吸光度,x代表蛋白质浓度)由此可得下表:表2 样品吸光度和蛋白质含量根据实验所得数据,计算系统的相比,蛋白在不同双水相系统中的分配系数及收率。
计算公式如下:表观分配系数 K=Ct/Cb相比 R=Vt/Vb收率 P=下相蛋白含量/上下相蛋白总含量=Vt*Ct/(Vt*Ct+Vb*Cb)=R*K/(1+R*K) 式中 Ct、Cb分别为上下相蛋白浓度;Vt、Vb分别为上下相体积。
表3 样品蛋白在不同双水相系统中的分配系数及收率分析讨论一、相图制备中误差1、在滴定硫酸铵前,滴定管已经清洗干净,但是没有用蒸馏水试漏,也没有用滴定液润洗,这在一定程度上稀释了滴定液,在滴定过程中也没有办法较好地控制活塞,以控制滴定量。
而且用滴定液润洗还可以将气泡排除,这点也没有做好,这些都是可能的误差来源。
2、滴定过程中,接近滴定终点时没有一滴一滴地加,加入几滴之后才摇晃试管的,这样,可能出现浑浊的点已经过了终点,数据产生误差。
而且读数也有误差,只由一位同学读数,使误差增大。
二、分离过程中误差1、相图绘制出之后,需取三个成相比例。
因为相图绘制有误差,在取点时也是取的大概位置,这使得之后计算出的PEG2000和硫酸铵的质量也是大概数值,这对之后对蛋白质的萃取有影响。
2、在测上下相体积时,有的试管上下相体积相差比较大,下相体积很小,因此体积测量可能存在误差。


双水相萃取牛血清蛋白一.实验目的1.了解双水相系统的成相原理和方法;2.了解制作双水相系统相图的方法,加深对相图的认识;3.掌握双水相溶液配制与双水相萃取的操作;4.掌握分配系数和萃取收率的计算方法。
二. 实验原理双水相系统是由两种互不相溶的聚合物(如聚乙二醇(PEG)与葡聚糖(DX))或者互不相溶的聚合物溶液和盐溶液(如PEG与(NH4)2SO4)组成。
双水相系统的制备一般是将两种溶质分别配制成一定浓度的水溶液,然后将两种溶液按照不同的比例混合,静止一段时间,当两种溶质的浓度超过某一浓度范围时,就会产生两相。
相图是研究双水相萃取的基础,双水相形成条件和定量关系常用相图来表示。
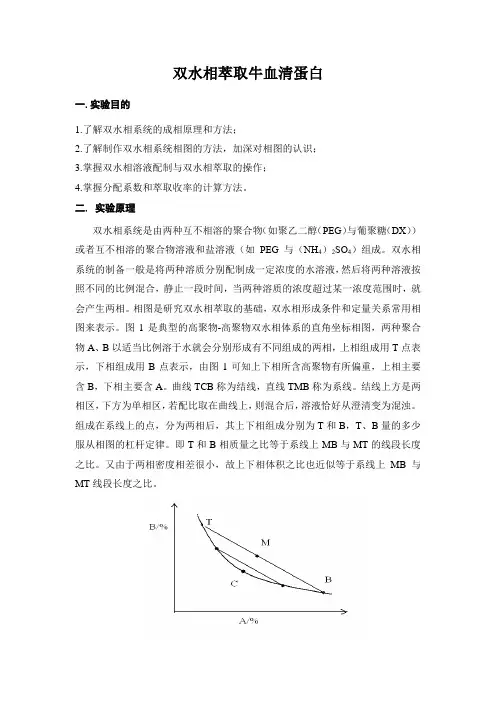
图1是典型的高聚物-高聚物双水相体系的直角坐标相图,两种聚合物A、B以适当比例溶于水就会分别形成有不同组成的两相,上相组成用T点表示,下相组成用B点表示,由图1可知上下相所含高聚物有所偏重,上相主要含B,下相主要含A。
曲线TCB称为结线,直线TMB称为系线。
结线上方是两相区,下方为单相区,若配比取在曲线上,则混合后,溶液恰好从澄清变为混浊。
组成在系线上的点,分为两相后,其上下相组成分别为T和B,T、B量的多少服从相图的杠杆定律。
即T和B相质量之比等于系线上MB与MT的线段长度之比。
又由于两相密度相差很小,故上下相体积之比也近似等于系线上MB与MT线段长度之比。
图1 A-B双水相体系相图双水相萃取与有机溶剂萃取原理相似,都是依据物质在两相间的选择性分配原则。
当物质进入双水相体系后,由于表面性质、电荷作用和各种力(如憎水性、氢键、离子键等)的存在,使得待分离的物质在上、下相中的浓度不同。
对于某一物质,只要选择合适的双水相体系,控制一定的条件就可以得到合适的分配系数,从而达到分离纯化的目的。
本实验选择PEG-硫酸铵双水相系统萃取牛血清蛋白。
双缩脲反应是指蛋白质在碱性溶液中与二价铜离子结合生成紫色络合物的反应。
含有两个或两个以上肽键的化合物都具有双缩脲反应,蛋白质含有多个肽键,因此有双缩脲反应,反应生成物颜色的深浅与蛋白质含量成正比,因此可以利用双缩脲反应进行蛋白质的定量测定。
实验一:双水相萃取的相图制作一、试验目的1了解双水相萃取的原理和发展历史、趋势2 掌握用浊点法制作双水相系统相图的方法。
二、试验原理某些亲水性高分子聚合物的水溶液超过一定浓度后可形成两相,并且在两相中水分占很大比例,即形成双水相。
常见的双水相系统可分为两类,即双聚合物体系和聚合物/盐体系。
双水相形成的条件和定量关系可用相图来表示,它是研究双水相萃取的基础。
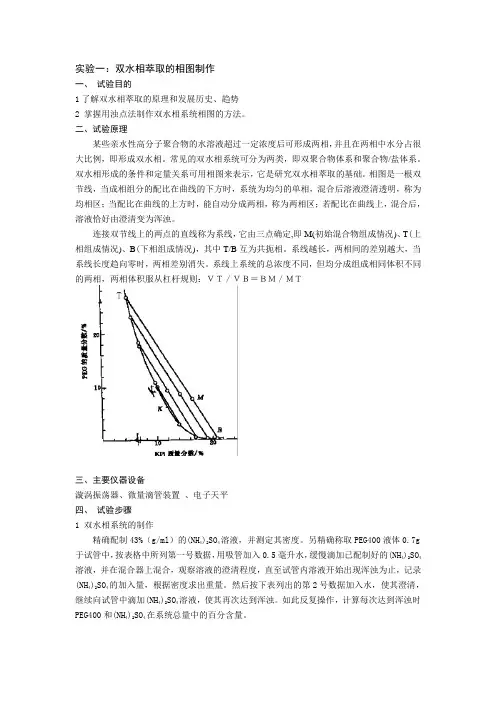
相图是一根双节线,当成相组分的配比在曲线的下方时,系统为均匀的单相,混合后溶液澄清透明,称为均相区;当配比在曲线的上方时,能自动分成两相,称为两相区;若配比在曲线上,混合后,溶液恰好由澄清变为浑浊。
连接双节线上的两点的直线称为系线,它由三点确定,即M(初始混合物组成情况)、T(上相组成情况)、B(下相组成情况),其中T/B互为共扼相。
系线越长,两相间的差别越大,当系线长度趋向零时,两相差别消失。
系线上系统的总浓度不同,但均分成组成相同体积不同的两相,两相体积服从杠杆规则:VT/VB=BM/MT三、主要仪器设备漩涡振荡器、微量滴管装置、电子天平四、试验步骤1 双水相系统的制作精确配制43%(g/ml)的(NH4)2SO4溶液,并测定其密度。
另精确称取PEG400液体0.7g 于试管中,按表格中所列第一号数据,用吸管加入0.5毫升水,缓慢滴加已配制好的(NH4)2SO4溶液,并在混合器上混合,观察溶液的澄清程度,直至试管内溶液开始出现浑浊为止,记录(NH4)2SO4的加入量,根据密度求出重量。
然后按下表列出的第2号数据加入水,使其澄清,继续向试管中滴加(NH4)2SO4溶液,使其再次达到浑浊。
如此反复操作,计算每次达到浑浊时PEG400和(NH4)2SO4在系统总量中的百分含量。
2 相图的绘制以PEG400的重量百分比浓度为纵坐标,(NH4)2SO4的重量百分比浓度为横坐标作图,即得到一条双节线的相图。
五、注意事项1、微量滴定管在使用前必须先洗涤干净,否则容易产生气泡或发生堵塞现象。


实验一:双水相萃取的相图制作一、试验目的1了解双水相萃取的原理和发展历史、趋势2 掌握用浊点法制作双水相系统相图的方法。
二、试验原理某些亲水性高分子聚合物的水溶液超过一定浓度后可形成两相,并且在两相中水分占很大比例,即形成双水相。
常见的双水相系统可分为两类,即双聚合物体系和聚合物/盐体系。
双水相形成的条件和定量关系可用相图来表示,它是研究双水相萃取的基础。
相图是一根双节线,当成相组分的配比在曲线的下方时,系统为均匀的单相,混合后溶液澄清透明,称为均相区;当配比在曲线的上方时,能自动分成两相,称为两相区;若配比在曲线上,混合后,溶液恰好由澄清变为浑浊。
连接双节线上的两点的直线称为系线,它由三点确定,即M(初始混合物组成情况)、T(上相组成情况)、B(下相组成情况),其中T/B互为共扼相。
系线越长,两相间的差别越大,当系线长度趋向零时,两相差别消失。
系线上系统的总浓度不同,但均分成组成相同体积不同的两相,两相体积服从杠杆规则:VT/VB=BM/MT三、主要仪器设备漩涡振荡器、微量滴管装置、电子天平四、试验步骤1 双水相系统的制作精确配制43%(g/ml)的(NH4)2SO4溶液,并测定其密度。
另精确称取PEG400液体0.7g 于试管中,按表格中所列第一号数据,用吸管加入0.5毫升水,缓慢滴加已配制好的(NH4)2SO4溶液,并在混合器上混合,观察溶液的澄清程度,直至试管内溶液开始出现浑浊为止,记录(NH4)2SO4的加入量,根据密度求出重量。
然后按下表列出的第2号数据加入水,使其澄清,继续向试管中滴加(NH4)2SO4溶液,使其再次达到浑浊。
如此反复操作,计算每次达到浑浊时PEG400和(NH4)2SO4在系统总量中的百分含量。
2 相图的绘制以PEG400的重量百分比浓度为纵坐标,(NH4)2SO4的重量百分比浓度为横坐标作图,即得到一条双节线的相图。
五、注意事项1、微量滴定管在使用前必须先洗涤干净,否则容易产生气泡或发生堵塞现象。

吉林化工学院生物分离工程专业实验报告课程类型:生物分离工程实验实验类型:设计型实验学年学期:2015-2016学年第一学期试验时间: 2015.10.8-2015.11.20 班级:学号:实验者:合作者:指导教师:提交日期:2015年11月29日吉林化工学院Jilin Institute of Chemical Technology两水相萃取蛋白质的相图制作实验摘要:目前在生化工业中常用的分离生物活性物质的方法,如有机溶剂萃取法等存在着一定的缺陷,例如由于有相的变化或有机溶剂的变性作用使得生物活性物质易于失活;在水—有机溶剂萃取中,界面上具有很强的界面张力,可破坏生物大分子的结构。
双水相萃取技术的发展趋势还体现在与其他生物分离技术的结合以及萃取机理和热力学模型的优化上。
关键词:双水相萃取,蛋白质,分离纯化分离纯化出高纯度有生物活性的蛋白质一直是项艰巨的工作。
由于蛋白质的市场价格昂贵,提高回收率能带来巨大的经济效益,所以有关蛋白质在分离纯化中的失活及其对策在近年来受到很大的关注。
双水相萃取是通过溶质在两水相之间分配系数的差异而进行萃取的技术,其应用于蛋白质的分离纯化具有以下优势:体系含水量高.可达80%以上。
萃取环境和操作条件温和,蛋白质在其中不易失活;界面张力远远低于水一有机溶剂两相体系的界面张力,有助于强化相际闸的质量传递;易于按比例放大和进行连续性操作等⋯。
正是由于双水相萃取技术的诸多优势,现已被广泛用于蛋白质的分离纯化,取得了很好的成效。
近年来,双水相萃取技术的分离对象进一步扩大,已包括了多肽、氨基酸、植物有效成分、重金属离子和抗生素等。
1 双水相萃取技术在生物分离工程中的应用1956年,瑞典Lund大学学者A1bertson首次利用双水相萃取技术分离生物分子,开始对A邛s进行比较系统的研究,测定了许多ATPs的相图,考察了蛋白质、核酸、病毒、细胞及细胞颗粒在ATPS中的分配行为,为发展双水相萃取技术奠定了坚实的基础。

离子液体双水相体系萃取分离牛血清白蛋白邓凡政*郭东方(淮北煤炭师范学院化学系,淮北235000)本文系安徽省教育厅自然科学研究项目(No. 2004kj319)资助摘要建立了由亲水性离子液体四氟硼酸1-甲基-3-丁基咪唑([Bmim]BF4)和KH2PO4形成的双水相体系萃取分离牛血清白蛋白(BSA)的新方法。
研究了不同盐及盐的浓度、离子液体浓度以及蛋白质用量、溶液酸度、其它共存物质对双水相成相及BSA萃取率的影响,结果表明,磷酸二氢钾盐浓度为80 g/L,离子液体浓度在160~240 mL/L,BSA的浓度为30~50 mg/L,溶液酸度在pH 4~8范围,离子液体双水相体系对BSA有较高的萃取率。
用加入不同类型表面活性剂探讨了离子液体与蛋白质之间的作用。
关键词离子液体,双水相,牛血清白蛋白,萃取分离1引言离子液体是在室温或室温附近由离子构成呈液态的物质,具有优异的化学热力学稳定性,其液态温度区间大、溶解范围广、没有显著的蒸气压以及极性较强且酸性可调等优点。
因此,它是一种极具吸引力的绿色溶剂,被称为环境友好液体、“可设计性”溶剂,是传统挥发性有机溶剂的理想替代品[1]。
近年来,离子液体也被用于萃取分离领域, Jonathan等[2]以甲基咪唑类离子液体作为萃取剂对多种有机物进行了萃取,离子液体还用于生物技术中的分离提取,如从生物燃料ABE的发酵液中回收丁醇[3];顾彦龙等[4]利用室温离子液体浸取分离牛磺酸与硫酸钠固体混合物;刘庆芬等[5]利用离子液体双水相体系对青霉素进行分离。
而利用该体系对于蛋白质萃取分离的报道还较少见。
为了扩大该领域应用范围,本研究用亲水性离子液体[Bmim]BF4和磷酸二氢钾,形成上相富集离子液体和下相富集磷酸盐的双水相体系对牛血清白蛋白进行萃取研究。
结果表明,该离子液体双水相体系,对牛血清白蛋白有较高的萃取率,为提纯分离蛋白质,提供一种新的方法。
2实验部分2.1仪器与试剂TU-1901双光束紫外可见分光光度计(北京普析通用仪器有限公司); 721型可见分光光度计(上海光谱仪器有限公司); pHs-3型精密酸度计(上海雷磁仪器厂)。
实训1 双水相萃取相图的制作一、实训目的1. 学习双水相分离萃取的原理和方法2. 学习双水相萃取相图的制作二、实训原理双水相萃取法是利用物质在互不相容的两个水相间分配系数的差异来进行萃取的方法。
两水相的形成:高聚物与无机盐在水中由于盐析的作用会形成两个相,如PEG 与硫酸盐或碱性磷酸盐。
两种亲水性高聚物在水中由于聚合物的不相容性也会形成两个相。
但是它们只有达到一定的浓度时,才能形成两相,双水相形成的定量关系可用相图来表示。
相图是一根双节线, 把均匀区和两相区分隔开来。
当成相组分的配比取在:线的下方时,为均相区; 曲线的上方时,为两相区;在曲线上,则混合后,溶液恰好从澄清变为浑浊。
相图中TMB 称为系线;T 代表上相组成;B 代表下相组成;同一条系线上各点分成的两相具有相同的组成,但体积比不同。
V T / V B = BM / MT三、实训器材、试剂、材料1.器材:试管,离心机,天平,离心管,三角瓶,滴定管。
2.试剂:聚乙二醇2000(PEG2000),硫酸铵。
四、实训操作步骤1.PEG2000(NH 4)2SO 4双水相体系相图的测定(1)取10%(g/ mL )PEG2000溶液10mL 于三角瓶中。
(2)用40%(g/mL )(NH 4)2SO 4溶液装入滴定管中滴定至三角并中溶液出现浑浊,记录)NH4)2SO 4溶液消耗的体积。
加入1mL 水使溶液澄清,继续用(NH 4)2SO 4溶液滴定至浑浊,重复7~8次,记录每次(NH 4)2SO 4溶液消耗的体积,计算每次出现浑浊时体系中PEG2000和(NH 4)2SO 4的浓度(g/mL )。
(3) 以(NH 4)2SO 4的浓度(g/mL )为横坐标,PEG2000的浓度(g/mL )为纵坐标,绘制PEG2000- (NH 4)2SO 4双水相体系相图。
2. 相图制作表10%PEG2000 10mL 温度T=20℃次H 2O 加量(NH 4)2SO 4纯(NH 4)2SO 4溶液累PEG2000(NH 4)2SO 4PEG2000 %(NH 4)2SO 4 %两相 均相数(mL) 溶液加量累计量(g)计总量(mL)(%) (%)(mL) (g)1 12 13 14 15 16 17 18 1五、结果与讨论1.如何正确绘制相图。
双水相萃取相图的绘制1.实验目的⑴掌握绘制双水相相图的方法⑵理解双水相形成条件和定量关系2.实验原理双水相是指某些高聚物之间或高聚物与无机盐之间在水中以一定的浓度混合而形成互不相容的两相,由于溶质在两相间的分配系数的差异而进行萃取的方法即为双水相萃取。
双水相形成条件和定量关系常用相图来表示(见图1)。
成相物质都能与水无限混合,当它们的组成位于曲线的上方时(用M点表示)体系就会分成两相,分别有不同的组成密度,轻相(或称上相)组成用T点表示,重相(或称下相)组成用B点表示,T、B点称为节点。
直线TMB称为系线,是相图的重要特征,关系到相的平衡组成。
所有组成在系线上的点,分成两相后,其上下相组成均分别为T、B,但是其体积比(V T/V B)不同。
相体积比可由相图上线段比(BM/MT)估算,即服从杠杆规则。
本实验绘制PEG/(NH4)2SO4体系双水相相图。
图1 双水相体系相图3.实验材料及仪器PEG1000原液(0.6g/mL,w/w=56.926%,密度1.054);PEG2000原液(0.4g/mL,密度1.02);硫酸铵原液(0.43g/mL,密度1.2)。
4.实验方法准确称取2.0mLPEG原液,加入25 mL具塞刻度试管中,然后逐滴加入硫酸铵原液,混合,直至试管中开始出现混浊为止,记录加入硫酸铵量,算出PEG和硫酸铵在系统中的质量百分浓度,再向试管中加入适量水(0.2~0.5~1.0 mL),使体系变澄清,记录加入水的量,并继续加入硫酸铵,使体系再次变混浊,如此反复操作二十几次,计算达到混浊时PEG 和硫酸铵在系统中的质量百分含量,得出不同相对分子量的PEG和硫酸铵的双节线相图节点。
以上述试验所得结点绘制出不同相对分子量的PEG/(NH4)2SO4体系双水相相图。
5.数据处理表1 相图节点数据序号PEG质量(g)体系中盐溶液(mL)盐质量(g)体系加水量(g)体系总质量(g)PEG质量分数(w/w)盐质量分数(w/w)1 02 0.33 0.5……………………n 1.5双水相萃取牛血清白蛋白1.实验目的⑴掌握PEG/无机盐体系双水相萃取蛋白质的方法⑵了解影响蛋白质在双水相体系中分配行为的主要参数2.实验原理双水相是指某些高聚物之间或高聚物与无机盐之间在水中以一定的浓度混合而形成互不相容的两相,由于溶质在两相间的分配系数的差异而进行萃取的方法即为双水相萃取。