药品批发企业自查自纠表
- 格式:doc
- 大小:47.50 KB
- 文档页数:2

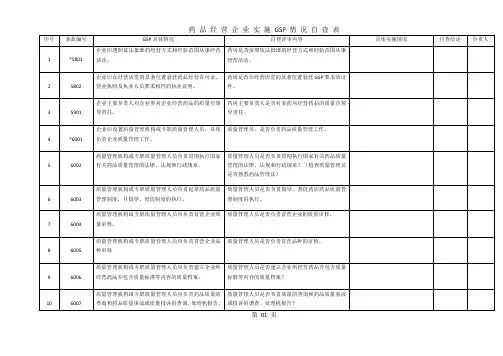
药品批发企业GSP自查情况表企业名称:自查期:年月日至年月日自查小组全体人员(签名):说明:1、本自查表中条款系指国家局《药品批发企业GSP认证检查评定标准(试行)》中的检查项目条款;企业自查时,应根据国家局制定的《药品批发企业<GSP 认证现场检查项目>》以及本表自查方法的有关内容执行;2、本自查表检查范围为本次自查期内企业实施GSP的具体情况;3、凡自查中结果为“否”的,应将缺陷具体情况详细记录在备注栏中;4、药品批发企业接受零售连锁企业药品配送业务的,委托部分内容由药品批发企业依据药品零售连锁企业GSP认证现场检查项目负责自查。
具体检查内容和方法如下:(1)0401-0901项:其中0802中涉及药品采购、仓贮、养护、配送的药品质量管理制度的内容由接受委托的药品批发企业负责自查,其他内容由零售连锁企业负责自查。
(2)1001-1702项:涉及药品购进、验收、保管、养护、配送有关岗位的人员,由接受委托的药品批发企业负责自查;其他岗位的工作人员,由零售连锁企业负责自查。
(3)1801-2603项:零售连锁企业总部的营业场所由零售连锁企业负责自查;涉及药品的验收、保管、养护、配送的设施设备由接受委托的药品批发企业负责自查。
[药品批发企业司应单独设置便于配货活动展开的配货场所(2603)(应将批发发货区域同连锁配货、配送区域有效分开,保证相对独立,避免物流的混乱和发货的差错)]。
(4)2701-3401项:其中3101、3401由零售连锁企业负责自查;其他涉及进货的条款由接受委托药品批发企业根据零售连锁企业总部从门店抽取的药品负责自查。
(5)3501-3701项:由接受委托药品批发企业负责自查。
(6)4001--4005项:分别由接受委托的药品批发企业以及零售连锁企业进行自查。
(7)4101-4209项:由接受委托的药品批发企业负责自查。
(8)4301-5301项:由接受委托的药品批发企业负责自查。

药店自查自纠情况一、药品采购1. 药品供应商合规性自查针对所有的药品供应商进行资质核实,查看营业执照、药品经营许可证等证照齐全性,确保与资质合规的药品供应商合作,杜绝非法渠道的药品进货。
2. 采购记录真实性核查每一次采购活动都要有相应的采购记录,包括采购数量、金额、日期等信息,确保记录准确无误,方便后续查询。
3. 药品质量检测对每一批购进的药品都要进行质量检测,确保符合国家药品质量标准,避免假冒伪劣药品进入销售环节。
二、药品储存1. 药品储存环境检查定期检查药品储存环境,包括温度、湿度、光线等因素,确保储存环境符合药品要求,避免药品变质。
2. 药品存储位置管理进行药品分类存储,保证不同种类的药品不混杂存放,避免交叉感染或者混淆。
3. 药品有效期监管对即将过期的药品进行专门管理,确保其在有效期内使用,避免过期药品对患者造成伤害。
三、药品销售1. 药品销售记录核查每一笔药品销售都要有相应的销售记录,包括销售时间、销售数量、销售金额等,确保记录真实性。
2. 药品销售许可核实对消费者购买药品需核查其处方是否合法,确保消费者购买的药品真实合法,避免买假药。
3. 药品使用说明提醒在销售药品时要向消费者提供药品使用说明,告知使用方法、副作用等信息,确保消费者正确使用药品。
四、定期自查1. 设立自查自纠小组为了做到全员参与,可设立自查自纠小组,定期召开自查自纠会议,对药店的经营情况进行检查。
2. 制定自查自纠计划制定自查自纠计划,明确各项工作任务,按照计划执行,确保每个环节都得到严格把控。
3. 定期自查自纠每隔一段时间对药店的各项工作进行检查,及时发现问题,整改措施要求及时,确保药店合法合规经营。
五、整改问题1. 发现问题后要及时核实问题原因,制定整改计划,并督促相关责任人落实整改措施。
2. 强化培训,提高员工业务水平,规范员工行为,确保每一位药店从业人员都遵守相关法规和规章制度。
以上是药店自查自纠的相关情况,通过自查自纠,药店可以发现问题并及时整改,确保经营合法合规,保障患者用药安全。
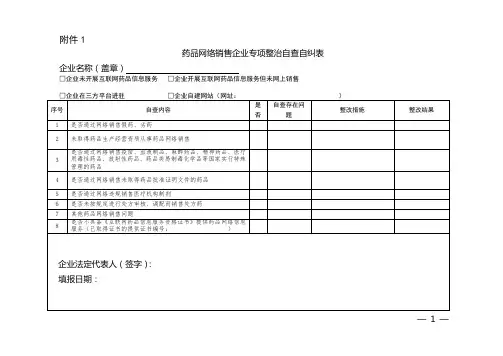

药品经营企业自查登记表填表单位(盖章):填表人:填表日期:企业基本信息企业名称法人代表企业地址联系人电话传真自查自纠内容1、有无完善的销售开票相关流程、制度有□无□2、有无完善的药品采购、入库相关流程、制度有□无□3、有无完善的票据管理相关制度有□无□4、有无完善的发票管理相关流程、制度有□无□5、有无完善的资金管理相关制度有□无□6、经营品种是否有供货方开具的合法销售凭证(包括加盖印章的销售发票、销售清单、出库单据等)有□无□7、药品购进有无验收入库记录及验收员签字有□无□8、药品销售是否向客户开具合法销售凭证(包括加盖印章的销售发票、销售清单等)有□无□9、是否与购进单位、销售单位签订购销合同有□无□10、向供货单位支付货款是否全部打入与购销合同或销售发票注明的供货单位统一的帐户有□无□11、有无客户货款打入个人帐号,而非公司统一帐户的现象有□无□12、业务员或客户以现金方式结算的,有无货款收讫凭证有□无□13、销售人员有无企业法人授权书有□无□14、销售人员有无完整的入职、离职、劳动合同、工资表、培训考核、健康体检、社会保险等证明材料有□无□15、有无医药代表挂靠经营的情况有□无□填表说明1、企业必须按照要求填表,并对所填内容的真实性负责,未经法定代表人或主要负责人签字、未加盖公章的自查表视为无效(主要负责人是指企业中具有主要决策权力的领导);2、填报相关栏目时,根据实际情况在“有”、“是”或“无”、“否”框内打√;3、自查时间范围为2011年1月至2012年3月;4、请在2012年3月26日前填好本表,报我局食品药品安全稽查大队,联系电话:83665185;5、如还有其它问题可附材料说明。
企业承诺本企业保证对上述申报材料和填写内容的真实性负责,并对因隐瞒情况而产生的一切后果负责。
法定代表人或主要负责人(签名)年月日。

2023年医药行业不正之风自查自纠表2023年医药行业不正之风自查自纠表随着社会的不断发展和医疗科技的不断进步,医药行业扮演着越来越重要的角色。
然而,随之而来的是医药行业不正之风的存在,这种不正之风可能包括药品质量不良、虚假宣传、滥用药物等一系列问题。
为了确保医药行业的健康发展,各相关方都应该积极进行自查自纠,促进医药行业的规范化和可持续发展。
【1】2023年医药行业不正之风自查自纠表1. 药品质量管理药品质量是医药行业的生命线,关乎人民的健康。
自查自纠时,企业应该对生产环节进行全面检查,确保生产的药物符合国家标准,并建立健全的质量管理体系。
监管部门也应加大执法力度,严厉打击假冒伪劣药品和不合格药品的生产和销售行为。
2. 营销宣传行为医药广告的宣传内容必须真实、准确,不得夸大疗效,更不能虚假宣传。
企业自查自纠时,应加强广告宣传的管理,建立真实、规范的宣传标准,杜绝虚假宣传和误导消费者的行为。
3. 药物滥用和滥用各级医疗机构和药企应该加强对药物滥用和滥用的管理,制定严格的处方管理制度,杜绝滥用和滥用现象。
也需要加强对药物滥用和滥用行为的监测和打击力度,保障患者用药安全。
4. 建立诚信机制诚信是医药行业的基石,企业应积极建立诚信机制,加强与客户、合作伙伴和社会的沟通与交流,做到真诚守信。
监管部门也应鼓励并支持企业加强诚信建设,同时严惩失信行为,维护行业的诚信形象。
【2】总结回顾在2023年,医药行业所面临的不正之风问题仍然比较突出。
为了实现医药行业的健康发展,我们需要全社会的共同努力。
医药企业应该加强自我管理,自查自纠,整顿内部管理,确保产品质量和企业信誉。
监管部门应该加大监管力度,深入执法,严厉打击违法违规行为,维护医药市场秩序。
广大患者和消费者也应提高识别能力,理性用药,维护自身权益。
只有这样,医药行业才能迈向更加规范、健康的发展道路。
【3】个人观点和理解个人认为,医药行业不正之风问题的存在既是问题,也是机遇。

附件2:
药品生产企业自查自纠表
自查自纠日期:质量受权人签字:
药品批发企业自查自纠表
企业名称:(盖章)
2.序号1、2、3、4项自查结果为“是”或其它项目自查结果为“否”时,
均应另附情况说明。
自查自纠日期:企业质量负责人:
药品零售连锁企业自查自纠表
企业名称:(盖章)
2.序号1、2、3、4项自查结果为“是”或其它项目自查结果为“否”时,
均应另附情况说明。
自查自纠日期:企业质量负责人:
药品零售企业自查自纠表
企业名称:(盖章)
2.序号1、2、3、4项自查结果为“是”或其它项目自查结果为“否”时,
均应另附情况说明。
自查自纠日期:企业质量负责人:。
GSP内审自查表序号项目细则规定内容检查要点检查结果、风险评估、风险控制、整改要求审核员一、总则1**00401 药品经营企业应依法经营。
1.《药品经营许可证》、《药品经营管理规范认证证书》、《营业执照》《税务登记证》《组织机构代码证》齐全有效。
2.经营场所与库房地址应与《药品经营许可证》标注相符;3.不得有超方式经营;4.不得有超范围经营行为;5.不得有出租出借经营许可证的行为。
1证照是否齐全有效是□否□2经营场所与库房地址与《药品经营许可证》标注是否相符是□否□3是否超范围、超方式经营及走票、挂靠等违法行为是□否□检查结果:风险评估:风险控制;整改要求2 **00402 药品经营企业应当坚持诚实守信,禁止任何虚假、欺骗行为。
应诚实守信,所提供的资质证明、票据凭证、数据记录等不得有虚假、欺骗的行为。
1所提供的资质证明,是否真实,是□否□2在经营活动中是否有虚假欺骗消费者的行为是□否□检查结果:风险评估:风险控制;整改要求二、质量管理体系3 *00501 企业应依据有关法律法规及本规范的要求建立质量管理体系。
应依据有关法律法规的要求,设置组织机构、人员、设施设备、质量管理体系文件及相应的计算机系统等。
1质量管理体系是否覆盖规范所要求的各个环节、各个部门及岗位是□否□2是否对质量管理活动的过程的识别存在明显的缺失或不合理是□否□检查结果:风险评估:风险控制;整改要求序号项目细则规定内容检查要点检查结果、风险评估、风险控制、整改要求审核员4 00502 企业应当确定质量方针,应当制定质量管理体系文件。
1.应建立质量方针文件,有企业负责人签发,并按文件管理要求予以控制;2.应制定质量管理体系文件,由企业负责人或质量负责人签发,并按文件管理要求对其予以控制。
1质量方针是否形成文件,质量方针是否包含保证药品质量的承诺是□否□2质量方针是否是最高管理者制定是□否□3企业员工是否了解企业质量方针是□否□检查结果:风险评估:风险控制;整改要求5 00503 开展质量策划、质量控制、质量保证、质量改进和质量风险管理等活动。
药品批发企业自查自纠表药品批发企业是药物的供应链中的关键环节,其负责将生产厂家生产出的药品销售给药店和医院等终端客户。
然而,由于药品本身的特殊性,药品批发企业面临着很多潜在的风险和挑战,如药品保管和储存问题、合规和法律风险等,因此,药品批发企业需要对自身的经营情况进行自查和自纠。
自查自纠表针对药品批发企业对自身的经营情况进行自查和自纠,可以采用自查自纠表的形式。
下面是一份简单的药品批发企业自查自纠表:第一部分:企业基本情况1.企业名称2.企业注册地址3.经营负责人姓名4.经营负责人联系方式(包括电话和电子邮件)5.药品经营许可证编号6.药品经营许可证有效期第二部分:药品储存和保管1.药品储存环境是否符合相关规定?2.药品储存是否分类保存,区分货品等级?3.药品储存区域是否整洁,有无异味、霉变等?第三部分:药品销售和配送1.收货、发货、销售单据是否合法、准确?2.药品是否按规定包装,加贴标识,如批号、有效期、储存条件等?3.配送车辆是否符合要求?车辆内是否装有温度记录器?4.药品配送是否按照规定的区域、时间、顺序、方法等进行?第四部分:药品采购和供应商管理1.药品采购是否遵循法律法规,有无购进假药或劣药的记录?2.药品采购前是否对供应商进行了充分调查和审核?3.是否与供应商签署了合同,合同中是否清晰表述了双方权利和义务?4.与供应商的质量管理是否有效,是否及时处理质量问题?第五部分:合规管理1.是否制定了公司规章制度?2.是否按照要求对员工进行了规定的培训?3.是否定期开展内部审计、评估和检查?4.是否按照相关规定备案进口或从境外进口的药品?药品批发企业经营涉及到药品的安全和质量,具有高度的社会关注度和责任性。
因此,药品批发企业需要时刻关注自身的经营情况,建立健全的自查自纠机制,保证药品的安全和质量。
上述的自查自纠表仅供参考,具体内容和形式还应根据具体情况进行适当的调整和完善。
附件1.1 药品批发企业或零售连锁总部安全隐患自查自纠参照表企业名称(盖章): 时间:年月日主要负责人签字:
附件1。
2 药品零售药店(含连锁门店)安全隐患自查自纠参照表企业名称(盖章):时间:年月日店长签字:
附件2
企业安全隐患自查自纠汇总表
填报单位(盖章):企业主要负责人姓名(签字): 填报时间:
说明:1。
企业可根据自身实际,在全面自查的基础上,完善汇总填报此表,并在安全大排查大整治期间每旬上报所在地行业主管部门.
2。
对一时不能整改的重大安全隐患,还应在“整改(防范)措施"栏中填报防范措施。
购进药品自查自纠报告一、前言作为一家从事药品销售的企业,我们深知自身的责任和义务,必须保证所售药品的质量和安全性,确保消费者的健康和权益。
然而,在实际操作中,我们也难以完全杜绝一些不规范的行为和问题的出现。
因此,及时对自身进行自查自纠,发现并解决问题,是我们必须要做的。
为了提高自身的管理水平和服务质量,特制定本次自查自纠报告,对过去一段时间内的行为和操作进行审核和总结,以便不断完善和改进我们的工作。
同时,也对未来的工作提出了一些建议和改进措施,希望能够得到领导和同事的支持和配合。
二、自查自纠情况1.采购环节在采购药品的过程中,我们注意到一些问题存在。
首先,我们的采购人员在选取供应商时,有时易于被价格所吸引,而忽视了药品的质量和来源。
因此,我们调整了采购策略,加强了对供应商的审核和筛选,确保所售药品的质量。
另外,我们也发现在采购过程中出现了一些杂乱的情况,比如订单不规范,信息不完整等。
因此,我们重新规范了采购流程和相关文件,做到了有序有据,方便管理和监督。
2.验收环节在验收药品的环节中,我们注意到一些问题。
首先是验收人员对药品的品质和包装的检查不够严格,导致一些次品或问题药品流入市场。
为此,我们加强了对药品的检查和验收工作,确保合格品才能进入市场销售。
另外,在验收过程中,我们也发现了一些药品信息登记不规范的情况,可能导致信息不全或者错误。
为了解决这一问题,我们对验收流程进行了调整和再培训,确保所有信息都能完整准确地登记。
3.保存和销售环节在保存和销售药品的过程中,我们也注意到了一些问题。
首先是药品的储存和温湿度控制不够到位,可能导致药品的质量受损。
因此,我们对仓库的环境和设备进行了调查和改进,确保药品的保存条件符合标准。
另外,我们也发现一些销售人员在销售过程中存在一些问题,比如未经认真培训和了解的情况下推销药品,可能存在误导和不当行为。
因此,我们对销售人员进行了再培训和考核,确保其具备必要的专业知识和操作技能。