高中化学 2.2 电解质教学设计1 鲁科版必修1
- 格式:doc
- 大小:38.50 KB
- 文档页数:4


鲁科版高中高一化学必修1《电解质》教案及教学反思一、教学背景本次课程是高中高一化学必修课程中的一堂课,主要内容是电解质。
学生已经在前几个课时学习过水的离子化性质,本次课程将进一步深入探讨电解质的相关知识点。
根据课程标准要求,学生需要掌握电解质和非电解质的区别、电离程度、电解质的分类等内容。
二、教学目标本次教学的目标是:1.确定电解质的定义和分类;2.了解电离程度及有关知识;3.掌握电解质的性质和实验方法;4.鼓励学生积极参与实验,在实验中发现问题和解决问题的能力。
三、教学内容与方法1. 教学内容本次教学的内容是电解质,具体分为以下几个方面:1.电解质的定义和分类;2.电离程度及有关知识;3.电解质的性质和实验方法。
2. 教学方法为了达到上述教学目标,我们采用以下多种教学方法:1.讲授法;2.实验探究法;3.互动讨论法;4.全体讨论法;5.团队合作法。
讲授法是本次课程的主要教学方法之一。
通过具体的例子和生动的比喻,让学生感受到电解质和非电解质的区别,并逐步理解电离程度的概念。
实验探究法也是本次课程的重要教学方法之一。
在实验中,学生能够直接观察电解质的性质和现象,更加深入地理解电离程度的概念。
在实验过程中,我们也将鼓励学生发现问题和解决问题的能力。
互动讨论法和全体讨论法都有利于调动学生的积极性和主动性,培养其实际操作能力。
在课堂上,老师可以采取互动讨论的方式,让学生参与到讨论中,自主探究知识。
团队合作法可以更好地培养学生的协作精神和团队意识,将本堂课中的实验内容分配给小组,让学生共同完成实验并分享实验结果。
四、教学过程1. 导入环节本课堂的导入环节,老师可以向学生提出一个问题:良好的电解质是什么样的?通过有趣的故事和生动的比喻,让学生更加深入地理解电解质的概念,迅速进入学习状态。
2. 理论知识部分在理论知识部分,主要讨论电解质和非电解质的区别,电离程度、电解质的分类等内容。
通过向学生简单明了地介绍电离程度和电解质的知识,让学生能够理解电解质的定义和分类。

第3节电能转化为化学能——电解第1课时电解的原理学习目标1.通过对电解池构成的探究,掌握电解池的工作原理。
2.通过对比四种电解类型,掌握不同类型电解的区别与联系。
学习任务1 探究电解池的工作原理1.电解的概念:将直流电通过熔融电解质或电解质溶液,在两个电极上分别发生氧化反应和还原反应的过程。
2.电解池及构成条件(1)电解池:将电能转化为化学能的装置。
(2)电解池构成条件。
①直流电源(电能提供装置)。
②固体电极材料(一般为金属、石墨或某些特殊导电性材料)。
③电解质(熔融或溶液状态)。
④构成闭合回路。
3.电解池电极的判断某同学用硫酸铜溶液作电解液,用铜管作电极连在电池的正极上,放入硫酸铜溶液中。
然后用鳄鱼夹夹住一枚硬币并连接在电池的负极上,然后把硬币放入硫酸铜溶液中。
过一段时间取出来,发现硬币变为铜币。
该同学认为这是一个电解装置。
这是否科学呢?我们一起探究。
探究电解池的工作原理问题1:直流电源在该装置(电解池)中的作用是什么?提示:直流电源为电解装置提供能量,并强制电子转移以达到发生氧化还原反应的目的。
问题2:该装置中硬币电极上发生什么反应?硬币是阳极还是阴极? 提示:由于电源电子流向该极,所以电极表面的氧化剂(Cu2+)就会在此电极上得电子发生还原反应,发生的电极反应为Cu2++2e-Cu,所以硬币表面析出Cu变为铜币;硬币是阴极。
问题3:该装置中铜管电极上发生什么反应?铜管是阳极还是阴极? 提示:由于电源强制移走了该电极的电子,所以该电极(Cu)发生氧化反应,发生的电极反应为Cu-2e-Cu2+;铜管是阳极。
电解的原理1.(2021·江苏扬州期中)如图所示的电解装置可实现低电位下高效催化还原CO2。
下列说法不正确的是( C )A.a极连接外接电源的负极B.b极的电极反应为Cl--2e-+2OH-ClO-+H2OC.电解过程中Na+从左池移向右池D.外电路上每转移1 mol电子,理论上可催化还原标准状况下CO2气体11.2 L解析:从图示中可以看出,b极上Cl-失去电子生成ClO-,b极为电解池阳极,a极上CO2得到电子生成CO,a极为电解池阴极;与b极相连的电源电极为正极,与a极相连的电源电极为负极。
第2节电解质
第1课时电解质及其电离
一、教材分析
本节课从一个新的角度来对化合物进行分类:电解质和非电解质对于学生来讲都是陌生的话题。
最好通过实验让学生去追寻电解质溶液导电的原因,帮助学生掌握用电离方程式来表示强电解质的电离过程。
教科书只是在知识点击里介绍弱电解质的电离方程式,离子反应要侧重于对概念和发生条件的认识及简单离子方程式的书写,教学时要根据学生的实际情况控制好难度,侧重于化学知识的综合运用能力的培养。
二、设计思路
通过对化合物进行新的分类,引入电解质非电解质的定义,并强调概念。
通过设计溶液导电性实验(氯化钠晶体、熔融氯化钠、氯化钠溶液的导电性实验),对比同是氯化钠但是不同状态的物质是否导电总结出导电的原因是有自由移动的离子。
最后,通过介绍氯化钠在水中的溶解和电离,引出电离的概念及氯化钠的电离方程式的书写。

第2节电解质第2课时电解质在水溶液中的反应【三维目标】(一)知识与技能1、使学生理解离子反应和离子方程式的含义。
2、掌握离子反应发生的条件和离子方程式的书写方法,并能准确书写常见的酸、碱、盐间相互反应的离子方程式。
(二)过程与方法1、通过稀硫酸与Ba(OH)2溶液反应实质的探究,使学生学会运用以实验为基础的实验探究方法。
2、通过质疑、归纳等活动,提高学生分析、联想、类比、迁移以及概括的能力。
(三)情感态度与价值观1、能以“观察·思考”激发学生的学习兴趣;2、能以“迁移·应用”让学生体验学习的成功感;3、能通过“交流·研讨”活动,培养学生合作学习的意识。
【重点、难点】(一)知识与技能电解质在水溶液中反应的实质、离子反应、简单离子方程式的书写。
(二)过程与方法:形成解决问题的方法及思维路径。
二、电解质在水溶液中的反应【引入】根据所学知识填写下表物质类别氯化钠溶液硫酸铜溶液氯化钡溶液电离方程式溶质粒子两两混合后的化学方程式【交流研讨】判断以上各溶液能否导电?两两混合后能发生反应的原因?现象又如何呢?【过渡】请动手实验验证你的结论【实验探究1】编号ⅠⅡⅢ实验为了确认电解质溶液中部分离子相互间能否发生反应,如上图做了如下三组实验。
(1)实验Ⅰ的目的是______________________________________________。
(2)实验Ⅱ证明了________离子之间发生了化学反应,根据什么现象证明溶液中的另两种离子没有发生化学反应______________________________________________________________。
(3)由此可见,Ba2+不与________大量共存,Cl-不与________大量共存。
【学生讨论归纳】(1)验证Cl-与Cu2+、SO2-4与Na+不反应(2)Ba2+与SO2-4溶液为蓝色说明Cu2+未参加反应(3)SO2-4Ag+实验探究2.现象1 现象2 现象3电流计指针读数由_大_ 到_小_ 溶液红色__退去__有__白色沉淀_____产生现象的原因离子浓度变小氢氧根离子浓度变小Ba SO4不溶于水实际反应的离子H+OH-SO42-Ba 2+【交流研讨】⑴、大家到观察溶液中的现象和电流表指针有何变化?⑵、观察到的白色沉淀物质是什么?电流表指针为何变化?⑶、实验现象对于你认识稀硫酸与氢氧化钡在水溶液中的反应有什么启示?【学生讨论并归纳】(教师引导学生沿着如下路径分析归纳)硫酸与Ba(OH)2分别属于酸、碱类电解质→从电离的角度分析,硫酸与Ba(OH)2溶液中的所含微粒分别是H+、SO42-、Ba2+、OH-→电流计指针读数变小,溶液导电能力减弱,自由离子浓度减小,离子有消耗,参加了化学反应→溶液由红变紫,即溶液酸性减弱,证明H+和OH-结合生成了水→不难推断,白色难溶物是Ba2+与SO42-结合生成的BaSO4沉淀→稀硫酸与Ba(OH)2溶液反应的实质是溶液中的H+、SO42-、Ba2+、OH-相互结合生成了水(难电离物)和BaSO4沉淀(难溶物)→电解质溶液间的反应实质是离子间的反应。

第2课时离子反应发展目标体系构建1.通过实验探究理解离子反应的本质是微粒间的相互作用,体会含有相同微粒的物质发生相同的离子反应。
2.能够依据电解质在水溶液中的电离结果和微粒间的相互作用推测离子反应的发生,写出离子方程式。
3.能够运用离子反应完成物质中常见离子的检验、杂质离子的除去等任务。
一、离子反应的含义1.探究电解质在水溶液中反应的实质实验操作实验现象随着H2SO4溶液的滴入,(1)电导率:读数先减小后增大(2)溶液:出现白色沉淀,溶液颜色由红色变浅至无色解释稀硫酸与Ba(OH)2溶液反应的实质是溶液中的H+与OH-结合生成难电离的水、Ba2+与SO2-4结合生成硫酸钡沉淀,导致溶液中离子浓度的降低(1)概念:在溶液中有离子参加的化学反应。
(2)实质:溶液中某种或某些离子的浓度发生改变。
(3)复分解型离子反应发生的条件微点拨:熟记可拆的强酸、强碱和易溶盐的口诀钾钠铵盐硝酸盐,都能溶于水中间;氯化物除银亚汞,硫酸不溶铅与钡;碳酸磷酸亚硫酸,可溶只有钾钠铵;易溶钾钠铵钡碱,不溶的酸是硅酸。
二、离子方程式1.表示:离子反应可以用离子方程式表示。
例如,NaOH溶液与稀盐酸反应的离子方程式为H++OH-===H2O。
2.书写步骤(以氯化钡溶液和硫酸钠溶液反应为例)3.意义(1)表示一个具体的化学反应。
(2)表示所有同一类型的化学反应。
三、离子反应的应用1.离子检验离子使用的反应现象反应离子方程式试剂Cl-AgNO3溶液、稀硝酸加入AgNO3溶液,产生白色沉淀,再加稀硝酸沉淀不溶解Cl-+Ag+===AgCl↓SO2-4BaCl2溶液、稀盐酸加足量稀盐酸无沉淀,再加BaCl2溶液产生白色沉淀Ba2++SO2-4===BaSO4↓2.食盐的精制粗食盐中含有Ca2+、Mg2+、SO2-4等杂质离子,除去它们发生反应的离子方程式分别是:(1)Ca2++CO2-3===CaCO3↓。
(2)Mg2++2OH-===Mg(OH)2↓。
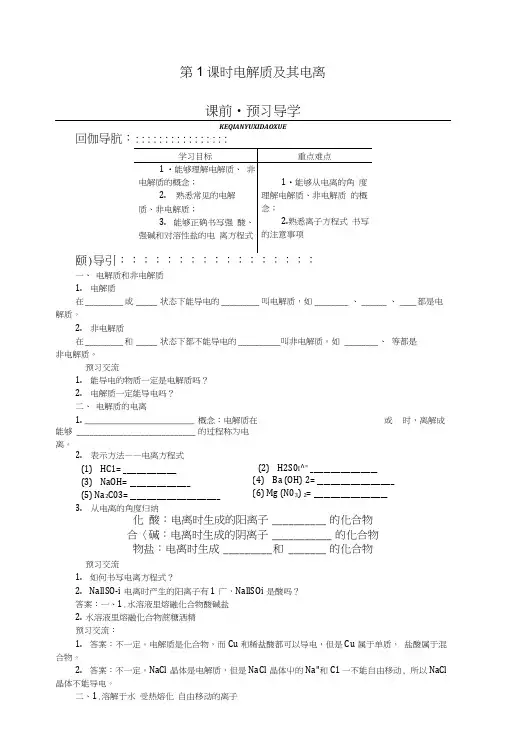
第1课时电解质及其电离课前•预习导学KEQIANYUXIDAOXUE回伽导肮:::::::::::::::::颐)导引:::::::::::::::::一、 电解质和非电解质1. 电解质在 _________ 或 _____ 状态下能导电的 _________ 叫电解质,如 ________ 、 ______ 、 ____ 都是电 解质。
2. 非电解质在 _________ 和 _____ 状态下都不能导电的 __________ 叫非电解质。
如 ________ 、 等都是 非电解质。
预习交流1. 能导电的物质一定是电解质吗?2. 电解质一定能导电吗?二、 电解质的电离1. ______________________ 概念:电解质在或 时,离解成能够 ____________________________ 的过程称为电 离。
化 酸:电离时生成的阳离子 __________ 的化合物 合〈碱:电离时生成的阴离子 ___________ 的化合物 物盐:电离时生成 _________ 和 _______ 的化合物预习交流1. 如何书写电离方程式?2. NallSO-i 电离时产生的阳离子有1广,NallSOi 是酸吗? 答案:一、1.水溶液里熔融化合物酸碱盐 2. 水溶液里熔融化合物蔗糖洒精预习交流:1. 答案:不一定。
电解质是化合物,而Cu 和稀盐酸都可以导电,但是Cu 属于单质, 盐酸属于混合物。
2. 答案:不一定。
NaCl 晶体是电解质,但是NaCl 晶体屮的Na"和C1 一不能自由移动, 所以NaCl晶体不能导电。
二、1.溶解于水 受热熔化 自由移动的离子2. 表示方法——电离方程式(1) HC1= ________________ (3) NaOH= __________________(5) Na 2C03= ___________________________ 3. 从电离的角度归纳(2) H2S0I ^= ____________________ (4) Ba (OH) 2= _______________________ (6) Mg (N03) 2= ______________________2.(1) H++C1"(2)2H++Sor(3)Na++OH~(4)Ba2++20H~(5)2Na++C0s_(6)Mg2++2N0;3.全部是盘离子全部是氢氧根离子金属离子酸根离子预习交流:1.答案:书写电离方程式一般分两步:(1)根据化合物中元素原子和原子团的化合价写出阴、阳离子(原子团除HSO「外一般不拆分);(2)根据电荷守恒配平电离方程式。


