中学常见的混合物和纯净物
- 格式:docx
- 大小:9.29 KB
- 文档页数:2

混合物与纯净物的区别混合物和纯净物是化学中常见的概念,它们分别指代了不同的物质性质和组成。
在本文中,我们将探讨混合物与纯净物之间的区别以及它们在日常生活中的应用。
一、混合物的定义和特点混合物是由两种或更多种不同物质组成的混合物质。
这些物质在混合物中保持各自的性质和化学组成。
混合物可以分为均匀混合物和非均质混合物两种。
1. 均匀混合物:均匀混合物也被称为溶液。
其中溶质(物质在溶液中被溶解的部分)均匀地分散在溶剂(物质用于溶解其他物质的部分)中,并且看起来只有一个相。
例如,盐水是均匀混合物的一个例子。
盐溶解在水中,形成了一个透明的液体。
2. 非均匀混合物:非均匀混合物包含两个或更多个相。
各种组成部分的比例可以不均匀地分布。
例如,沙与水混合的物质,看起来像是两个不同的层,即上方是沙,下方是水。
二、纯净物的定义和特点纯净物是由同一种物质组成的纯净物质。
纯净物具有特定的化学组成和明确的物理性质。
1. 元素:元素是由具有相同原子数量和类型的原子组成的纯净物。
例如,氧气(O2)是由两个氧原子组成的纯净物。
2. 化合物:化合物是由两个或更多个不同元素的原子以一定比例结合而成的纯净物。
化合物具有固定的化学组成,可以通过化学反应分解为原子。
例如,水(H2O)是由两个氢原子和一个氧原子组成的化合物。
三、混合物与纯净物的比较混合物和纯净物在下面几个方面有所不同:1. 组成:混合物由两种或更多种不同组分组成,每个组分在混合物中保持其自身的性质。
而纯净物是由同一种物质组成,并且具有唯一的化学组成。
2. 分离:混合物可以通过物理手段进行分离,如过滤、蒸发等。
而纯净物的分离通常需要化学反应或其他复杂的方法。
3. 性质:混合物的性质取决于组分之间的相互作用和比例。
每个组分的性质保持不变。
纯净物具有特定的物理和化学性质,这些性质可以用于其鉴定和分类。
四、混合物与纯净物的应用混合物和纯净物在日常生活中有广泛的应用。
1. 混合物的应用:- 食品和饮料中的混合物提供了多种口味和营养。


纯净物和混合物的例子混合物:不同物质组成的纯净物。
下面我们来详细看看吧。
1.纯净物有固定组成,混合物没有固定组成。
组成纯净物的物质只能是一种物质。
组成混合物的物质可以是两种也可以是多种,物质种数不固定。
混合物中每种物质的质量分数可多可少也无固定值。
但有些问题必须清楚,纯净物中元素的百分含量一定是定值。
而所含元素百分含量是定值的物质不一定是纯净物。
如含碳100%的物质可以是金刚石,也可以是石墨的纯净物。
或是金刚石和石墨两种物质混合成的混合物。
纯净物一定有固定不变的化学式。
如纯水的化学式为H2O。
但有确定化学式的物质不一定是纯净物。
如化学式为C2H6O的物质可以是纯净物乙醇或甲醚(一种有机物)。
也可以是乙醇和甲醚混合而成的混合物。
这就说是,判断一种物质是纯净物还是混合物,仅凭物质组成还远远不够。
2.纯净物有固定结构,混合物没有固定结构。
结构一般指构成物质的微粒间的结合方式、排列顺序和空间的构型等。
相同物质,结构相同。
不同种物质,结构不同。
纯净物只有一种物质组成,因此纯净物有固定结构。
混合物由于组成物质的成分不固定,结构也就不固定。
判断一种物质是纯净物还是混合物,结构是首要条件。
3.纯净物有固定性质,混合物没有固定的性质。
物质的性质取决于物质的组成和结构,特别是结构。
由于混合物本身就没有固定的组成和结构,因而它的性质将了随着组成和结构的变化而变化。
所以混合物一般来说没有固定的性质。
相反,由一种物质组成的纯净物因组成的结构固定,因而性质就固定。
如纯净物有固定的熔点、沸点等。
纯净物如果掺入杂质变成混合物,则它的熔点、沸点就随杂质的多少而发生变化。
有一点我们必须注意到性质固定与否不是判断纯净物和混合的唯一标准。
因为有恒沸点的混合物也有固定的沸点,如98%的浓硫酸沸点是338 ℃。
还有一点值得注意的是,绝对纯净的物质是不存在的。
通常所说的纯净物也都含少量杂质,其杂质含量限度要以对生产和科研不产生有害影响为标准,纯净与否是相对的。

化学物质分类混合物和纯净物LG GROUP system office room 【LGA16H-LGYY-LGUA8Q8-LGA162】●混合物和纯净物1、概念单质:由同种元素组成的纯净物例:氢气、氧气、红磷等化合物:由不同种元素组成的纯净物例:水、高锰酸钾等氧化物:由两种元素组成,且含有氧元素的纯净物例:二氧化硫、氧化铁等注意:单质、化合物前提必须是纯净物,即划分单质、化合物的标准是根据纯净物的元素种类来划分的。
若只含一种元素的纯净物就属于单质;若含有几种元素的纯净物就属于化合物2、物质分类的步骤①根据物质种类分为纯净物与混合物②写出纯净物的化学符号③根据元素种类将纯净物分为单质与化合物④在化合物中根据氧化物的概念找出氧化物冰与水混合是纯净物。
名称中有“某化某”“某酸某”的都是纯净物,是化合物。
12、氧化物:由两种元素组成的化合物中,其中有一种元素是氧元素纯净物:由一种物质组成混合物:由两种或两种以上纯净物组成,各物质都保持原来的性质3.混合物:是由两种或两种以上的物质混合而成(或由不同种物质组成)例如,空气,溶液(盐酸、澄清的石灰水、碘酒、矿泉水),矿物(煤、石油、天然气、铁矿石、石灰石),合金(生铁、钢)注意:氧气和臭氧混合而成的物质是混合物,红磷和白磷混合也是混合物。
纯净物、混合物与组成元素的种类无关。
即一种元素组成的物质可能是纯净物也可能是混合物,多种元素组成的物质可能是纯净或混合物。
4.纯净物:由一种物质组成的。
例如:水、水银、蓝矾(CuSO4·5H2O)都是纯净物十三、物质的化学式A单质:由同种(或一种)元素组成的纯净物。
1、金属单质(按金属活动性顺序由强至弱排列)钡钾钙钠镁铝锌铁锡铅(氢)铜汞银铂金BaKCaNaMgAlZnFeSnPbCuHgAgPtAu2、非金属单质氢气H2氧气O2氮气N2氯气Cl2氟气(F2)溴(Br2)碘(I2)碳C硅Si磷P硫S臭氧(O3)3、稀有气体氦气He氖气Ne氩气ArB化合物:由不同种元素组成的纯净物。
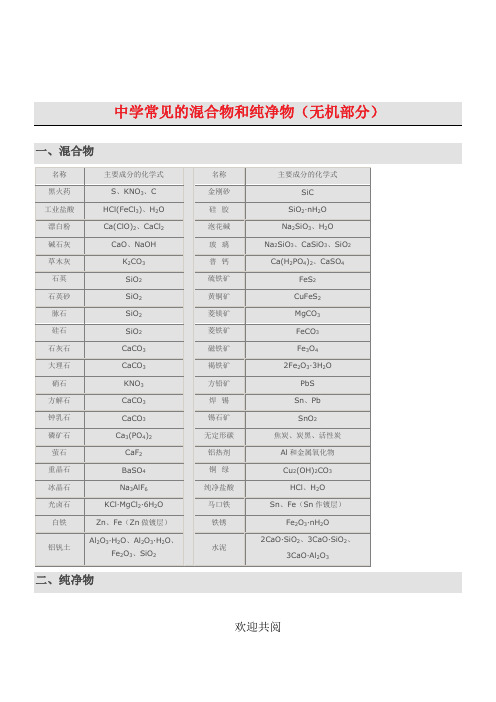

在化学中,物质可以分成纯净物和混合物。
本专题将从此处开始讨论:一、混合物混合物是由两种或两种以上物质混合而成的物质。
下面列举常见的混合物:分散系:溶液、胶体、浊液等高分子化合物:蛋白质、纤维素、淀粉、塑料等其他物质:石油及其各种馏分、天然气、油脂、福尔马林、氨水、王水、碱石灰等二、纯净物纯净物与混合物相对,是由一种物质组成,有固定的物理性质和化学性质的物质。
纯净物有专门的化学符号,能用一个化学式表示。
继续细化纯净物的组成可将其分为:1.单质单质是由同一种元素组成的纯净物。
金属单质:例如:K、Ca、Na、Mg、Al 等非金属单质:例如:S、Cl2、He 等注意:只含一种元素的物质不一定是纯净物。
如氧气O2 和臭氧O3 混合得到的物质是混合物同种元素的同位素单质混合得到的物质是纯净物。
如氢的同位素氕氘氚组成的双原子分子H2、D2、T2 混合在一起得到的是纯净物含水的物质不一定是混合物。
如胆矾CuSO4 • 5H2O、绿矾FeSO4 • 7H2O、明矾KAl(SO4)2 • 12H2O 都是纯净物2.化合物化合物是由两种或两种以上的元素组成的纯净物。
A. 按化合物的性质分类①氧化物氧元素与另外一种化学元素组成的二元化合物叫做氧化物。
氧化物可分为:I. 酸性氧化物酸性氧化物指与水反应生成相应价态的酸,或与碱反应只生成一种相应价态的盐和水的氧化物。
例如:SO2、SO3、P2O5、SiO2、Mn2O7 等注意:酸性氧化物不一定是非金属氧化物。
如高锰酸酐Mn2O7 既是酸性氧化物,又是金属氧化物非金属氧化物不一定是酸性氧化物。
如一氧化碳CO、一氧化氮NO、二氧化氮NO2 都是不成盐氧化物酸性氧化物不一定能与水反应生成相应的酸。
如二氧化硅SiO2 不与水反应能与碱反应生成盐和水的氧化物不一定是酸性氧化物。
如二氧化氮NO2 是不成盐氧化物,氧化铝Al2O3 是两性氧化物酸性氧化物一定是酸酐,但酸酐不一定是酸性氧化物。
●混合物和纯净物1、概念单质:由同种元素组成的纯净物例:氢气、氧气、红磷等化合物:由不同种元素组成的纯净物例:水、高锰酸钾等氧化物:由两种元素组成,且含有氧元素的纯净物例:二氧化硫、氧化铁等注意:单质、化合物前提必须是纯净物,即划分单质、化合物的标准是根据纯净物的元素种类来划分的;若只含一种元素的纯净物就属于单质;若含有几种元素的纯净物就属于化合物2、物质分类的步骤①根据物质种类分为纯净物与混合物②写出纯净物的化学符号③根据元素种类将纯净物分为单质与化合物④在化合物中根据氧化物的概念找出氧化物冰与水混合是纯净物;名称中有“某化某”“某酸某”的都是纯净物,是化合物;12、氧化物:由两种元素组成的化合物中,其中有一种元素是氧元素纯净物:由一种物质组成混合物:由两种或两种以上纯净物组成,各物质都保持原来的性质3.混合物:是由两种或两种以上的物质混合而成或由不同种物质组成例如,空气,溶液盐酸、澄清的石灰水、碘酒、矿泉水,矿物煤、石油、天然气、铁矿石、石灰石,合金生铁、钢注意:氧气和臭氧混合而成的物质是混合物,红磷和白磷混合也是混合物;纯净物、混合物与组成元素的种类无关;即一种元素组成的物质可能是纯净物也可能是混合物,多种元素组成的物质可能是纯净或混合物;4.纯净物:由一种物质组成的;例如:水、水银、蓝矾CuSO4·5H2O都是纯净物十三、物质的化学式A单质:由同种或一种元素组成的纯净物;1、金属单质按金属活动性顺序由强至弱排列钡钾钙钠镁铝锌铁锡铅氢铜汞银铂金BaKCaNaMgAlZnFeSnPbCuHgAgPtAu2、非金属单质氢气H2氧气O2氮气N2氯气Cl2氟气F2溴Br2碘I2碳C硅Si磷P硫S臭氧O33、稀有气体氦气He氖气Ne氩气ArB化合物:由不同种元素组成的纯净物;一有机物:含碳元素的化合物除CO、CO2和CO32-的化合物甲烷CH4乙醇C2H5OH甲醇CH3OH乙酸CH3COOH乙炔C2H2尿素CONH22二氧化物:由两种元素组成,其中一种是氧元素的化合物;1、非金属氧化物大部分非金属氧化物通常是酸性氧化物,跟水化合成同价的含氧酸水一氧化碳二氧化碳二氧化硅五氧化二磷二氧化硫三氧化硫H2OCOCO2SiO2P2O5SO2SO32、金属氧化物氧化钡氧化钾氧化钙氧化钠氧化镁氧化铝氧化锌BaOK2OCaONa2OMgOAl2O3ZnO氧化铁氧化亚铁四氧化三铁氧化铜氧化亚铜氧化汞氧化银二氧化锰Fe2O3FeOFe3O4CuOCu2OHgOAg2OMnO2三酸:名称中最后一个字是“酸”,通常化学式的第一种元素是“H”硫酸盐酸硝酸磷酸氢硫酸碳酸亚硫酸H2SO4HClHNO3H3PO4H2S H2CO3H2SO3四碱:由金属离子和氢氧根离子构成,碱的名称通常有“氢氧化某”化学式的最后面是“OH”五盐:由金属离子和酸根离子构成碱1、碳酸盐2、硫酸盐3、硝酸盐4.氯化物5.亚硫酸盐氢氧化钾碳酸钾硫酸钾硝酸钾氯化钾亚硫酸钾KOHK2CO3K2SO4KNO3KClK2SO3氢氧化钠碳酸钠硫酸钠硝酸钠氯化钠亚硫酸钠NaOHNa2CO3Na2SO4NaNO3NaClNa2SO3氢氧化银碳酸银硫酸银硝酸银氯化银AgOHAg2CO3Ag2SO4AgNO3AgCl氨水碳酸铵硫酸铵硝酸铵氯化铵NH3·H2ONH42CO3NH42SO4NH4NO3NH4Cl氢氧化钙碳酸钙硫酸钙硝酸钙氯化钙亚硫酸钙CaOH2CaCO3CaSO4CaNO32CaCl2CaSO3氢氧化钡碳酸钡硫酸钡硝酸钡氯化钡BaOH2BaCO3BaSO4BaNO32BaCl2氢氧化镁碳酸镁硫酸镁硝酸镁氯化镁MgOH2MgCO3MgSO4MgNO32MgCl2氢氧化铜碳酸铜硫酸铜硝酸铜氯化铜CuOH2CuCO3CuSO4CuNO32CuCl2氢氧化锌碳酸锌硫酸锌硝酸锌氯化锌ZnOH2ZnCO3ZnSO4ZnNO32ZnCl2硝酸汞氯化亚铜HgNO32 CuCl氢氧化亚铁碳酸亚铁硫酸亚铁硝酸亚铁氯化亚铁FeOH2FeCO3FeSO4FeNO32FeCl2氢氧化铁硫酸铁硝酸铁氯化铁FeNO33FeCl3FeOH3Fe2SO43氢氧化铝硫酸铝硝酸铝氯化铝AlOH3Al2SO43AlNO33AlCl36、酸式盐多元酸里的氢部分被金属取代,H夹在中间碳酸氢钠NaHCO3,碳酸氢钙CaHCO32磷酸二氢钠NaH2PO4磷酸二氢钾KH2PO4硫酸氢钠NaHSO4,硫酸氢钾KHSO47、碱式盐化学式的中间有“OH”:碱式碳酸铜Cu2OH2CO38、其他盐高锰酸钾KMnO4锰酸钾K2MnO4氯酸钾KClO3硫化钠Na2S碘酸钾KIO3亚硝酸钠NaNO2硫化钾K2S5.单质:由同种或一种元素组成的纯净物;例如:铁氧气液氧、氢气、水银;6.化合物:由不同种两种或两种以上元素组成的纯净物;名称中有“某化某”“某酸某”的是化合物;7.有机物有机化合物:含碳元素的化合物除CO、CO2和含碳酸根化合物外无机物:不含碳元素的化合物以及CO、CO2和含碳酸根的化合物8.氧化物:由两种元素组成,其中一种是氧元素的化合物;a.酸性氧化物:跟碱反应生成盐和水的氧化物;CO2,SO2,SO3大部分非金属氧化物都是酸性氧化物,跟水反应生成同价的含氧酸;CO2+H2O=H2CO3SO2+H2O=H2SO3SO3+H2O=H2SO4b.碱性氧化物:跟酸反应生成盐和水的氧化物;CaONa2OMgOFe2O3CuO大部分金属氧化物都是碱性氧化物,BaOK2OCaONa2O溶于水立即跟水反应生成相应的碱,其他碱性氧化物不溶于水,跟水不反应;CaO+H2O=CaOH2BaO+H2O=CaOH2Na2O+H2O=2NaOHK2O+H2O=2KOHc.注意:CO和H2O既不是酸性氧化物也不是碱性氧化物,是不成盐氧化物;9.酸:电离时生成的阳离子全部是氢离子的化合物;酸溶液的PH值小于7酸的名称中最后一个字是“酸”,通常化学式的第一种元素是“H”,酸由氢和酸根离子组成紫色石蕊试液遇酸变红色,无色酚酞试液遇酸不变色根据酸的组成,通常有以下两种分类方法:酸的电离方程式:酸=nH++酸根离子n-a.根据酸分子电离所能生成的氢离子的个数分为:一元酸HCl、HNO3、二元酸H2SO4、H2S、H2CO3和三元酸H3PO4b.根据酸分子里有无氧原子分为:含氧酸H2SO4,HNO3,H3PO4名称为:某酸无氧酸HCl,H2S名称为:氢某酸鉴定酸鉴定H+的方法有:①加紫色石蕊试液变红色的是酸溶液;②加活泼金属Mg、Fe、Zn等有氢气放出10.碱:电离时生成的阴离子全部是氢氧根离子的化合物;碱通常由金属离子和氢氧根离子构成溶碱有五种:钾钙钠钡氨KOH,CaOH2,NaOHBaOH2,氨水它们的溶液无色;有颜色的碱不溶于水:红褐色的氢氧化铁FeOH3↓、蓝色的氢氧化铜CuOH2↓其他固体碱是白色;碱的名称通常有“氢氧化某”,化学式的最后面是“OH”可溶性碱的溶液PH值大于7,紫色石蕊试液遇溶碱变蓝色,无色酚酞试液遇溶碱变红色鉴定可溶性碱溶液鉴定OH-方法一:加紫色石蕊试液变蓝色,加无色酚酞试液变红色是碱.方法二:加铁盐溶液有红褐色沉淀生成;加铜盐溶液有蓝色沉淀的是碱;11.盐:电离时生成金属离子和酸根离子的化合物;第一种分类方法:a.正盐酸碱完全中和的产物,没有可电离的氢离子或氢氧根离子,例如NaCl、Na2SKNO3无氧酸正盐叫“某化某”Na2S_______MgCl2__________FeS__________含氧酸盐叫“某酸某”K NO3_________BaSO4______________Na2CO3______b.酸式盐多元酸里的氢部分被金属取代,H夹在中间NaHCO3____________、CaHCO32_____________、NaH2PO4_____________常见的酸式盐的酸根有:HCO3-、HSO4-、H2PO4-、HPO42-c.碱式盐化学式的中间有“OH”:Cu2OH2CO3第二种分类方法按盐中相同部分的离子称为某类盐:含碳酸根离子的盐称为碳酸盐、含硫酸根离子的盐称为硫酸盐、含硝酸根离子的盐称为硝酸盐、含铁离子的盐称为铁盐,等等;12.酸碱指示剂石蕊试液、无色酚酞和PH值:酸溶液的PH值小于7如盐酸、稀硫酸、硝酸,酸性越强PH值越小,酸性越弱PH值越大;水、中性的硫酸盐、硝酸盐和盐酸盐溶液不能使指示剂变色,PH值等于7;不能使指示剂变色;可溶的碱溶液PH值大于7;碱性越强PH值越大,碱性越弱PH越小13.酸碱盐溶解性口诀:钾钠硝铵溶溶碱有五种钡钾钙钠氨不溶氯化物AgCl不溶硫酸盐BaSO4碳酸盐只溶钾钠铵口诀的含义:含有钾、钠、硝酸根、铵根的物质都溶于水溶于水的碱有:氢氧化钡、氢氧化钾、氢氧化钙、氢氧化钠和氨水,其他碱不溶于水含Cl的化合物只有AgCl不溶于水,其他都溶于水;含SO42-的化合物只有BaSO4不溶于水,其他都溶于水含CO32-的物质只有含K+Na+NH4+溶于水,其他都不溶于水14.沉淀物中AgCl和BaSO4不溶于稀硝酸,FeOH3是红褐色沉淀,CuOH2是蓝色沉淀其他沉淀是白色包括FeOH2有以下常见的沉淀:MgOH2AlOH3CaCO3BaCO3Ag2CO3推断题中,往沉淀物加稀硝酸:若讲沉淀不溶解,则沉淀中一定有AgCl或BaSO4;若讲沉淀全部溶解,则沉淀中一定没有AgCl或BaSO4;若讲沉淀部分溶解,则沉淀中一定有AgCl或BaSO4中的一种,且还有另一种可溶于稀硝酸的沉淀;。
高中化学之物质分类知识点一、混合物混合物是由两种或两种以上物质混合而成的物质。
下面列举常见的混合物:分散系:溶液、胶体、浊液等。
高分子化合物:蛋白质、纤维素、淀粉、塑料等。
其他物质:石油及其各种馏分、天然气、油脂、福尔马林、氨水、王水、碱石灰等。
二、纯净物纯净物与混合物相对,是由一种物质组成,有固定的物理性质和化学性质的物质。
纯净物有专门的化学符号,能用一个化学式表示。
继续细化纯净物的组成可将其分为:1.单质单质是由同一种元素组成的纯净物。
金属单质:例如:K、Ca、Na、Mg、Al等。
非金属单质:例如:S、Cl2、He等。
注意:只含一种元素的物质不一定是纯净物。
如氧气O2和臭氧O3混合得到的物质是混合物。
同种元素的同位素单质混合得到的物质是纯净物。
如氢的同位素氕氘氚组成的双原子分子H2、D2、T2混合在一起得到的是纯净物。
含水的物质不一定是混合物。
如胆矾CuSO4·5H2O、绿矾FeSO4·7H2O、明矾KAl(SO4)2·12H2O都是纯净物。
2.化合物化合物是由两种或两种以上的元素组成的纯净物。
A.按化合物的性质分类①氧化物氧元素与另外一种化学元素组成的二元化合物叫做氧化物。
氧化物可分为:I.酸性氧化物酸性氧化物指与水反应生成相应价态的酸,或与碱反应只生成一种相应价态的盐和水的氧化物。
例如:SO2、SO3、P2O5、SiO2、Mn2O7等。
注意:酸性氧化物不一定是非金属氧化物。
如高锰酸酐Mn2O7既是酸性氧化物,又是金属氧化物非金属氧化物不一定是酸性氧化物。
如一氧化碳CO、一氧化氮NO、二氧化氮NO2都是不成盐氧化物酸性氧化物不一定能与水反应生成相应的酸。
如二氧化硅SiO2不与水反应能与碱反应生成盐和水的氧化物不一定是酸性氧化物。
如二氧化氮NO2是不成盐氧化物,氧化铝Al2O3是两性氧化物。
酸性氧化物一定是酸酐,但酸酐不一定是酸性氧化物。
如乙酸酐CH3COOOCCH3含有三种元素,不是氧化物,故不是酸性氧化物。
混合物和纯净物的区别举例
纯净物是指由一种单质或一种化合物组成的物质,组成固定,有固定的物理性质和化学性质的物质,有专门的化学符号,能用一个化学式表示。
混合物是由两种或多种物质混合而成的物质。
混合物没有固定的化学式,无固定组成和性质,组成混合物的各种成分之间没有发生化学反应,将他们保持着原来的性质。
混合物和纯净物区别混合物:是由两种或两种以上的物质混合而成(或由不同种物质组成)例如,空气,溶液(盐酸、澄清的石灰水、碘酒、矿泉水),矿物(煤、石油、天然气、铁矿石、石灰石),合金(生铁、钢)。
注意:氧气和臭氧混合而成的物质是混合物,红磷和白磷混合也是混合物。
纯净物、混合物与组成元素的种类无关。
即一种元素组成的物质可能是纯净物也可能是混合物,多种元素组成的物质可能是纯净或混合物。
纯净物:由一种物质组成的。
例如:水、水银、蓝矾(CuSO4·5H2O)都是纯净物。
纯净物与混合物的定义1、纯净物:有一种物质组成的物质;特点:纯净物有固定的物理和化学性质纯净物可以用一个化学式表示,可以用化学式表示的一定是纯净物举例:1、氧气:由氧气一种物质组成的纯净物,化学式:O2有固定的物理性质:无色无味的气体,熔点-183.℃有固定的化学性质:助燃性、氧化性,可以与碳反应生成二氧化碳、与金属反应生成金属氧化物等。
2、混合物:有两种或两种以上的物质组成的物质特点:混合物没有固定的物理和化学性质;混合物没有固定的化学式,不能用化学式表示;举例:1、空气:由氧气、氮气、二氧化碳等多种物质组成的混合物,不能用化学式表示,
没有固定的物理和化学性质。