医疗器械不良反应报告记录
- 格式:doc
- 大小:52.50 KB
- 文档页数:1

医疗器械不良反应上报内容及流程下载温馨提示:该文档是我店铺精心编制而成,希望大家下载以后,能够帮助大家解决实际的问题。
文档下载后可定制随意修改,请根据实际需要进行相应的调整和使用,谢谢!并且,本店铺为大家提供各种各样类型的实用资料,如教育随笔、日记赏析、句子摘抄、古诗大全、经典美文、话题作文、工作总结、词语解析、文案摘录、其他资料等等,如想了解不同资料格式和写法,敬请关注!Download tips: This document is carefully compiled by theeditor.I hope that after you download them,they can help yousolve practical problems. The document can be customized andmodified after downloading,please adjust and use it according toactual needs, thank you!In addition, our shop provides you with various types ofpractical materials,such as educational essays, diaryappreciation,sentence excerpts,ancient poems,classic articles,topic composition,work summary,word parsing,copy excerpts,other materials and so on,want to know different data formats andwriting methods,please pay attention!医疗器械不良反应上报的内容与流程详解医疗器械在医疗过程中起着至关重要的作用,然而,任何设备都可能存在潜在的风险和不良反应。

附件1:国家食品药物监督管理局制
可疑医疗器械不良事件报告表
报告日期:年月日编码: 报告来源: 生产公司 经营公司 使用单位单位名称:
联系地址:邮编:联系电话:
报告人签名:
例子:
附
件
1
:国家食品药物监督管理局制
可疑医疗器械
不良事件报告表
报告日期:10月25日 编 码:
报告来源: 生产公司 经营公司 √使用单位 单位名称:按实际填写
联系地址:按实际填写 邮 编: 联系电话:
报告人: 医师 技师 护士 其她
报告人签名:
例子2 附
件
1
:
国家食品药物监督管理局制
可疑医疗器械不良事件报告表 报告日期: 年 10 月 8日 编 码: 报告来源: 生产公司 经营公司 √ 使用单位 单位名称:
报告人: 医师 √ 技师 护士 其她
联系地址: 邮 编: 联系电话:
报告人签名:
报告人: 医师 技师
护士 √ 其她。
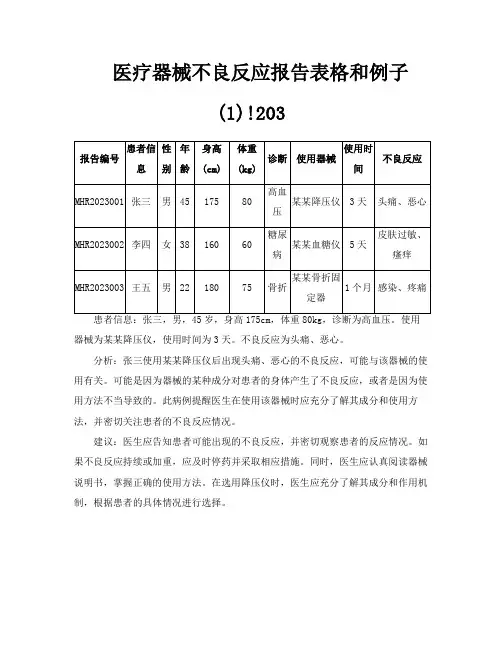
医疗器械不良反应报告表格和例子
(1)!203
患者信息:张三,男,45岁,身高175cm,体重80kg,诊断为高血压。
使用器械为某某降压仪,使用时间为3天。
不良反应为头痛、恶心。
分析:张三使用某某降压仪后出现头痛、恶心的不良反应,可能与该器械的使用有关。
可能是因为器械的某种成分对患者的身体产生了不良反应,或者是因为使用方法不当导致的。
此病例提醒医生在使用该器械时应充分了解其成分和使用方法,并密切关注患者的不良反应情况。
建议:医生应告知患者可能出现的不良反应,并密切观察患者的反应情况。
如果不良反应持续或加重,应及时停药并采取相应措施。
同时,医生应认真阅读器械说明书,掌握正确的使用方法。
在选用降压仪时,医生应充分了解其成分和作用机制,根据患者的具体情况进行选择。

国家食品药品监督管理可疑医疗器械不良事件报告表报告日期: 年 月□ □口 口报告来源:口生产企业 联系地址: 日编码:□□口□□口 口□经营企业口使用单位单位名称: 邮编:联系电话:A 。
患者资料1。
姓名:2。
年龄: 3、性别口男□女 4 .预期治疗疾病或作用:B 。
不良事件情况5。
事件主要表现: 6. 事件发生日期: 年 月曰 7. 发现或者知悉时间: 年 月 日8;医疗器械实际使用场所:口医疗机构 口家庭口其它(请注明): 9、事件后果□死亡 ____________________________________ (时间); □危及生命;□机体功能结构永久性损伤:□可能导致机体功能机构永久性损伤; □需要内、外科治疗避免上述永久损伤; □ 苴它(在事件陈述中说明)。
附件1: 局制依据、使用情况、出现得不良事件情况、对受害者影响、采取得治疗措施、器械联合使用情况)报告人:医师口技师口护士口其她口报告人签名:例子:附件1:国家食品药品监督管理局制可疑医疗器械不良事件报告表报告日期:2010 年 10 月 2 5日编码:□□□□□□□□□ □口报告来源:口生产企业□经营企业口 J使用单位单位名称:按实际填写联系地址:按实际填写邮编:联系电话:A.患者资料1.姓名:|2.年龄:| 3、性别□男□女丁4。
预期治疗疾病或作用:输液B.不良事件情况5.事件主要表现:穿刺部位红肿6.事件发生日期:2010年 1 0月22日7。
发现或者知悉时间:2010年 1 0月22日8、医疗器械实际使用场所:□ V医疗机构口家庭□其它(请注明):5。
事件主要表现:监护仪黑屏6。
事件发生日期:20 1 0年1 0月6日7.发现或者知悉时间:2010年10月6日8^医疗器械实际使用场所:□ J医疗机构□家庭口其它(请注明):9、事件后果□死亡_____________________________________ (时间);□危及生命;□机体功能结构永久性损伤:□可能导致机体功能机构永久性损伤;□需要内、外科治疗避免上述永久损伤:口 J其它(在事件陈述中说明).10、事件陈述:(至少包括器械使用时间、使用目得、使用依据、使用情况、出现得不良事件情况、对受害者影响、采取得治疗描施、器械联合使用情况)患者因心脏病发作到我科治疗,于2 010年10月6 日10时20分使用多参数监护仪监护病人,至30分钟,多参数监护仪显示屏突然黑屏,因而无法监测到病人生命体征,立即更换多参数监护仪,对患者没有造成不良影响.报告人:医师口技师口护士其她□报告人签名:。

器械不良反应报告制度范本尊敬的领导:我根据《器械不良反应报告制度》的要求,就近期发生的器械不良反应进行了整理和归纳,现将报告如下:1. 器械名称:XXXXX简要描述:XXXXX是一种用于治疗血压异常的药物。
使用过程中,出现了一起严重的过敏反应,患者出现呼吸困难、皮肤潮红、心悸等症状。
添附患者病历和医院护理记录。
处理情况:立即停止使用该药物,给予抗过敏治疗,并密切监测患者情况。
后续随访显示症状缓解。
2. 器械名称:XXXXX简要描述:XXXXX是一种外科手术器械。
使用过程中,医生反馈该器械存在操作不便、易滑脱等问题。
这导致手术过程中的不稳定情况。
处理情况:经过与生产商的沟通和反馈,生产商承诺对器械进行改进,并提供了使用手册的更新版本。
医院将与生产商密切合作,确保新版本的器械安全使用。
3. 器械名称:XXXXX简要描述:XXXXX是一种心脏搏动监测仪器。
在使用过程中,出现了一起数据显示不准确的情况,导致医生误判了患者的心脏状况。
处理情况:立即停止使用该监测仪器,并通知生产商进行检修。
同时对患者进行其他检查以确保病情的准确评估。
以上是近期发生的几起器械不良反应报告,根据《器械不良反应报告制度》,我已将这些情况上报给相关部门,并与生产商进行了沟通,以取得进一步解决的方案。
我将继续密切关注器械的使用情况,并推动完善器械安全管理制度。
谢谢!XX医院器械不良反应报告人XX日期器械不良反应报告制度范本(2)引言:随着科技的发展和医疗水平的提高,医疗器械在诊断、治疗和康复中起到了越来越重要的作用。
但是,与之相对应的也是器械使用过程中不可避免的风险和不良反应。
为了确保患者的安全和权益,以及推动医疗器械的安全性和质量的提升,建立器械不良反应报告制度显得尤为重要。
本文将从不良反应报告制度的意义、目标、程序、评估和监督等方面进行详细阐述,以期为制定、完善和落实器械不良反应报告制度提供参考。
一、不良反应报告制度的意义制定器械不良反应报告制度的意义在于:1. 保障患者权益。

国家食品药品监督管理局制可疑医疗器械不良事件报告表报告日期:报告来源: 联系地址:A. 患者资料1.姓名:2 .年龄: 3•性别 男 女4 .预期治疗疾病或作用:B. 不良事件情况5. 事件主要表现: 6 .事件发生日期: 年 月曰 7 •发现或者知悉时间: 年 月曰8. 医疗器械实际使用场所:医疗机构 家庭 其它(请注明):9. 事件后果死亡 _________________________________ (时间); 危及生命;机体功能结构永久性损伤; 可能导致机体功能机构永久性损伤; 需要内、外科治疗避免上述永久损伤; 其它(在事件陈述中说明)。
10. 事件陈述:(至少包括器械使用时间、使用目的、使 用依据、使用情况、出现的不良事件情况、对受害者影 响、采取的治疗措施、器械联合使用情况)报告人: 医师 技师 护士 其他邮 编:联系电话:报告人签名:附件1:年 月曰生产企业经营企业例子:附件1:可疑医疗器械不良事件报告表报告日期:2010年10月25日 编 码:邮 编:联系电话:A. 患者资料1.姓名:2 .年龄:3•性别男女"4 •预期治疗疾病或作用:输液B. 不良事件情况5•事件主要表现:穿刺部位红肿 6.事件发生日期: 2010年10 月22日7 .发现或者知悉时间: 2010年10月22日8. 医疗器械实际使用场所:V 医疗机构 家庭 其它(请注明):9. 事件后果死亡 _________________________________ (时间); 危及生命;机体功能结构永久性损伤; 可能导致机体功能机构永久性损伤; 需要内、外科治疗避免上述永久损伤;V 其它(在事件陈述中说明)。
国家食品药品监督管理局制报告来源: 生产企业 经营企业 "使用单位 单位名称:按实际填写联系地址:按实际填写10. 事件陈述:(至少包括器械使用时间、使用目的、使用依据、使用情况、出现的不良事件情况、对受害者影响、采取的治疗措施、器械联合使用情况)患者于2010年10月20日在我院留医治疗使用一次性使用静脉留置针,穿刺部位于穿刺输液后2天出现皮肤红肿,无发热等现象,拔除一次性使用静脉留置针1天后症状消失。

器械不良反应报告制度范文尊敬的主管领导:我是XXX部门的员工,根据公司要求,特向您汇报我在工作中发现的器械不良反应情况。
具体情况如下:时间:2022年XX月XX日地点:XXX部门实验室事件描述:该次实验中,我们使用了新购进的实验仪器,按照说明书和操作手册的指导进行使用。
然而,在实验过程中发现该仪器存在以下不良反应:1. 仪器在操作过程中突然停止工作,无法正常启动。
经过排查,发现是电源线连接不牢固导致的,重新连接后仪器恢复正常工作。
2. 在操作过程中,仪器显示屏出现反复闪烁的情况,导致实验数据无法正常显示和记录。
尝试重启和调整设置均无效,最终只能放弃该实验项目。
3. 使用该仪器进行多次实验后发现,仪器在高温环境下使用工作不稳定,容易出现停机现象。
处理过程:在发现以上问题后,我立即向实验室主管报告了情况,并请求其指导和协助解决问题。
实验室主管与供应商联系,对仪器进行检修和维修,并提出了以下解决方案:1. 提醒使用该仪器的员工,在操作仪器前,务必检查电源线连接是否牢固,确保线路正常。
2. 与供应商协商,寻找解决仪器显示屏闪烁问题的办法,确保实验数据准确可靠。
3. 在高温环境下使用该仪器时,适当调整实验温度,控制仪器工作环境,以减少停机现象的发生。
经过以上措施的实施,仪器的功能恢复正常,不良反应的情况得到了解决。
建议:鉴于该仪器存在的一系列不良反应问题,建议公司采取以下措施:1. 给予员工相关的仪器使用培训和操作指导,提高其对仪器故障排除和处理的能力。
2. 对购进的仪器进行更加严格的质量检查和验收,确保其质量符合要求。
3. 定期对仪器进行维护和保养,减少不良反应的发生。
总结:通过对该次不良反应情况的处理,我们不仅解决了实验中的问题,还提出了相应的建议和改进措施。
希望公司能够重视我提出的问题和建议,并采取相应的措施,以确保未来工作过程中仪器使用的稳定性和安全性。
谢谢您的关注和支持!此致敬礼XXX日期器械不良反应报告制度范文(二)一、目的及范围为确保对医疗器械不良反应的及时收集、评估和汇总,保障器械使用安全,制定本制度。

可疑医疗器械不良反应报告表范文英文回答:Adverse Event Reporting Form for Suspected Medical Device Adverse Reactions.Name: [Your Name]Date: [Date]Patient Information:Name: [Patient's Name]Age: [Patient's Age]Sex: [Patient's Gender]Medical History: [Brief summary of patient's medical history]Device Information:Device Name: [Name of the medical device]Manufacturer: [Name of the manufacturer]Model/Serial Number: [Model/Serial Number of the device]Date of Implantation/Use: [Date of deviceimplantation/use]Description of the Adverse Event:Please provide a detailed description of the adverse event experienced by the patient, including any signs or symptoms observed.Example: I recently used a blood pressure monitoring device on a patient. The patient experienced severe painand discomfort during the procedure. The device seemed tobe malfunctioning as it was displaying inconsistentreadings. The patient's blood pressure was also abnormally high, which was concerning.Actions Taken:Please describe any actions taken in response to the adverse event, such as discontinuation of device use, medical intervention, or device replacement.Example: As soon as I noticed the patient's discomfort and the device malfunction, I immediately stopped using the device. I informed the patient about the situation and provided them with alternative methods for monitoring their blood pressure. I also reported the incident to thehospital's medical device department for further investigation.Outcome:Please describe the outcome of the adverse event, including any medical interventions or treatments provided to the patient.Example: After discontinuing the use of the blood pressure monitoring device, the patient's pain and discomfort subsided. The patient was closely monitored for any further complications and was eventually switched to a different device for blood pressure monitoring. No further adverse events were reported.Preventive Measures:Please suggest any preventive measures that can be taken to avoid similar adverse events in the future.Example: To prevent similar adverse events in the future, it is important to conduct regular maintenance and calibration checks on medical devices. Additionally, healthcare professionals should receive proper training on device usage and troubleshooting. It is also crucial to establish a robust reporting system for adverse events to ensure prompt investigation and appropriate action.中文回答:可疑医疗器械不良反应报告表。
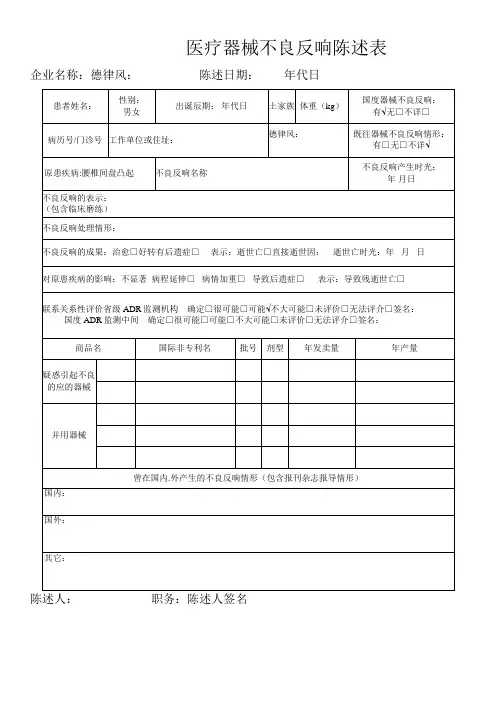

附件1:国家食品药品监督管理局制
可疑医疗器械不良事件报告表
报告日期: 年月日编码:
报告来源: 生产企业 经营企业 使用单位单位名称:联系地址: 邮编: 联系电话:
报告人:医师 技师 护士 其他
例子:
可疑医疗器械不良事件报告表
报告日期:2010年10月25日编码:
报告来源: 生产企业 经营企业 √使用单位单位名称:按实际填写联系地址:按实际填写邮编:联系电话:
报告人:医师 √技师 护士 其他
例子2
可疑医疗器械不良事件报告表
报告日期: 2010 年 10 月 8日编码:
报告来源: 生产企业 经营企业 √使用单位单位名称:联系地址:邮编:联系电话:
报告人: 医师 技师 护士 √其他。

附件1:《可疑医疗器械不良事件报告表》及填写要求可疑医疗器械不良事件报告表报告日期:报告来源:联系地址:年月曰生产企业经营企业编码:使用单位单位名称:邮编:联系电话:A •患者资料1.姓名: 2 .年龄:3•性别男女4 •预期治疗疾病或作用:B.不良事件情况5 •事件主要表现:6•事件发生日期:年月曰7 •发现或者知悉时间:年月曰8.医疗器械实际使用场所:医疗机构家庭其他(请注明):9.事件后果死亡(时间);危及生命;机体功能结构永久性损伤;可能导致机体功能结构永久性损伤;需要内、外科治疗避免上述永久损伤;其他(在事件陈述中说明)。
10.事件陈述:(至少包括器械使用时间、使用目的、使用依据、使用情况、岀现的不良事件情况、对受害者影响、采取的治疗措施、器械联合使用情况)报告人:医师技师护士其他填写要求《可疑医疗器械不良事件报告表》由题眉、患者资料、不良事件情况、医疗器械情况、关联性评价、不良事件评价及题末7部分组成1. 题眉A.报告日期:是指填报人填报该次不良事件时的确切时间。
B.编码:由省(区、市)医疗器械不良事件监测技术机构填写,按以下排列方式:省(区、市)年份流水号□□ □□□□ □□□□□ 注:省(区、市)编码按中华人民共和国行政区划代码填写。
在医疗器械不良事件监测系统中,编码由系统自动生成。
C.报告来源:是指填报可疑医疗器械不良事件单位的类别,填写时请选择相应的选项,并在“□”中划“。
D.单位名称:是指填报可疑医疗器械不良事件单位的全称,不可用简称。
E.联系地址、电话及邮编:是指填报可疑医疗器械不良事件单位的联系地址、电话及邮编。
2. 患者资料A.患者姓名:是指患者真实全名。
若患者姓名无法获知,应填写未知;新生儿无姓名,应填写XX子或XX女。
B.年龄:是指患者发生可疑医疗器械不良事件时的实际年龄,字体为阿拉伯数字。
若患者年龄小于1 岁,应填写具体的月份或天数,如6 个月。
C.性别:是指患者的性别,填写时请选择相应的选项,并在“口D.预期治疗疾病或作用:是指涉及不良事件的医疗器械用于治疗的疾病或者预计使用该医疗器械所发挥的作用,例如血管内支架用于治疗急性心肌梗死。
医疗器械不良事件报告范例近年来,随着社会经济的发展和医疗技术的突破,医疗器械在医疗行业中的应用越来越广泛。
然而,与之同时,医疗器械不良事件也时有发生,给人们的生命安全带来了一定的威胁。
为了更好地管理和控制医疗器械不良事件,必须建立一个完善的报告系统。
本文将以一个医疗器械不良事件的报告范例为例,详细介绍该报告的内容和形式。
报告主题:医用电动吸引器失灵一、事件描述根据我院2021年5月1日至5月30日期间发生的医疗器械不良事件报告,报告编号:12345678。
事发时间为2021年5月15日上午10点,患者王某(男,65岁)在我院进行鼻窦炎手术后出现呼吸困难的不良状况。
经过紧急救治,患者目前病情稳定。
二、器械信息患者在手术时使用了我院购买的医用电动吸引器丙型型号(批次号:ABC123456)。
该器械主要用于排除呼吸道分泌物,确保患者的通畅呼吸。
三、失灵情况描述据手术室护士陈某的描述,手术期间,电动吸引器突然停止运转,无法完成抽吸任务。
护士随即通知同事切换到备用吸引器继续手术。
经过后续的检查和调查,确定该电动吸引器发生了严重故障,导致了此次意外。
四、结果由于电动吸引器故障,患者出现呼吸困难。
幸好我们的医护人员反应及时,迅速采取了紧急救治措施,患者目前病情稳定。
五、原因分析根据技术人员的分析,初步判断电动吸引器失灵的原因是设备内部的电线连接问题,导致电路中断,使得设备无法正常运行。
六、整改措施1. 停止使用该型号的电动吸引器,并将其送至供应商修理。
2. 加强器械设备的定期检查和维护,确保设备的正常运行。
3. 设立医疗器械不良事件报告制度,加强对医疗器械的质量监管。
七、教训与总结本次医疗器械不良事件表明,医疗机构在选择和使用医疗器械时必须十分谨慎。
对于设备故障要及时发现和排除,并加强对设备的定期检查和维护。
同时,建立医疗器械不良事件报告制度,及时报告和处理医疗器械不良事件,以提高患者的安全性和医疗服务质量。
附件1:国家食品药品监督管理局制
可疑医疗器械不良事件报告表
报告日期:年月日编码:
报告来源: 生产企业 经营企业 使用单位单位名称:
联系地址: 邮编:联系电
话:
报告人签名:
例子:
附件
1:
国家食品药品监督管理局制
可疑医疗器
械不良事件报告表
报告日期:2010年10月25日 编 码:
报告来源: 生产企业 经营企业 √使用单
位 单位名称:按实际填写
联系地址: 按实际填写邮 编: 联系电话:
报告人: 医师
技师 护士 其她
报告人签名:
例子2
附件1:
国家食品药品监督管理局制
可疑医疗器械不良事件报告表
报告日期: 2010 年 10 月 8日 编 码:
报告来源: 生产企业 经营企业 √ 使用单位 单位名称:
联系地址: 邮 编: 联系电话报告人: 医师 √ 技师 护士 其她
报告人签名:
报告人: 医师 技师 护士 √ 其她。
附件1:《可疑医疗器械不良事件报告表》及填写要求可疑医疗器械不良事件报告表报告日期: 年 月 日 编 码: 报告来源: 生产企业 经营企业 使用单位 单位名称:联系地址: 邮 编: 联系:报告人签名:国家食品药品监督管理局制填写要求《可疑医疗器械不良事件报告表》由题眉、患者资料、不良事件情况、医疗器械情况、关联性评价、不良事件评价及题末7部分组成。
1.题眉A.报告日期:是指填报人填报该次不良事件时的确切时间。
B.编码:由省(区、市)医疗器械不良事件监测技术机构填写,按以下排列方式:省(区、市)年份流水号□□□□□□□□□□□注:省(区、市)编码按中华人民国行政区划代码填写。
在医疗器械不良事件监测系统中,编码由系统自动生成。
C.报告来源:是指填报可疑医疗器械不良事件单位的类别,填写时请选择相应的选项,并在“□”中划“√”。
D.单位名称:是指填报可疑医疗器械不良事件单位的全称,不可用简称。
E.联系地址、及邮编:是指填报可疑医疗器械不良事件单位的联系地址、及邮编。
2.患者资料A.患者:是指患者真实全名。
若患者无法获知,应填写未知;新生儿无,应填写××子或××女。
B.年龄:是指患者发生可疑医疗器械不良事件时的实际年龄,字体为阿拉伯数字。
若患者年龄小于1岁,应填写具体的月份或天数,如6个月。
C.性别:是指患者的性别,填写时请选择相应的选项,并在“□”中划“√”。
D.预期治疗疾病或作用:是指涉及不良事件的医疗器械用于治疗的疾病或者预计使用该医疗器械所发挥的作用,例如血管支架用于治疗急性心肌梗死。
3.不良事件情况A.事件主要表现:是指使用医疗器械后引发的、可能与该医疗器械使用有关的有害事件(且与质量、医疗事故无关)。
填写不良事件主要表现要明确、具体,如放置节育器后,出现意外脱落者,可填写“节育器脱落”。
B.事件发生日期:是指不良事件发生的确切时间,如:×年×月×日,字体为阿拉伯数字。
器械不良反应报告表器械不良反应报告表作为医疗行业中不可或缺的工具,被广泛应用于医疗器械不良反应的监测和报告。
这一表格的使用不仅帮助医护人员及时识别和处理器械使用过程中可能出现的不良反应,还有助于相关管理机构了解和控制不良反应的情况,进一步提高医疗器械的安全性和可靠性。
近年来,医疗器械行业快速发展,新型器械层出不穷。
然而,随着器械使用范围的扩大,不良反应的发生频率也相应增加。
因此,及时、全面地对器械不良反应进行监测和报告,显得尤为重要。
器械不良反应报告表通常包括器械基本信息、不良反应识别和分类、报告者信息等几个方面。
首先,器械基本信息部分包括器械的名称、型号、生产日期、产地等内容,有助于准确标识出问题器械的具体信息。
其次,不良反应识别和分类部分是这一表格中最为重要的部分。
在这个部分,必须准确描述患者在使用某种器械后出现的不良反应症状,如过敏、疼痛、刺激等。
同时,根据不良反应的症状和严重程度,对反应进行分类,有助于对不同程度的不良反应进行合理评估和处理。
然而,当前的器械不良反应报告表仍然存在一些问题和挑战,需要进一步改进和完善。
首先,目前的报告表对不良反应的描述仅限于文字形式,这种表达方式可能存在主观性、不准确性的问题。
为了更准确描述不良反应,可以引入图像或多媒体方式,如添加照片或视频,使报告更加直观。
其次,当前的不良反应分类并不统一,不同地区、不同医疗机构对不良反应的分类标准存在差异,这给不良反应的监测和评估带来一定的困难。
因此,有必要在报告表中引入统一的分类标准,以便更好地对不良反应进行整合和分析。
此外,为了加强对器械不良反应的监测和报告,相关管理机构还应建立健全的信息交流和共享机制。
一方面,通过建立器械不良反应数据库,将各地的不良反应信息集中存储和管理,避免信息孤岛的问题。
另一方面,医疗机构应加强与患者的沟通和联络,鼓励患者及时报告不良反应,以便第一时间采取措施。
综上所述,器械不良反应报告表在医疗器械行业中具有重要作用。
附件1:国家食品药品监督管理局制
可疑医疗器械不良事件报告表
报告日期:年月日编码:
报告来源: 生产企业 经营企业 使用单位单位名称:
联系地址: 邮编:联系电
话:
报告人签名:
例子:
附件
1:
国家食品药品监督管理局制
可疑医疗器
械不良事件报告表
报告日期:2010年10月25日 编 码:
报告来源: 生产企业 经营企业 √使用单
位 单位名称:按实际填写
联系地址: 按实际填写邮 编: 联系电话:
报告人: 医师
技师 护士 其她
报告人签名:
例子2
附件1:
国家食品药品监督管理局制
可疑医疗器械不良事件报告表
报告日期: 2010 年 10 月 8日 编 码:
报告来源: 生产企业 经营企业 √ 使用单位 单位名称:
联系地址: 邮 编: 联系电话报告人: 医师 √ 技师 护士 其她
报告人签名:
报告人: 医师 技师 护士 √ 其她。