病毒鉴定的方法有哪些
- 格式:docx
- 大小:699.14 KB
- 文档页数:4

植物病毒鉴定方法有
植物病毒鉴定是一种诊断学技术,用于识别植物病毒,鉴定植物病毒是防治植物病害的关键。
目前,植物病毒鉴定在植物病理研究、病原鉴定和其他生物技术领域都得到了很高的应用价值。
植物病毒鉴定可分为微生物学分析、化学分析、生物学分析和分子生物学分析4个方面,以尽可能准确地评估病毒引起的病害发生可能性。
1. 微生物学分析:主要检测病原体的传播性的分布特征,以及病原物的特异性和症状,如植物病理学、扫描电镜网织菌病毒鉴定等。
2. 化学分析:检测病原体的化学物质,如叶绿窿面农物质、唾液核酸酶鉴定等。
3. 生物学分析:采用分子大小分离技术,如集群分析、放射致性等,检测病原体的细胞结构特征。
4. 分子生物学分析:采用分子分析来识别和鉴定不同种类的病毒,如质粒克隆鉴定(PCR)、单克隆抗体试验、DNA杂交等。
植物病毒鉴定可以有效地准确定位病原,及早识别病原体,起到重要的防治作用。
因此,正确无误地使用植物病毒鉴定技术对植物病害的防治至关重要。

植物病毒的鉴别和检测方法研究植物病毒是影响植物健康和产量的主要因素之一。
对于农业和园艺领域,发现和鉴别植物病毒是至关重要的。
然而,由于病毒的微小尺寸、繁殖速度快且具有高度变异性和适应性等特性,在不加以特殊处理的情况下很难鉴别和检测。
因此,开发高效的植物病毒鉴别和检测方法已成为当前研究热点之一。
一、植物病毒的鉴别方法1. 细菌性斑点病法(Bacterial Spot Test)该方法通过施加细菌性斑点病感染物质,并观察植物叶片上斑点的形成来确定是否感染病毒。
该方法操作简单、直观易懂,但只能用于一些植物病毒的初步鉴定,无法确定所感染的具体类型和种类。
2. 酶联免疫吸附检测法(Enzyme-Linked Immunosorbent Assay, ELISA)该方法通过利用特定的抗体与病毒抗原反应,形成免疫复合物,再用酶作为信号反应物进行检测。
该方法的优点在于检测灵敏度高、精准度高、直观易懂,同时适用于多种植物病毒的鉴别。
但是,该方法对于一些种类不太熟悉的病毒,需要提前准备特定的抗体和病毒抗原,且操作过程比较繁琐。
3. 聚合酶链反应(Polymerase Chain Reaction, PCR)该方法通过利用特定引物和酶,扩增目标病毒基因序列,并通过凝胶电泳等方式进行验证和鉴别。
该方法优点在于操作快速、准确度高、适用范围广,可以扩增低浓度的病毒Ap发现,同时还可以检测多个病毒基因序列,具有一定的实用性。
但是该方法的缺点在于设备成本高,且无法确定扩增物中病毒成分的比例。
二、植物病毒的检测方法1. 病毒杂交法(Virus Hybridization)该方法通过利用核酸探针与目标病毒中特定序列的杂交,形成稳定的杂交产物,并通过凝胶电泳等方式进行检测。
该方法优点在于具有较高的检测敏感性和特异性,同时可以定量分析病毒的含量,而且不受病毒变异性的影响。
该方法的局限性在于需要提前准备特定的核酸探针,对于多个病毒的检测需要分别合成多个核酸探针,操作较为繁琐。

病毒的分离与鉴定简介:病毒是一种微生物,属于病原体的一种。
它可以寄生于宿主细胞中,并利用宿主细胞的代谢系统繁殖。
为了进行研究和控制病毒的传播,科学家们需要对病毒进行分离和鉴定。
本文将介绍病毒的分离和鉴定的方法和步骤。
一、病毒的分离病毒的分离是指将病毒从混合物中单独提取出来。
以下是一些常用的病毒分离方法:1. 细胞培养法:这是一种常用的病毒分离方法。
首先,将病毒样本接种到细胞培养基中培养,待病毒感染细胞后,观察细胞形态的改变、病毒颗粒的释放等现象,进而证实病毒的存在。
2. 动物接种法:这是一种直接将病毒样本接种到实验动物体内的方法。
通过观察动物是否出现病征,如发热、无食欲等,可以初步判断病毒的存在。
3. 超速离心法:这是一种利用离心的原理将病毒从样本中分离出来的方法。
通过对病毒样本进行一系列的离心操作,可以使病毒沉积于管底,从而得到纯净的病毒悬液。
二、病毒的鉴定病毒的鉴定是指确定分离的病毒属于哪一种或某一类病毒的过程。
以下是一些常用的病毒鉴定方法:1. 电子显微镜观察法:使用电子显微镜观察病毒的形态、结构和大小等特征。
这种方法可以给出病毒的直接信息,帮助科学家们确定病毒的种类。
2. 免疫学方法:通过免疫学方法如酶联免疫吸附试验(ELISA)、免疫荧光等,检测病毒与抗体的特异性反应。
根据反应结果,可以初步鉴定病毒的种类。
3. 分子生物学方法:利用PCR、基因测序等分子生物学方法,可以对病毒样本进行基因分析,进一步确认病毒的物种。
这些技术可以检测病毒的基因序列,通过与已知病毒的序列进行比对,鉴定病毒的种类和亲缘关系。
结论:病毒的分离和鉴定是研究和控制病毒传播的重要步骤。
通过适当的分离方法,可以有效地将病毒从样本中提取出来,并通过鉴定方法确定病毒的种类和特性。
病毒的分离和鉴定是研究和治疗病毒相关疾病的基础,也为疾病的监控和防控工作提供了重要的支持。
注意,为了确保实验室安全,病毒的分离和鉴定应在合适的实验条件下进行,并且遵循相关的实验规范和操作流程。

肺炎支原体感染的病毒分离与鉴定方法近年来,肺炎支原体感染成为全球范围内的公共卫生问题。
该病原体引起的肺炎病例逐年上升,对人类健康造成了严重威胁。
为了及时诊断和治疗肺炎支原体感染,科学家们开发了一系列有效的分离和鉴定方法。
本文将对肺炎支原体感染的病毒分离与鉴定方法进行介绍。
一、流行病学调查在分离和鉴定肺炎支原体感染的病毒之前,进行流行病学调查是十分重要的。
通过调查病例发生的地点、时间、人群等信息,可以迅速锁定病原体分布的区域和特点,为下一步的分离和鉴定提供指导。
二、病毒分离病毒分离是检测肺炎支原体感染的基础步骤,常用的方法主要有以下几种:1. 细胞培养法:将临床标本中的病原体与合适的培养基和细胞共同培养,利用病原体在细胞内生长繁殖的特性,最终将病毒分离出来。
2. 动物接种法:将临床标本中的病原体接种到实验动物体内,观察其是否出现与肺炎支原体感染相类似的症状,通过实验动物的复制,最终得到病毒分离物。
三、病毒鉴定病毒分离后,需要进行鉴定以确认其是否为肺炎支原体感染的病毒。
常用的鉴定方法主要有以下几种:1. 免疫学方法:利用免疫学技术,如免疫荧光法、酶联免疫吸附试验等,对分离得到的病毒进行特异性检测和鉴定。
2. 分子生物学方法:利用PCR、实时荧光定量PCR等技术,通过分析病毒基因的特征序列,快速鉴定肺炎支原体感染的病毒。
四、抗体检测除了分离和鉴定病毒本身以外,通过检测患者体内产生的抗体,也可以对肺炎支原体感染进行诊断。
常用的抗体检测方法有血清学试验和免疫层析试验等。
五、药敏试验药敏试验可以评估肺炎支原体感染的病毒对不同抗生素的敏感性。
通过对分离的病毒进行不同抗生素的药物敏感性测试,可以指导临床医生开展合理的抗生素治疗。
六、实时监测和报告随着肺炎支原体感染的增加,实时监测和报告已成为防控的重要环节。
利用PCR等快速诊断技术,可将分离和鉴定的结果及时反馈给相关部门,以便及时采取防控措施,降低感染的传播风险。

生物医学中的病毒诊断技术病毒是引起各种传染病的主要病原体之一。
随着科技的进步,生物学领域的诊断技术也得到了飞速的发展,从传统的病原体分离鉴定到现代的分子诊断技术,不断提高了病毒感染的检出率、速度和准确性。
本文将主要介绍目前生物医学中的病毒诊断技术。
传统的病原体分离鉴定技术传统的病原体诊断方法包括细菌、病毒、真菌、寄生虫等多个类型,而因病毒种类复杂与特异性较低,传统的病原体分离鉴定技术对于病毒的检测并不敏感和准确。
采用细胞学技术和病毒培养方法进行病毒诊断,具有直观、可靠、最为经典的特点,也是检测病毒传播和流行趋势变化的一个有效方法。
但是,这种方法需要等待培养结果甚至需要几天时间,同时操作复杂、成本较高,且需要高度专业化的实验室和技术人员,因此也面临着一定的限制。
核酸检测技术目前,核酸检测被认为是最常用的检测方法。
PCR检测技术以及其改进型技术如实时荧光定量PCR、巢PCR都可以快速地检测出病毒核酸,且具有高灵敏度和准确性。
另外,原位PCR和巢DNA芯片技术在病毒诊断方面也得到了广泛的应用。
原位PCR技术像是一种新型的免疫组化染色法,它能够直接进行分子检测,并可以快速检测出一系列病毒,不仅有助于快速确定病毒感染的类型,并且不需要忍受长时间的处理。
除了PCR检测技术外,还有一些新兴的技术多用于新型病毒的检测,如基于下一代测序技术(NGS)的病毒检测,其可对病毒全基因组进行检测或序列后的比对,具有高通量、高灵敏度和快速性的特点。
同时,NGS技术不受病能毒重组的影响,可有效克服PCR技术在病毒序列方面存在的偏差性和代表性问题。
这一技术可以更快更方便地检测出新型病毒,克服病毒突变的问题。
蛋白质检测技术蛋白质检测技术是一种补充其它检测方法的技术,因为病毒感染后会产生大量的病毒抗原和抗体,所以基于病毒抗体的检测方法也是常用的一种诊断手段。
ELISA是目前最常使用的病毒抗体检测技术,是一种固相酶联免疫吸附检测技术,它可以通过甲苯胺染色的方法定性和半定量地检测出病毒抗原和抗体。

临床微生物—病毒的诊断病毒学实验诊断有三个方面:①直接检测和分离鉴定;②检测病毒蛋白抗原成分和核酸;③检测抗体。
一、标本采集、运送及处理1.标本采集①采样时机:应在病人急性期或发病初期采集标本。
②标本种类。
呼吸道鼻咽洗漱液或痰液,肠道粪便,脑内脑脊液,发疹疱疹积液,血液。
2.标本的运送及保存大多数病毒抵抗力较弱,在室温中易被灭活,所以标本要快速送检,及时处理和接种。
采集和运送过程注意冷藏。
如不能立即处理和接种,可在4℃保存数小时,长时间保存需置-70℃。
对于在冻融过程中易失去感染性的标本,冻存时应加入适当的保护剂如甘油或二甲基亚砜等。
二、分离培养与鉴定1.分离培养(1)组织培养:包括组织块培养和细胞培养。
目前常用的方法是细胞培养。
关键是针对不同的欲检测病毒,选择适当的培养细胞。
细胞培养根据细胞的来源、染色特征及传代次数主要分3种类型:①原代和次代细胞培养;②二倍体细胞株;③传代细胞系。
(2)鸡胚接种:乙型脑炎病毒以接种卵黄囊为最佳,羊膜腔和尿囊腔适合于流感病毒和腮腺炎病毒,绒毛尿囊膜对痘类病毒和疱疹病毒敏感。
(3)动物接种:实验室常用新生小鼠或乳鼠进行病毒分离。
根据病毒种类不同,需选择相应的敏感动物,还需接种相应的合适部位。
2.病毒鉴定(1)初步鉴定:根据临床症状、流行病学特点、标本来源、易感动物范围、细胞病变特征及生物学特征、理化性质可初步判断病毒的科及属。
(2)最终鉴定:将分离到的病毒和已知病毒的参考血清学试验。
如中和试验、补体结合试验、血凝抑制试验、免疫荧光试验、酶免疫试验等。
3.分子生物学方法:核酸检测(新冠病毒用的是逆转录实时聚合酶链式反应RT- PCR)三、快速诊断1.显微镜检查(1)光学显微镜检查病毒包涵体。
(2)电子显微镜检查病毒颗粒,应用免疫电镜灵敏度更高。
2.病毒抗原检查利用特异性免疫血清检测标本中的病毒抗原。
常用方法有:免疫荧光技术、酶免疫技术等。
此外还有放射免疫法、反相间接血凝和对流免疫电泳等方法。

病毒滴度测定方法
病毒滴度测定是一种用于确定病毒在溶液中的浓度的方法。
它通常用于病毒学研究、疫苗生产和药物研发等领域。
正确的病毒滴度测定方法可以帮助科研人员准确地评估病毒的活性和浓度,从而为相关研究工作提供可靠的数据支持。
下面将介绍几种常用的病毒滴度测定方法。
一、细胞培养法。
细胞培养法是一种常用的病毒滴度测定方法。
首先,将待测病毒样品与细胞培养基混合,然后在培养皿中接种一定数量的细胞,并将混合液加入培养皿中。
接下来,将培养皿放入恒温培养箱中,培养一定时间后观察细胞的感染情况,根据感染细胞的数量可以计算出病毒的滴度。
二、血凝法。
血凝法是另一种常用的病毒滴度测定方法。
这种方法利用病毒对红细胞的凝集作用来确定病毒的滴度。
首先,将一定浓度的病毒样品与红细胞混合,然后在琼脂培养皿中进行凝集反应。
根据凝集的程度和范围可以计算出病毒的滴度。
三、动物接种法。
动物接种法是一种直接将病毒样品接种到动物体内,通过观察动物的感染情况来确定病毒滴度的方法。
这种方法通常用于病毒毒力的测定。
通过确定50%动物传染单位(TCID50)或50%致死剂量(LD50)来表示病毒的滴度。
总结。
以上介绍了几种常用的病毒滴度测定方法,每种方法都有其特点和适用范围。
在进行病毒滴度测定时,需要根据实际情况选择合适的方法,并严格按照操作规程进行操作,以确保测定结果的准确性和可靠性。
希望本文对您有所帮助。

微生物生化鉴定【微生物生化鉴定】微生物生化鉴定是一种鉴定微生物种类和特性的方法,它通过检测微生物代谢产物和酶的活性等生化特性来对微生物进行鉴定。
在微生物的研究、诊断和治疗等方面都有着广泛的应用。
下面我们将分别介绍鉴定细菌、真菌和病毒的微生物生化鉴定方法。
一、细菌的微生物生化鉴定1. 常规生化试验:包括氧化-发酵试验、铁锰试验、利用光对紫杆菌的鉴别、胶原酶酶切试验等。
2. 抗生素敏感试验:对于致病菌的抗生素敏感试验是非常重要的生化鉴定方法。
在临床上,通过检测微生物对各种抗生素的敏感性来确定选用哪种抗生素进行治疗。
3. 酸碱度试验:对于肠道菌等产生乳酸的菌株,可以通过酸碱度试验来鉴定其种类。
4. 糖代谢试验:细菌不同的糖代谢方式也是一种微生物生化鉴定方法。
二、真菌的微生物生化鉴定1. 吸附凝集实验:可用于白色念珠菌的鉴定。
2. 纸片扩散法:可用于真菌药物敏感性试验。
3. 不同培养基的试验:对于不同种类的真菌,它们对不同培养基有不同的适应性,可以通过这种方法来进行鉴定。
4. 营养需求试验:真菌的营养需求也不同,通过对真菌在培养基上的生长情况进行观察,可以对其种类进行初步鉴定。
三、病毒的微生物生化鉴定1. 免疫荧光试验:通过对病毒进行免疫染色等手段来进行鉴定。
2. 基于PCR技术的鉴定:包括标准PCR、荧光PCR和荧光定量PCR等方法。
3. 细胞培养法:将病毒在细胞培养基上培养,观察病毒在细胞上的生长和变化,以进行鉴定。
总之,微生物生化鉴定方法是一种基础的、重要的微生物鉴定方法,对于微生物的研究、诊断和治疗等方面都具有重要的意义。
不同类型的微生物鉴定方法不同,需要根据具体的情况进行选择和操作。
通过合理地运用微生物生化鉴定方法,可以更准确地鉴定不同类型的微生物,为其应用提供有力的支持。
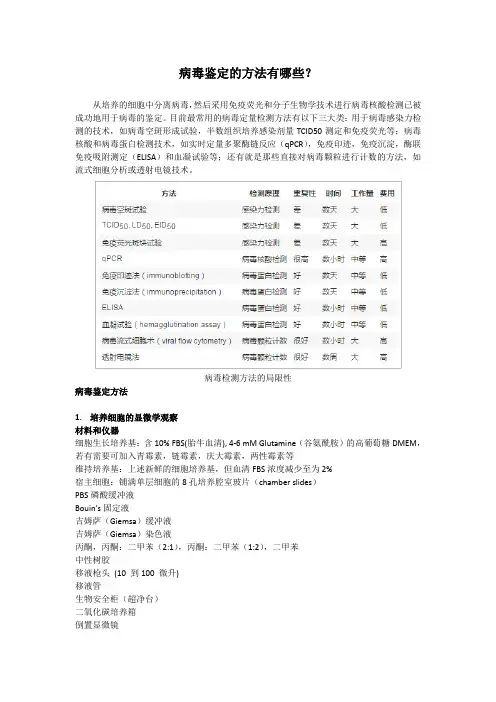
病毒鉴定的方法有哪些?从培养的细胞中分离病毒,然后采用免疫荧光和分子生物学技术进行病毒核酸检测已被成功地用于病毒的鉴定。
目前最常用的病毒定量检测方法有以下三大类:用于病毒感染力检测的技术,如病毒空斑形成试验,半数组织培养感染剂量TCID50测定和免疫荧光等;病毒核酸和病毒蛋白检测技术,如实时定量多聚酶链反应(qPCR),免疫印迹,免疫沉淀,酶联免疫吸附测定(ELISA)和血凝试验等;还有就是那些直接对病毒颗粒进行计数的方法,如流式细胞分析或透射电镜技术。
病毒检测方法的局限性病毒鉴定方法1.培养细胞的显微学观察材料和仪器细胞生长培养基:含10% FBS(胎牛血清), 4-6 mM Glutamine(谷氨酰胺)的高葡萄糖DMEM,若有需要可加入青霉素,链霉素,庆大霉素,两性霉素等维持培养基:上述新鲜的细胞培养基,但血清FBS浓度减少至为2%宿主细胞:铺满单层细胞的8孔培养腔室玻片(chamber slides)PBS磷酸缓冲液Bouin's固定液吉姆萨(Giemsa)缓冲液吉姆萨(Giemsa)染色液丙酮,丙酮:二甲苯(2:1),丙酮:二甲苯(1:2),二甲苯中性树胶移液枪头(10 到100 微升)移液管生物安全柜(超净台)二氧化碳培养箱倒置显微镜实验方案接种宿主细胞至Chamber Slides:选择合适的细胞接种密度(比如8-孔Chamber Slides,接种30,000细胞/孔),培养基为细胞生长培养基(10%FBS-DMEM)。
轻轻地前后左右摇晃chamber slides使细胞分布均匀。
将细胞置培养箱培养过夜,第二天,显微镜下观察细胞确认细胞是否分布均匀并达到80%以上的融合度。
制备不同稀释度的病毒液:标记6支无菌离心管,第1管加入990 μl细胞生长培养基,剩下5管加入900μl细胞生长培养基。
按以下方法进行梯度稀释:在第1管中加入10 μl 病毒原液(稀释度1:100)充分混匀,然后从第1管吸100 μl至第2管中混匀,依次类推,进行10倍梯度稀释。

病毒的分离与鉴定病毒是一类微小的病原体,其特点是不能自主繁殖,必须寄生在宿主细胞内才能完成复制过程。
为了有效地控制和治疗病毒引起的疾病,研究人员需要对病毒进行分离和鉴定。
本文将介绍病毒的分离与鉴定的方法和步骤。
一、病毒的分离方法1. 细胞培养法:病毒通常寄生于宿主细胞内,通过培养宿主细胞,可以将病毒从样本中分离出来。
这种方法适用于许多病毒,如流感病毒、乙肝病毒等。
2. 动物接种法:某些病毒只能在特定宿主动物中复制,通过向实验动物接种疾病样本,可以使病毒复制并分离出来。
例如,用小鼠进行实验可以分离出小鼠肝炎病毒等。
3. 组织切片法:对于某些病毒,它们会引起组织的明显病变,此时可以取得感染组织的切片进行病毒分离。
例如,用患病动物的脑组织切片进行病毒分离,可用于研究狂犬病病毒等。
二、病毒的鉴定方法1. 电镜观察法:电子显微镜(TEM)可以观察到病毒的形态和结构特征,通过观察病毒的颗粒形状、大小、壳结构等特征,可以初步确定病毒的种类。
2. 免疫学方法:根据病毒与宿主细胞之间的免疫反应,可以采用免疫学方法进行病毒鉴定。
包括免疫荧光法、酶联免疫吸附试验(ELISA)等,可以检测病毒的抗原或抗体存在。
3. 分子生物学方法:利用PCR(聚合酶链式反应)技术、序列分析等分子生物学方法,可以对病毒的基因组进行检测和鉴定。
这些方法对于那些无法用传统手段鉴定的病毒,如新型冠状病毒等,具有重要意义。
4. 勒芒氏法:这是一种用于病毒核酸的立体构建鉴定方法。
勒芒氏法根据病毒核酸在Denhardt液中染色的不同程度进行鉴定。
在进行病毒的分离与鉴定时,研究人员需要注意采取适当的实验室安全措施,避免交叉感染和意外暴露。
此外,病毒的分离与鉴定是一个复杂的科研过程,需要综合运用各种实验技术和方法,推动疾病防控工作的进展。
总结起来,病毒的分离与鉴定是关键的实验工作,它们为了研究病毒的性质、传播途径以及寻找有效的防治策略提供了基础性的支持。

自然环境中常见病毒的分离与鉴定随着科技的发展,人们对于自然环境中常见的病毒进行研究的需求也越来越高,因为一旦这些病毒被暴露出来并对人类造成危害,便会对社会和人类的健康带来重大的影响。
因此,对这些病毒进行分离和鉴定便成为了一项重要的研究工作。
一、病毒的分离如何将病毒从自然环境样品中分离出来是病毒学研究的一个难点,因为病毒具有很小的尺寸,同时活性和稳定性也很低。
常见的病毒分离方法包括通过细胞培养法、动物实验、PCR和免疫学检测等手段。
1、细胞培养法细胞培养法是常用的病毒分离方法之一,其原理是将携带病毒的样品接种到适合的细胞上培养,经过一段时间后,根据细胞死亡或出现病变的情况来判断是否存在病毒的感染。
但是,这种方法需要适宜的培养条件以及消耗很长时间,对于一些病毒来说不是很适用。
2、动物实验动物实验是比较可靠的病毒分离方法,其原理是将携带病毒的样品接种到动物体内,通过观察动物的症状、组织病变以及病原体分离和鉴定等指标来确认是否存在病毒感染。
然而,这种方法存在伦理和操作等方面的限制,不适用于所有病毒的分离。
3、 PCRPCR是一种用于扩增病毒DNA或RNA的技术,其原理是利用引物特异性酶切靶标DNA或RNA,通过不断进行反复循环来扩增病毒的核酸,从而达到病毒检测的目的。
但是,PCR技术存在一定的假阳性和假阴性的风险,需要注意检测结果的准确性。
4、免疫学检测免疫学检测是通过检测病毒的抗原或抗体来确认病毒是否存在的方法。
这种方法的优点是具有灵敏度高、速度快、成本低等特点,但是其针对病毒抗原或抗体的特异性要求也比较高,需要对病毒样品进行精确的处理和筛选。
二、病毒的鉴定病毒鉴定的目的是要对分离出来的病毒进行分类、鉴别和确定病毒株的特征,从而为病毒研究和疫苗设计提供依据。
常见的病毒鉴定方法包括电镜、免疫电镜、PCR、序列分析等。
1、电镜电镜是病毒鉴定的重要手段之一,其原理是利用高电压下加速电子的运动,从而通过对病毒粒子的形态和结构特征进行观察和比对,从而确定病毒属、种和型等分类信息。
微生物学中的病原体鉴定方法病原体是指能引起疾病的微生物,包括细菌、病毒、真菌、寄生虫等,这些病原体的有效鉴定对于疾病的诊断、预防和治疗具有非常重要的意义。
本文将从细菌、病毒和真菌三个角度,介绍微生物学中的病原体鉴定方法。
一、细菌的鉴定方法在细菌的鉴定过程中,主要涉及菌落形态、生理和生化反应、抗生素敏感性等方面的检测。
1. 菌落形态观察法菌落形态观察法是识别和鉴定细菌的传统方法。
通过观察菌落的形态、大小、密度、色泽、透明度等特征来判断菌种的种类。
2. 生理和生化反应法细菌的生长需求、代谢产物和特有的生物学变化都可以用来鉴定菌株的种类。
这些生理生化反应测试包括碳源利用能力、氧气需求、滴虫试验、酸碱度,氧化/发酵测试,酵母浸出液(urease)、氧化酶和嗜热水解酶等不同试验。
3. 抗生素敏感性测试抗生素敏感性测试可以检测不同菌株对抗生素的响应,来确定特定抗生素在抗菌疗法中的实际应用,包括纸片扩散法、微量肠道溶菌素试验(MIC)、抑菌浓度梯度测定等方法。
二、病毒的鉴定方法虽然病毒之间的差异在微观上很大,但从体积和复制机理上看,它们都是非常相似的。
因此,病毒的鉴定更限制于其在寄主细胞中的复制并累积反应。
1. 细胞培养法病毒检验的传统方法之一是细胞培养法。
通过在不同的细胞培养基中培养病毒来检测病毒的存在。
细胞培养法的优点是对样品的极少要求和相对便宜的成本。
2. 免疫学检测法免疫学检测法作为病毒鉴定的一种有效方法,包括免疫荧光法、免疫酶标记技术(ELISA)和放射性免疫测定技术(RIA)。
免疫学检测法基于免疫学反应的原理,将样品内的病毒和抗原或抗体结合,并在试剂盒中定性或定量鉴定病毒的存在。
3. 分子生物学检测法PCR技术和巢式PCR技术(nest PCR)是两种病毒检测领域中常用的分子生物学技术。
PCR基于病毒核酸的产生进行鉴定。
巢式PCR技术可以提高PCR反应的灵敏度和特异性。
三、真菌的鉴定方法真菌鉴定主要基于其菌落形态、生理和生化特性、分子生物学特性等方面进行检测。
病原微生物检测方法病原微生物是指能引起疾病的微生物,包括细菌、病毒、真菌和寄生虫等。
准确快速地检测和鉴定病原微生物对于疾病的预防、诊断和治疗具有重要意义。
随着科技的发展,病原微生物检测方法也在不断更新和改进。
一、传统的病原微生物检测方法1. 细菌检测:传统的细菌检测方法包括细菌培养和形态学观察。
细菌培养是将样品接种在含有适宜营养物质的培养基上,利用培养条件培养出细菌。
形态学观察则是通过显微镜观察细菌的形态和结构特征。
这种方法需要较长的时间,且存在一定的局限性,如对于难以培养的细菌或细菌数量很少的样品,检测结果可能不准确。
2. 病毒检测:传统的病毒检测方法主要包括电镜观察和病毒培养。
电镜观察是通过电子显微镜观察病毒的形态和结构特征。
病毒培养则是将样品接种在适宜的细胞培养基上,利用细胞培养条件培养出病毒。
这些方法需要较长的时间,且对设备和技术要求较高。
3. 真菌检测:传统的真菌检测方法包括真菌培养和形态学观察。
真菌培养是将样品接种在含有适宜营养物质的培养基上,利用培养条件培养出真菌。
形态学观察则是通过显微镜观察真菌的形态和结构特征。
这种方法需要较长的时间,且对于某些真菌的鉴定存在困难。
4. 寄生虫检测:传统的寄生虫检测方法主要包括显微镜检查和血液检测。
显微镜检查是通过显微镜观察寄生虫的形态和结构特征。
血液检测是通过检测患者的血液中是否存在寄生虫的相关抗体或遗传物质。
这些方法需要专业技术和设备支持,且有一定的局限性。
二、现代的病原微生物检测方法1. 分子生物学方法:分子生物学方法是一种快速、准确的病原微生物检测方法。
其中,PCR(聚合酶链反应)技术可以通过扩增病原微生物的特定基因序列来检测和鉴定病原微生物。
这种方法具有高灵敏度和特异性,且能够快速得到结果。
此外,还有实时荧光定量PCR和循环扩增反应等技术,可以进一步提高检测的灵敏度和准确性。
2. 免疫学方法:免疫学方法是通过检测病原微生物与宿主免疫系统的相互作用来进行检测和鉴定。
病毒学研究的方法和技术病毒学是研究病毒的学科,主要关注病毒的生物学特性、分类、传播和致病机制。
病毒学的研究方法和技术种类繁多,本文将按照其研究方向和用途进行介绍。
一、病毒分类和鉴定方法病毒分类是研究病毒的基础,也是为寻找针对特定病毒的治疗手段提供重要依据。
常用的病毒分类方法包括形态学分类、生物物理化学分类、分子生物学分类等。
其中最具代表性的是分子生物学分类方法。
该方法通过对病毒遗传物质的DNA或RNA序列进行分析,建立起了病毒系统发育树,依依分类病毒,如爱滋病病毒(HIV)、流感病毒等。
利用PCR扩增技术可以快速鉴定出病毒特异性DNA/RNA序列,为病毒的快速检测和鉴定提供了重要的技术支持。
二、病毒核酸和蛋白质的分离与分析方法分离和分析病毒核酸和蛋白质是研究病毒基因组和蛋白质组成为了进一步探究病毒的生物学特性和致病机制。
常用的方法包括电泳分离、质谱分析、荧光定量PCR等。
其中,电泳分离技术被广泛应用。
根据不同的电泳方式,电泳分离技术可以分为凝胶电泳、毛细管电泳和微流管电泳等。
凝胶电泳主要用于分离病毒核酸和蛋白质;毛细管电泳主要用于分析病毒核酸序列;微流管电泳则可在微量样品中分离和分析病毒核酸和蛋白质。
质谱分析技术主要用于检测病毒蛋白质的质量、结构、组成,提供理论支持和新的治疗靶标;荧光定量PCR则是目前病毒检测中最常用的一种快速检测技术,尤其适用于新型冠状病毒检测。
三、病毒培养和检测方法病毒培养技术是研究病毒生长和复制规律的基础。
通过极端条件下的体外培养,可以从体外获得大量相同的病毒实验体,实现对病毒生物学特性的深入分析以及寻找针对特定病毒的治疗手段的研发。
病毒的检测技术主要分为传统检测和分子检测两大类。
传统检测方法包括免疫荧光技术(IFA)、酶联免疫吸附试验(ELISA)等,主要基于病毒特异性蛋白质或其他病毒成分的检测;分子检测技术则主要利用PCR方法,检测病毒特异性DNA或RNA序列,如RT-PCR、LAMP等。
病毒植物的鉴定方法有哪些病毒在植物界中是一种常见病害,能够给农作物的产量和质量带来严重影响。
因此,及早准确地鉴定病毒植物是一项重要的工作。
下面将介绍几种常用的病毒植物鉴定方法。
观察症状法观察病变症状是最常见的病毒鉴定方法之一。
通过观察植物叶片、茎部或果实出现的病变症状,如叶片弯曲、颜色改变、疮痂等,可以初步判断植物是否感染了病毒。
但这种方法只能做出初步判断,不能确定具体的病毒种类。
检测病毒RNA法利用分子生物学技术,如逆转录聚合酶链式反应(RT-PCR)和多重逆转录聚合酶链式反应(RT-qPCR),可以检测植物体内是否存在病毒RNA。
通过比对已知的病毒序列,可以确定感染的具体病毒种类,这种方法准确性较高。
酶联免疫吸附试验法酶联免疫吸附试验(ELISA)是一种常用的病毒鉴定方法。
该方法通过使用特异性的抗体来检测植物体内的病毒抗原,从而确定是否感染了特定的病毒。
ELISA 方法快速、简便,广泛应用于病毒鉴定领域。
电子显微镜观察法电子显微镜观察是一种直接观察病毒颗粒的方法,通过该方法可以清晰地观察到病毒在植物细胞内的形态特征,从而确定植物是否感染了病毒。
虽然这种方法需要昂贵的设备和专业的技术,但是对于一些病毒形态较为特殊的情况非常有效。
检测病毒蛋白法有些病毒感染植物后会在其体内表达一些病毒特异性的蛋白,利用这些蛋白可以进行病毒的鉴定。
常用的方法包括Western blot和免疫荧光法等。
这些方法对于特定的病毒鉴定具有很高的准确性。
综上所述,病毒植物的鉴定方法包括观察症状法、检测病毒RNA法、酶联免疫吸附试验法、电子显微镜观察法和检测病毒蛋白法等多种方式。
在实际工作中,可以根据情况选择合适的鉴定方法,以确保病毒植物的及时诊断和治疗。
植物病毒的主要检测方法植物病毒是一种对农作物和植物造成严重危害的病原体,因此及时准确地检测植物病毒对于保障农作物生产的健康至关重要。
现代生物技术的发展为植物病毒的检测提供了更多更精准的方法。
以下将介绍几种主要的植物病毒检测方法:1. 核酸检测法核酸检测法是目前应用最广泛的植物病毒检测方法之一。
通过提取植物组织中的核酸,利用PCR(聚合酶链式反应)技术扩增目标病毒的特定序列,然后进行电泳分析或基因测序,从而确定是否存在目标病毒。
核酸检测法具有高灵敏度和特异性,能够准确快速地对植物病毒进行检测。
2. ELISA法ELISA(酶联免疫吸附试验)是一种常用的免疫学检测方法,也被广泛应用于植物病毒的检测。
ELISA法通过将植物提取物或纯化的病毒蛋白等与特定抗体结合,再通过酶标记的二抗对检测结果进行信号增强,最终通过颜色变化等方式进行病毒的检测和鉴定。
ELISA法操作简便,且可以同时检测多个病毒。
3. 样品接种法样品接种法是一种传统的植物病毒检测方法,通常用于对植物病毒进行初步筛选或确认。
将待检测样品接种在对病毒易感染的植物上,观察接种植物是否出现症状,并通过传统的病毒学鉴定方法确认病毒的存在。
虽然样品接种法操作简单,但对病毒的检测灵敏度相对较低。
4. 蛋白质检测法蛋白质检测法通过检测植物组织中的病毒蛋白来确定病毒的存在与否。
常用的蛋白质检测方法包括免疫印迹法(Western blot)和质谱法等。
这些方法通过检测植物组织或病毒颗粒中特定的蛋白质结构来准确鉴定植物病毒的种类和数量。
结语植物病毒的及时检测对于预防和控制病毒病害具有重要意义。
以上介绍的几种主要植物病毒检测方法各有优势和局限性,可以根据具体的实验需求选择合适的方法进行检测。
未来随着科技的不断发展,植物病毒的检测方法也将不断更新和完善,为植物病毒防控工作提供更多更好的技术支持。
病毒鉴定的方法有哪些?
从培养的细胞中分离病毒,然后采用免疫荧光和分子生物学技术进行病毒核酸检测已被成功地用于病毒的鉴定。
目前最常用的病毒定量检测方法有以下三大类:用于病毒感染力检测的技术,如病毒空斑形成试验,半数组织培养感染剂量TCID50测定和免疫荧光等;病毒核酸和病毒蛋白检测技术,如实时定量多聚酶链反应(qPCR),免疫印迹,免疫沉淀,酶联免疫吸附测定(ELISA)和血凝试验等;还有就是那些直接对病毒颗粒进行计数的方法,如流式细胞分析或透射电镜技术。
病毒检测方法的局限性
病毒鉴定方法
1.培养细胞的显微学观察
材料和仪器
细胞生长培养基:含10% FBS(胎牛血清), 4-6 mM Glutamine(谷氨酰胺)的高葡萄糖DMEM,若有需要可加入青霉素,链霉素,庆大霉素,两性霉素等
维持培养基:上述新鲜的细胞培养基,但血清FBS浓度减少至为2%
宿主细胞:铺满单层细胞的8孔培养腔室玻片(chamber slides)
PBS磷酸缓冲液
Bouin's固定液
吉姆萨(Giemsa)缓冲液
吉姆萨(Giemsa)染色液
丙酮,丙酮:二甲苯(2:1),丙酮:二甲苯(1:2),二甲苯
中性树胶
移液枪头(10 到100 微升)
移液管
生物安全柜(超净台)
二氧化碳培养箱
倒置显微镜
实验方案
接种宿主细胞至Chamber Slides:选择合适的细胞接种密度(比如8-孔Chamber Slides,接种30,000细胞/孔),培养基为细胞生长培养基(10%FBS-DMEM)。
轻轻地前后左右摇晃chamber slides使细胞分布均匀。
将细胞置培养箱培养过夜,第二天,显微镜下观察细胞确认细胞是否分布均匀并达到80%以上的融合度。
制备不同稀释度的病毒液:标记6支无菌离心管,第1管加入990 μl细胞生长培养基,剩下5管加入900μl细胞生长培养基。
按以下方法进行梯度稀释:在第1管中加入10 μl病毒原液(稀释度1:100)充分混匀,然后从第1管吸100 μl至第2管中混匀,依次类推,进行10倍梯度稀释。
管1至管6的稀释度分别为10-3 到10-7。
感染细胞:吸去培养孔中的培养液,每孔加入0.5 mL维持培养液(2%FBS-DMEM),再加入100 μl不同稀释度(10-2 至10-7稀释)的病毒液至其中一孔,留一孔不加作为空白对照。
将细胞置二氧化碳培养箱37oC 或34oC 培养1-4周,追踪观察致细胞病变效应(CPE)发生情况。
吉姆萨染色:一旦观察到细胞病变效应,轻轻地用PBS将细胞洗3次,每次5min,然后加入Bouin's固定液固定10 min。
用吉姆萨缓冲液洗3次,然和加入Giemsa染液染色1 h,再用吉姆萨缓冲液清洗后依次用丙酮处理15s,2:1的丙酮-二甲苯处理30s,1:2的丙酮-二甲苯处理30s,最后用二甲苯处理10 min紧接着用中性树胶封片。
显微镜下观察CPE,包涵体,细胞融合及病毒空泡形成情况。
病毒感染细胞后形成的CPE图片范例可以在很多图谱,网站和博客上找到,例如ASM Microbe Library
2.免疫荧光(IF)检测方法
材料和仪器
细胞生长培养基:含10%FBS(胎牛血清), 4-6mM Glutamine(谷氨酰胺)的高葡萄糖DMEM,若有需要可加入青霉素,链霉素,庆大霉素,两性霉素等
宿主细胞:铺满单层细胞的8孔培养腔室玻片(chamber slides)
PBS磷酸缓冲液
一抗
FITC标记的二抗
细胞核染料DAPI
5-4 %多聚甲醛(PFA,pH7.4),或者甲醇
移液枪头(10 到100 微升)
离心管
生物安全柜(超净台)
二氧化碳培养箱
荧光显微镜
实验方案
接种宿主细胞至Chamber Slides:选择合适的细胞接种密度(比如8-孔Chamber Slides,接种30,000细胞/孔),培养基为细胞生长培养基(10%FBS-DMEM)。
轻轻地前后左右摇晃chamber slides使细胞分布均匀。
将细胞置培养箱培养过夜,第二天,显微镜下观察细胞确认细胞是否分布均匀并达到80%以上的融合度。
病毒感染:每孔细胞加0.1 mL病毒储存液,留一孔不加作为阴性对照。
将细胞放回CO2 培养箱,37°C 或34°C 培养48h。
免疫荧光染色观察:病毒感染48h后,吸去培养液,将细胞用预冷的甲醇固定5min(也可用新鲜制备的4%多聚甲醛固定)后,用含0.2% triton X的PBS室温破膜5min。
将细胞用PBS清洗后,加入推荐浓度的一抗孵育2h,PBS清洗5遍,然后再加入荧光(Alexa fluor 488 或FITC)标记的二抗进行孵育,PBS清洗5遍,加入DAPI染细胞核,在相差及荧光显微镜下观察结果。
3.分子学方法
用实时定量逆转录PCR(Real-time RT-PCR)来检测流感病毒比终点检测方法更为快捷,且敏感度跟细胞培养法相当甚至更佳
用分子技术从临床样本中直接对病毒基因组进行鉴定是21世纪的重大发现之一。
核酸扩增技术包括PCR、基于核酸序列的扩增(NASBA)和劳伦斯利弗莫尔微生物检测阵列(LMDA)等都无疑是快速检测和鉴定大多数已知人类病毒的领先技术。
PCR可以在体外将DNA序列的一段特定区域扩增106倍,因此是一种极其敏感的检测手段。
PCR还可以用于病毒RNA 的鉴定,只需先将RNA逆转录成DNA,然后再进行PCR分析,这一方法被称之为逆转录PCR (RT-PCR)。
采用特异性的引物鉴定甲型流感病毒。
M:Marker,阳性对照(+),阴性对照(-),泳道
1-10为扩增的212 bp甲型流感病毒片段
用实时定量逆转录PCR(Real-time RT-PCR)来检测流感病毒比终点检测方法更为快捷,且敏感度跟细胞培养法相当甚至更佳
Real-time PCR实验原理图。