碱金属助剂对Au-Pt_CeO2催化剂催化水煤气变换反应活性的影响
- 格式:pdf
- 大小:340.94 KB
- 文档页数:6

碱金属碱土金属对神府煤焦气化活性的影响樊文克;崔童敏;李宏俊;常清华;郭庆华;于广锁;王辅臣【摘要】利用热重法和X射线衍射法,研究了神府煤热解焦CO2气化过程中,碱金属碱土金属( AAEM)催化剂对气化活性和微晶结构的影响。
比较了负载方式(先热解后负载和先负载后热解)、催化剂种类( Na、K、Ca)以及催化剂添加量(金属原子质量分数1%、3%、5%)的影响。
结果表明,对碱金属催化剂,先热解后负载焦样的反应活性比先负载后热解的更好,而碱土金属负载方式对活性的影响则相反;Na和K的催化能力相接近,且两者都比Ca强;煤焦气化活性随AAEM负载量的增加而增强。
负载AAEM催化剂均能抑制煤焦石墨化进程,其中,K的抑制作用最强,Ca的抑制作用最弱;抑制作用随添加量增加而增强。
%The gasification reactivity and crystallite structure of Shenfu char were measured via thermogravimetric analysis ( TGA) and X-ray diffraction technology ( XRD) to investigate the catalytic effect of AAEM during CO2 gasification. The interest was focused on effects of loading method ( pyrolysis before loading or pyrolysis after loading) , catalyst species ( Na, K, Ca) and loading amount (1%, 3%, 5% on metal atom) . For Na and K, the reactivity of char pyrolyzed before loading catalyst is better than that pyrolyzed after loading. The order of catalytic efficiency is Na~K>Ca. In addition, catalytic efficiency of AAEM catalyst increases with the increasing of loading amount. Catalyst addition inhibits the progress of char graphitizing during pyrolysis. The order of inhibition is K>Na>Ca, and the inhibition is enhanced with the increase of loading amount.【期刊名称】《燃料化学学报》【年(卷),期】2016(044)008【总页数】7页(P897-903)【关键词】催化气化;AAEM;负载方式;气化活性;微晶结构【作者】樊文克;崔童敏;李宏俊;常清华;郭庆华;于广锁;王辅臣【作者单位】华东理工大学煤气化及能源化工教育部重点实验室,上海 200237; 煤基能源化工协同创新中心,上海 200237;华东理工大学煤气化及能源化工教育部重点实验室,上海 200237; 煤基能源化工协同创新中心,上海 200237;华东理工大学煤气化及能源化工教育部重点实验室,上海 200237; 煤基能源化工协同创新中心,上海 200237;华东理工大学煤气化及能源化工教育部重点实验室,上海200237; 煤基能源化工协同创新中心,上海 200237;华东理工大学煤气化及能源化工教育部重点实验室,上海 200237; 煤基能源化工协同创新中心,上海200237;华东理工大学煤气化及能源化工教育部重点实验室,上海 200237; 煤基能源化工协同创新中心,上海 200237;华东理工大学煤气化及能源化工教育部重点实验室,上海 200237; 煤基能源化工协同创新中心,上海 200237【正文语种】中文【中图分类】TQ541煤气化技术是煤炭清洁高效转化的核心技术,是发展整体气化联合循环发电(IGCC)及煤基多联产、制氢、燃料电池等新的煤炭清洁转化系统的基础[1,2]。

助剂CeO2对CoAl2O3催化剂上F-T合成反应性能的影响
助剂CeO2对Co/Al2O3催化剂上F-T合成反应性能的影响
在用于F-T合成的Co/Al2O3催化剂中加入少量助剂,能够提高CO 转化率和C5+烃选择性.主要考察了助剂CeO2添加量和催化剂焙烧温度等因素对F-T合成反应的影响,并通过程序升温还原、程序升温氧化及X射线衍射等手段对催化剂进行了表征.结果表明,在Co/Al2O3催化剂中加入少量CeO2(n(Ce)/n(Co)=0.1~0.14),能够有效提高催化剂的催化活性和C5+烃选择性;焙烧温度则以相反的趋势控制F-T反应活性和链增长几率;助剂的加入降低了催化剂的起始还原温度,改善了催化剂的还原性能.但是,催化剂的积碳量有所增加,经10h反应后,催化剂上存在两种类型的积碳.
作者:代小平余长春沈师孔作者单位:石油大学(北京)中国石油天然气集团公司催化重点实验室, 北京102249 刊名:催化学报 ISTIC SCI PKU英文刊名:CHINESE JOURNAL OF CATALYSIS 年,卷(期):2001 22(2) 分类号:O643 关键词:费-托合成二氧化铈钴催化剂氧化铝程序升温还原程序升温氧化积碳。

碱金属催化剂碱金属催化剂是一类在化学反应中起催化作用的重要物质。
碱金属催化剂具有高活性、高选择性和良好的稳定性等特点,在有机合成、能源转化和环境保护等领域发挥着重要作用。
碱金属催化剂在有机合成中具有广泛的应用。
有机合成是一种重要的化学领域,用于合成各种有机化合物。
碱金属催化剂可以催化有机反应,提高反应速率和产率。
例如,碱金属催化剂可以催化醇与醛或酮的缩合反应,生成醚化合物。
此外,碱金属催化剂还可以催化酯的加成反应、烯烃的氢化反应等。
这些反应在医药、农药、香料等化学领域具有重要应用价值。
碱金属催化剂在能源转化中也发挥着重要作用。
能源转化是指将一种形式的能源转化为另一种形式的能源,如化学能转化为电能、光能或热能。
碱金属催化剂可以催化燃料电池中的氧还原反应,提高电池的能量转化效率。
此外,碱金属催化剂还可以催化氢气的生成和氧化反应,促进氢能的利用。
碱金属催化剂在能源领域的应用有助于提高能源利用效率,减少能源消耗和环境污染。
碱金属催化剂在环境保护中也起到了积极的作用。
环境保护是指保护和改善环境质量,维护生态平衡,促进可持续发展。
碱金属催化剂可以催化废水中有机物的降解和氧化反应,净化废水中的有害物质。
同时,碱金属催化剂还可以催化废气中有害气体的转化和去除,减少大气污染物的排放。
碱金属催化剂在环境保护领域的应用有助于改善环境质量,保护生态环境。
碱金属催化剂是一类重要的催化剂,具有广泛的应用前景。
在有机合成、能源转化和环境保护等领域,碱金属催化剂发挥着重要作用。
通过催化反应,碱金属催化剂可以提高反应速率和产率,促进化学反应的进行。
同时,碱金属催化剂具有高选择性和稳定性,可以在复杂的化学环境中发挥作用。
未来的研究应进一步深化对碱金属催化剂的理解,开发新型催化剂,提高催化效率和选择性,推动碱金属催化剂在化学工业和环境保护中的应用。


AuCeO2催化剂的制备及其对CO催化氧化性能的研究
Au/CeO2催化剂的制备及其对CO催化氧化性能的研究
采用水溶液沉淀法和沉积-沉淀法分别制备了CeO2载体及相应Au/CeO2催化剂,以CO氧化反应为表征反应,考察了载体制备条件,催化剂的焙烧温度、预处理温度和气氛以及活性组分负载量对催化剂性能的影响,并对催化剂进行了BET、XRD和TEM表征,分析了影响催化剂活性的原因.结果表明,载体的制备条件对催化剂的活性有一定影响,经微波处理的载体负载活性组分后,由于活性组分和载体的.接触较紧密,因此有利于催化剂活性的提高.催化剂的最佳焙烧温度为300℃,最佳活化温度为300℃,气氛为空气,最佳金负载量为4%.
作者:海锋李彦锋白风荣萨嘎拉召日格照日格图贾美林 HAI feng LI Yan-feng BAI Feng-rong SAGALA ZHAORIGE ZHAORIGETU JIA Mei-lin 作者单位:海锋,HAI feng(内蒙古师范大学,化学与环境科学学院,内蒙古,呼和浩特,010022;兰州大学,化学化工学院,甘肃,兰州,730000)
李彦锋,LI Yan-feng(兰州大学,化学化工学院,甘肃,兰州,730000)
白风荣,BAI Feng-rong(内蒙古工业大学,化工学院,内蒙古,呼和浩特,010051)
萨嘎拉,召日格,照日格图,贾美林,SAGALA,ZHAORIGE,ZHAORIGETU,JIA Mei-lin(内蒙古师范大学,化学与环境科学学院,内蒙古,呼和浩特,010022)
刊名:分子催化ISTIC PKU 英文刊名:JOURNAL OF MOLECULAR CATALYSIS(CHINA) 年,卷(期): 2007 21(4) 分类号:O643.3 关键词:金催化剂 CeO2 CO催化氧化。
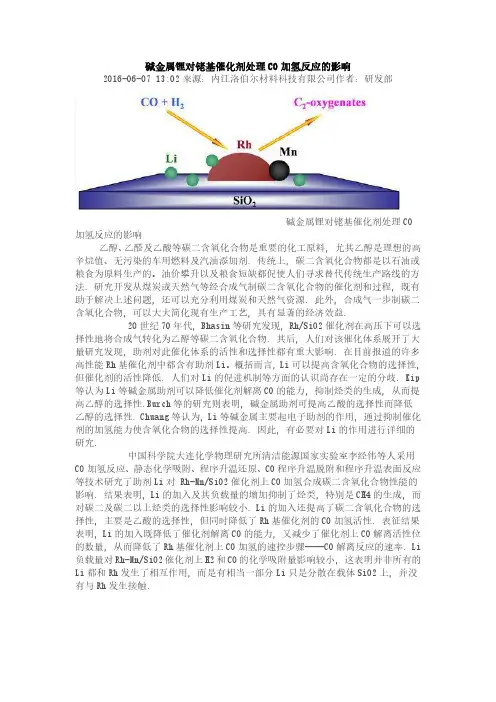
碱金属锂对铑基催化剂处理CO加氢反应的影响2016-06-07 13:02来源:内江洛伯尔材料科技有限公司作者:研发部碱金属锂对铑基催化剂处理CO加氢反应的影响乙醇、乙醛及乙酸等碳二含氧化合物是重要的化工原料, 尤其乙醇是理想的高辛烷值、无污染的车用燃料及汽油添加剂. 传统上, 碳二含氧化合物都是以石油或粮食为原料生产的。
油价攀升以及粮食短缺都促使人们寻求替代传统生产路线的方法. 研究开发从煤炭或天然气等经合成气制碳二含氧化合物的催化剂和过程, 既有助于解决上述问题, 还可以充分利用煤炭和天然气资源. 此外, 合成气一步制碳二含氧化合物, 可以大大简化现有生产工艺, 具有显著的经济效益.20世纪70年代, Bhasin等研究发现, Rh/SiO2催化剂在高压下可以选择性地将合成气转化为乙醇等碳二含氧化合物. 其后, 人们对该催化体系展开了大量研究发现, 助剂对此催化体系的活性和选择性都有重大影响. 在目前报道的许多高性能Rh基催化剂中都含有助剂Li。
概括而言, Li可以提高含氧化合物的选择性, 但催化剂的活性降低. 人们对Li的促进机制等方面的认识尚存在一定的分歧. Kip 等认为Li等碱金属助剂可以降低催化剂解离CO的能力, 抑制烃类的生成, 从而提高乙醇的选择性.Burch等的研究则表明, 碱金属助剂可提高乙酸的选择性而降低乙醇的选择性. Chuang等认为, Li等碱金属主要起电子助剂的作用, 通过抑制催化剂的加氢能力使含氧化合物的选择性提高. 因此, 有必要对Li的作用进行详细的研究.中国科学院大连化学物理研究所清洁能源国家实验室李经伟等人采用CO加氢反应、静态化学吸附、程序升温还原、CO程序升温脱附和程序升温表面反应等技术研究了助剂Li对 Rh-Mn/SiO2催化剂上CO加氢合成碳二含氧化合物性能的影响. 结果表明, Li的加入及其负载量的增加抑制了烃类, 特别是CH4的生成, 而对碳二及碳二以上烃类的选择性影响较小. Li的加入还提高了碳二含氧化合物的选择性, 主要是乙酸的选择性, 但同时降低了Rh基催化剂的CO加氢活性. 表征结果表明, Li的加入既降低了催化剂解离CO的能力, 又减少了催化剂上CO解离活性位的数量, 从而降低了Rh基催化剂上CO加氢的速控步骤——CO解离反应的速率. Li 负载量对Rh-Mn/SiO2催化剂上H2和CO的化学吸附量影响较小, 这表明并非所有的Li都和Rh发生了相互作用, 而是有相当一部分Li只是分散在载体SiO2上, 并没有与Rh发生接触.。

化工进展Chemical Industry and Engineering Progress2023 年第 42 卷第 3 期逆水煤气变换反应研究进展王晓月,张伟敏,姚正阳,郭晓宏,李聪明(太原理工大学省部共建煤基能源清洁高效利用国家重点实验室,山西 太原 030024)摘要:逆水煤气变换(RWGS )反应是将二氧化碳(CO 2)加氢转化为甲醇、低碳烯烃、芳烃以及汽油等高附加值化学品和燃料的关键步骤,对于实现CO 2资源化利用具有重要意义。
本文综述了近年来RWGS 反应的研究进展,包括RWGS 反应热力学分析、催化机理、可选择的催化剂种类以及提升催化剂性能策略等方面。
文章从热力学角度分析,RWGS 反应在高温下有利,而低温下存在甲烷化竞争反应。
RWGS 反应机理主要包括氧化还原机理以及缔合机理,其中缔合机理包括甲酸盐路径和羧酸盐路径等。
相比于其他催化体系,负载型金属催化剂展现出较优异的RWGS 反应性能。
另外,通过添加碱金属助剂、形成双金属合金以及选择合适载体和减小金属颗粒尺寸以优化金属-载体相互作用等手段可实现低温高效稳定的RWGS 反应催化剂的设计开发。
关键词:逆水煤气变换反应;二氧化碳;一氧化碳;热力学;催化剂中图分类号:TQ073 文献标志码:A 文章编号:1000-6613(2023)03-1583-12Research progress of reverse water gas shift reactionWANG Xiaoyue ,ZHANG Weimin ,YAO Zhengyang ,GUO Xiaohong ,LI Congming(State Key Laboratory of Clean and Efficient Coal Utilization, Taiyuan University of Technology, Taiyuan 030024, Shanxi, China)Abstract: Reverse water gas conversion (RWGS) reaction is a key step in the catalytic hydrogenation ofcarbon dioxide (CO 2) to high value-added chemicals and fuels such as methanol, light olefins, aromatics and gasoline, which is of great significance for the utilization of CO 2. This review summarizes the research progress of RWGS reaction in recent years, including thermodynamic analysis of RWGS reaction, catalytic mechanisms, selective catalysts and strategies to improve the performance of catalysts. From the perspective of thermodynamics, RWGS reaction is favorable at high temperature, as methanation reaction emerges at low temperature. The mechanisms of RWGS reaction mainly consist of redox mechanism and association mechanism, and the latter further contains a formate route and/or carboxylate route. Compared with other catalyst system, supported metal catalysts commonly exhibit a superior RWGS reaction performance. In addition, the rational design of RWGS reaction catalysts with high reactivity and durability could be realized by adding alkali metal additives, forming bimetallic alloy as well as modulating the metal-support interaction via selecting a good support or reducing the metal particle size.Keywords: reverse water gas shift reaction; carbon dioxide; carbon monoxide; thermodynamics; catalyst综述与专论DOI :10.16085/j.issn.1000-6613.2022-0816收稿日期:2022-05-05;修改稿日期:2022-07-13。

逆水汽变换反应铜基催化剂研究进展吕扬平;张耀远;王瑞浦;吴芹;史大昕;陈康成;黎汉生【期刊名称】《工业催化》【年(卷),期】2024(32)5【摘要】逆水汽变换(RWGS)反应是将CO_(2)转化为化学品或碳氢化合物的关键步骤,在CO_(2)资源化利用中发挥着重要作用。
综述逆水汽变换反应的热力学分析、反应机理,以及近十年来国内外逆水汽变换反应催化剂的研究进展。
总结发现,Cu基催化剂具有低成本、高活性和高CO选择性优势。
但在反应中易积炭失活,且在高温条件下容易烧结团聚导致稳定性下降。
目前,研究者对Cu基催化剂的研究主要集中在Cu活性中心调控和优化反应操作条件两个方面。
Cu活性中心调控主要包括:①调控Cu位点的结构特性,如分散度、粒径大小等;②助剂的添加,包括碱金属助剂(Na、K)、过渡金属助剂(Fe、Ce、Co)等;③引入适宜载体,如Al_(2)O_(3)、Mo_(2)C、CeO_(2)等以增强金属-载体的相互作用。
操作工艺条件优化主要通过改变反应温度、空速、调节H_(2)/CO_(2)物质的量比增强RWGS反应中CO选择性和CO_(2)转化率。
最后指出基于RWGS反应将CO_(2)与其它产氢反应进行耦合,如低碳烷烃脱氢、甲醇芳构化等,可达到目标产物收率提升与CO_(2)减排目的。
【总页数】17页(P1-17)【作者】吕扬平;张耀远;王瑞浦;吴芹;史大昕;陈康成;黎汉生【作者单位】北京理工大学化学与化工学院;中国石油石油化工研究所【正文语种】中文【中图分类】TQ426.6;O643.36【相关文献】1.MoOx促进的Pt基催化剂用于低温水汽变换反应2.Cr基催化剂在逆水汽变换反应中的研究3.铜基低温水汽变换催化剂HF中毒热力学分析4.不同载体铜基催化剂生物质热解气低温变换反应性能研究5.铜基水汽变换催化剂NH3中毒热力学研究因版权原因,仅展示原文概要,查看原文内容请购买。

金属-载体相互作用对多相催化反应的影响王珍【摘要】多相催化反应体系中,金属催化剂与载体之间通过电荷转移、物质输运等机理产生相互作用.这种金属-载体相互作用对催化反应性能的影响具有多样性,既可以抑制或促进某个反应的发生,造成选择性的不同;也可以在反应中诱导活性中心的生成,提高反应活性,因此在实际研究中需要对特定催化体系进行充分了解,并加以有效利用.【期刊名称】《广州化工》【年(卷),期】2013(041)024【总页数】4页(P20-23)【关键词】金属-载体相互作用;SMSI;电荷转移;物质输运【作者】王珍【作者单位】神华准能资源综合开发有限公司,内蒙古鄂尔多斯010300【正文语种】中文【中图分类】O643.32+21 金属-载体相互作用 (SMSI)概念在催化科学发展的初期,催化剂载体一直被认为是惰性的,只起到支撑、分散活性组分的简单作用,不会影响到催化剂的性能。
但随着研究的深入,人们逐渐认识到,催化剂性能通常会不可避免地受到所用载体的影响[1-2]。
Tauster等[3-5]于1978年首先提出金属-载体强相互作用 (Strong Metal-Support Interaction,SMSI)的概念,他们研究了TiO2载体上负载的第八族贵金属催化剂(Pt、Pd、Ir、Ru、Rh等)对CO和H2的吸附能力,实验发现低温(473 K)氢气还原对气体吸附没有影响,而高温(>700 K)还原之后,CO和H在金属表面的吸附几乎为零,表明高温还原降低了金属对气体的吸附能力。
利用X射线衍射、电镜等测试分析,首先排除了金属烧结、载体包覆、还原不完全等因素的影响,Tauster等由此提出金属与载体之间可能存在着某种相互作用,从而在一定程度上减弱了气体的吸附。
随后,他们将此项研究拓展到十余种氧化物载体上,发现这种抑制效应在不同载体负载的金属催化剂上表现不同,在一些可被还原的氧化物载体上作用比较明显,如 TiO2、V2O5、Nb2O5和Ta2O5,而且这种吸附性能随处理温度的变化是可逆的。

碱金属助剂对MnOxZrO2催化合成甲醇及异丁醇反应性能的
影响
碱金属助剂对MnOx/ZrO2催化合成甲醇及异丁醇反应性能的影响
研究了MnOx/ZrO2催化剂中添加的碱金属助剂对以合成气合成甲醇及异丁醇反应的影响,并采用BET,XRD和NH3-TPD等表征技术,考察了碱金属助剂的添加对催化剂结构和表面性质的影响. 结果表明,碱金属助剂对MnOx/ZrO2催化剂的催化性能有明显影响. 在实验条件下,添加1.0%K(K2CO3作为前驱物)的催化剂,其催化性能最好,醇的选择性高达74.8%,异丁醇选择性达16.3%. 添加碱金属助剂也使MnOx/ZrO2催化剂的表面性质发生了很大变化,从而影响催化剂的催化性能.
作者:何代平丁云杰尹红梅王涛朱何俊作者单位:中国科学院大连化学物理研究所天然气化工与应用催化研究室,辽宁大连,116023 刊名:催化学报 ISTIC SCI PKU 英文刊名: CHINESE JOURNAL OF CATALYSIS 年,卷(期):2003 24(2) 分类号:O643 关键词:氧化锰氧化锆碱金属助剂一氧化碳加氢异丁醇甲醇。

㊀第24卷第4期洁净煤技术Vol.24㊀No.4㊀㊀2018年7月Clean Coal TechnologyJuly㊀2018㊀碱和碱土金属对气化焦气化反应性的影响武琳琳1,2,朱㊀川1,2(1.煤炭科学技术研究院有限公司煤化工分院,北京㊀100013;2.煤炭资源高效开采与洁净利用国家重点实验室,北京㊀100013)摘㊀要:碱和碱土金属是气化焦气化反应的重要催化剂,其催化效果直接影响气化焦的气化效率㊂对不同碱或碱土金属与气化焦的混合物,以及不同比例Na 2CO 3的气化焦进行气化反应,研究催化剂种类和用量对气化焦气化反应的催化效果㊂结果表明,1000ħ和1050ħ下,催化剂的催化活性顺序为:K 2CO 3>Na 2CO 3>CaCO 3;1100ħ下因催化剂高温释放以及Na 2CO 3催化活性显著提高,催化活性顺序变为:Na 2CO 3>K 2CO 3>CaCO 3㊂气化焦碳转化率由高到低为:5%Na 2CO 3>1%Na 2CO 3>2%Na 2CO 3>0.5%Na 2CO 3>无Na 2CO 3,气化焦的催化活性㊁最大反应速率和反应活性指数排序与气化焦炭转化率一致,表明催化活性并非一直随催化剂添加比例的增加而增加㊂关键词:碱金属;碱土金属;气化焦;气化;催化剂;热重分析中图分类号:TQ54㊀㊀㊀文献标志码:A㊀㊀㊀文章编号:1006-6772(2018)04-0078-06Effect of alkali and alkaline earth metal on the gasification reactivityof gasified cokeWU Linlin 1,2,ZHU Chuan 1,2(1.Coal Chemistry Branch of China Coal Research Institute ,Beijing ㊀100013,China ;2.State Key Laboratory of Coal Mining and Clean Utilization ,Beijing ㊀100013,China )Abstract :Alkali and alkaline earth metals are important catalysts for gasification reaction of gasified coke,and their catalytic effect directly affect the gasification efficiency of gasified coke.The gasification of mixtures of several alkali or alkaline earth metals with gasified coke and gasified coke with different proportions of Na 2CO 3were carried out.Effect of catalyst type and dosage on catalytic effect of gasifiedcoke gasification was studied.Results show that at 1000ħand 1050ħ,the catalytic activity has the tendency of K 2CO 3>Na 2CO 3>CaCO 3,meanwhile at 1100ħ,the catalytic activity tendency changes to Na 2CO 3>K 2CO 3>CaCO 3because of high temperature release of catalyst and catalytic activity improvement of Na 2CO 3.The conversion rate of gasification coke carbon from high to bottom is 5%Na 2CO 3>1%Na 2CO 3>2%Na 2CO 3>0.5%Na 2CO 3>no Na 2CO 3.It is also found that the order of the catalytic activity,the maximum reaction rate and the reactivity index is in the same order as the conversion rate of gasified coke,which indicates that catalytic activity does not increase with the increase of addition proportion.Key words :alkali metal;alkaline earth metal;gasified coke;gasification;catalyst;thermogravimetric analysis收稿日期:2018-01-22;责任编辑:白娅娜㊀㊀DOI :10.13226/j.issn.1006-6772.18012202基金项目:国家重点研发计划资助项目(2016YFB060040201)作者简介:武琳琳(1987 ),女,山东临沂人,助理研究员,研究方向为煤质学㊁煤岩学㊂E -mail :lin500lin@ 引用格式:武琳琳,朱川.碱和碱土金属对气化焦气化反应性的影响[J].洁净煤技术,2018,24(4):78-83.WU Linlin,ZHU Chuan.Effect of alkali and alkaline earth metal on the gasification reactivity of gasified coke[J].Clean Coal Technology,2018,24(4):78-83.0㊀引㊀㊀言煤中矿物质是煤的重要组成部分,许多学者提到煤中矿物对气化的催化作用,但并非所有矿物质对煤气化反应都有催化作用[1-2]㊂一般来说,煤中碱金属㊁碱土金属及过渡金属有催化作用,而含有SiO 2和Al 2O 3等的矿物质与催化剂作用,使催化剂失活㊂Skodeas 等[3]研究表明,无机矿物质对煤气化反应起重要作用,碱金属盐在C -H 2O 和C -CO 2气化反应过程中的反应速率变化相似㊂Mckee 等[4-5]研究了在CO 2和水蒸气等不同气氛下碱金属对煤焦和石墨气化的催化作用㊂87武琳琳等:碱和碱土金属对气化焦气化反应性的影响2018年第4期Franklin等[6]发现含钙矿物质可降低焦油产率,认为钙对煤中的羟基裂解具有催化作用㊂Longwell 等[7]认为添加CaO能明显增加煤中芳香化合物的热解速率和程度㊂Jiang等[8]发现气化中钙的存在能抑制K的失活,表现协同影响促进气化反应㊂Taylor最早对煤气化催化作用进行研究,发现Na2CO3和K2CO3是煤气化反应的有效催化剂[9]㊂Yeboah等[10]对常见的碱和碱土金属催化剂活性排序:K2CO3>K2SO4>Na2CO3>CaSO4>CaCO3㊂矿物质对煤气化反应性的影响极其复杂,其活性随气化条件的变化而变化,且各矿物质之间还可能相互作用,因此要使矿物质发挥较高的催化效果,还需针对具体煤种进行大量研究㊂气化焦是低阶煤与部分黏结性烟煤混配热解后的具有一定强度的气化原料㊂由于低阶煤混配比例较高,气化焦中碱和碱土金属含量较高㊂因此通过添加碱金属和碱土金属进行气化反应研究,可认识气化焦中碱和碱土金属对气化反应的催化作用,也可通过外加催化剂进一步降低气化反应活化能,为实现低温温和条件下的气化催化反应提供理论基础㊂1㊀试㊀㊀验1.1㊀气化焦性质气化焦(QHJ-R)煤质指标见表1㊂表1㊀气化焦基本性质Table1㊀basic properties of gasified coke工业分析/%M ar M ad A d V d FC d元素分析/%C daf H daf N daf O daf S dafQ gr,d/(MJ㊃kg-1)1.501.6414.461.8083.7495.711.441.230.011.6128.53灰成分分析/%SiO2Al2O3Fe2O3TiO2CaO MgO K2O Na2O MnO2SO3P2O5 40.7828.4917.761.364.641.160.580.350.313.480.421.2㊀催化剂及样品制备本文采用的催化剂为碱和碱土金属㊂碱金属催化剂主要为Na2CO3和K2CO3;碱土金属催化剂为CaCO3㊂为考察催化剂种类对气化焦气化反应的催化效果,催化剂添加比例均为5.0%㊂气化焦添加5.0%的Na2CO3㊁K2CO3和CaCO3后分别记为QHJ-5.0Na㊁QHJ-5.0K和QHJ-5.0Ca;无催化剂记为QHJ-R㊂为考察催化剂添加比例对催化效果的影响,选择催化剂Na2CO3,添加比例分为5.0㊁2.0㊁1.0和0.5%㊂气化焦添加2.0㊁1.0和0.5%的Na2CO3后分别记为QHJ-2.0Na㊁QHJ-1.0Na和QHJ-0.5Na㊂称取一定量煤样,按添加比例称取催化剂,将其研磨充分混合㊂混合好的样品置入80ħ干燥箱干燥4h,待用㊂1.3㊀气化试验采用德国Netsch公司生产的STA449F3型DSC/TG同步热分析仪进行恒温法气化反应㊂称量(30ʃ1)mg粒度<0.2mm的样品(原煤焦或负载催化剂的煤焦),均匀平铺于平盘坩埚上,在流量100mL/min的N2保护下以20ħ/min升温速率从室温加热到设定温度,恒温5min后切换为100mL/min的纯CO2气氛,在设定温度下进行恒温法气化反应(时间为60min)㊂考虑煤焦与纯CO2气化反应的速率和效率,分别在1000㊁1050和1100ħ下测试气化反应的TG-DTG曲线㊂1.4㊀气化特征参数1)气化转化率及反应速率转化率α为反应的物质质量除以物质总质量,%㊂气化反应速率rᶄ表示转化率随时间的变化率,%/min㊂α和rᶄ公式为α=m0-mm0-m eˑ100%(1)rᶄ=dαd t(2)式中,m0为气化反应开始时样品质量,kg;m为反应过程中任意时刻样品质量,kg;m e为样品反应完全后的质量,kg㊂2)最大气化反应速率及对应时间气化反应速率rᶄ的最大值(V m)及对应时间972018年第4期洁净煤技术第24卷(t m)可表征气化焦气化反应的快慢㊂3)气化反应性指数Takayuki等定义的反应性指数R0.5是评价含碳物质反应活性的指标[11],表示气化焦从气化反应开始到转化率达到50%的平均反应速率,具体如下:R0.5=0.5t0.5(3)式中,t0.5为煤焦转化率达到50%时所需时间,min㊂2㊀试验结果与讨论2.1㊀温度对气化焦气化反应的催化作用2.1.1㊀1000ħ下碱和碱土金属的催化作用气化焦在1000ħ下添加5.0%的Na2CO3㊁K2CO3和CaCO3等催化剂后,气化焦碳转化率及反应速率随时间变化如图1所示㊂由图1可知,相同反应时间下,气化焦碳转化率由高到低依次为:QHJ-5.0K>QHJ-5.0Na>QHJ-5.0Ca>QHJ-R;反应速率在最大反应速率后也与上述变化顺序相同㊂表明1000ħ下催化剂活性排序为:K2CO3>Na2CO3>CaCO3㊂通过图1可获得气化焦在1000ħ下的气化特征参数,具体见表2㊂图1㊀1000ħ下添加不同催化剂的气化焦碳转化率及反应速率随时间变化Fig.1㊀Gasification coke conversion and reaction rate change with time after adding different catalysts at1000ħ表2㊀1000ħ下添加不同催化剂后的气化反应特征参数Table2㊀Characteristic parameters of gasification reaction after adding different catalysts at1000ħ样品反应初始质量损失/%V m/(%㊃min-1)t m/min t0.5/min R0.5/min-1反应残余率/% QHJ-R2.534.431.2121.600.023134.68 QHJ-5.0Na5.7811.750.617.480.066823.14 QHJ-5.0K6.2419.940.414.680.106820.11 QHJ-5.0Ca3.9511.330.4110.140.049327.64㊀㊀反应初始质量损失是由于高温下煤焦热解损失㊁催化剂分解或挥发引起,而反应残余率则反映了经历60min气化反应后的反应程度㊂由表2可知,惰性气氛升温至1000ħ时,QHJ-R煤焦热解损失为2.53%;催化剂由高到低损失顺序为:K2CO3> Na2CO3>CaCO3,其中K2CO3和Na2CO3损失主要为挥发损失,CaCO3损失主要为分解损失㊂V m和R0.5变化顺序与催化剂活性相同,即活性越高的催化剂具有更大的最大反应速率和反应活性指数㊂反应残余率明显高于气化焦灰分,说明样品在1000ħ下经历60min并未完全反应㊂添加不同催化剂的气化焦反应速率随转化率变化如图2所示㊂由图2可知,反应速率随转化率的增加先增大后减小㊂QHJ-5.0Ca和QHJ-图2㊀1000ħ下添加不同催化剂的气化焦反应速率随转化率变化Fig.2㊀Reaction rate of gasification coke changes with conversion rate after adding different catalysts at1000ħ5.0Na在转化率小于5.0%时差异并不明显;转化率>5.0%时,同转化率下,QHJ-5.0Na对应的反应速率明显高于QHJ-5.0Ca㊂以50%转化率为平08武琳琳等:碱和碱土金属对气化焦气化反应性的影响2018年第4期均指标,则催化剂的催化活性排序为:K 2CO 3>Na 2CO 3>CaCO 3㊂2.1.2㊀1050ħ下碱和碱土金属的催化作用气化焦在1050ħ下添加5.0%的Na 2CO 3㊁K 2CO 3和CaCO 3催化剂后,气化焦碳转化率及反应速率随时间变化如图3所示㊂由图3可知,相同反应时间下,1050ħ气化焦碳转化率排序与1000ħ相同,为QHJ -5.0K>QHJ -5.0Na>QHJ -5.0Ca>QHJ -R,1050ħ下催化剂活性排序为:K 2CO 3>Na 2CO 3>CaCO 3㊂通过图3可获得气化焦在1050ħ下的气化反应特征参数,具体见表3㊂图3㊀1050ħ下添加不同催化剂的气化焦碳转化率及反应速率随时间变化Fig.3㊀Gasification coke conversion and reaction rate change with time after adding different catalysts at 1050ħ表3㊀1050ħ下添加不同催化剂后的气化反应特征参数Table 3㊀Characteristic parameters of gasification reaction after adding different catalysts at 1050ħ样品反应初始质量损失/%V m /(%㊃min -1)t m /min t 0.5/min R 0.5/min -1反应残余率/%QHJ -R3.319.051.08.500.058815.62QHJ -5.0Na 7.7514.670.75.430.092116.64QHJ -5.0K 5.2217.520.74.570.109415.94QHJ -5.0Ca 3.6414.670.85.600.089319.39㊀㊀由表3可知,惰性气氛升温至1050ħ时,QHJ -R 的煤焦热解损失为3.31%;催化剂由高到低损失顺序为:K 2CO 3>Na 2CO 3>CaCO 3㊂V m 和R 0.5变化顺序与催化剂活性相同,活性越高的催化剂具有更大的最大反应速率和反应活性指数㊂1050ħ下反应55min 后,样品失重率基本无变化,表明残余率是碳完全反应的残余率㊂从图3可获得添加不同催化剂的气化焦反应速率随转化率变化关系,如图4所示㊂由图4可知,气化焦反应速率随转化率的增加先增大后减小㊂QHJ -5.0Ca 和QHJ -5.0Na 的反应速率差异不明显㊂如果以50%转化率作为平均指标,则催化剂的催化活性变化排序为:K 2CO 3>Na 2CO 3>CaCO 3㊂2.1.3㊀1100ħ下碱和碱土金属的催化作用气化焦在1100ħ下添加5.0%的Na 2CO 3㊁K 2CO 3和CaCO 3等催化剂后,气化焦碳转化率及反应速率随时间变化如图5所示㊂可知,相同反应时间下,碳转化率由高到低依次为:QHJ -5.0Na>QHJ -5.0K>QHJ -5.0Ca>QHJ -R,表明1100ħ下催化剂活性排序为:Na 2CO 3>K 2CO 3>CaCO 3,与1050和1000ħ的催化活性顺序不同㊂通过图5可获得气化焦在1100ħ下的气化反应特征参数见表4㊂图4㊀1050ħ下添加不同催化剂的气化焦反应速率随转化率的变化Fig.4㊀Reaction rate of gasification coke changes withconversion rate after adding different catalysts at 1050ħ由表4可知,惰性气氛升温至1100ħ时,QHJ -R 煤焦热解损失为4.90%;催化剂由高到低损失顺序为:K 2CO 3>Na 2CO 3>CaCO 3㊂V m 和R 0.5变化顺序182018年第4期洁净煤技术第24卷与催化剂活性相同,即活性越高的催化剂具有更大的最大反应速率和反应活性指数㊂但与1050和1000ħ的催化活性顺序不同,主要因为K 2CO 3在1100ħ高温下释放率显著高于Na 2CO 3,QHJ -5.0K 的有效催化剂降低㊂1100ħ下反应50min 后,样品失重率基本无变化,表明残余率是碳完全反应的残余率㊂从图5可获得添加不同催化剂的气化焦反应速率随转化率变化关系,如图6所示㊂图5㊀1100ħ下添加不同催化剂的气化焦碳转化率及反应速率随时间变化Fig.5㊀Gasification coke conversion and reaction rate change with time after adding different catalysts at 1100ħ表4㊀1100ħ下添加不同催化剂后的气化反应特征参数Table 4㊀Characteristic parameters of gasification reaction after adding different catalysts at 1100ħ样品反应初始质量损失/%V m /(%㊃min -1)t m /min t 0.5/min R 0.5/min -1反应残余率/%QHJ -R4.9013.460.76.060.082515.81QHJ -5.0Na 7.6520.610.53.810.131213.99QHJ -5.0K 8.5120.300.34.030.124114.16QHJ -5.0Ca 6.7319.220.34.400.113615.26图6㊀1100ħ下添加不同催化剂的气化焦反应速率随转化率的变化Fig.6㊀Reaction rate of gasification coke changes withconversion rate after adding different catalysts at 1100ħ㊀㊀由图6可知,反应速率随转化率的增加先增大后减小㊂QHJ -5.0Ca 和QHJ -5.0Na 的反应速率差异不明显㊂以50%转化率作为平均指标,则催化剂的催化活性变化排序为:Na 2CO 3>K 2CO 3>CaCO 3㊂这与1050ħ结果不同,主要原因可能是1100ħ时K 2CO 3的挥发释放损失大于Na 2CO 3导致㊂2.2㊀催化剂添加量对气化焦反应的催化作用㊀㊀1050ħ下,气化焦及添加0.5%㊁1.0%㊁2.0%和5.0%的Na 2CO 3等催化剂,获得气化焦碳转化率及反应速率随时间变化,如图7所示㊂图7㊀添加不同比例催化剂的气化焦碳转化率及反应速率随时间变化Fig.7㊀Gasification coke conversion and reaction rate change with time in different catalyst addition ratios由图7可知,相同反应时间下,气化焦碳转化率由高到低依次为:QHJ -5.0Na >QHJ -1.0Na >QHJ -2.0Na>QHJ -0.5Na >QHJ -R;反应速率在最28武琳琳等:碱和碱土金属对气化焦气化反应性的影响2018年第4期大反应速率后与上述变化顺序相同㊂在气化焦活性位变化和催化剂挥发释放共同作用下,催化剂对煤焦气化反应的催化效果随添加量增加不一定呈现线性增加㊂通过图7可获得添加不同比例Na2CO3后气化焦在1050ħ下的气化特征参数,具体见表5㊂表5㊀不同比例催化剂的气化反应特征参数Table5㊀Characteristic parameters of gasification reaction in different catalyst addition ratios样品反应初始质量损失/%V m/(%㊃min-1)t m/min t0.5/min R0.5/min-1反应残余率/% QHJ-R3.319.051.08.500.058815.62 QHJ-0.5Na4.829.620.88.400.059514.18 QHJ-1.0Na5.7910.820.87.390.067714.07 QHJ-2.0Na6.699.950.98.290.060317.40 QHJ-5.0Na7.7514.670.75.430.092116.64㊀㊀由表5可知,惰性气氛升温至1050ħ时,QHJ-R显示煤焦热解损失为3.31%;催化剂由高到低损失顺序为:5.0%>1.0%>2.0%>0.5%㊂V m和R0.5变化顺序与催化剂活性相同,活性越高的催化剂具有更大的最大反应速率和反应活性指数㊂3㊀结㊀㊀论1)1000和1050ħ下,催化剂的催化活性顺序为:K2CO3>Na2CO3>CaCO3;1100ħ下因催化剂高温释放及Na2CO3的催化活性显著提高,催化活性顺序变为:Na2CO3>K2CO3>CaCO3㊂V m和R0.5变化顺序与催化剂活性相同㊂2)添加不同比例Na2CO3后,气化焦碳转化率由高到低的顺序为:QHJ-5.0Na>QHJ-1.0Na>QHJ-2.0Na>QHJ-0.5Na>QHJ-R,催化活性㊁V m和R0.5排序均为:5.0%>1.0%>2.0%>0.5%,表明催化活性不一定随催化剂添加比例线性增加㊂参考文献(References):[1]㊀朱廷钰,张守玉,黄戒介,等.氧化钙对流化床煤温和气化半焦性质的影响[J].燃料化学学报,2000,28(1):40-43.ZHU Tingyu,ZHANG Shouyu,HUANG Jiejie,et al.Effect of CaO on the properties of coal bed gasification and semi coke gasification [J].Journal of Fuel Chemistry,2000,28(1):40-43.[2]㊀LI Shufen,CHENG Yuanlin.Catalytic gasification of gas-coal charin CO2[J].Fuel,1995,74(3):456-458.[3]㊀SKODRAS G.Mineral matter effects in lignite gasification[J].FuelProcessing Technology,2002,77:151-158.[4]㊀MCKEE D W,SPIRO C L,KOSKY P C,et al.Catalysis ofcoal char gasification by alkali metal salts[J].Fuel,1983,62(2):217-220.[5]㊀MCKEE D W.Gasification of graphite in carbon dioxide and watervapor-the catalytic effects of alkali metal salts[J].Carbon,1982, 20(1):59-66.[6]㊀FRANKLIN H D,PETERS W A,CARTELLO F,et al.Effectof calcium minerals on the rapid pyrolysis of bitumino us coal[J].Industrial&Engineering Chemistry Process Design&Develop-ment,1981,20(4):670-674.[7]㊀LONGWELL J R,LAI C K,WILLIAMS G C,et al.Thermal reac-tion of aromatics with CaO[R].Cambridge:Massachusetts Institute of Technology,1982.[8]㊀JIANG Mingquan,ZHOU Rong,HU Jie,et al.Calcium-promo-ted catalytic activity of potassium carbonate for steam gasification of coal char:Influences of calcium species[J].Fuel,2012,99: 64-71.[9]㊀谢克昌.煤的结构与反应性[M].北京:科学出版社,2002.[10]㊀YEBOAH Y D,XU Y,SHETH A.Catalytic gasification of coalusing eutectic salts:Identification of eutectics[J].Carbon,2003,41(2):203-214.[11]㊀HAGA T,NOGI K,AMAYA M,et posite catalysts for car-bon gasification[J].Applied Catalysis,1991,67(1):189-202.38。
2017年第36卷第7期 CHEMICAL INDUSTRY AND ENGINEERING PROGRESS·2473·化 工 进展逆水煤气变换(RWGS )催化剂研究进展代必灿1,周桂林1,2(1重庆工商大学环境与资源学院,催化与环境新材料重庆市重点实验室,重庆400067;2废油资源化技术与装备教育部工程研究中心,重庆400067)摘要:CO 2经逆水煤气变换(RWGS )反应制得合成气(CO 和H 2),通过费托反应合成C x H y 燃料和含氧化学品,将对环境与未来能源结构产生重大影响,且催化剂起着决定性作用。
本文概述了RWGS 反应催化剂体系研究现状,详细介绍了Pt 、Pd 、Cu 、Ni 和Fe 基等催化剂的RWGS 反应性能,尤其是对金属与载体间的相互作用、制备方法和掺杂元素的电子效应等对相应催化剂的RWGS 反应性能进行了分析,进而探讨了Ce 基催化剂在RWGS 反应中的应用。
通过催化剂活性组分的优化能有效地调控相应催化剂的RWGS 反应性能,实现CO 2有效氢化还原制得合成气,为RWGS 反应工业化奠定基础。
最后对比总结了贵金属与非贵金属催化剂在制备方法、反应条件及RWGS 反应性能间的差异,提出新型催化剂材料开发是RWGS 反应工业化应用的关键。
关键词:二氧化碳;催化剂;合成气;逆水煤气变换;资源化中图分类号:TQ073;O643.36 文献标志码:A 文章编号:1000–6613(2017)07–2473–08 DOI :10.16085/j.issn.1000-6613.2016-2074Perspective on catalyst investigation for reverse water-gas shift reaction(RWGS )DAI Bican 1,ZHOU Guilin 1,2(1Chongqing Key Laboratory of Catalysis & Environmental New Materials ,College of Environment and Resources ,Chongqing Technology and Business University ,Chongqing 400067,China; 2Engineering Research Center for Waste OilRecovery Technology and Equipment ,Ministry of Education ,Chongqing 400067,China )Abstract :CO 2 can be converted into syngas via reverse water-gas shift (RWGS )reaction ,followed by the F-T reaction to produce C x H y fuels or oxygenated chemicals ,which have a significant impact on the environment and the energy structure of the future society and the catalyst plays a key role. The catalyst systems of RWGS reaction are reviewed ,especially for the effect of interaction between metal and support ,the preparation methods ,and the electronic effect of doping elements on RWGS reaction performance of the corresponding catalyst are analyzed. Further ,the application of Ce-based catalyst in RWGS reaction was discussed. Optimizing the active component can effectively improve the RWGS reaction performance of the corresponding catalysts for the hydrogenation reduction of CO 2 into syngas ,and provide a foundation for the industrialization of RWGS reaction. The differences between noble metal and non-noble metal catalysts are also evaluated from points of the preparation methods ,reaction conditions ,and RWGS reaction performance. The development of novel catalyst material is the key to the industrial application of the RWGS reaction.Key words :carbon dioxide ;catalyst ;syngas ;reverse water-gas shift reaction ;resource utilization第一作者:代必灿(1991—),女,硕士研究生。
制备工艺对氧化铈载体金催化剂活性2016-07-25 14:14来源:内江洛伯尔材料科技有限公司作者:研发部水煤气变换反应前后金催化剂的XRD图谱水煤气变换反应已广泛应用于合成氨、汽车尾气净化等方面。
利用该反应可以有效降低直接甲醇燃料电池中CO浓度,提高H2的含量。
目前,已工业化的水煤气变换催化剂包括铁系高温变换催化剂、铜系低温变换催化剂和钴钼系耐硫宽温变换催化剂等。
1996年Andreeva等将共沉淀法制备的Au/α-Fe2O3催化剂用于水煤气变换反应,发现其低温活性明显高于铜系催化剂。
此后,许多氧化物载体被用于负载型纳米金催化剂的制备及其水煤气变换反应研究。
结果表明,载体的本性及其与金粒子的相互作用对高活性金催化剂的氧化态、结构、催化性能等具有非常重要的影响。
CeO2是一种典型的氧化还原性质载体,具有良好的储放氧能力。
在汽车尾气净化催化剂中,添加CeO2不仅能提高催化活性,而且能改善催化剂的热稳定性。
在CO氧化、CH4与CO2重整制合成气等许多反应中,CeO2也常用作催化剂的载体或助剂。
对水煤气变换反应,CeO2负载金催化剂的活性及稳定性明显高于其他载体负载的金催化剂。
Andreeva认为这主要源于活性组分金的高分散,CeO2对生成氧空位的能力有重要影响。
Fu等认为活性位的数目与CeO2表面积和结晶度密切相关,Au的存在减弱了CeO2表面CeO2键的结合,提高了CeO2的储氧能力,有利于CO分子与表面氧的相互作用。
虽然CeO2是金催化剂用于水煤气变换反应的首选载体,但CeO2比表面积小、强度较差。
将CeO2分散在比表面积大、强度好的Al2O3载体上,得到的CeO2-Al2O3复合氧化物既能保持CeO2本身的特性,又具有较大的比表面积和较好的机械强度。
Damyanova等对CeO2-Al2O3复合氧化物进行了结构表征,发现CeO2在Al2O3上的形貌和分散与其负载量和焙烧温度有关。
杨成等研究了CeO2-Al2O3复合氧化物负载Pd催化剂对甲醇分解反应活性。
化工进展Chemical Industry and Engineering Progress2023 年第 42 卷第 8 期CuO-CeO 2/TiO 2高效催化CO 低温氧化反应性能李润蕾1,王子彦2,王志苗1,李芳1,薛伟1,赵新强1,王延吉1(1 河北工业大学化工学院,天津 300401;2 中国船舶重工集团公司第七一八研究所,河北 邯郸 056027)摘要:利用等体积浸渍法制备了CuO-CeO 2/TiO 2催化剂,用于低温CO 氧化反应。
考察了焙烧温度、Cu-Ce 负载量和Ce/Cu 摩尔比等对CuO-CeO 2/TiO 2催化性能的影响,利用XRD 、N 2等温吸附-脱附、XPS 、H 2-TPR 等方法对催化剂进行了表征。
结果表明,当n Ce /n Cu 为1.6,Cu-Ce 负载量为30%时,经500℃焙烧所制得催化剂具有最佳催化活性;当空速为24000mL/(g·h ),在该催化剂上90℃时CO 可完全氧化。
表征发现,CuO-CeO 2/TiO 2催化剂表面较高的Ce 3+、Cu +和吸附氧含量有利于催化CO 氧化反应。
制备条件通过影响催化剂表面的Ce 3+、Cu +和吸附氧含量,影响催化剂活性。
其中,焙烧温度、Cu-Ce 负载量和n Ce /n Cu 均会影响CuO-CeO 2/TiO 2表面Cu +和吸附氧含量,而催化剂表面Ce 3+含量仅受Cu-Ce 负载量的影响较大。
关键词:一氧化碳;氧化;催化剂;制备条件中图分类号:O643 文献标志码:A 文章编号:1000-6613(2023)08-4264-11Efficient catalytic performance of CuO-CeO 2/TiO 2 for CO oxidation atlow-temperatureLI Runlei 1,WANG Ziyan 2,WANG Zhimiao 1,LI Fang 1,XUE Wei 1,ZHAO Xinqiang 1,WANG Yanji 1(1 School of Chemical Engineering and Technology, Hebei University of Technology, Tianjin 300401, China; 2 PurificationEquipment Research Institute of CSIC, Handan 056027, Hebei, China)Abstract: CuO-CeO 2/TiO 2 catalyst was prepared by incipient impregnation method and then used for COoxidation at low temperature. The effects of calcination temperature, Cu-Ce loading and Ce/Cu molar ratioon the catalytic performance of CuO-CeO 2/TiO 2 were investigated. The catalyst was characterized by XRD, N 2 isothermal adsorption-desorption, XPS and H 2-TPR. When n Ce /n Cu was 1.6, and Cu-Ce loading was 30%, the catalyst calcined at 500℃ showed the best catalytic activity. When GHSV was 24000mL/(g·h), CO can be completely oxidized on the catalyst at 90℃. It was found that the high content of Ce 3+, Cu + and adsorbed oxygen on the surface of CuO-CeO 2 /TiO 2 catalyst was favorable to catalyze CO oxidation. The preparation conditions could affect the catalyst activity by regulating the content of Ce 3+, Cu + and adsorbed oxygen on the catalyst surface. Among them, calcination temperature, Cu-Ce loading and n Ce /n Cu wouldinfluence the contents of Cu + and adsorbed oxygen on CuO-CeO 2/TiO 2 surface, while Cu-Ce loading has greatly impact on the Ce 3+ content on catalyst surface.Keywords: carbon monoxide; oxidation; catalyst; preparation conditions研究开发DOI :10.16085/j.issn.1000-6613.2022-1832收稿日期:2022-09-30;修改稿日期:2023-02-04。
碱金属,碱土金属和过渡金属对煤的催化氧化作用碱金属、碱土金属和过渡金属作为催化剂,在煤的催化氧化反应中发挥着重要的作用。
它们能够促进煤的氧化反应,提高煤的氧化速率和转化效率。
本文将分别介绍碱金属、碱土金属和过渡金属在煤的催化氧化作用中的机理和应用。
首先,我们来看碱金属在煤的催化氧化作用中的作用。
碱金属常见的有钠、钾等。
碱金属可以通过两个主要的方式促进煤的氧化反应。
首先,碱金属可以作为催化剂的活性位点,提供有效的氧化剂,例如氧分子或氧酸根离子,给予煤反应所需要的氧化剂。
其次,碱金属本身具有较高的电子亲合能,可以与煤中的氧化性官能团相互作用,发生电子转移反应,使煤分子被激发和激活,从而促进煤的氧化反应。
碱金属的催化氧化作用主要包括直接氧化和间接氧化两种方式。
在直接氧化中,碱金属作为活性位点,接触煤表面的氧化性官能团,给予氧化剂,使官能团氧化为相应的氧化产物。
在间接氧化中,碱金属作为催化剂的活性位点,吸附反应物分子,通过碱金属与反应物分子之间的相互作用,使反应物分子发生形变,进而氧化。
直接氧化和间接氧化都能够促使煤的氧化反应发生,提高煤的氧化速率和转化效率。
下面我们来看碱土金属在煤的催化氧化作用中的作用。
碱土金属主要包括镁、钙、锶、钡等。
碱土金属与碱金属不同,碱土金属不仅能够作为催化剂的活性位点,提供氧化剂,而且还能够作为还原剂,参与煤的氧化反应。
碱土金属可以与煤中的氧化性官能团发生反应,提供电子给予官能团,使官能团发生电子转移反应,从而促进氧化反应的进行。
此外,碱土金属也能够形成碱土氧化物,例如氧化镁、氧化钙等,进一步提供氧化剂给予煤反应所需要的氧化剂。
过渡金属是指位于周期表中3B到12B族元素之间的元素,如铁、铜、锌等。
过渡金属在煤的催化氧化作用中的作用主要是提供氧化剂和催化剂的活性位点。
过渡金属可以通过提供氧原子或氧化剂分子来给予煤所需要的氧化剂。
过渡金属还可以参与煤的氧化反应,作为活性位点,发生电子转移反应,激发和激活煤分子,从而促进氧化反应的进行。
碱金属修饰的催化剂 以碱金属修饰的催化剂为标题,我们来探讨一下碱金属修饰催化剂在化学反应中的应用和优势。催化剂是一种能够加速化学反应速率的物质,而碱金属修饰的催化剂则是指通过添加碱金属元素,如钠、钾等,来改善催化剂的性能和活性。
碱金属修饰催化剂在许多重要的化学反应中发挥着重要作用。首先,碱金属修饰能够增加催化剂的表面活性位点,提高反应速率。碱金属元素的加入可以改变催化剂的电子结构,使得催化剂表面的活性位点增加,从而提高反应速率。此外,碱金属修饰还可以改善催化剂的选择性,使得反应产物更加纯净和理想。这是因为碱金属修饰可以调节催化剂表面的酸碱性质,从而控制催化剂与反应物之间的相互作用,提高反应的选择性。
碱金属修饰催化剂在一些重要的化学反应中具有广泛应用。例如,在石油工业中,碱金属修饰催化剂常用于催化裂化反应,用于将重质石油馏分转化为轻质馏分,提高石油产品的产率和质量。此外,碱金属修饰催化剂也常用于氢气生成反应、氧化反应、还原反应等多种重要的工业反应中。在有机合成领域,碱金属修饰催化剂也被广泛应用于有机合成反应,如羰基化反应、氢化反应、醇醚化反应等。这些反应都是通过碱金属修饰催化剂的作用,实现高效、高选择性的有机合成。 碱金属修饰催化剂具有一系列优势。首先,碱金属修饰可以提高催化剂的活性和选择性,使得反应更加高效和经济。其次,碱金属修饰可以增加催化剂的稳定性,延长催化剂的使用寿命。此外,碱金属修饰还可以改善催化剂的反应条件,使得反应更加温和和环保。最后,碱金属修饰催化剂具有较好的可再生性,可以通过再生和循环利用,降低催化剂的成本和环境污染。
在实际应用中,选择合适的碱金属修饰催化剂是非常重要的。不同的反应需要不同的催化剂,而不同的碱金属修饰也会对催化剂的性能产生不同的影响。因此,在设计和选择碱金属修饰催化剂时,需要考虑催化剂的活性、选择性、稳定性以及反应条件等因素,以实现最佳的催化效果。
碱金属修饰的催化剂在化学反应中具有重要的应用和优势。通过增加催化剂的活性位点和调节催化剂的酸碱性质,碱金属修饰可以提高催化剂的活性、选择性和稳定性,实现高效、高选择性的化学反应。在未来的研究和应用中,我们可以进一步探索碱金属修饰催化剂的性能和机理,以开发更加高效、环保和可持续的催化剂技术。
碱和碱土金属对催化热解的影响
碱和碱土金属在催化热解中起着重要作用。
它们可以作为催化剂参与热解反应,促进反应的进行。
碱金属如钠、钾等和碱土金属如镁、钙等在催化热解中常常表现出良好的催化活性,能够降低反应的活化能,加速热解反应的进行。
这种催化作用可以提高热解产物的产率和质量,有利于提高热解过程的效率。
其次,碱和碱土金属对热解反应的选择性也有影响。
它们可以调控热解反应的产物分布,影响热解产物的种类和比例。
例如,碱金属催化剂在生物质热解中有助于提高生物油的产率,而抑制焦油和气体的生成,从而提高生物质能源的利用效率。
碱土金属催化剂则可能对生物质热解产物的选择性有所不同,可能更有利于特定产物的生成。
此外,碱和碱土金属还可能影响热解反应的动力学过程和热解产物的性质。
它们可以影响热解反应的速率常数,改变反应动力学行为。
同时,催化剂的种类和性质也会影响热解产物的化学性质和物理性质,如碳含量、氧含量、分子结构等。
这些性质的变化可能会影响热解产物的后续利用和加工。
总的来说,碱和碱土金属对催化热解的影响是多方面的,涉及催化活性、选择性、动力学和产物性质等多个方面。
因此,在研究和应用催化热解过程中,需要充分考虑和理解碱和碱土金属对热解过程的影响,以实现更高效、更可控的热解反应。