(2012)有机化学 第三章 烯烃炔烃二烯烃
- 格式:ppt
- 大小:386.50 KB
- 文档页数:66
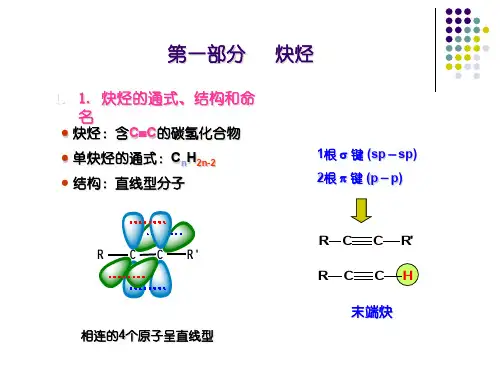









炔烃二烯烃分子中含有碳碳双键的烃称为烯烃。
碳碳双键是烯烃的官能团。
烯烃的通式为。
乙烯是最简单的烯烃。
乙烯、丙烯、丁烯等组成了烯烃的同系列。
烯烃以游离状态存在于自然界的不多,主要以其衍生物的形态存在于自然界中。
杂化轨道理论认为:在烯烃分子中,组SP2杂化轨道城建。
轨道进行杂化,形杂化轨道,并对称地分布在碳原子周围,其对称轴在同一平1200。
所以,SP2杂化又称为平面三角杂化。
杂化碳原子各以一个SP2杂化的轨道沿着对称轴的方向相互重叠形π键,π键的电子键所在平面的上下方。
烯烃的异构体比烷烃的复杂。
除有碳链异构体外,还有因双键位置不同而产生的官能团位置异构。
例如丁烯就有以下同分C H CH3CH2C CH3CH32-甲基丁烯丁烯是官能团双键的位置不同而产生的异构,成为官能团位置异构,简称位置异构。
此外,烯烃还由于碳碳双键两侧连有不同原子或原子团而产生顺反异构。
顺反异构又称为几何异构,是立体异构的一种。
一般是由于分子中具有双键或环状结构使键的自由旋转受阻,与双键或环相连的不同原子或原子团可能存在不同的空间排布,由此而产生的立体异构现象称为顺丁烯的顺反异构。
烯反-2-丁烯IUPAC系统命名法。
它的命名原则和烷烃相似:、选择的主链必须包括碳碳双键,按主链碳原子数称为某烯。
如果主链碳原子数超过十,则称为某碳烯。
、从靠近双键的一端对主链碳原子编号,并以双键碳原子中编号较小的数字表示双键的位次,写在烯烃名称的前面。
例C H CH CCH 3CH 2CH 3CH 3CH 3CH 33,5,6,6-四甲基-3-庚烯当烯烃分子中去掉一个氢原子后剩下的C H 2C CH 3C CH 2H 烯丙基异丙烯基烯基的碳原子编号应从自由价的碳原子开始:2顺反异构体命名时,常把两个双键碳原子上所连接的两个相同或近似的基团在双键同一侧称为顺式,在双键异侧称为反式。
HC CCH3-2-丁烯以上方法虽然简明,但如果双键碳原子上连接有四个不相同的原子或原子团,就命名法。
第三章烯烃炔烃二烯烃Ⅰ学习要求1. 了解不饱和烃的结构特点,熟练掌握烯烃、炔烃、二烯烃及烯烃顺反异构体的系统命名。
2. 掌握不饱和烃的化学反应及其应用,熟练掌握应用亲电加成反应历程,马氏规则及其影响因素判断加成反应的主要产物(或方向)。
3. 了解共轭体系的类型,掌握应用诱导效应和共轭效应判断亲电加成反应的速率。
4. 掌握鉴别烯烃、炔烃的化学方法。
5. 掌握各类碳正离子的稳定性顺序。
Ⅱ内容提要一.不饱和烃的结构1. 烯烃的官能团是碳碳双键,形成双键的两个碳原子是sp2杂化。
碳碳双键是由一个碳碳σ键和一个碳碳π键组成,具有刚性,不能绕碳碳双键自由旋转。
π键的键能较小,易被极化,容易和亲电试剂发生亲电加成反应。
2. 在炔烃分子中碳碳叁键是官能团,形成叁键的两个碳原子是sp杂化,碳碳叁键是直线型,其中两个π键相互垂直。
sp杂化的碳原子的电负性较sp2杂化的碳原子电负性大,所以炔烃中的π键比烯烃的π键较难极化,亲电加成反应炔烃较烯烃难。
3. 共轭二烯烃在结构特征上是指碳碳单键和碳碳双键交替排列的情况。
即分子中有四个sp2杂化的碳原子依次相连,称做共轭链。
共轭二烯烃的四个sp2碳原子共存在于同一平面,形成两个π键的四个p轨道相互平行,π键电子可在共轭链上离域,这种共轭体系的π键又称离域大π键。
它更易极化,亲电反应活性高于独立的π键。
4. 共轭体系是指在分子、离子或自由基中能够形成π键或p轨道离域的体系,在共轭体系中π键电子或p轨道电子不是定域,而是离域的。
这种电子在共轭体系中离域并传递的电子效应称共轭效应。
共轭体系与非共轭体系相比较,具有较低的热力学能,有较高的化学反应活性和特有的化学性质,存在有键长平均化现象。
共轭体系又具体分为:π–π共轭体系、p–π共轭体系、p–p共轭体系、σ–π超共轭体系和σ–p超共轭体系。
5. 共轭效应是指π键电子或p轨道电子在共轭体系中间离域并传递而产生的电子效应,仅存在于共轭体系中;诱导效应则是指σ键电子在σ键中偏移并传递的电子效应,存在于所有的极性σ键中。