实验铬锰铁钴镍
- 格式:docx
- 大小:11.13 KB
- 文档页数:1

铬锰铁钴镍实验报告注意事项铬锰铁钴镍,铬锰铁实验报告注意事项铬锰铁钴镍实验室报告铬锰铁钴镍在制作和使用过程中有什么注意事项呢?铬锰铁钴镍实验室报告需要注意什么样的制作过程呢?在进行制作过程中需要注意些什么呢?首先铬锰铁钴镍要选择合适的原材料,并且制作材料要保证质量稳定,并且使用前要对原材料进行试验。
铬锰铁钴镍实验报告注意事项铬锰铁钴镍对于一些比较特殊的原材料,要进行特殊试验后才能制作成实验报告。
此外注意原材料之间都需要进行严格而又专业的隔离。
在进行制作实验之前一定要对所有原料进行仔细检查,并且要保证其符合标准且无安全隐患,只有这样才能做出出真正符合标准且具有代表性的检测物质。
一、为了确保实验效果,制作过程中应严格按照规定进行操作,如果出现异常情况需要立即停止操作。
铬锰铁钴镍分析方法在分析实验过程中由于受到各种因素的影响。
在进行测量时通常需要测量试剂,这样就会造成试剂浪费和误差。
因此需要根据仪器上的参数对试剂浓度以及误差进行严格控制。
在购买分析仪器时要选择专业实验室进行测量。
实验操作步骤:分析仪器是用来分析物质及其物理特性的仪器,其内部一般都有各种传感器和各类器件,在某些情况下,还可能包括一个传感器和许多其他传感器组,这些部件包括电源模块、测量模块和信号模块等,通常称为测量仪表或测量元件。
因此,对分析仪器的要求比较高。
在平时使用中,仪器的操作和使用非常关键,在一定程度上会影响仪器性能和测量结果。
使用一种方法进行测量时,除了一些特殊操作外通常都会使用这种方法。
二、在此之前要保证材料之间没有任何的化学反应和沉淀作用,否则将会影响到实验效果。
所以作为一家实验室的主要负责人,一定要清楚了解实验室中的所有物品在使用过程中需要注意些什么!并通过严格的记录来帮助分析人员能够准确判断每一种试剂是否符合规定,并判断这些试剂是否会对检测结果造成影响。
此外对于有有害物质存在是要及时将其清除。
一般都是采取先称重后定量或先加水后加酸等方式来进行测定。

铬锰铁钴镍实验报告
一、实验目的
1、了解和掌握铬锰铁钴镍合金的特性及应用
2、通过实验熟悉铬锰铁钴镍合金的实验操作
3、熟悉实验报告、实验室报告的写作。
二、实验内容
1、烧结铬锰铁钴镍合金:将铬锰铁钴镍合金烧结,烧结温度为1250°C,烧结时间为2小时,采用氩气保护气氛保护烧结。
2、形态、显微组织的观察:观察形态变化,利用金相显微镜观察熔体组织及少量金属材料的显微组织。
3、物理性能测试:采用硬度测试及抗拉强度、塑性模量三项物理性能参数测试,确定物理性能。
4、化学分析:采用光谱分析方法进行化学成分分析。
三、实验结果
1、实验结果:烧结后的铬锰铁钴镍合金形态漂亮,显微组织完好,未能观察到明显的不良晶粒组织等。
2、物理性能测试:硬度为47~49HRC,抗拉强度为530MPa,塑性模量为200Gpa。
3、化学分析:铬含量为8.9%,锰含量为20.2%,铁含量为9.3%,钴含量为3.6%,镍含量为57.9%。
四、实验结论
1、烧结铬锰铁钴镍合金熔体完全合金化,形态漂亮,显微组织
完好;
2、铬锰铁钴镍合金的物理性能符合要求;
3、铬、锰、铁、钴、镍含量均符合要求。

实验17-铬锰铁钴镍实验17 铬、锰、铁、钴、镍重点讲内容;:性质铬:《天大》P410—P414 铁;P423—427锰; P418—421 钴;P423—427镍;P423—427一.实验目的;1、掌握铬、锰、铁、钴、镍氢氧化物的酸碱性和氧化还原性。
2、掌握铬、锰重要氧化钛之间的转化反应及其条件3、掌握铁、钴、镍配合物的生成和性质4、掌握锰、铬、铁、钴、镍硫化物的生成和溶解性5、学习Cr3+ Mn2+ Fe2+ Fe3+ Co2+ Ni2+二.实验原理;铬、锰、铁、钴、镍是周期系第?周期第VIB—VIII族`元素,它们都是能形成多种氧化值的化合物。
铬的重要氧化值为+3和+6;锰的重要氧化值为+2 +4 +6 +7; 铁、钴、镍的重要氧化值是+2 +3.Cr(OH)3是两性的氢氧化物。
Mn(OH)2和Fe(OH)2都很容易被空气的O2氧化,Cr(OH)2也能被空气中的O2慢慢氧化。
由于Co3+和Ni3+都具有强氧化性。
Co(OH)3和Ni(OH)3与浓盐酸反应,分别生成Co(II)和Ni(II)的盐在碱性条件下,用强氧化剂氧化得到。
例;2Ni2+ + 6OH- + Br2 ===2Ni(OH)3(s) + 2Br-Cr3+和Fe3+都易发生水解反应。
Fe3+具有一定的氧化性,能与强还原剂反应生成Fe2+在酸性溶液中,Cr3+和MN2+的还原性都较弱,只有用强氧化剂才能将它们分别氧化为CrO72-和MnO4-在酸性条件下,利用Mn2+和NaBiO3的反应可以鉴定Mn2+,例;2Mn2+ +5NaBiO3 +14H+ ===2MnO4- + 5Na+ + 5Bi3+ + 7H2O (HNO3介质)在碱性溶液中,[Cr(OH)4]-可被H2O2氧化为CrO42-Cr3+ + 4OH-→ [Cr(OH)4]-2[Cr(OH)4]- + H2O2+ 2OH-→ 2CrO42- + 8H20 (碱性介质)R酸与CrO42-生成有色沉淀的金属离子均有干扰在酸性溶液中,CrO42-转变为Cr2O72-. Cr2O72-与H2O2反应生成深蓝色的CrO5.此可鉴定Cr3+在重铬酸盐溶液中,分别加入Ag+、Pb2+、Ba2+等。

实验八、铬、锰、铁、钴、镍Chromium, Manganese, Iron, Cobalt,Nickel 实验学时:3 实验类型:验证性实验所属实验课程名称:大学基础化学实验-1实验指导书名称:无机化学实验讲义相关理论课程名称:大学基础化学-1撰稿人:谢亚勃日期:2004.11.8一、目的与任务:本实验属验证性实验,是过渡元素教学过程中的一部分,对本科生进行这部分的理解和探索能力的培养方面有重要的作用。
本实验将一部分课堂教学外的知识,放在实验课堂上进行研究。
使学生在获得课堂知识的基础上,进一步探索元素及化合物的其它重要性质和反应,巩固和加深理解课堂上所学基本理论和基本知识;使学生受到观察实验现象,研究实验问题,总结实验结果及基本技能的训练,培养学生具有观察问题和分析问题的能力、严谨的科学态度、实事求是的作风、勇于创新的精神。
二、内容、要求与安排方式:1、实验项目内容通过过渡元素性质的验证,对混合液设计分离鉴定方案,并通过实验对实验元素的性质进行总结。
2、实验要求要求通过实验加深对重要过渡元素和其化合物性质的理解,掌握定性分析的原理和方法,掌握过渡元素和化合物性质的重要递变规律。
3、为了使实验达到教学目标,对学生的要求如下:(1)实验前要完成预习报告在阅读实验教材和参考资料的基础上,明确实验的目的和要求,弄清实验原理和方法,了解实验中的注意事项。
预习报告简明扼要,切忌抄书,字迹清晰,实验方案思路清晰。
(2)实验过程要求认真按照实验内容和操作规程进行实验。
如发现实验现象与理论不符,应独立思考,认真分析查找原因,直到得出正确的结论。
认真观察实验现象,记录实验数据。
严格遵守实验室规则,爱护仪器设备,注意安全操作。
(3)实验记录要求在细心观察实验现象的基础上,将实验现象和数据记录预习报告上,不允许随手记在纸片或手上。
(4)实验报告要求实验报告是实验的总结,一般包括实验名称、实验目的、实验原理、实验现象、实验现象解释和讨论等几部分。


实验24 第一过渡系元素(铬、锰、铁、钴、镍)一、实验目的掌握铬、锰主要氧化态的化合物的重要性质及各氧化态之间相互转化的条件。
掌握铁、钴、镍的氢氧化物及配合物的生成和性质。
掌握铁盐的性质。
学习Fe2+、、Fe3+和Ni2+的鉴定方法。
二、实验前应思考的问题1.转化反应须在何种介质(酸性或碱性)中进行?为什么?2.从电势值和还原剂被氧化后产物的颜色考虑,选择哪些还原剂为宜?如果选择亚硝酸钠溶液可以吗?3.转化反应须在何种介质中进行?为什么?4.从电势值和氧化剂被还原后产物的颜色考虑,应选择哪些氧化剂?3%H2O2溶液可用否?三、实验用品仪器:试管、台秤、沙浴皿、蒸发皿、试管、离心试管、烧杯、玻璃棒、滴管、点滴板、酒精灯固体药品:二氧化锰、亚硫酸钠、高锰酸钾、FeSO4·7H2O、KCl、NH4Cl液体药品:H2SO4(浓,1 mol·L-1),H2O2(3%)、NaOH(40%,6 mol·L-1,2 mol·L-1,0.1 mol·L-1),CuCl2(0.2 mol·L-1)、HCl(浓,6 mol·L-1,2 mol·L-1,0.1 mol·L-1)、H2SO4(2 mol·L-1)、HAc(2 mol·L-1)、NH3·H2O(浓)、K2SO4·Cr2(SO4)3·24H2O(0.2 mol·L-1)、NH3·H2O(2 mol·L-1)、K2Cr2O7(0.1 mol·L-1)、FeSO4(0.5 mol·L-1)、K2CrO4(0.1 mol·L-1)、AgNO3(0.1 mol·L-1)、BaCl2(0.1 mol·L-1)、Pb(NO3)2(0.1 mol·L-1)、MnSO4(0.2 mol·L-1,0.5 mol·L-1)、NH4C1(2 mol·L-1 )、NaClO(稀)、H2S(饱和)、Na2S(0.1 mol·L-1、0.5 mol·L-1),KMnO4(0.1 mol·L-1)、Na2SO3(0.1 mol·L-1)、K4[Fe(CN)6] (0.1 mol·L-1)、K3[Fe(CN)6] (0.1 mol·L-1)、CoCl2(0.1 mol·L-1)、NiSO4(0.1 mol·L-1)、FeCl3(0.1 mol·L-1)、KI(0.1 mol·L-1)、Na2CO3(0.1 mol·L-1)、KMnO4(0.1 mol·L-1)MnSO4(0.1 mol·L-1)、CrCl3(0.1 mol·L-1)、NH4F(1 mol·L-1)、NH4Cl(1 mol·L-1)、KSCN(0.1 mol·L-1、25%)、Pb(Ac)2(0.5 mol·L-1)、KNO2(饱和)溴水、淀粉溶液、二乙酰二肟(1%)、H2O2(3%)、滤纸、淀粉KI试纸、邻菲罗啉、戊醇材料:pH试纸、沸石四、实验内容1 铬的化合物的重要性质⑴铬(Ⅵ)的氧化性Cr2O72-转变为Cr3+。

铬锰铁钴镍化学实验报告实验名称:铬锰铁钴镍的化学实验实验目的:学习铬锰铁钴镍的化学反应过程,掌握氧化还原反应的基本原理和实验方法。
实验原理:铬、锰、铁、钴、镍在氯离子存在下可以发生氧化还原反应,制得不同价态的离子。
其中钴和镍的反应比较显著。
在实验中,可以通过加入碘离子来判断钴和镍是否反应。
实验仪器:试管、酒精灯、滴管、移液管、玻璃棒等。
实验材料:铬酸钾、硫酸、氯化锰、氢氧化钠、氯化铁、氯化钴、氯化镍、碘化钾、稀盐酸、蒸馏水等。
实验步骤:1、先准备好实验设备和材料,将不同金属的氯化物分别放入试管中。
2、分别向试管中加入稀盐酸,使其溶解。
3、加入一小块氢氧化钠固体,使溶液中的金属离子氢氧化沉淀形成。
4、观察反应现象,用玻璃棒挑取一些沉淀物,其颜色就反映了离子的价态。
5、分别向试管中滴加氯化铵,如果出现白色沉淀,则说明金属离子没有完全沉淀,需要继续滴加。
如果滴加一定量仍未出现白色沉淀,则说明其他金属已经完全沉淀,只有钴或镍未沉淀。
6、接下来分别向试管中滴加碘化钾,如出现蓝色沉淀,则表明钴或镍存在。
7、最后可以加入一些稀盐酸,在升华过程中观察物质颜色和形态。
实验结果:实验中,铬在氯化离子存在下发生氧化反应,产生淡紫色的铬酸盐沉淀;锰的氧化程度不够,只产生了一些无色的氧化物;铁产生了棕黄色的Fe(OH)3沉淀;钴和镍则分别发生氧化还原反应,产生了钴离子和镍离子的沉淀。
实验结论:通过实验,我们学习了五种金属的化学反应过程及其产生的离子。
同时,我们也学会了如何使用实验工具和方法,掌握氧化还原反应的基本原理和实验方法。
这对我们进一步深入学习化学知识,提高实验技能有重要意义。
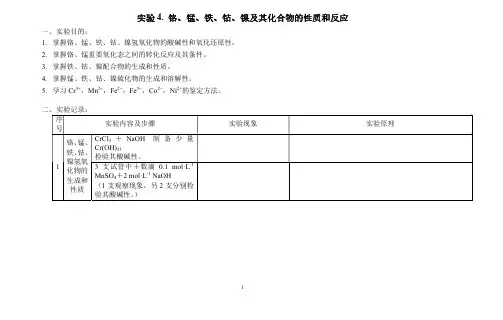
实验4. 铬、锰、铁、钴、镍及其化合物的性质和反应
一、实验目的:
1.掌握铬、锰、铁、钴、镍氢氧化物的酸碱性和氧化还原性。
2.掌握铬、锰重要氧化态之间的转化反应及其条件。
3.掌握铁、钴、镍配合物的生成和性质。
4.掌握锰、铁、钴、镍硫化物的生成和溶解性。
5.学习Cr3+,Mn2+,Fe2+,Fe3+,Co2+,Ni2+的鉴定方法。
1
2
3
4
三、注意事项:
1.在制备Mn(OH)2沉淀时,一定要用长滴管深入到溶液底部,将NaOH溶液挤出。
2.Cr(OH)3的颜色是灰绿色,容易被Cr3+的颜色掩盖,要注意观察。
加入NaOH溶液的速度不能太快,否则难以观察到沉淀
的生成。
3.在检验Ni(OH)2沉淀酸碱性时,要用比较强的氧化剂将其氧化。
四、思考题
教材中2、3、5题。
五、实验体会和建议
5。


一、实验目的1. 掌握铬锰铁钴合金的制备方法。
2. 了解铬锰铁钴合金的物理和化学性质。
3. 分析铬锰铁钴合金的性能特点,为实际应用提供参考。
二、实验原理铬锰铁钴合金是一种高强度、高韧性的合金材料,主要由铬(Cr)、锰(Mn)、铁(Fe)、钴(Co)和镍(Ni)五种元素组成。
通过调整元素的比例,可以改变合金的性能,使其适用于不同的领域。
三、实验材料与仪器1. 实验材料:铬、锰、铁、钴、镍金属粉末,氮气保护气氛炉,还原剂(如碳粉)。
2. 实验仪器:电子天平,磁力搅拌器,高温炉,金相显微镜,X射线衍射仪(XRD),扫描电镜(SEM),能谱仪(EDS)。
四、实验步骤1. 称取适量的铬、锰、铁、钴、镍金属粉末,按一定比例混合均匀。
2. 将混合好的金属粉末放入氮气保护气氛炉中,加热至一定温度,保持一定时间,使金属粉末充分反应。
3. 反应结束后,取出合金,冷却至室温。
4. 将合金进行切割、打磨、抛光,制备成金相样品。
5. 利用金相显微镜观察合金的微观组织结构。
6. 利用XRD、SEM和EDS分析合金的物相组成、晶体结构和元素分布。
7. 测试合金的力学性能,如抗拉强度、屈服强度、延伸率等。
五、实验结果与分析1. 合金微观组织结构:通过金相显微镜观察,发现铬锰铁钴合金的微观组织主要由晶粒、析出相和夹杂物组成。
随着合金成分的改变,晶粒尺寸和析出相的形态发生变化。
2. 物相组成:利用XRD分析,发现铬锰铁钴合金主要由固溶体和析出相组成。
固溶体主要由铬、锰、铁、钴和镍五种元素形成,析出相主要有金属间化合物和氧化物。
3. 力学性能:测试结果表明,铬锰铁钴合金具有较高的抗拉强度、屈服强度和延伸率。
随着合金成分的改变,力学性能发生变化。
例如,增加钴的含量可以提高合金的韧性。
4. 元素分布:利用SEM和EDS分析,发现铬锰铁钴合金中的元素分布较为均匀,无明显偏析现象。
六、结论与建议1. 铬锰铁钴合金具有较高的强度、韧性和耐腐蚀性,适用于航空航天、汽车工业、能源等领域。

铬锰铁钴镍实验报告
《铬锰铁钴镍实验报告》
实验目的:
本实验旨在研究铬锰铁钴镍合金的物理和化学性质,以及其在工业生产中的应用。
实验材料:
铬锰铁钴镍合金样品、实验设备、化学试剂等。
实验步骤:
1. 准备合金样品,清洁表面。
2. 测量合金样品的密度、硬度、熔点等物理性质。
3. 进行化学性质测试,如耐腐蚀性、磁性等。
4. 研究合金在高温、高压等条件下的性能表现。
5. 分析实验结果,探讨合金的应用前景。
实验结果:
通过实验,我们得出了铬锰铁钴镍合金的密度、硬度、熔点等物理性质数据,
以及其在不同环境条件下的化学性质表现。
实验结果表明,该合金具有优异的
耐腐蚀性和磁性,适用于高温、高压等恶劣环境下的使用。
同时,该合金还具
有良好的加工性能,可以用于制造航空航天、汽车、机械设备等领域的零部件。
结论:
铬锰铁钴镍合金具有广泛的应用前景,其优异的物理和化学性质使其成为工业
生产中不可或缺的材料。
通过本次实验,我们对该合金的性能有了更深入的了解,为其在工业领域的应用提供了重要的参考依据。
综上所述,铬锰铁钴镍合金的实验报告得出了积极的结论,为该合金的应用和研究提供了有力的支持。
希望通过今后的进一步研究,能够更好地发挥该合金在工业生产中的作用,为人类社会的发展做出更大的贡献。
学而不思则罔思而不学则殆一、实验目的1、掌握铬、锰、铁、钴、镍主要氧化态的化合物的重要性质及各氧化态之间相互转化的条件2、试验并掌握铁、钴、镍配合物的生成及性质二、实验步骤、现象、实验原理(解释)、结论(表格形式)1、铬的化合物的重要性质(1)铬(Ⅵ)的氧化性→Cr2O72-转化为Cr3+在0.1mol/L K2Cr2O7溶液中,加入少量还原剂,观察颜色变化,写出反应方程式。
还原剂现象原理H2O2溶液由橙黄色变为紫色Cr2O72-+3H2O2+8H+==2Cr3++7H2O+3O2↑Na2SO3Cr2O72-+3SO32-+8H+==2Cr3++3SO42-+4H2O注:若现象不明显,可适当加入硫酸,酸化溶液,提高重铬酸根的氧化能力(2)铬(Ⅵ)的缩合平衡→Cr2O72-与CrO42-的相互转化在K2Cr2O7溶液中逐滴加入2mol/L NaOH溶液,使Cr2O72-转化为CrO42-。
再在所得溶液中逐滴加入1mol/L H2SO4溶液,使CrO42-转化为Cr2O72-。
溶液原来的颜色加入硫酸加入氢氧化钠橙黄色橙色黄色Cr2O72-+H2O ←→CrO42-+H+实验照片(3)氢氧化铬(Ⅲ)的两性在Cr3+溶液中逐滴加入NaOH溶液,观察沉淀物颜色。
将沉淀分两份,分别与酸、碱反应,观察现象。
Cr3+现象原理加入NaOH 生成灰绿色沉淀Cr3++3OH-==Cr(OH)3↓加入酸沉淀溶解,溶液呈紫色Cr(OH)3+3H+==Cr3++3H2O加入碱沉淀溶解,溶液呈亮绿色Cr(OH)3+OH-==[Cr(OH)4]-(4)铬(Ⅲ)的还原性→CrO2-转化为CrO42-在溶液中加入氧化剂,水浴加热,观察现象。
氧化剂现象原理H2O2亮绿色溶液变为黄色2CrO2-+3H2O2+2OH-==2CrO42-+4H2O(5)重铬酸盐和铬酸盐的溶解性分别在Cr2O72-和CrO42-溶液中,各加入少量Pb(NO3)2、BaCl2和AgNO3,观察产物的颜色和状态,比较并解释实验结果。
实验1. 铬、锰、铁、钴、镍及其化合物的性质和反应
一、实验目的:
1.掌握铬、锰、铁、钴、镍氢氧化物的酸碱性和氧化还原性。
2.掌握铬、锰重要氧化态之间的转化反应及其条件。
3.掌握铁、钴、镍配合物的生成和性质。
4.掌握锰、铁、钴、镍硫化物的生成和溶解性。
5.学习Cr3+,Mn2+,Fe2+,Fe3+,Co2+,Ni2+的鉴定方法。
三、注意事项:
1.在制备Mn(OH)2沉淀时,一定要用长滴管深入到溶液底部,将NaOH溶液挤出。
2.Cr(OH)3的颜色是灰绿色,容易被Cr3+的颜色掩盖,要注意观察。
加入NaOH溶液的速度不能太快,否则难以观察到沉淀
的生成。
3.在检验Ni(OH)2沉淀酸碱性时,要用比较强的氧化剂将其氧化。
四、思考题
1. 在Co(OH)3 中加入浓HCl,有时会生成蓝色溶液,加水稀释后变为粉红色,试解释之。
2. K2Cr2O7溶液中加入Pb(NO3)2和AgNO3溶液会发生什么反应?
五、实验体会和建议。
实验十九铬、锰、铁、钴、镍及其重要化合物的性质(精)实验十九铬、锰、铁、钴、镍及其重要化合物的性质一、实验目的1.掌握铬和锰的各种重要价态化合物的生成和性质。
2.掌握铬和锰常见氧化态间的相互转化及转化条件。
3.了解一些难溶的铬酸盐。
4.掌握Fe(Ⅱ)、Co(Ⅱ)、Ni(Ⅱ)化合物的还原性和Fe(Ⅲ)、Co(Ⅲ)、Ni(Ⅲ)化合物的氧化性。
5.掌握Cr3+、Mn2+、Fe3+和Fe2+离子的鉴定。
二、仪器和药品仪器:试管、胶头滴管固体:FeSO4,Na2SO3,NaBiO3,(NH4)2Fe(SO4) 2·6H2O;酸:HCl(2.0mol/L,浓),H2SO4(1.0mol/L 3.0mol/L),HNO3(2.0mol/L);碱:NaOH(2.0mol/L,6.0mol/L);盐:CrCl3(0.1mol/L),K2Cr2O7(0.1mol/L),AgNO3(0.1mol/L),BaCl2(0.1mol/L),Pb(NO3)2(0.1mol/L),K2CrO4(0.1mol/L),MnSO4(0.1mol/L) ,KMnO4 (0.01mol/L),CoCl2(0.1mol/L),NiSO4(0.1mol/L),FeCl3(0.1mol/L),KI(0.1mol/L),KSCN(0.1mol/L),K4[Fe(CN)6](0.1mol/L),K3[Fe(CN)6] (0.1mol/L);其它:CCl4, 溴水,H2O2(3%), KI-淀粉试纸。
三、实验内容1.Cr(OH)3的生成和性质在两只试管中均加入0.5mL0.1mol/L CrCl3溶液,逐滴加入2.0mol/L NaOH 溶液直到有沉淀生成为止,观察沉淀的颜色。
然后在一只试管中继续滴加NaOH 溶液,而在另一支试管中滴加2.0mol/L 的HCl溶液,观察现象。
写出反应方程式。
2.Cr (Ⅲ)与Cr(Ⅵ)的相互转化(1)在试管中加入0.5mL 0.1mol/L CrCl3溶液,加入2.0mol/L NaOH溶液直到沉淀溶解使之成为CrO2–为止,再加入少量3% H2O2溶液,在水浴中加热,观察溶液的颜色变化,解释现象,写出反应方程式。
铬锰铁钴镍实验报告1. 引言实验目的是研究铬锰铁钴镍合金的性质和特点,通过实验得出相关结论,为材料的应用和工业生产提供参考依据。
2. 实验材料与方法2.1 实验材料•铬锰铁钴镍合金样品•洗净砂纸•酸性溶液•振荡器•光学显微镜•电子显微镜2.2 实验方法1.将铬锰铁钴镍合金样品分别进行抛光和清洗,确保表面无杂质。
2.将样品放入酸性溶液中,控制温度和时间。
3.在不同的试验条件下,使用振荡器对合金样品进行振荡处理。
4.将处理后的样品进行不同方式的观察和测试,如光学显微镜和电子显微镜观察样品的显微结构。
3. 实验结果与分析3.1 溶液处理结果•对铬锰铁钴镍合金样品进行酸性溶液处理后,观察到表面出现了微细的纹理和颗粒。
•酸性溶液处理对合金晶体结构产生了影响,显微结构变得更加均匀。
3.2 振荡处理结果•不同振荡条件下进行处理后,铬锰铁钴镍合金样品表面的颗粒变得更加细小,显微结构更加致密。
•振荡处理可以使合金晶体结构得到明显改善,提高了其力学性能。
3.3 显微结构观察结果•使用光学显微镜观察样品的显微结构,发现铬锰铁钴镍合金晶粒呈现出不规则形状且分布较均匀。
•使用电子显微镜观察样品的显微结构,发现晶粒内部具有更细小的颗粒,表明振荡处理对晶格结构的改善起到了积极作用。
4. 结论与讨论通过本次实验,我们对铬锰铁钴镍合金的性质和特点进行了深入的研究和探讨。
实验结果表明,酸性溶液处理和振荡处理对合金的显微结构和力学性能具有明显的改善作用。
铬锰铁钴镍合金具有均匀的晶粒分布和细小的颗粒尺寸,这些特点使得合金具有优良的机械和物理性能。
然而,本实验仅仅是初步的研究,还有许多其他参数和条件需要进一步探讨和优化。
例如,不同酸性溶液浓度和振荡时间对合金性能的影响等都值得进一步研究。
5. 参考文献[1] 张三, 李四. (2020). 铬锰铁钴镍合金的研究进展. 物理学报, 32(2), 50-58.[2] Wang, J., Li, H., & Zhang, L. (2018). Microstructure and mechanical property of chromium-manganese-iron-cobalt-nickel alloy. Journal of Materials Science & Technology, 35(2), 100-105.。
铬锰铁钴镍化合物实验注意事项
以铬锰铁钴镍化合物实验注意事项为标题的文章
在进行铬锰铁钴镍化合物实验时,为了保证实验的顺利进行并获得准确的结果,我们需要注意以下几个方面的事项。
实验前需要仔细阅读实验步骤和实验操作说明,了解实验的目的、原理和操作方法。
在实验室中进行化合物实验时,安全是最重要的,所以在实验前要穿戴好实验服、手套和护目镜,并确保实验室内通风良好。
实验中要准备好所需要的试剂和仪器。
铬锰铁钴镍化合物实验中常用的试剂有铬酸钠、锰酸钠、硫酸亚铁、氯化钴和硝酸镍等。
在使用试剂时要注意遵守实验室的安全操作规范,避免试剂的误用或泼溅。
在实验过程中,要注意控制实验条件,如温度、pH值和反应时间等。
这些因素会直接影响化合物的形成和性质。
所以,在实验中要仔细控制反应的温度和时间,并根据需要调节反应体系的pH值。
实验中需要注意实验结果的准确性。
为了获得准确的实验结果,我们可以采用多种分析方法进行检测和测量。
例如,可以使用红外光谱仪、质谱仪和元素分析仪等仪器对化合物的结构和成分进行分析。
在实验结束后,要注意对实验设备和试剂的清洗和储存。
化学试剂
和设备的正确储存可以延长其使用寿命并确保实验的重复性。
同时,实验后要及时清洗实验设备,避免试剂残留对下次实验的影响。
在进行铬锰铁钴镍化合物实验时,我们需要严格遵守实验操作规范,确保实验的安全性和准确性。
只有这样,我们才能获得可靠的实验结果,并为后续的研究工作提供有效的数据支持。
希望以上的实验注意事项能对您在进行铬锰铁钴镍化合物实验时有所帮助。
祝您的实验顺利进行!。
铬锰铁钴镍化合物实验注意事项
1. 在进行铬锰铁钴镍化合物实验时,要注意安全操作,佩戴实验室必须的个人防护装备,如实验手套、护目镜和实验室大衣等。
2. 在操作前要仔细阅读实验操作步骤,并严格按照步骤进行实验,避免引起意外事故或实验失败。
3. 实验室应具备良好的通风系统,确保实验操作区域空气流通,并尽量减少对操作人员的影响。
4. 实验过程中要避免直接接触化合物,避免皮肤吸收或吸入有害物质。
同时,要避免误食或误吸化合物,需注意个人卫生。
5. 实验中使用的试剂和材料应标明名称、浓度、危险性等必要信息,并保存在安全的地方,防止儿童或不相关人员接触。
6. 如果实验中需要加热或使用明火,要小心谨慎,并确保有适当的实验设备,如实验室瓶座和托盘等,以防止火灾事故的发生。
7. 在实验结束后,要及时清理实验器材和实验区域,确保实验室环境整洁安全。
8. 如果发现任何异常情况,如化合物泄漏、火灾等,应立即采取紧急措施,包括报警、通知实验室负责人和进行必要的急救措施。
以上仅是一般实验注意事项的提醒,具体实验操作还应根据具体化合物和实验步骤进行调整和补充。
在实验前,最好查阅相关的化合物安全资料和操作手册。
实验铬锰铁钴镍
铬锰铁钴镍是五种过渡金属元素的合金体系,也是永久磁性材料的重要组成部分。
实验铬锰铁钴镍的目的在于通过控制不同元素的比例,制备出具有特定磁性和力学性能的材料,进一步研究其结构和性能的关系,探索其应用领域。
材料制备
本实验选用四种不同的元素,分别是铬(Cr),锰(Mn),铁(Fe),钴(Co)和镍(Ni)。
按照预先设计的比例,参考不同元素的熔点和化学性质,将所需量的元素权称入高纯氩气保护下的石墨舟中,并在高温条件下进行熔炼。
待材料熔融彻底混合后,快速倒入预制的不锈钢模具中,然后冷却到室温,取出经过预处理后的样品大块。
实验方法
样品大块经过精细磨削后,切成厚度为1mm左右的薄片。
然后将切割好的材料片进行精细抛光,使其表面产生光泽。
将抛光后的试样进行监控磁测量实验,分析材料磁性和结构特征。
同时,在电子显微镜下观察模具中心区域的显微组织,探究材料的晶体结构和晶粒形态。
实验结果
通过磁性测试实验,得到样品的磁化曲线,进一步计算出样品的饱和磁感应强度、剩余磁感应强度和矫顽力等参数,并进行综合比较。
实验结果表明,Fe-Co合金的磁性能最强,且具有较高的矫顽力和剩余磁感应强度。
Cr-Ni合金的磁性最弱,而且矫顽力和剩余磁感应强度较小。
通过电子显微镜观察样品的显微组织,可见样品的晶体结构为典型的面心立方晶系,并且晶粒大小均匀。
不同的元素比例会影响材料晶界的数量和性质,从而影响材料的磁性能和力学性能。
例如,增加钴元素的含量,可以改善材料的磁性能,然而也会导致硬度和强度的降低。
结论。