实验八铬锰铁钴镍.doc
- 格式:doc
- 大小:77.50 KB
- 文档页数:4

实验9 铬、锰及其化合物的性质一、实验目的掌握铬、锰主要氧化态化合物的性质。
二、实验原理1、铬及其化合物的性质Cr 价电子构型:3d 54s 1 ,VIB 族,常见的氧化态为+6,+3,+2Cr 2O 72-Cr 3+Cr 2+Cr 1.33-0.41-0.91-0.74E A 0/VE B 0/VCrO 42-Cr(OH)3Cr(OH)2Cr-0.13-1.1-1.4在酸性介质中,+2氧化态具有强的还原性,+6氧化态具有氧化性,Cr 3+的还原性都较弱,只有用强氧化剂才能将它们分别氧化为Cr 2O 72-;在碱性介质中,+6氧化态稳定(CrO 42-)。
Cr 2O 3和Cr (OH )3显两性。
Cr 3+Cr(OH)34]-((绿色)--铬(VI )最重要的化合物为K 2Cr 2O 7,在水溶液中Cr 2O 72-和CrO 42-存在下列平衡:Cr 2O 72-CrO 42-+2H 2OH+2+(橙红色)(黄色)在碱性溶液中,[Cr(OH)4]-可以被过氧化氢氧化为CrO 42-。
在酸性溶液中CrO 42-转变为Cr 2O 72-。
Cr 2O 72-与过氧化氢反应能生成深蓝色的CrO 5,由此可以鉴定Cr 3+。
2、Mn价电子结构3d 54s 3 ,VIIB 族,常见的氧化态为+6,+7,+4,+3,+2 Mn 2+在酸性溶液中的稳定性大于在碱性溶液中:酸性介质:只有很强的氧化剂(铋酸钠、二氧化铅)才能氧化Mn 2+H 2O7Mn2+NaBiO 3H+Na +Bi 3+MnO 4-25145+++5+2+碱性介质:Mn 2+2+OH -Mn(OH)2(白色沉淀)O 2MnO(OH)2(棕色)Mn (IV )化合物重要的是MnO 2,在酸性溶液中具有氧化性。
Mn (VI )化合物重要的是MnO 42-,Mn (VII )化合物重要的是MnO 4-E A 0/VE B 0/VMnO 4-MnO 42-MnO 2MnO 4-MnO 42-MnO20.562.260.560.60MnO 42-存在于强碱溶液中,在酸性,中性环境中均发生歧化。

锰铁钴镍实验报告锰铁钴镍实验报告引言:锰铁钴镍是一种重要的合金材料,具有优异的力学性能和磁性能,广泛应用于电子、汽车、航空航天等领域。
本实验旨在通过制备锰铁钴镍合金,并对其力学性能和磁性能进行测试和分析,以便更好地了解该合金材料的特性。
实验方法:1. 实验材料准备:- 锰铁钴镍粉末- 氧化铝粉末- 碳化硼粉末- 碘化镍粉末- 碳化钴粉末2. 实验步骤:a. 将锰铁钴镍粉末、氧化铝粉末、碳化硼粉末按照一定的比例混合均匀。
b. 将混合粉末放入高温炉中,在氮气保护下进行烧结反应,升温至适宜的温度。
c. 经过一定时间的烧结反应后,取出试样进行冷却。
d. 对制备的锰铁钴镍合金试样进行力学性能和磁性能测试。
实验结果与分析:1. 力学性能测试:a. 强度测试:通过拉伸实验测定锰铁钴镍合金的抗拉强度和屈服强度。
b. 硬度测试:使用布氏硬度计测定锰铁钴镍合金的硬度值。
c. 韧性测试:通过冲击试验测定锰铁钴镍合金的韧性指标。
2. 磁性能测试:a. 磁化曲线测试:使用霍尔效应磁强计测定锰铁钴镍合金的磁化曲线。
b. 矫顽力测试:通过磁化曲线中的矫顽力值,评估锰铁钴镍合金的抗磁性能。
实验结论:通过实验测试和分析,得出以下结论:1. 锰铁钴镍合金具有较高的抗拉强度和屈服强度,适用于承受高强度载荷的工程结构。
2. 锰铁钴镍合金的硬度较高,具有较好的耐磨性和耐久性。
3. 锰铁钴镍合金的韧性较好,能够在受到冲击载荷时具有较好的变形和吸能能力。
4. 锰铁钴镍合金具有较高的磁化强度和矫顽力,适用于磁性材料的制备和应用。
结语:本实验通过制备锰铁钴镍合金,并对其力学性能和磁性能进行测试和分析,全面了解了该合金材料的特性。
锰铁钴镍合金的优异性能使其在工程领域有着广泛的应用前景。
未来的研究可以进一步探索该合金的微观结构与性能之间的关系,以及进一步优化合金配方,提升其性能。


实验八铁钴镍铁、钴、镍1. 实验目的试验并掌握二价铁、钴、镍的还原性和三价铁、钴、镍的氧化性。
试验并掌握铁、钴、镍配合物的生成及性质。
2. 实验用品仪器:试管、离心试管固体药品:硫酸亚铁铵、硫氰酸钾液体药品:H2SO4(6mol·L-1,1mol·L-1)、HCl(浓)、NaOH(6mol·L-1,2mol·L-1)、(NH4)2Fe(SO4)2(0.1mol·L-1)、CoCl2(0.1mol·L-1)、NiSO4(0.1mol·L-1)、KI(0.5mol·L-1)、K4[Fe(CN)6](0.5mol·L-1)、氨水(6mol·L-1,浓)、氯水、碘水、四氯化碳、戊醇、乙醚、H2O2(3%)、FeCl3(0.2mol·L-1)、KSCN(0.5mol·L-1)。
材料:碘化钾淀粉试纸3. 实验原理铁、钴、镍是周期系第(Ⅷ)族元素的第一个三元素组,性质很相似,在化合物中常见的氧化值为+2、+3。
铁、钴、镍的+2价氢氧化物都是呈碱性,具有不同颜色,空气中氧对它们的作用情况各不相同,Fe(OH)2很快被氧化成红棕色Fe(OH)3,但是在氧化过程中可以生成绿色到几乎黑色的各种中间产物,而Co(OH)2缓慢地被氧化成褐色Co(OH)3,Ni(OH)2与氧则不起作用,若用强氧化剂,如溴水,则可使Ni(OH)2氧化成Ni(OH)3。
NiSO4 + Br2 + 3NaOH = Ni(OH)3↓+ NaBr + Na2SO4除Fe(OH)3外,Ni(OH)3、Co(OH)3与HCl作用,都能产生氯气:2Ni(OH)3 + 6HCl = 2NiCl2 + Cl2↑+6H2O2Co(OH)3 + 6HCl = 2CoCl2 + Cl2 ↑+6H2O由此可以得出+2价铁、钴、镍氧化物的还原性及+3价铁、钴、镍氢氧化物的氧化性的变化规律。

一、实验目的1. 掌握锰铁钴镍合金的制备方法。
2. 了解锰铁钴镍合金的物理、化学性质。
3. 分析锰铁钴镍合金的微观结构。
4. 研究锰铁钴镍合金的应用领域。
二、实验材料与仪器1. 实验材料:锰铁、钴、镍金属粉末,石墨粉,氧化铝坩埚,还原剂(碳粉)。
2. 实验仪器:高温炉,搅拌器,电炉,X射线衍射仪,扫描电子显微镜,能谱仪,拉伸试验机,硬度计。
三、实验方法1. 合金制备:将锰铁、钴、镍金属粉末按照一定比例混合,加入适量的石墨粉作为还原剂,放入氧化铝坩埚中,高温熔炼制备合金。
2. 性能测试:采用X射线衍射仪、扫描电子显微镜、能谱仪等手段对合金进行物相分析、微观结构分析;利用拉伸试验机和硬度计测定合金的力学性能;采用电化学测试方法研究合金的耐腐蚀性能。
四、实验结果与分析1. 物相分析:通过X射线衍射仪对合金进行物相分析,结果表明,合金主要由面心立方(FCC)结构组成,含有少量的体心立方(BCC)结构。
2. 微观结构分析:采用扫描电子显微镜和能谱仪对合金进行微观结构分析,发现合金中存在晶界、析出相等组织,晶粒大小均匀。
3. 力学性能:通过拉伸试验机测定合金的力学性能,结果表明,合金具有较高的强度和硬度,抗拉强度达到600MPa,硬度达到HV500。
4. 耐腐蚀性能:采用电化学测试方法研究合金的耐腐蚀性能,结果表明,合金具有良好的耐腐蚀性能,在腐蚀介质中表现出较低的腐蚀速率。
五、结论与建议1. 结论:通过高温熔炼法制备的锰铁钴镍合金具有优异的物理、化学性能和力学性能,是一种具有广泛应用前景的合金材料。
2. 建议:在合金制备过程中,可根据实际需求调整锰铁、钴、镍的比例,优化合金成分;在制备过程中,严格控制温度和时间,以获得理想的合金组织;进一步研究合金的微观结构与性能之间的关系,为合金的应用提供理论依据。
六、实验总结本次实验成功制备了锰铁钴镍合金,并对其性能进行了研究。
通过实验,我们掌握了锰铁钴镍合金的制备方法,了解了其物理、化学性质,分析了其微观结构,为锰铁钴镍合金的应用提供了理论依据。

铬锰铁钴实验报告实验报告铬锰铁钴实验报告一、实验目的本次实验旨在合成铬锰铁钴合金,并对其性质进行研究。
二、实验原理铬锰铁钴合金是一种强度高、韧性好的合金材料,主要的作用是用来制造高强度的结构钢和耐蚀合金。
其合成的主要反应方程式如下:MnO2 + 4Fe2++ 2Cr2O72- + 8Co2+ → 4MnO4- + 4Fe3+ + 4Cr3+ + 4Co3+ (1)Fe3+ + 3Co2+ → Fe2+ + 3Co3+ (2)通过反应方程式可以看出,该合金的制备需要四种金属离子Mn2+、Fe2+、Cr2O72-、Co2+。
在实验过程中,首先将氧化钴、氧化铁、氧化钙和过量的硫酸进行混合,再在高温条件下升温反应,反应后得到的铬锰铁钴合金是一种具有高强度和良好的低温韧性的优质材料。
三、实验步骤1.将氧化钴、氧化铁、氧化钙和过量的硫酸进行混合。
2.混合物按照化学计量比置于反应釜中,升温至600℃。
3.将Cr2O72-、Co2+和过量的硫酸溶液混合后,滴加至反应中。
4.反应完成后,将反应釜取出,待其冷却。
5.将反应产物分别进行打磨、抛光,制备样品。
四、实验结果和分析通过XRD和SEM测试,得到了以下实验结果:1. XRD测试结果表明,反应产物为铬锰铁钴合金,合金中铬、锰、铁、钴的质量分数分别为15.2%、16.5%、44.8%、23.5%。
2. SEM测试图像表明,合金晶粒较为均匀,平均尺寸约为2.5μm。
3. 实验结果表明,所合成的铬锰铁钴合金的强度高、韧性好,很适合用来制造结构钢和耐蚀材料。
五、实验结论本次实验成功合成了铬锰铁钴合金,结果表明该合金具有较高的强度和韧性,很适合用来制造高强度的结构钢和耐蚀材料。
本实验为合成铬锰铁钴合金提供了一种可行的方法。
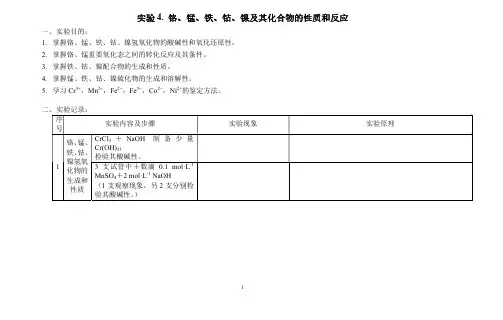
实验4. 铬、锰、铁、钴、镍及其化合物的性质和反应
一、实验目的:
1.掌握铬、锰、铁、钴、镍氢氧化物的酸碱性和氧化还原性。
2.掌握铬、锰重要氧化态之间的转化反应及其条件。
3.掌握铁、钴、镍配合物的生成和性质。
4.掌握锰、铁、钴、镍硫化物的生成和溶解性。
5.学习Cr3+,Mn2+,Fe2+,Fe3+,Co2+,Ni2+的鉴定方法。
1
2
3
4
三、注意事项:
1.在制备Mn(OH)2沉淀时,一定要用长滴管深入到溶液底部,将NaOH溶液挤出。
2.Cr(OH)3的颜色是灰绿色,容易被Cr3+的颜色掩盖,要注意观察。
加入NaOH溶液的速度不能太快,否则难以观察到沉淀
的生成。
3.在检验Ni(OH)2沉淀酸碱性时,要用比较强的氧化剂将其氧化。
四、思考题
教材中2、3、5题。
五、实验体会和建议
5。

一、实验目的1. 掌握铬锰铁钴合金的制备方法。
2. 了解铬锰铁钴合金的物理和化学性质。
3. 分析铬锰铁钴合金的性能特点,为实际应用提供参考。
二、实验原理铬锰铁钴合金是一种高强度、高韧性的合金材料,主要由铬(Cr)、锰(Mn)、铁(Fe)、钴(Co)和镍(Ni)五种元素组成。
通过调整元素的比例,可以改变合金的性能,使其适用于不同的领域。
三、实验材料与仪器1. 实验材料:铬、锰、铁、钴、镍金属粉末,氮气保护气氛炉,还原剂(如碳粉)。
2. 实验仪器:电子天平,磁力搅拌器,高温炉,金相显微镜,X射线衍射仪(XRD),扫描电镜(SEM),能谱仪(EDS)。
四、实验步骤1. 称取适量的铬、锰、铁、钴、镍金属粉末,按一定比例混合均匀。
2. 将混合好的金属粉末放入氮气保护气氛炉中,加热至一定温度,保持一定时间,使金属粉末充分反应。
3. 反应结束后,取出合金,冷却至室温。
4. 将合金进行切割、打磨、抛光,制备成金相样品。
5. 利用金相显微镜观察合金的微观组织结构。
6. 利用XRD、SEM和EDS分析合金的物相组成、晶体结构和元素分布。
7. 测试合金的力学性能,如抗拉强度、屈服强度、延伸率等。
五、实验结果与分析1. 合金微观组织结构:通过金相显微镜观察,发现铬锰铁钴合金的微观组织主要由晶粒、析出相和夹杂物组成。
随着合金成分的改变,晶粒尺寸和析出相的形态发生变化。
2. 物相组成:利用XRD分析,发现铬锰铁钴合金主要由固溶体和析出相组成。
固溶体主要由铬、锰、铁、钴和镍五种元素形成,析出相主要有金属间化合物和氧化物。
3. 力学性能:测试结果表明,铬锰铁钴合金具有较高的抗拉强度、屈服强度和延伸率。
随着合金成分的改变,力学性能发生变化。
例如,增加钴的含量可以提高合金的韧性。
4. 元素分布:利用SEM和EDS分析,发现铬锰铁钴合金中的元素分布较为均匀,无明显偏析现象。
六、结论与建议1. 铬锰铁钴合金具有较高的强度、韧性和耐腐蚀性,适用于航空航天、汽车工业、能源等领域。

一、实验目的1. 了解铬锰铁钴合金的制备过程;2. 掌握铬锰铁钴合金的成分及特性;3. 分析铬锰铁钴合金的性能;4. 评价铬锰铁钴合金在工程应用中的潜力。
二、实验原理铬锰铁钴合金是一种重要的合金材料,具有良好的耐腐蚀性、耐磨性和高温强度。
在本次实验中,我们通过熔融法制备铬锰铁钴合金,并对其成分、性能进行分析。
三、实验材料1. 铬(Cr):99.99%,金属粉末;2. 锰(Mn):99.99%,金属粉末;3. 铁(Fe):99.99%,金属粉末;4. 钴(Co):99.99%,金属粉末;5. 硼砂(Na2B4O7·10H2O):分析纯,用于熔融剂;6. 硅砂(SiO2):分析纯,用于熔融剂;7. 砂芯模具:用于制备合金锭;8. X射线衍射仪(XRD):用于分析合金的晶体结构;9. 红外光谱仪(IR):用于分析合金的表面成分;10. 扫描电镜(SEM):用于观察合金的微观形貌;11. 能谱仪(EDS):用于分析合金的元素成分。
四、实验步骤1. 称取适量的铬、锰、铁、钴金属粉末,按照一定比例混合均匀;2. 将混合后的金属粉末放入砂芯模具中;3. 将砂芯模具放入电阻炉中,升温至1500℃,保持2小时,使金属粉末熔融;4. 将熔融的金属液倒入预先准备好的砂芯模具中,自然冷却至室温;5. 使用X射线衍射仪(XRD)分析合金的晶体结构;6. 使用红外光谱仪(IR)分析合金的表面成分;7. 使用扫描电镜(SEM)观察合金的微观形貌;8. 使用能谱仪(EDS)分析合金的元素成分。
五、实验结果与分析1. 晶体结构分析:X射线衍射仪(XRD)结果显示,铬锰铁钴合金主要由面心立方(FCC)结构组成。
2. 表面成分分析:红外光谱仪(IR)结果显示,合金表面存在一定量的氧化物。
3. 微观形貌分析:扫描电镜(SEM)结果显示,铬锰铁钴合金具有较好的微观形貌,表面光滑,无明显的缺陷。
4. 元素成分分析:能谱仪(EDS)结果显示,合金中铬、锰、铁、钴的成分比例符合实验设计要求。

第1篇一、实验目的本次实验旨在通过一系列化学反应和物理实验,研究铁、钴、镍三种金属的性质,包括它们的还原性、氧化性、配合物生成以及磁性等。
通过对比实验结果,加深对这三种金属化学性质的理解。
二、实验原理1. 还原性:在还原反应中,金属原子失去电子,氧化态降低。
铁、钴、镍在酸性或碱性介质中表现出不同的还原性。
2. 氧化性:在氧化反应中,金属原子获得电子,氧化态升高。
铁、钴、镍的三价离子具有氧化性。
3. 配合物生成:金属离子与配体形成配合物,配体提供孤对电子与金属离子配位。
4. 磁性:铁、钴、镍为铁磁性材料,其磁性能受温度、磁场等因素影响。
三、实验内容1. 还原性实验(1)铁(II)的还原性:在酸性介质中,铁(II)具有还原性,可还原溴水中的溴离子。
实验结果显示,加入(NH4)2Fe(SO4)2溶液后,溶液颜色由黄色变为棕色,说明铁(II)具有还原性。
(2)钴(II)和镍(II)的还原性:在酸性介质中,钴(II)和镍(II)的还原性较弱,氯水不能将它们氧化。
实验结果显示,加入氯水后,溶液颜色无变化,说明钴(II)和镍(II)的还原性较弱。
2. 氧化性实验(1)三价铁的氧化性:在碱性介质中,三价铁具有氧化性,可将亚铁离子氧化为铁离子。
实验结果显示,加入氯水后,溶液颜色由浅绿色变为棕色,说明三价铁具有氧化性。
(2)三价钴和三价镍的氧化性:在碱性介质中,三价钴和三价镍具有氧化性,可被还原为二价离子。
实验结果显示,加入NaOH溶液后,溶液颜色由浅绿色变为蓝绿色,说明三价钴具有氧化性;加入氯水后,溶液颜色由蓝绿色变为棕色,说明三价钴具有氧化性。
3. 配合物生成实验(1)铁(II)配合物:在氨水存在下,铁(II)难以形成稳定的氨配合物。
实验结果显示,加入氨水后,溶液中出现白色沉淀,说明铁(II)难以形成稳定的氨配合物。
(2)钴(II)和镍(II)配合物:在氨水存在下,钴(II)和镍(II)可形成稳定的氨配合物。
实验结果显示,加入氨水后,溶液颜色由浅绿色变为深蓝色,说明钴(II)和镍(II)与氨形成了稳定的配合物。

实验七、八铬、锰、铁、铜、镍实验七、铬、锰、铁的分离实验原理铬酸钾是强氧化剂,可以氧化两性离子铁离子(Fe2+)和锰离子(Mn2+)为铁(Ⅲ)离子(Fe3+)和高锰酸钾(KMnO4),从而达到分离铁、锰的目的。
而对于铬离子(Cr3+),它稳定性较强,一般不受铬酸钾的氧化影响,所以通常需要采用还原剂还原铬离子。
实验步骤1. 取1ml Cr(SO4)3、2ml FeSO4+2、2ml MnSO4+4、2ml酒石酸溶液,放入试管中,加入10ml H2O。
2. 滴加2ml铬酸钾溶液,不断摇晃,加完静置5min,用移液器取样看有否沉淀。
3. 如出现沉淀,再滴加铬酸钾溶液至试管液体变为橙黄色,即Cr 3+反应完毕。
4. 向剩余液体中滴加过量柠檬酸钠溶液,完全还原Cr3+生成深绿色h2[Cr(C2O4)2]的沉淀。
5. 过滤, 分别收集上清液和沉淀, 洗涤。
6. 上清液置换直到呈红色,将滤液与分离的沉淀一同还原为各自的碳酸盐。
7. 过滤,将滤液收集。
8. 用稀盐酸取代锌粉还原出Mn2+与Fe2+溶解,观察颜色的变化,直至完全还原后色消失。
9. 分别加盐酸与氢氧化钠试液调节pH,使Mn红色,Fe红棕色。
再各自用氢氧化氨和氢醋酸沉淀Fe3+和Mn2+,并用去离子水来洗涤沉淀。
10. 过滤得到Fe3+和Mn2+的混合溶液。
实验八、铜、镍的分离实验原理对于含铜、镍的混合溶液,首先加入氨水,使其保持弱碱性,然后加入巯基乙酸(NH2CH2CH2SCH2COOH)。
巯基乙酸(H2L)可与铜离子生成成分子配合物,但对镍离子无影响。
在一定pH范围内,Cu(HL)+的络合物与[Ni(H2O)6]2+在NH3存在下的竞争,使镍离子不络合,从而实现了两种离子的分离。
实验步骤1. 取混合溶液1ml,加入NH3水溶液使其保持弱碱性,具体pH值需要用pH计测定。
2. 加入适量巯基乙酸溶液,凉过去放置约5分钟。
3. 用氯仿从混合溶液中提取得Cu(HL)2,NH3钠合对中所含有的镍离子的比较不溶的Ni(OH)2。
一、实验目的1. 了解铁钴镍合金的制备方法和特点;2. 掌握电解铁钴镍时的反应机理及控制技术;3. 熟悉常规化学分析方法的操作;4. 培养实验观察能力。
二、实验原理铁(Fe)、钴(Co)、镍(Ni)是周期表中的过渡金属元素,它们具有相似的化学性质。
在实验中,我们将通过电解法制备铁钴镍合金,并观察其物理和化学性质。
三、实验材料与仪器1. 实验材料:- 铁、钴、镍金属片- 硫酸- 硫酸铜- 氢氧化钠- 氯化钠- 碘化钾- 氢氧化铵- 氨水- 硫氰酸钾- 银氨溶液- 氢氧化钠溶液- 硫酸亚铁铵溶液2. 实验仪器:- 电解槽- 铂电极- 银电极- 滴定管- 烧杯- 烧瓶- 烧杯夹- 玻璃棒- 铁架台- 热水浴四、实验步骤1. 制备铁钴镍合金- 将铁、钴、镍金属片分别放入硫酸中,去除表面的氧化物。
- 将去除氧化物的金属片放入电解槽中,加入适量的硫酸铜溶液。
- 将铂电极和银电极分别插入电解槽中,连接电源。
- 开启电源,进行电解反应,直至金属片表面形成合金层。
- 关闭电源,取出金属片,用热水清洗。
2. 观察合金的性质- 将制备好的铁钴镍合金进行外观观察,记录其颜色、硬度等性质。
- 将合金进行导电性测试,记录其电阻值。
3. 分析合金成分- 将合金样品溶解于硫酸中,制备成溶液。
- 采用化学滴定法,分别测定铁、钴、镍的含量。
- 计算合金中各元素的摩尔比。
4. 研究合金的化学性质- 将合金样品溶解于氢氧化钠溶液中,观察其颜色变化。
- 将合金样品与碘化钾溶液反应,观察其颜色变化。
- 将合金样品与硫氰酸钾溶液反应,观察其颜色变化。
- 将合金样品与银氨溶液反应,观察其颜色变化。
五、实验结果与分析1. 铁钴镍合金的制备- 通过电解法制备的铁钴镍合金呈银灰色,硬度较高。
- 合金具有良好的导电性,电阻值为1.5×10^-4Ω·m。
2. 合金成分分析- 铁钴镍合金中,铁、钴、镍的摩尔比为2:1:1。
3. 合金的化学性质- 铁钴镍合金在氢氧化钠溶液中呈灰绿色,表明其具有一定的还原性。
实验1. 铬、锰、铁、钴、镍及其化合物的性质和反应
一、实验目的:
1.掌握铬、锰、铁、钴、镍氢氧化物的酸碱性和氧化还原性。
2.掌握铬、锰重要氧化态之间的转化反应及其条件。
3.掌握铁、钴、镍配合物的生成和性质。
4.掌握锰、铁、钴、镍硫化物的生成和溶解性。
5.学习Cr3+,Mn2+,Fe2+,Fe3+,Co2+,Ni2+的鉴定方法。
三、注意事项:
1.在制备Mn(OH)2沉淀时,一定要用长滴管深入到溶液底部,将NaOH溶液挤出。
2.Cr(OH)3的颜色是灰绿色,容易被Cr3+的颜色掩盖,要注意观察。
加入NaOH溶液的速度不能太快,否则难以观察到沉淀
的生成。
3.在检验Ni(OH)2沉淀酸碱性时,要用比较强的氧化剂将其氧化。
四、思考题
1. 在Co(OH)3 中加入浓HCl,有时会生成蓝色溶液,加水稀释后变为粉红色,试解释之。
2. K2Cr2O7溶液中加入Pb(NO3)2和AgNO3溶液会发生什么反应?
五、实验体会和建议。
实验八第一过渡系元素(二) (铁、钴、镍)
实验摘要:
为了了解铁、钴、镍的氧化还原性质和配合物特征,本实验用简单的方法完成了铁、钴、镍(Ⅱ、Ⅲ)氧化态的化合物的氧化还原及配合物实验。
结果表明铁、钴、镍(Ⅱ)均具有一定的还原性,并且依次减弱,而其(Ⅲ)氧化态化合物具有一定氧化性,且依次增强;铁、钴、镍(Ⅱ、Ⅲ)氧化态离子具有较强的形成配合物的能力,且与氨、硫氰根等能形成具有特殊颜色的配合物。
关键词:
铁(Ⅱ) 钴(Ⅱ) 镍(Ⅱ) 还原性铁(Ⅲ) 钴(Ⅲ) 镍(Ⅲ) 氧化性配合物
实验用品:
试管离心试管碘化钾淀粉试纸
实验内容:
二.铁(Ⅲ)、钴(Ⅲ)、镍(Ⅲ)化合物的氧化性
三.配合物的形成
1.铁的配合物
3.钴的配合物
4.镍的配合物
结果及讨论:
铁、钴、镍的氧化还原规律:二价氧化态均具有氧化性,其还原性依次减小,还原性受介质酸碱性影响,Fe2+无论在酸性介质还是碱性介质中均表现较强还原性,而Co2+、 Ni 2+主要在碱性介质中表现还原性;Fe3+、Co3+、Ni 3+均具有一定的氧化性,其氧化性依次增强,Fe3+在酸性溶液中有中等氧化能力。
铁、钴、镍的配合物特征: Fe2+、Co2+、 Ni2+、Fe3+、Co3+、Ni3+均具有较强的配位能力,主要形成四配位、六配位、八配位的配合物;不同配合物表现出特殊的颜色,配合物的电极电势降低,使得配合物氧化性低。
第一过渡系元素(铬、锰、铁、钴、镍)(3学时)一、实验目的及要求1.掌握铬、锰主要性质及个氧化态之间相互转化的条件。
2.练习沙浴加热操作。
3.试验并掌握二价铁、钴、镍的还原性和三价铁、钴、镍的氧化性。
4.实验并掌握铁、钴、镍配合物的生成及性质。
二、实验药品MnSO(0.2mol/L)、NaOH(aq)、HCl(aq)、重铬酸钾溶液、NH4C l(2mol/L)、H2SO4(6mol/L)、CoCl2(aq)、NiSO4(aq)、FeCl3(aq)、K4[Fe(CN)6]、氨水、MnO2(s)、KMnO4(aq)、NH4Cl(s)三、实验内容及步骤1、铬的化合物的重要性质(1).铬(Ⅵ)的氧化性Cr2O72-转变为Cr3+(2).铬(Ⅵ)的缩合平衡Cr2O72-与CrO42-相互转化(3).Cr(OH)3的两性(4).铬(Ⅲ)的还原性(5).重铬酸钾和铬酸盐的溶解性分别在CrO42-、Cr2O72-溶液中各加入少量的Pb(NO3)2、BaCl2、AgNO3、观察产物的颜色。
2、锰的化合物的重要性质(1).氢氧化锰的生成和性质第一份、往0.2mol/L MnSO4中加入少量氢氧化钠,观察沉淀的颜色。
第二份往0.2mol/L MnSO4中加入少量氢氧化钠,再加过量的氢氧化钠,观察现象第三份往0.2mol/L MnSO4中加入少量氢氧化钠,再加入盐酸,观察现象第四份往0.2mol/L MnSO4中加入少量氢氧化钠,再加氯化铵,观察现象(2).锰的化合物的重要性质1)Mn2+的氧化2)硫化锰的生成和性质3)二氧化锰的生成和氧化性(2).高锰酸钾的性质分别试验高锰酸钾与亚硫酸钠在中性、酸性、碱性介质中的反应。
3、铁(Ⅱ)、钴(Ⅱ)、镍(Ⅱ)的化合物的还原性(1)、铁(Ⅱ)的还原性1)酸性介质2)碱性介质(2).钴(Ⅱ)的还原性1)往盛有CoCl2溶液的试管中加入氯水,观察现象。
2)往两支分别盛有0.5mL0.5mol/L CoCl2溶液的试管中,滴加2mol/L NaOH溶液,制得两份沉淀,一份置于空气中,一份加入新配制的氯水,观察。
第十三章 过渡元素 (二) 铬 锰 铁 钴 镍 第一节 铬及其化合物第二节 锰及其化合物 第三节 铁 钴 镍第一节 铬及其化合物 1.1 铬单质 1.2 铬的化合物 1.3 铬盐1.4 含个废水的处理1.1铬单质1.铬分族(VIB ):Cr Mo W2. 价电子构型:(n-1)d 4~5ns 1~23. 铬以铬铁矿Fe(CrO 2)2的形式存在4. 单族的获得方式如下: 单质铬的性质 (1) 铬元素的电势图1.33 -0.41 -0.91 -0.74-1.3 -1.1 -1.4-1.3 2.性质(1)灰白色,熔点沸点高,硬度大 (2)活泼金属,表面已形成一层氧化膜, 活泼性下降(2) 无膜金属与盐酸的反应CrCr Cr O Cr /23272A ++-E Cr Cr(OH) Cr(OH) /CrO 2424B --E22)(2H Cr →+++(蓝)稀3+(紫)在冷,浓硝酸中钝化 1.2 铬的化合物 (1).Cr2O 3(铬绿)制备: 性质:(2).Cr(OH)3适量OH - 灰绿 OH - 亮绿色 Cr 3+ Cr(OH)3 Cr(OH)-4H 2O + Cr 2O 3(绿) 1.3 铬盐(1).Cr 3+盐Cr 2(SO 4)3, KCr(SO 4)212H O CrCl 3 1).水解2).还原性OH SO 3SO Cr )(SO 2H 2Cr 2234242++→+)(浓O4H N O Cr O Cr )(NH O 2Cr 3O 4Cr 2232Δ722432Δ2++−→−−→−+--+∆+→+++−→−+43222332Cr(OH)2OH O Cr O 3H O3H Cr H 6O Cr Δ++++H ]O Cr(OH)(H []O Cr(H [252362))410-≈K )g (3CO )s (2Cr(OH O 3H 3CO Cr 2)g (S 3H )s (Cr(OH O 6H 3S Cr 2232-23323223+−→−+++−→−+++-+))3).氧化性:(2).Cr 2O 72-与CrO 4-间的转化 ①pH 值的影响(黄) (橙)P h <2: Cr 2O 7为主 Ph>6: CrO42- 为主 ②溶解度的影响 (3).Cr 2O 7的氧化性O8H CrO 2OH O 3H 2Cr(OH)V 12.0)Cr(OH)/CrO (14H SO O Cr O H 7O S 32Cr V33.1)Cr /O Cr (224224-4424272Ag 228233272+→++-=++−−→−++=----+---++-+碱性条件:酸性条件:E E )配合物的多种颜色()蓝色III Cr 4Zn )(2Cr Zn(s)Cr 223++++→+绿色)蓝绿色)紫色,)O H 2Cl ]Cl O Cr(H [O H Cl ]Cl O Cr(H [Cl ]O Cr(H [22422252262⋅⋅O H O Cr 2HCrO 2H 2CrO 2272424+↔↔+--+-+-++-++-+--+−→−+++−→−+++−→−++⨯=⨯=2H )(s,2PbCrO O H O Cr 2Pb 2H )(s,2BaCrO O H O Cr 2Ba 2H )(s,CrO 2Ag O H O Cr 4Ag 10.02)O Cr (Ag 101.1)CrO (Ag 4227224227224222727722sp 1242sp 黄柠檬黄砖红K K O7H 2Cr 3Sn 14H 3Sn O Cr O 7H 2Cr 6Fe 14H 6Fe O Cr O7H 2KCl 2CrCl 3Cl )14HCl((s)O Cr K O7H 2Cr 3I 14H 6I O Cr O 7H 2Cr 3S 8H S 3H O Cr O H 4Cr 23SO H 83SO O Cr 1.33V)/Cr O (Cr 234227223322722327222322722322722324232723272++−→−++++−→−+++++−→−+++−→−++++−→−++++−→−++=++++-++++-++--++-+-+--+-浓E洗液:K 2Cr 2O 7饱和溶液+H 2SO 4(浓)暗红色,针状 (3) Cr (Ⅲ)的鉴定 H +蓝色 (乙醇)(戊醇)第二节 锰及其化合物1 锰单质 2. 锰的化合物1. 锰单质2.锰分族(ⅦB ):Mn Te Re 价电子构型:(n-1)d 5ns 2锰的存在:软锰矿(MnO 2*H 2O )锰单质的性质 ①白色金属,硬度脆②活泼金属:OH (s)2CrO SO K )(SO H O Cr K 234242722++−→−+浓---+−−−→−−−→−242243CrO O H Cr(OH)OH Cr-−−−−←2722222O Cr O H )2CrO(O O5H )2CrO(O 2H O 4H O Cr 22222272+−→−+++-O )H (C )CrO(O )CrO(O 2522222⋅−−→−乙醚O)H (C )CrO(O )CrO(O 2522222⋅−−→−乙醚 1.18V /Mn)(Mn 2-=+E 22222H (s)Mn(OH)O 2H Mn H Mn )(2H Mn +−→−++−→−+++稀③④ 2、锰的化合物 Mn 的价态电子构型:3d 54s 2 可形成多种氧化态:从+2~+7最高氧化数=价电子数 锰的电势图 酸性溶液E A /V1.695 1.23碱性溶液E B /V0.588 -0.05Mn (OH )2 (白色)二羧氧锰结论:Mn (Ⅱ)在碱性条件下不稳定(还原性强) 在酸性条件下稳定(还原性强) MnO 2①黑色无定形粉末,不溶于水和硝酸 ②不稳定性34222432MnF MnF F Mn F)(X MnX X Mn O Mn ΔO 2Mn 和−→−+≠−→−+−→−+O 2H MnO 2K 3O 4KOH 2Mn 2422+−−→−++熔融Mn18.1Mn 51.1Mn 95.0MnO 67.2MnO 564.0MnO 232244-++--Mn 56.1Mn(OH)10.0OH)(Mn 20.0MnO 60.0MnO 564.0MnO 232244-----),s (MnO(OH)O 21Mn(OH))(s,Mn(OH)2OH Mn 222222O无棕黄色白−→−+−−→−+-+O 2H Mn 2H Mn(OH))O(s,xH MnO O 1)H (x MnO(OH)2222222+−→−+⋅−→−-+++黑褐色2432O O Mn 3MnO C 530+−−−→−︒③氧化性强(主)④还原性(一定程度)浓碱溶液 MnS (肉色)重要反应方程式第三节 铁 钴 镍1 铁、钴、镍的单质2 铁、钴、镍的化合物 1. 铁、胡、镍的单质 Ⅶ族 Fe Co Ni 铁系 Ru Rh Pd Os Ir Pt 最高氧化值不等于族序数1. 单质的存在 赤铁矿:Fe 2O 3: 磁铁矿:Fe 3O 4黄铁矿:FeS 2O 2H O MnSO 2)(SO H 22MnO O 2H MnCl Cl )4HCl(MnO 2244222222++−→−+++−→−+浓浓O2H 3MnO 4OH 2MnO MnO 22442+−→−++----+++++−→−++−→−++2Ac S H Mn 2HAc MnS 2NH )MnS(s,2NH S H Mn 224322肉色+-++--++-++++-+++++−→−++++−→−++++−→−+++++−→−++6HO 7H 5HIO 2MnO O 8H (s)IO 5H 2Mn 16H 10SO 2MnO O 8H O 5S 2Mn O 2H 5Pb 2MnO 4H (s)5PbO 2Mn O 7H 5Na 5Bi2MnO 14H (s)5NaBiO 2Mn 23426222442-28222242223432-2342224242242CO 2MnO MnO 2CO 3MnO O2H 2MnO MnO 4H 3MnO ++−→−+++−→−+---+-OH SO 2MnO )(OH 2SO 2MnO 2OH SO 32MnO O H 3SO 2MnO O 3H 5SO 2Mn 6H 5SO 2MnO 224-24234-24222342242234++−→−++++−→−++++−→−++--------++--浓铂系辉铁矿:CoAsS 镍黄铁矿:NiS • FeS ; 2. 单质的物理性质(1) 白色金属,磁性材料 (2) m.p. Fe>CoNi 3. 单质的化学性质(1) Co.Ni 反应缓慢 (2)钝化浓、冷HNO 3可使Fe 、Co 、Ni 钝化 浓H2SO 4可使Fe 钝化(4) 纯Fe 、Co 、Ni 在水、空气中稳定加热时,Fe.,Co ,Ni 可与O2\ S ,X 2等反应 2、铁、钴、镍的化合物铁的重要化合物22H M )(2H M +−→−+++稀氢氧化物(慢)氯化羧铬(碱式氯化钴)还原性:Fe (Ⅱ)>Co (Ⅱ)>Ni (Ⅱ) 卤化物①FeCl 3有明显的共价性,易潮解。
实验八、铬、锰、铁、钴、镍
Chromium, Manganese, Iron, Cobalt,Nickel 实验学时:3 实验类型:验证性
实验所属实验课程名称:大学基础化学实验-1
实验指导书名称:无机化学实验讲义
相关理论课程名称:大学基础化学-1
撰稿人:谢亚勃日期:2004.11.8
一、目的与任务:
本实验属验证性实验,是过渡元素教学过程中的一部分,对本科生进行这部分的理解和探索能力的培养方面有重要的作用。
本实验将一部分课堂教学外的知识,放在实验课堂上进行研究。
使学生在获得课堂知识的基础上,进一步探索元素及化合物的其它重要性质和反应,巩固和加深理解课堂上所学基本理论和基本知识;使学生受到观察实验现象,研究实验问题,总结实验结果及基本技能的训
练,培养学生具有观察问题和分析问题的能力、严谨的科学态度、实事求是的作风、勇于创新的精神。
二、内容、要求与安排方式:
1、实验项目内容通过过渡元素性质的验证,对混合液设计分离鉴定方案,并通过实验对实验元素的性质进行总结。
2、实验要求要求通过实验加深对重要过渡元素和其化合物性质的理解,掌握定性分析的原理和方法,掌握过渡元素和化合物性质的重要递变规律。
3、为了使实验达到教学目标,对学生的要求如下:
(1)实验前要完成预习报告在阅读实验教材和参考资料的基础上,明确实验的目的和要求,弄清实验原理和方法,了解实验中的注意事项。
预习报告简明扼要,切忌抄书,字迹清晰,实验方案思路清晰。
(2)实验过程要求认真按照实验内容和操作规程进行实验。
如发现实验现象与理论不符,应独立思考,认真分
析查找原因,直到得出正确的结论。
认真观察实验现象,记录实验数据。
严格遵守实验室规则,爱护仪器设备,注意安全操作。
(3)实验记录要求在细心观察实验现象的基础上,将实验现象和数据记录预习报告上,不允许随手记在纸片或手上。
(4)实验报告要求实验报告是实验的总结,一般包括实验名称、实验目的、实验原理、实验现象、实验现象解释和讨论等几部分。
4、实验安排方式:本实验要求每一个学生独立完成,即1人/组。
三、场地与设备:
1、实验室名称:环化楼无机化学实验室,环化楼1407,使用面积100平方米
2、所用设备:pHS-3c酸度仪9台
3、消耗性器材:玻璃器
皿、化学试剂四、考核与成绩评定
1.考核内容对实验原理和基本知识的理解。
对基本操作和基本技术的掌握,对实验方法的掌握。
实验方案设计的是否合理。
实验报告书写的完整性和工整程度。
实验过程中的学习态度、综合能力、科学品德、科学精神。
2.成绩评定的方法:实验预习报告20%,实验操作30%,实验记录20%,实验报告30%。