2018版高中化学二轮复习训练题: 高考压轴大题特训 题型六 物质结构与性质(选考)
- 格式:doc
- 大小:534.50 KB
- 文档页数:7


河南省名校2018届高三压轴第二次考试理综化学试题1. 下列说法正确的是A. 天然植物油常温下一般呈液态,难溶于水,有恒定的熔点、沸点B. 饱和石灰水中加入少量CaO,恢复至室温后溶液的pH值不变C. 乙醇中含乙酸杂质:加入碳酸钠溶液洗涤,分液D. KClO3和SO3溶于水后能导电,故KClO3和SO3为电解质【答案】B【解析】A项,天然植物油常温下一般呈液态,难溶于水,天然植物油属于混合物,没有恒定的熔点、沸点,A项错误;B项,饱和石灰水中加入少量CaO,CaO与水发生反应:CaO+H2O=Ca (OH)2,溶剂水减少,Ca(OH)2增多,恢复至室温后析出Ca(OH)2固体,所得溶液仍为Ca (OH)2的饱和溶液,c(OH-)不变,溶液的pH不变,B项正确;C项,加入Na2CO3与乙酸反应生成CH3COONa、H2O和CO2,但乙醇与水以任意比互溶,不会出现分层现象,不能用分液法分离,C项错误;D项,KClO3属于电解质,SO3溶于水后能导电,但导电的离子不是SO3电离产生的,而是SO3与水反应生成的H2SO4电离产生的,SO3为非电解质,D项错误;答案选B。
点睛:本题考查天然油脂的物理性质、影响固体溶解度的因素、物质的分离和提纯、电解质的判断。
易错点是电解质的判断,电解质溶于水或熔融状态下能导电,导电的离子必须是电解质自身电离产生的,如SO2、SO3、NH3等化合物的水溶液也能导电,但导电的离子是由它们与水反应的生成物电离产生的,SO2、SO3、NH3等化合物属于非电解质。
2. 用N A表示阿伏加德罗常数的值,下列说法中正确的数目是①12.0g熔融的NaHSO4中含有的阳离子数为0.2N A②1mol Na2O 和Na2O2混合物中含有的阴、阴离子总数是3N A③常温常压下,92g的NO2和N2O4混合气体含有的原子数为6N A④7.8g中含有的碳碳双键数目为0.3N A⑤用1L1.0 mol/LFeCl3溶液制备氢氧化铁胶体,所得氢氧化铁胶粒的数目为N A⑥1mol SO2与足量O2在一定条件下充分反应生成SO3,共转移2N A个电子⑦在反应KIO3+6HI=KI+3I2 +3H2O 中,每生成3molI2转移的电子数为5N A⑧常温常压下,17 g甲基(一14CH3)中所含的中子数为9N AA. 3B. 4C. 5D. 6【答案】A【解析】①n(NaHSO4)==0.1mol,NaHSO4在熔融状态下的电离方程式为NaHSO4=Na++HSO4-,12.0g熔融的NaHSO4中含有的阳离子物质的量为0.1mol,①错误;②Na2O和Na2O2中阴、阳离子个数之比都为1:2,1molNa2O和Na2O2混合物中含有的阴、阳离子总物质的量为3mol,②正确;③NO2和N2O4的实验式都是NO2,n(NO2)==2mol,常温常压下92g的NO2和N2O4混合气体中所含原子物质的量为6mol,③正确;④苯中不含碳碳双键,④错误;⑤n(FeCl3)=1.0mol/L1L=1mol,根据反应FeCl3+3H2O Fe(OH)3(胶体)+3HCl,生成1molFe(OH)3,氢氧化铁胶粒是一定数目Fe(OH)3的集合体,氢氧化铁胶粒的物质的量小于1mol,⑤错误;⑥若1molSO2全部反应则转移2mol电子,而SO2与O2的反应是可逆反应,1molSO2与足量O2在一定条件下充分反应生成SO3,转移电子物质的量小于2mol,⑥错误;⑦用双线桥分析该反应:,每生成3molI2转移5mol电子,⑦正确;⑧n(-14CH3)==1mol,所含中子物质的量为8mol,⑧错误;正确的有②③⑦,答案选A。
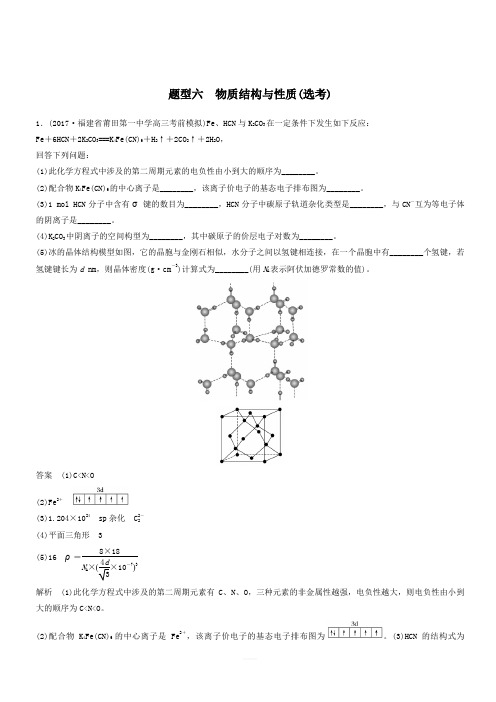
题型六 物质结构与性质(选考)1.(2017·福建省莆田第一中学高三考前模拟)Fe 、HCN 与K 2CO 3在一定条件下发生如下反应: Fe +6HCN +2K 2CO 3===K 4Fe(CN)6+H 2↑+2CO 2↑+2H 2O , 回答下列问题:(1)此化学方程式中涉及的第二周期元素的电负性由小到大的顺序为________。
(2)配合物K 4Fe(CN)6的中心离子是________,该离子价电子的基态电子排布图为________。
(3)1 mol HCN 分子中含有σ键的数目为________,HCN 分子中碳原子轨道杂化类型是________,与CN -互为等电子体的阴离子是________。
(4)K 2CO 3中阴离子的空间构型为________,其中碳原子的价层电子对数为________。
(5)冰的晶体结构模型如图,它的晶胞与金刚石相似,水分子之间以氢键相连接,在一个晶胞中有________个氢键,若氢键键长为d nm ,则晶体密度(g·cm -3)计算式为________(用N A 表示阿伏加德罗常数的值)。
答案 (1)C<N<O(2)Fe 2+(3)1.204×1024sp 杂化 C 2-2 (4)平面三角形3 (5)16 ρ=8×18N A ×(4d 3×10-7)3解析 (1)此化学方程式中涉及的第二周期元素有C 、N 、O ,三种元素的非金属性越强,电负性越大,则电负性由小到大的顺序为C<N<O 。
(2)配合物K 4Fe(CN)6的中心离子是 Fe 2+,该离子价电子的基态电子排布图为。
(3)HCN 的结构式为H—C≡N,1 mol HCN分子中含有σ键的数目为2N A,HCN分子中碳原子轨道杂化类型是sp杂化,CN-有2个原子和10个价电子,则与CN-互为等电子体的阴离子为C2-2。


题型六物质结构与性质(选考)1.自然界存在的元素中,金属元素种类更多,非金属元素丰度更大。
Ⅰ.80%左右的非金属元素在现代技术包括能源、功能材料等领域占有极为重要的地位。
(1)氮及其化合物与人类生产、生活息息相关,基态N原子的价电子排布图是________________,N2F2分子中N原子的杂化方式是________,1 mol N2F2含有________个σ键。
(2)高温陶瓷材料Si3N4晶体中键角N—Si—N________(填“>”、“<”或“=”)Si—N—Si,原因是________________________________________________________________________。
Ⅱ.金属元素在现代工业中也占据极其重要的地位。
其中钛也被称为“未来的钢铁”,具有质轻、抗腐蚀、硬度大,是宇航、航海、化工设备等的理想材料,是一种重要的战略资源,越来越受到各国的重视。
(1)基态钛原子核外共有________种运动状态不相同的电子。
金属钛晶胞如下图1所示,为________(填堆积方式)堆积。
(2)纳米TiO2是一种应用广泛的催化剂,其催化的一个实例如下图2。
化合物乙的沸点明显高于化合物甲,主要原因是__________________________________________________。
化合物乙中采取sp3杂化的原子的电负性由大到小的顺序为________________________________________________________________________。
(3)钙钛矿晶体的结构如图3所示。
假设把氧离子看作硬球接触模型,钙离子和钛离子填充氧离子的空隙,氧离子形成正八面体,钛离子位于正八面体中心,钙离子位于立方晶胞的体心,一个钙离子被________个氧离子包围。
钙钛矿晶体的化学式为________________。

2018全国Ⅱ卷高考压轴卷理科综合化学测试可能用到的相对原子质量:H 1 Li 7 C 12 N 14 O 16 S 32 K39 Cr 52 Mn 55 Fe 567. X、Y、Z、W为原子序数依次增大的四种短周期主族元素,X的一种单质具有杀菌、消毒能力,Y单质与X单质在不同条件下反应会生成两种不同化合物,Z简单离子半径是同周期元素简单离子中最小的,W原子最外层电子数是其电子层数的2倍。
下列说法不正确的是A. 气态氢化物的稳定性:X>WB. Y、Z、W的最高价氧化物对应水化物之间能两两反应C. 原子半径:Y>Z>W>XD. 工业上获得Y、Z单质的主要方法是电解其熔融的氯化物...8.下列有关物质的分类或归类不正确的是()①混合物:石炭酸、福尔马林、水玻璃、水银②化合物:CaCl2、烧碱、苯乙烯、HD③电解质:明矾、冰醋酸、硫酸钡④纯净物:干冰、冰水混合物、浓硫酸、水晶⑤同素异形体:足球烯、石墨、金刚石⑥同系物:CH2O2、C2H4O2、C3H6O2、C4H8O2.A.①②③④ B.②④⑤⑥ C.①③④⑤ D.①②④⑥9.N A代表阿伏加德罗常数,下列说法正确的是()A.同一物质的固、液、气三种状态的熵相同B.0.1 mol铁在0.1 mol Cl2中充分燃烧,有0.3N A个电子转移C.等物质的量的钠分别在足量的氧气和氯气中燃烧,转移电子数相等D.1.5 mol NO2与足量H2O反应,转移的电子数为2N A10.下列有关实验装置进行的相应实验,能达到实验目的是()A .用图1装置制取并收集干燥纯净的NH 3B .用图2所示装置可除去NO 2中的NOC .用图3所示装置可分离CH 3COOC 2H 5和饱和碳酸钠溶液D .用图4装置制备Fe (OH )2并能较长时间观察其颜色11.有机物A 的结构简式为:则A 的同分异构体中带苯环的化合物共有( ) A .3种 B .4种 C .5种 D .6种12.进行化学实验,观察实验现象,通过分析推理得出正确的结论是化学学习的方法之一。
1.(1)元素的第一电离能:N________O(填“>”或“<”)。
(2)基态Fe2+的电子排布式为___________________________________________________。
(3)在N、Mg、Al、Si四种元素中,有一种元素的电离能数据如下:电离能I1I2I3I4…I n/kJ·mol-1578 1 817 2 745 11 575 …则该元素的元素符号是________。
(4)NO-3的空间构型______________________________(用文字描述),SO2-4中硫原子的杂化方式为________________________。
(5)硅烷(Si n H2n+2)的沸点与其相对分子质量的变化关系如图所示,呈现这种变化关系的原因是_________________________________________________。
(6)金属铜原子的堆积方式为面心立方最密堆积,铜的原子半径为r nm,则铜晶胞的体积表达式为________ cm3。
答案:(1)>(2)1s22s22p63s23p63d6(3)Al(4)平面三角形sp3杂化(5)硅烷是分子晶体,相对分子质量越大,沸点越高(6)1.6 2×10-20r32.氟在自然界中常以CaF2的形式存在。
(1)下列有关CaF2的表述正确的是________。
a.Ca2+与F-间仅存在静电吸引作用b.F-的离子半径小于Cl-,则CaF2的熔点高于CaCl2c.阴阳离子比为2∶1的物质,均与CaF2晶体构型相同d .CaF 2中的化学键为离子键,因此CaF 2在熔融状态下能导电(2)CaF 2难溶于水,但可溶于含Al 3+的溶液中,原因是________(用离子方程式表示)。
已知AlF 3-6在溶液中可稳定存在。
(3)F 2通入稀NaOH 溶液中可生成OF 2,OF 2分子构型为________,其中氧原子的杂化方式为________。
物质结构1.X、Y、Z、W是原子序数依次增大的四种短周期元素。
Y和Z位于同一周期,可组成常见的共价化合物YZ和YZ2,X和Z的原子最外层电子数之和等于W的原子最外层电子数,25℃时0.01mol/L X和W形成化合物的水溶液pH为2。
下列说法正确的是()A.Y元素含氧酸的酸性比W的弱B.Z和W在自然界均能以游离态存在C.YZ和YZ2均可以被NaOH溶液吸收D.X和Y能形成既含极性键又含非极性键的分子【答案】D2.X、Y、Z、W、R均为短周期主族元素,原子序数依次增加,X、与W、Y与R分别同主族。
Z在短周期元素中金属性最强,W元素原子的次外层电子数为最外层电子数的2倍,R的原子序数是Y的2倍。
下列叙述错误的是()A.原子半径:W>YB.最高价含氧酸酸性:W>RC.气态氢化物稳定性:Y>RD.简单离子半径:Y>Z【答案】B3.短周期主族元素X、Y、Z、W的原子序数依次增大,X、Y、Z原子的最外层电子数之和为12,Y、Z、W位于同一周期,Z原子的最外层电子数既是X原子内层电子总数的3倍,又是Y原子最外层电子数的3倍。
下列说法不正确的是()A.原子半径:Y>X,离子半径Z<WB.元素Y的单质能与元素X的最高价氧化物发生置换反应C.元素Y和W能形成YW2型离子化合物D.W的单质有毒,能使湿润的有色布条褪色【答案】A4.下列事实不能..用元素周期律解释的是()A.气态氢化物的稳定性:HBr > HIB.0.1 mol·L-1溶液的pH:NaOH > LiOHC.向Na2SO3溶液中加盐酸,有气泡产生D.Mg、Al与同浓度盐酸反应,Mg更剧烈【答案】C5.短周期元素X、Y、Z、W在元素周期表中的相对位置如图所示,其中Y原子的最外层电子数是其电子层数的3倍。
下列说法正确的是()A.元素Y和元素Z的最高正化合价相同B.单核阴离子半径的大小顺序为:r(W)>r(Y)>r(Z)C.气态氢化物的热稳定性顺序为:X<Y<ZD.元素W的最高价氧化物对应水化物的酸性最强【答案】D6.元素X、Y、Z原子序数之和为36,X、Y在同一周期,X+与Z2-具有相同的核外电子层结构.下列推测不正确的是()A.同周期元素中X的金属性最强B.原子半径X>Y,离子半径X+>Z2-C.同族元素中Z的氢化物稳定性最高D.同周期元素中Y的最高价含氧酸的酸性最强【答案】B7.原子序数依次增大的元素a、b、c、d,它们的最外层电子数分别为1、6、7、1。
第15讲物质结构与性质(选考)非选择题(本题包括5个小题,共100分)1.(2017江苏化学,21)铁氮化合物(Fe x N y)在磁记录材料领域有着广泛的应用前景。
某Fe x N y的制备需铁、氮气、丙酮和乙醇参与。
(1)Fe3+基态核外电子排布式为。
(2)丙酮()分子中碳原子轨道的杂化类型是,1 mol丙酮分子中含有σ键的数目为。
(3)C、H、O三种元素的电负性由小到大的顺序为。
(4)乙醇的沸点高于丙酮,这是因为。
(5)某Fe x N y的晶胞如图1所示,Cu可以完全替代该晶体中a位置Fe或者b位置Fe,形成Cu 替代型产物Fe(x-n)Cu n N y。
Fe x N y转化为两种Cu替代型产物的能量变化如图2所示,其中更稳定的Cu替代型产物的化学式为。
图1Fe x N y晶胞结构示意图图2转化过程的能量变化2.(2017福建泉州二模)M、R、X、Y为原子序数依次增大的短周期主族元素,Z是一种过渡元素。
M基态原子L层中p能级电子数是s能级电子数的2倍,R是同周期元素中最活泼的金属元素,X和M形成的一种化合物是引起酸雨的主要大气污染物,Z的基态原子4s和3d能级半充满。
请回答下列问题:(1)R基态原子的电子排布式是,X和Y中电负性较大的是(填元素符号)。
(2)X的氢化物的沸点低于与其组成相似的M的氢化物,其原因是。
(3)X与M形成的XM3分子的立体构型是。
(4)M和R所形成的一种离子化合物R2M晶体的晶胞如下图所示,则图中黑球代表的离子是(填离子符号)。
(5)在稀硫酸中,Z的最高价含氧酸的钾盐(橙色)氧化M的一种氢化物,Z被还原为+3价,该反应的化学方程式是。
3.(2017安徽黄山二模)金属钛性能优越,被誉为继Fe、Al后应用广泛的“第三金属”。
(1)Ti基态原子的价电子排布式为。
(2)钛能与B、C、N、O等非金属元素形成稳定的化合物。
电负性:C B(填“>”或“<”,下同);第一电离能:N O,原因是。
题型六 物质结构与性质(选考)1.(2017·福建省莆田第一中学高三考前模拟)Fe 、HCN 与K 2CO 3在一定条件下发生如下反应: Fe +6HCN +2K 2CO 3===K 4Fe(CN)6+H 2↑+2CO 2↑+2H 2O ,回答下列问题:(1)此化学方程式中涉及的第二周期元素的电负性由小到大的顺序为________。
(2)配合物K 4Fe(CN)6的中心离子是________,该离子价电子的基态电子排布图为________。
(3)1 mol HCN 分子中含有σ键的数目为________,HCN 分子中碳原子轨道杂化类型是________,与CN -互为等电子体的阴离子是________。
(4)K 2CO 3中阴离子的空间构型为________,其中碳原子的价层电子对数为________。
(5)冰的晶体结构模型如图,它的晶胞与金刚石相似,水分子之间以氢键相连接,在一个晶胞中有________个氢键,若氢键键长为d nm ,则晶体密度(g·cm -3)计算式为________(用N A 表示阿伏加德罗常数的值)。
答案 (1)C<N<O(2)Fe 2+(3)1.204×1024 sp 杂化 C 2-2(4)平面三角形 3(5)16 ρ=8×18N A ×(4d 3×10-7)3 解析 (1)此化学方程式中涉及的第二周期元素有C 、N 、O ,三种元素的非金属性越强,电负性越大,则电负性由小到大的顺序为C<N<O 。
(2)配合物K4Fe(CN)6的中心离子是 Fe2+,该离子价电子的基态电子排布图为。
(3)HCN的结构式为H—C≡N,1 mol HCN分子中含有σ键的数目为2N A,HCN分子中碳原子轨道杂化类型是sp杂化,CN-有2个原子和10个价电子,则与CN-互为等电子体的阴离子为C2-2。
(4)CO2-3中碳原子价层电子对个数=3+12(4+2-3×2)=3,且不含孤电子对,所以C原子采用sp2杂化,空间构型为平面三角形。
(5)每个冰晶胞平均占有分子个数=4+18×8+6×12=8,H2O的氧原子中含有2个σ键和2个孤电子对,金刚石中每个碳原子含有4个σ键且没有孤电子对,所以水中的O和金刚石中的C都是sp3杂化,且水分子间的氢键具有方向性,每个水分子中一个氧原子可以和另外2个水分子中的氢原子形成2个氢键,2个氢原子可以和另外2个水分子中的氧原子形成氢键,所以每个水分子可与相邻的4个水分子形成4个氢键,即平均每个水分子可形成2个氢键,每个晶胞中共有2×8=16个氢键;若氢键键长为d nm,晶胞的对角线为4d nm,设晶胞边长为a nm,则a=4d3nm,晶胞的体积为(a nm)3,晶胞的质量为8×18 gN A,晶体密度=8×18 gN A÷(a nm)3=8×18N A×(4d3×10-7)3g·cm-3。
2.(2017·广东省华南师大附中高三三模)X、Y、Z、W、U五种元素,均位于周期表的前四周期,它们的核电荷数依次增加,且核电荷数之和为54。
X的激发态原子电子排布式为2p1,Y原子的基态原子有3个不同的能级,且各能级中电子数相等,Z的基态原子中有3个未成对电子,W的电离能如下表所示,U原子的K层电子数与最外层电子数之比为2∶1,其d轨道处于全充满状态。
(1)U原子电子排布式为________________________。
(2)X与Z 形成的化合物Z2X4,Z原子采取的杂化轨道类型为________,Y的最高价氧化物的水化物的正盐的阴离子的空间构型为____________。
(3)W的氯化物和Mg的氯化物中,熔点较高的是________________________(填化学式),原因是________________________________________________________________________________________________________________________________________________。
(4)I4O9由一种阳离子和一种阴离子按物质的量比1∶3构成,阴离子的空间构型为三角锥形,中心原子杂化类型为sp3杂化,写出I4O9的电离方程式_______________________________________________________________________________________________________。
(5)Nb(黑球)和I(白球)能形成一种线性的无机高分子化合物,其结构是许多八面体通过棱边而联结起来的长链,如下图所示。
则该化合物中Nb和I的原子个数比为________。
答案(1)1s22s22p63s23p63d104s1(2)sp3平面三角形(3)MgCl2NaCl和MgCl2都为离子晶体,Mg2+半径小,电荷数大,因此MgCl2晶体的晶格能大,熔点高(4)I4O9===I3++3IO-3(5)1∶4解析X、Y、Z、W、U五种元素,均位于周期表的前四周期,它们的核电荷数依次增加,且核电荷数之和为54。
X的激发态原子电子排布式为2p1,X是H;Y原子的基态原子有3个不同的能级,且各能级中电子数相等,Y是C;Z的基态原子中有3个未成对电子,Z是N;W的第二电离能远大于第一电离能,所以W是第ⅠA族元素,W是Na;U原子的K层电子数与最外层电子数之比为2∶1,其d轨道处于全充满状态,所以U是铜。
(1)铜的原子序数是29,原子电子排布式为1s22s22p63s23p63d104s1。
(2)X与Z 形成的化合物N2H4的分子中N原子的价层电子对数是4,含有一对孤对电子,则N原子采取的杂化轨道类型为sp3;C的最高价氧化物的水化物的正盐的阴离子CO2-3中C原子的价层电子对数是3,不存在孤对电子,其空间构型为平面三角形。
(3)由于NaCl和MgCl2都为离子晶体,Mg2+半径小,电荷数大,因此MgCl2晶体的晶格能大,熔点高。
(4)I4O9由一种阳离子和一种阴离子按物质的量比1∶3构成,阴离子的空间构型为三角锥形,中心原子杂化类型为sp3杂化,所以阴离子是IO-3,则阳离子是I3+,因此I4O9的电离方程式为I4O9===I 3++3IO-3。
(5)根据晶胞结构可知一个正八面体中含有1个Nb,I原子个数是2+4×12=4,所以该化合物中Nb和I的原子个数比为1∶4。
3.(2017·桂林市第十八中学高三下学期适应性考试)硒化锌是一种透明色半导体,也可作为红外光学材料,熔点是1 520 ℃。
(1)基态锌原子的价电子排布式是____________________________________。
(2)根据元素周期律,电负性Se________S,第一电离能Se________As(填“>”或“<”)。
(3)H2S分子的电子式:________________,H2Se分子构型是________________,其中硒原子的杂化轨道类型是________。
(4)H2O的沸点高于H2Se的沸点(-42 ℃),其原因是___________________________________________________________________________________________________。
(5)晶体Zn为六方最密堆积,其配位数是________。
(6)ZnSe晶胞如图,假设阿伏加德罗常数的值为N A,则144 g ZnSe晶体中的晶胞数是________。
答案(1)3d104s2(2)< <(3) V 形 sp 3(4)水分子间存在氢键、H 2Se 分子间无氢键(5)12 (6)N A 4解析 (1)本题考查价电子和排布式,Zn 位于第四周期ⅡB 族,价电子包括最外层电子和次外层d 能级,排布式为3d 104s 2。
(2)考查电负性规律和第一电离能规律,非金属性越强,电负性越强,同主族从上到下非金属性减弱,即电负性:Se<S ;同周期从左向右第一电离能增大,但第ⅡA>第ⅢA,第ⅤA>第ⅥA,因此第一电离能:Se<As 。
(3)考查电子式书写、分子构型的判断,H 2S 的电子式为,H 2Se 中心原子Se 有2个σ键,孤电子对数为(6-2×1)/2=2,分子构型为V 形。
(4)考查分子间氢键对物质物理性质的影响,H 2O 中存在分子间氢键,H 2Se 不存在分子间氢键,因此H 2O 的熔、沸点高于H 2Se 。
(5)考查金属晶体堆积方式,Zn 是六方最密堆积,其配位数为12。
(6)考查晶胞的计算,根据晶胞的结构,Zn 位于内部,Se 位于顶点和面心,因此1个晶胞中含有4个ZnSe ,其质量为4N A ×144 g,因此144 g ZnSe 含有晶胞的个数为N A 4。
4.(2017·河北省衡水中学高三第二次模拟考试)氮和磷元素的单质和化合物在农药生产及工业制造业等领域用途非常广泛,请根据提示回答下列问题:(1)科学家合成了一种阳离子为“N n +5”,其结构是对称的,5个N 排成“V”形,每个N 原子都达到8电子稳定结构,且含有2个氮氮三键;此后又合成了一种含有“N n +5”化学式为“N 8”的离子晶体,其电子式为_______________________________________________________________________________________________________________________, 其中的阴离子的空间构型为________。
(2)2001年德国专家从硫酸铵中检出一种组成为N 4H 4(SO 4)2的物质,经测定,该物质易溶于水,在水中以SO 2-4和N 4H 4+4两种离子的形式存在。
N 4H 4+4根系易吸收,但它遇到碱时会生成类似白磷的N 4分子,不能被植物吸收。
1个N 4H 4+4中含有________个σ键。
(3)氨(NH 3)和膦(PH 3)是两种三角锥形气态氢化物,其键角分别为107°和93.6°,试分析PH 3的键角小于NH 3的原因____________________________________________________________________________________________________________________________________________________________________________________________________。