化学自制教具——启普发生器
- 格式:doc
- 大小:21.00 KB
- 文档页数:1

启普发生器制备二氧化碳及二氧化碳的性质探究( 韦春莉 10111550109 )一、启普发生器制备二氧化碳1、启普发生器是一种实验室常用的气体发生装置,以荷兰的D.J.启普的姓命名。
它用普通玻璃制成,构造见下图。
适用于块状固体与液体在常温下反应制取难溶的气体,如氢气、二氧化碳,硫化氢等。
块状固体在反应中很快溶解或变成粉末时,不能用启普发生器。
只要生成的气体难溶于反应液才可,如二氧化碳可溶于水,但难溶于盐酸,故用石灰石与盐酸反应制二氧化碳时可用启普发生器。
启普发生器不能加热。
2、工作原理(以用稀盐酸和碳酸钙固体制取氢气为例)打开活塞,容器内压强与外界大气压相同,球形漏斗内的稀盐酸在重力作用下流到容器中,与碳酸钙接触,产生二氧化碳气体;关上活塞后,由于酸液继续与碳酸钙接触,二氧化碳气体依然生成,此时容器内部压强大于外界大气压,压力将酸液压回球形漏斗,使酸液与碳酸钙脱离接触,二氧化碳气体不再产生。
3、使用范围启普发生器是用固体与液体试剂在常温条件(不用加热)下起反应制取气体的典型装置。
如氢气、二氧化碳、硫化氢等均可以用它来制取。
但对于固体呈粉末状或固体与液体相遇后溶解或反应时产生高温者,如二氧化硫、二氧化氮等,都不适宜用此装置制取。
(一)启普发生器的使用方法1、启普发生器的气密性检查方法关闭导气管的活塞,继续从球形漏斗注入水至漏斗1/2处时,停止加水,并标记水面的位置,静置如下图(图1),然后观察水面是否下降。
若水面不下降,则表明不漏气。
若漏气,则应检查原因,可从导气管活塞、容器和胶塞以及球形漏斗的连接处去检查,并加以处理。
图一2、反应中途固体和液体反应的添换方法通常在反应中,固体反应物将近用完或液体(或溶液)浓度变稀时,反应变得缓慢,生成的气体不够用,则应添加固体或更换液体(或溶液)。
添加固体的方法:先关闭导气管的活塞,将球体内的液体压出,使其与固体脱离接触,然后用橡皮塞塞严球形漏斗的上口(防止球形漏斗里的液体下降冲入容器球体部分,使反应发生)。


简介英文名:Gas generators启普发生器一种实验室常用的气体发生装置,是荷兰科学家启普(Petrus Jacobus Kipp 1808~1864)发明,并以他的姓命名。
它用普通玻璃制成,构造见图。
它由球形漏斗、容器和导气管三部分组成。
适用于块状固体与液体在常温下反应制取气体,如氢气、硫化氢等。
块状固体在反应中很快溶解、或变成粉末时,不能用启普发生器。
如果生成气体难溶于反应液,可以使用。
如二氧化碳可溶于水,但难溶于盐酸;故用石灰石与盐酸反应制二氧化碳时可用启普发生器。
注意!启普发生器不能用于加热!气密性检查使用前应先检查装置的气密性。
方法:开启旋塞,向球形漏斗中加水。
当水充满容器下部的半球体时,关闭旋塞。
继续加水,使水上升到长颈漏斗中。
静置片刻,若水面不下降,则说明装置气密性良好,反之则说明装置漏气。
漏气处可能是容器上气体出口处的橡皮塞、导气管上的旋塞或长颈漏斗与容器接触的磨口处。
如漏气,应塞紧橡皮塞或在磨口处涂上一薄层凡士林。
启普发生器具体操作固体试剂由容器上的气体出口加入,加固体前应在容器的球体中加入一定量的玻璃棉或放入橡胶垫圈,以防固体掉入半球体中。
加固体的量不得超过球体容积的1/3。
液体试剂从长颈漏斗口注入,注液方法与上述注水方法相同。
液体的量以反应时刚刚浸没固体,液面不高过导气管的橡胶塞为宜。
使用时,打开导气管上的旋塞,长颈漏斗中的液体进入容器与固体反应,气体的流速可用旋塞调节。
停止使用时,关闭旋塞,容器中的气体压力增大,将液体压回长颈漏斗,使液体和固体脱离,反应停止。
为保证安全,可在球形漏斗口加安全漏斗(见图),防止气体压力过大时炸裂容器。
特点:符合“随开随用、随关随停”的原则。
能节约药品,控制反应速率和反应的发生和停止,可随时向装置中添加药品。
2规格容量/ml 底直径/mm中球直径/mm上球直径/mm全高/mm容量/ml底直径/mm中球直径/mm上球直径/mm全高/mm25012082903141000175130140450 5001459811036020002101601705803发明者启普发生器的发明人叫启普,是荷兰人,他生于1808年3月5日,1864年2月3日病故,终年57岁。
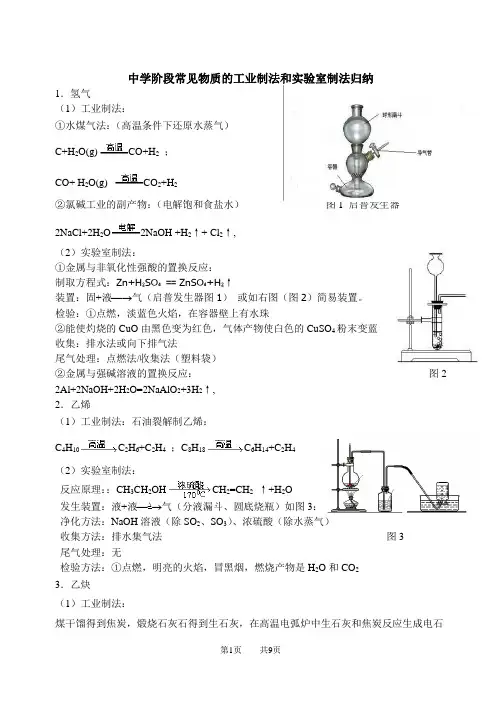
中学阶段常见物质的工业制法和实验室制法归纳1.氢气(1)工业制法:①水煤气法:(高温条件下还原水蒸气)C+H2O(g)CO+H2;CO+ H2O(g) CO2+H2②氯碱工业的副产物:(电解饱和食盐水)图1 启普发生器2NaCl+2H2O2NaOH +H2↑+ Cl2↑,(2)实验室制法:①金属与非氧化性强酸的置换反应:制取方程式:Zn+H₂SO₄== ZnSO₄+H₂↑装置:固+液−→气(启普发生器图1)或如右图(图2)简易装置。
检验:①点燃,淡蓝色火焰,在容器壁上有水珠②能使灼烧的CuO由黑色变为红色,气体产物使白色的CuSO4粉末变蓝收集:排水法或向下排气法尾气处理:点燃法/收集法(塑料袋)②金属与强碱溶液的置换反应:图2 2Al+2NaOH+2H2O=2NaAlO2+3H2↑,2.乙烯(1)工业制法:石油裂解制乙烯:C4H10C2H6+C2H4;C8H18C6H14+C2H4(2)实验室制法:反应原理::CH3CH2OH CH2=CH2↑+H2O发生装置:液+液−∆→气(分液漏斗、圆底烧瓶)如图3:净化方法:NaOH溶液(除SO2、SO3)、浓硫酸(除水蒸气)收集方法:排水集气法图3尾气处理:无检验方法:①点燃,明亮的火焰,冒黑烟,燃烧产物是H2O和CO23.乙炔(1)工业制法:煤干馏得到焦炭,煅烧石灰石得到生石灰,在高温电弧炉中生石灰和焦炭反应生成电石和一氧化碳,电石和饱和食盐水反应生成熟石灰和乙炔。
3C+CaO CaC2+CO↑;CaC2+2H2O Ca(OH)2+C2H2↑(2)实验室制法:反应原理:CaC2+2H2O −→ CH≡CH↑+Ca(OH)2发生装置:固+液−→气(分液漏斗、圆底烧瓶)如图4净化方法:CuSO4溶液、浓硫酸(除水蒸气)收集方法:排水集气法/向上排空气法尾气处理:无图4 4.一氧化碳(1)工业制法:①水煤气法:(高温条件下还原水蒸气)C+H2O(g)CO+H2;②焦炭还原二氧化硅(工业制备粗硅的副产物):2C+SiO2Si+2CO↑③工业制备电石的副产物:3C+CaO CaC2+CO↑;(2)实验室制法:制取原理:浓硫酸对有机物的脱水作用在蒸馏烧瓶里加入浓硫酸,在分液漏斗里盛放甲酸①甲酸分解法:HCOOH CO↑+H2O装置:分液漏斗,圆底烧瓶(图5)检验:燃烧,蓝色火焰,无水珠,产生气体能使澄清石灰水变浑浊除杂:通入浓硫酸(除水蒸气)收集:排水法尾气处理:点燃法/收集法(塑料袋)②草酸分解法:H2C2O4 CO↑+CO2↑+H2O ;混合气体通过碱石灰得到一氧化碳。
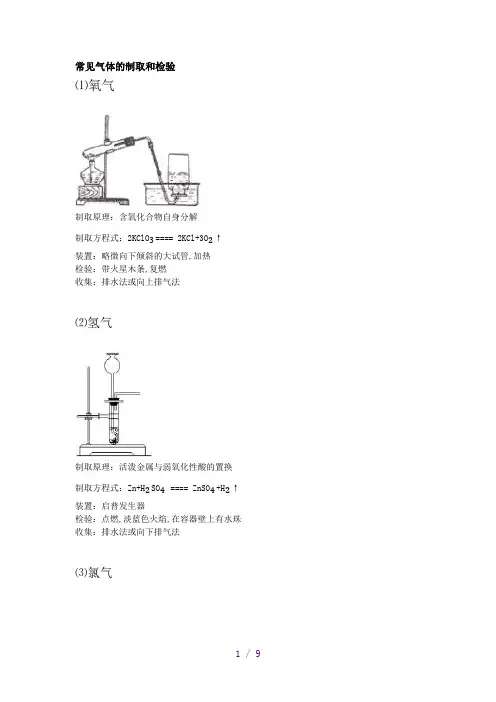
常见气体的制取和检验⑴氧气制取原理:含氧化合物自身分解制取方程式:2KClO₃==== 2KCl+3O₂↑装置:略微向下倾斜的大试管,加热检验:带火星木条,复燃收集:排水法或向上排气法⑵氢气制取原理:活泼金属与弱氧化性酸的置换制取方程式:Zn+H₂SO₄ ==== ZnSO₄+H₂↑装置:启普发生器检验:点燃,淡蓝色火焰,在容器壁上有水珠收集:排水法或向下排气法⑶氯气制取原理:强氧化剂氧化含氧化合物制取方程式:MnO₂+4HCl(浓) ====MnCl₂+Cl₂↑+2H₂O装置:分液漏斗,圆底烧瓶,加热检验:能使湿润的蓝色石蕊试纸先变红后褪色;除杂:先通入饱和食盐水(除HCl),再通入浓H₂SO₄ (除水蒸气)收集:排饱和食盐水法或向上排气法尾气回收:Cl₂+2NaOH==== NaCl+NaClO+H₂O⑷硫化氢制取原理:强酸与强碱的复分解反应制取方程式:FeS+2HCl====FeCl₂+H₂S↑装置:启普发生器检验:能使湿润的醋酸铅试纸变黑除杂:先通入饱和NaHS溶液(除HCl),再通入固体CaCl₂ (或P₂O5)(除水蒸气) 收集:向上排气法尾气回收:H₂S+2NaOH==== Na₂S+H₂O或H₂S+NaOH==== NaHS+H₂O ⑸二氧化硫制取原理:稳定性强酸与不稳定性弱酸盐的复分解制取方程式:Na₂SO₃+H₂SO₄==== Na₂SO₄+SO₂↑+H₂O 装置:分液漏斗,圆底烧瓶检验:先通入品红试液,褪色,后加热又恢复原红色;除杂:通入浓H₂SO₄ (除水蒸气)收集:向上排气法尾气回收:SO₂+2NaOH==== Na₂SO₃+H₂O⑹二氧化碳制取原理;稳定性强酸与不稳定性弱酸盐的复分解制取方程式:CaCO₃+2HCl====CaCl₂+CO₂↑+H₂O装置:启普发生器检验:通入澄清石灰水,变浑浊除杂:通入饱和NaHCO₃溶液(除HCl),再通入浓H₂SO₄ (除水蒸气) 收集:排水法或向上排气法⑺氨气制取原理:固体铵盐与固体强碱的复分解制取方程式:Ca(OH)₂+2NH₄Cl====CaCl₂+NH₃↑+2H₂O装置:略微向下倾斜的大试管,加热检验:湿润的红色石蕊试纸,变蓝除杂:通入碱石灰(除水蒸气)收集:向下排气法⑻氯化氢制取原理:高沸点酸与金属氯化物的复分解制取方程式:NaCl+H₂SO₄====Na₂SO₄+2HCl↑装置:分液漏斗,圆底烧瓶,加热检验:通入AgNO₃溶液,产生白色沉淀,再加稀HNO₃沉淀不溶除杂:通入浓硫酸(除水蒸气) 收集:向上排气法⑼二氧化氮制取原理:不活泼金属与浓硝酸的氧化—还原;制取方程式:Cu+4HNO₃(浓)====Cu(NO₃)₂+2NO₂↑+2H₂O 装置:分液漏斗,圆底烧瓶(或用大试管,锥形瓶)检验:红棕色气体,通入AgNO3溶液颜色变浅,但无沉淀生成收集:向上排气法尾气处理:3NO₂+H₂O====2HNO₃+NONO+NO₂+2NaOH====2NaNO₂+H₂O⑽一氧化氮制取原理:不活泼金属与稀硝酸的氧化—还原;制取方程式:Cu+8HNO₃ (稀) ====3Cu(NO₃)₂+2NO↑+4H₂O 装置:分液漏斗,圆底烧瓶(或用大试管,锥形瓶)检验:无色气体,暴露于空气中立即变红棕色收集:排水法⑾一氧化碳制取原理:浓硫酸对有机物的脱水作用在蒸馏烧瓶里加入浓硫酸,在分液漏斗里盛放甲酸制取方程式:HCOOH====CO↑+H₂O装置:分液漏斗,圆底烧瓶检验:燃烧,蓝色火焰,无水珠,产生气体能使澄清石灰水变浑浊除杂:通入浓硫酸(除水蒸气)收集:排水法⑿甲烷制取方程式:CH₃COONa+NaOH==== CH₄↑+Na₂CO₃装置:略微向下倾斜的大试管,加热收集:排水法或向下排空气法⒀乙烯制取原理:浓硫酸对有机物的脱水作用制取方程式:CH₃CH₂OH==== C₂H₄↑+H₂O装置:分液漏斗,圆底烧瓶,加热除杂:通入NaOH溶液(除SO₂,CO₂),通入浓硫酸(除水蒸气)收集:排水法⒁乙炔制取原理:电石强烈吸水作用制取方程式:CaC₂+2H₂O====Ca(OH)₂ +CH CH↑装置:分液漏斗,圆底烧瓶(或用大试管,锥形瓶)检验:无色气体,能燃烧,产生明亮的火焰,并冒出浓的黑烟除杂:通入硫酸铜溶液(除H₂S,PH3),通入浓硫酸(除水蒸气)收集:排水法或向下排气法(注:文档可能无法思考全面,请浏览后下载,供参考。

初高中化学衔接——启普发生器的构造和原理第一部分:知识点讲解知识点1:了解启普发生器的结构及工作原理启普发生器的构造和工作原理如图所示,启普发生器由三部分构成:1.球型漏斗 2.容器部分 3.带活塞的导管部分。
以实验室制氢气为例,使用时,开启活塞,酸由球形漏斗流入容器至其与锌粒接触,反应产生氢气。
关闭活塞,由于氢气压强增大,酸被压回球形漏斗,与锌粒脱离接触,反应停止。
知识点2 :理解启普发生器气密性检验原理启普发生器气密性检验关闭导气管上的活塞,从球形漏斗口处加入水,当水浸没球形漏斗下端后,继续加入水,球形漏斗内外会出现液面差,观察液面,在一段时间内不发生变化,表明气密性良好。
知识点3:掌握启普发生器简易装置的设计及原理第二部分教材剖析初中课标:不做要求高中课标:对启普发生器不做要求,但要求学生掌握由中学化学常见仪器组成的简易装置建议:作为实验教学衔接内容,补充启普发生器的有关知识第三部分教案示例启普发生器知识目标 1.了解启普发生器的结构及工作原理2. 掌握启普发生器简易装置的设计及原理能力目标能进行启普发生器简易装置的设计情感目标体验实验装置的设计和评价教学方法讲练结合教学过程一、展示并讲解启普发生器的结构及工作原理如图所示,启普发生器由三部分构成:1.球型漏斗,2.容器部分,3.带活塞的导管部分。
以实验室制氢气为例,使用时,开启活塞,酸由球形漏斗流入容器至其与锌粒接触,反应产生氢气。
关闭活塞,由于氢气压强增大,酸被压回球形漏斗,与锌粒脱离接触,反应停止。
二学生讨论:如何检验启普发生器的气密性?提示:启普发生器不能加热结论:使用液封法----关闭导气管上的活塞,从球形漏斗口处加入水,当水浸没球形漏斗下端后,继续加入水,球形漏斗内外会出现液面差,观察液面,在一段时间内不发生变化,表明气密性良好。
三、练习在没有现成的CO2气体发生器的情况下,请你选用下图中的部分仪器,装配成一个简易的、能随开随用、随关随停的CO2气体发生装置。

启普发生器的构造启普发生器是一种独特的、可重复使用的可靠电力供应设备,是一种基于磁学原理制作而成。
此类发生器是一种将动力转换成电能的装置,可以将交流电或直流电转换成另一种电能,以满足客户的电源需求。
其应用的范围不断拓宽,已经广泛应用在家庭应用、工业应用以及军事应用等领域。
启普发生器的结构可分为三部分:驱动机构、控制机构和动力机构。
驱动机构由发动机、变速箱、蜗轮蜗杆机构组成,是推动发生器转动的主要部件。
控制机构由控制器、调速器、安全阀和保护装置等组成,是控制发生器转速的关键部分。
动力机构由发电机、电器等组成,能够根据驱动机构的转动频率产生所需的能量,并提供稳定的电源电压和电流输出。
启普发生器的配备有许多保证发电安全、可靠性的设备。
例如,发电机就配备有温度传感器、湿度传感器,冷却系统,以及电子保护系统等,这些设备可以检测负荷状况,调节发电机的工作状态,并确保发电安全可靠。
此外,启普发生器还配备有调压调速装置、调压阀、故障报警装置,以及自检系统等设备,确保发电过程的安全稳定。
启普发生器的控制系统是由传感器、计算机和控制装置等组成的,负责实现发生器的自动化控制及状态监测等功能。
它能够实时检测发生器的运行状态,根据实时数据对发生器的控制参数进行调整和优化,从而有效地提高发生器的可靠性和安全性。
在控制系统和其他设备之外,启普发生器还拥有一种独特的磁结构,它起到了极大的作用。
启普发生器的核心部件是磁极体,它的磁性质对发电和调整转速至关重要。
磁极体结构的优点在于可以调整转速,并且转速变化时产生的磁力能够抵消摩擦和消除噪声,从而使发生器运行更加平稳、可靠。
总而言之,启普发生器之所以具有可靠性和高效性,是由其独特的结构及其精心配备的各种安全设备所决定的。
它们在家庭、工业生产以及军事应用中发挥着重要作用。
未来,启普发生器将会应用到更多领域,一定程度上改变我们的生活。

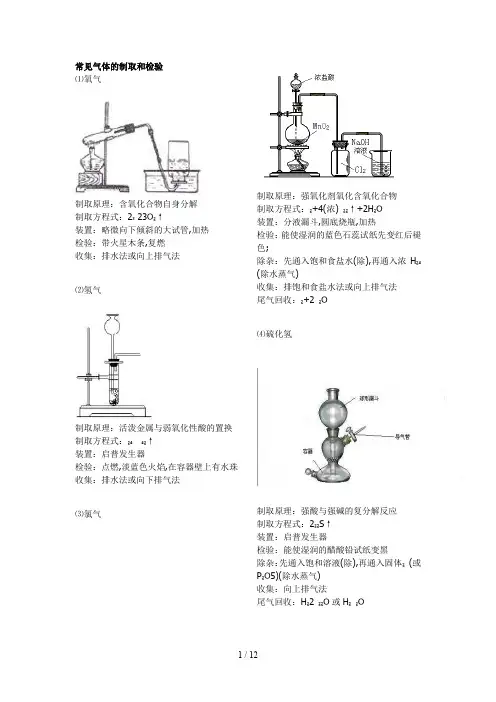
常见气体的制取和检验⑴氧气制取原理:含氧化合物自身分解制取方程式:2₃ 23O₂↑装置:略微向下倾斜的大试管,加热检验:带火星木条,复燃收集:排水法或向上排气法⑵氢气制取原理:活泼金属与弱氧化性酸的置换制取方程式:₂₄₄₂↑装置:启普发生器检验:点燃,淡蓝色火焰,在容器壁上有水珠收集:排水法或向下排气法⑶氯气制取原理:强氧化剂氧化含氧化合物制取方程式:₂+4(浓)₂₂↑+2H₂O装置:分液漏斗,圆底烧瓶,加热检验:能使湿润的蓝色石蕊试纸先变红后褪色;除杂:先通入饱和食盐水(除),再通入浓H₂₄(除水蒸气)收集:排饱和食盐水法或向上排气法尾气回收:₂+2 ₂O⑷硫化氢制取原理:强酸与强碱的复分解反应制取方程式:2₂₂S↑装置:启普发生器检验:能使湿润的醋酸铅试纸变黑除杂:先通入饱和溶液(除),再通入固体₂(或P₂O5)(除水蒸气)收集:向上排气法尾气回收:H₂2 ₂₂O或H₂₂O⑸二氧化硫制取原理:稳定性强酸与不稳定性弱酸盐的复分解制取方程式:₂₃₂₄₂₄₂↑₂O装置:分液漏斗,圆底烧瓶检验:先通入品红试液,褪色,后加热又恢复原红色;除杂:通入浓H₂₄(除水蒸气)收集:向上排气法尾气回收:₂+2 ₂₃₂O⑹二氧化碳制取原理;稳定性强酸与不稳定性弱酸盐的复分解制取方程式:₃+2₂₂↑₂O装置:启普发生器检验:通入澄清石灰水,变浑浊除杂:通入饱和₃溶液(除),再通入浓H₂₄(除水蒸气)收集:排水法或向上排气法⑺氨气制取原理:固体铵盐与固体强碱的复分解制取方程式:()₂+2₄₂₃↑+2H₂O装置:略微向下倾斜的大试管,加热检验:湿润的红色石蕊试纸,变蓝除杂:通入碱石灰(除水蒸气)收集:向下排气法⑻氯化氢制取原理:高沸点酸与金属氯化物的复分解制取方程式:₂₄₂₄+2↑装置:分液漏斗,圆底烧瓶,加热检验:通入₃溶液,产生白色沉淀,再加稀₃沉淀不溶除杂:通入浓硫酸(除水蒸气)收集:向上排气法⑼二氧化氮制取原理:不活泼金属与浓硝酸的氧化—还原;制取方程式:4₃(浓)(₃)₂+2₂↑+2H₂O装置:分液漏斗,圆底烧瓶(或用大试管,锥形瓶)检验:红棕色气体,通入3溶液颜色变浅,但无沉淀生成收集:向上排气法尾气处理:3₂₂2₃₂+22₂₂O⑽一氧化氮制取原理:不活泼金属与稀硝酸的氧化—还原;制取方程式:8₃ (稀)3(₃)₂+2↑+4H₂O装置:分液漏斗,圆底烧瓶(或用大试管,锥形瓶)检验:无色气体,暴露于空气中立即变红棕色收集:排水法⑾一氧化碳制取原理:浓硫酸对有机物的脱水作用在蒸馏烧瓶里加入浓硫酸,在分液漏斗里盛放甲酸制取方程式:↑₂O装置:分液漏斗,圆底烧瓶检验:燃烧,蓝色火焰,无水珠,产生气体能使澄清石灰水变浑浊除杂:通入浓硫酸(除水蒸气)收集:排水法高中化学实验总结一.中学化学实验操作中的七原则掌握下列七个有关操作顺序的原则,就可以正确解答“实验程序判断题”。

2016.7(总第94期)科技尚品 PREMIERE摘 要:启普发生器是制作氢气常用的实验装置,对闲置的启普发生器加以改造,同时辅以软木塞、橡皮塞、改造后的玻璃管、乳胶管、铁夹等材料,将启普发生器改造成制作果酒、果醋的发酵装置,进一步提高了制作果酒、果醋实验的可操作性,也同时完成了果酒发酵过程中产生的气体成分和酒精鉴定、发酵液中酵母菌种群数量变化的实验探究。
关键词:启普发生器;制作;果酒;果醋启普发生器是中学化学教学中常用于制作氢气的实验仪器,随着时代的发展,制作氢气的实验装置已被其他装置所替代,很多中学至今仍然存有启普发生器,由于长时间不用,大量的启普发生器被束之高阁,造成资源的浪费。
为了更好地发挥启普发生器在教学中的作用,我们对其进行了适当的改造,将其用来完成果酒和果醋的制作实验、探究果酒发酵过程中酵母菌种群数量变化的实验,取得了良好的教学效果,现将其的改造和使用方法介绍给大家。
1 启普发生器的改造(1)选取适当的橡皮塞,打孔备用,切取一段玻璃管,在酒精喷灯上加热、弯曲成一定的角度,插入橡皮塞的孔中,玻璃管的另一端套上一截乳胶管,乳胶管另一端套上一个去掉胶头的滴管,乳胶管中间夹上铁夹,制成导气管。
(启普发生器原有的导气装置的材质是磨砂玻璃,涂上凡士林以防漏气,但该装置的缺陷是,一旦启普发生器内的果汁在发酵过程中产生气体,使装置内的压力增加,就会将其冲脱出来)(2)收集喝葡萄酒后遗留下的酒瓶软木塞(开瓶时尽量不要损坏),用打孔器打孔,插入一截玻璃管,另一端套上一截乳胶管,用铁夹夹住,制成出料口装置。
(3)将启普发生器的漏斗取出不用,另取合适的橡皮塞,把启普发生器的上端瓶口塞住,启普发生器即改装成制备果酒、果醋的装置(见上图)。
2 使用2.1 果酒的制作(1)取新鲜的葡萄(或苹果等水果),或根据各地的实际情况,用当地所产的特有水果,将其冲洗干净,去其果枝,稍晾干。
(2)将榨汁机、启普发生器及其附属装置清洗干净,晾干,并用70%的酒精进行消毒。

自制教具的文字说明
一、教具名称:启普发生器
二、使用材料
一个广口瓶、一个胶塞、打孔器、一个注射器、一个小塑料瓶、弹簧夹、一截橡胶管、两个玻璃导管、若干根铁丝、剪刀等
三、简单制作
用打孔器给胶塞钻两个孔,一个孔上插注射器,另一个孔插带胶塞的导管。
用剪刀在小塑料瓶底部剪几个小孔。
用铁丝将小塑料瓶连接在注射器的活塞上。
用橡胶管将两个玻璃导管连接,然后将弹簧夹夹在橡胶管上。
这样一个简易的启普发生器就制作成功了。
四、使用方法:在打了孔的小塑料瓶中加入固体药品,酸直接加在广口瓶中。
打开弹簧夹,压下注射器的内管(即活塞),使带孔的小塑料瓶伸入液体中,这样小塑料瓶里的固体药品就和酸接触,从而发生反应。
关闭弹簧夹,稍等片刻,注射器的内管在压力作用下升起,带动着打孔的小塑料瓶共同上升,从而使固体药品和液体脱离,反应停止。
五、教具特点:
这个教具设计具有简单性、易行性、美观性,操作起来方便、可行,并且还具有自身的一些特点。
所使用的材料简单易得,可以拆洗,相对传统的启普发生器更方便使用。
传统启普发生器的原理是使液体排出。
此装置的原理是使固体脱离液体,能够调动学生的学习兴趣,促进学生的创新意识。
六、教具用途:
该教具用于化学反应中的固体和液体产生气体的反应,如实验室制取二氧化碳、氢气等
七、运用对象:八年级学生
29。
初三化学上册,启普发⽣器与其改进装置的应⽤讲解化学实验中,能随时控制反应的发⽣与停⽌的实验装置,对整个实验现象的观察起到⾮常重要的作⽤。
下⾯以稀盐酸和⼤理⽯反应制取⼆氧化碳为例,介绍⼏种能够控制反应发⽣与停⽌实验装置。
⼀、启普发⽣器启普发⽣器⼜称启⽒⽓体发⽣器,是荷兰科学家⽪特鲁斯-杰克巴斯-启普发明,并以他的姓命名。
启普发⽣器常⽤于固体颗粒物(块状固体)与液体反应制取⽓体的实验装置。
启普发⽣器的结构:球形漏⽃、容器、带旋塞的导⽓管。
启普发⽣器适⽤条件如下:①块状固体+液体⽣成⽓体的实验如:稀盐酸和⼤理⽯制取⼆氧化碳;稀盐酸和锌粒制取氢⽓;②固体必须是块状且不能溶于⽔;③反应不可产⽣⼤量热;④不需要加热的反应;启普发⽣器优点如下:①可以控制反应的发⽣与停⽌;②可以做到“随开随⽤、随关随停”;③可随时向装置中添加液体药品。
1、启普发⽣器的使⽤⽅法1.1、⽓密性的检查关闭放废液⼝的活塞,打开导⽓管上的旋塞,向球形漏⽃中加⽔,将球形漏⽃的下端浸没在⽔中,关闭导⽓管上的旋塞,继续向球形漏⽃中加⽔,待球形漏⽃中的⽔,与容器中的⽔⾯形成⼀段液⾯差后,停⽌加⽔,观察球形漏⽃中的液⾯不下降,说明⽓密性良好。
若液⾯下降,说明漏⽓。
漏⽓的部分可能为:导⽓管上的旋塞或球形漏⽃与容器接触的磨⼝处。
可在此处涂上凡⼠林来改善漏⽓。
1.2、加⼊药品块状固体药品从上端的出⽓⼝加⼊,加⼊固体药品的量不得超过上部球体的1/3。
液体药品从球形漏⽃中加⼊,液体的量以反应时刚刚浸没固体即可。
液⾯不可⾼于导⽓管的橡胶塞。
1.3、控制反应的发⽣与停⽌⽅法打开旋塞,球形漏⽃中的液体进⼊容器中,容器中的液⾯上升与固体药品接触反应放出⽓体,关闭导⽓管上的旋塞,⽣成⽓体⽆法排除,导致容器内的⽓压升⾼,将液体压⼊球形漏⽃中,液体与固体脱离,反应停⽌。
若再打开旋塞,容器内的⽓体导出,容器内的⽓压降低,球形漏⽃中的液体⼜进⼊容器中,液⾯上升,与固体药品接触,⼜发⽣反应。
自制简易启普发生器制取二氧化碳一、改进的理由教学中,有同学提出问题:启普发生器能不能实现随用随制,不用即关的效果。
光和学生讲理论方面的知识学生没有良好的认识。
所以我决定自制一个简易启普发生器。
在教学中实际使用情况良好,演示效果极佳。
该装置真实可用,可以达到随用随制,不用即关的效果。
再者本实验具有一定的趣味性,探究性,实用性,能够很好的激发学生学习兴趣,开拓学生思维,现在我将做法总结出来,与大家交流分享。
二、改进的方法(1)实验器材及药品:空饮料瓶2个(本实验选择材质较硬的萨姆奶茶饮料瓶);玻璃管1支(10厘米);橡胶管两根(3厘米);带孔橡皮塞1个;医用输液管 1根(去掉针头部位);鹅卵石若干;带孔塑料片一个(比饮料瓶底部面积略小);剪刀一把;酒精灯一盏;火柴;铁钉一枚;止水夹一个;盐酸适量;碳酸钙适量。
(2)制作原理与方法利用U型管连通器的原理,当开关打开时两瓶上方压强相同,(1号瓶中装盐酸)盐酸由1号瓶进入2号瓶与碳酸钙发生反应既而生成二氧化碳气体。
不用时关闭开关,2号瓶气体压强变大将盐酸压回1号瓶。
2号瓶底部垫有鹅卵石用以反应停止时隔离盐酸与碳酸钙。
1.取两个矿泉水塑料瓶,1支玻璃管。
点燃酒精灯把玻璃管烧热,用烧热的玻璃管插入塑料瓶下部拔出。
用同样的方法处理这两个塑料瓶。
2.此时我们得到两个下方有小孔的塑料瓶。
用剪刀把橡胶管剪两小段(长约3厘米),将两段橡胶管分别塞入小孔内,两个橡胶管露出部分用玻璃管连接。
此时U型连通器制作完成。
(注意连接部位确保不漏液,一般材质较硬的饮料瓶不会出现漏液)3.将铁钉烧至红热后,在一个塑料片上穿几个小孔,塑料薄片用以分开碳酸钙和稀盐酸。
不与盐酸反应),鹅卵石上4.向2号瓶底部装入适量鹅卵石(主要成分SiO2方放一个带有多个小孔的塑料片,塑料片上方装入药品碳酸钙,塞上橡皮塞。
将医用输液管插入橡皮塞,止水夹夹住透气的管道以防漏气,装置制作成功。
1.使用和演示方法:1、打开开关,盐酸由1号瓶进入2号瓶与石灰石发生反应气体生成,,既而生成二氧化碳气体。
说明书一种简易式启普发生器技术领域本实用新型涉及气体制备实验中的气体发生装置,特别是一种简易式启普发生器。
背景技术启普发生器是由一个底部半球装的葫芦形容器和一个球形漏斗装容器组成,该装置在使用中存在以下明显不足:1.仪器容积过大,使用剩余的药品已经被污染,不可回收再用,造成实验药品的浪费。
2.反应过程中的停止控制过于迟钝,且再次开启时气流不稳定,存在安全隐患。
3.装置复杂,操作繁琐,气密性容易被破坏而无法收集到制备气体,导致实验失败。
实用新型内容本实用新型的目的是提供一种简易式启普发生器,以解决现有启普发生器存在的药品浪费严重,控制设计不合理,气密性容易遭破坏等问题。
本实用新型装置包括铁架台(1),具支锥形瓶(2),特制导管(5),铁圈(7),储液瓶(8)四部分,所述的特制导管(5)两端带有类似针头的导管端口,储液瓶瓶塞(6)由铁夹(3)固定于铁架台(1),特制导管(5)悬挂于铁架台,并通过特制的端口分别插入橡胶塞(4)和储液瓶瓶塞(6)。
本实用新型结构简单,制作简便,安全可靠,可在众多气体制备实验中进行使用。
下面结合附图对本实用新型作进一步说明。
附图说明图1是本实用新型的结构示意图。
具体实施方式本实用新型装置包括铁架台(1),具支锥形瓶(2),特制导管(5),铁圈(7),储液瓶(8)四部分,所述的特制导管(5)两端带有类似针头的导管端口,储液瓶瓶塞(6)由铁夹(3)固定于铁架台(1),特制导管(5)悬挂于铁架台,并通过特制的端口分别插入橡胶塞(4)和储液瓶瓶塞(6)。
所述的特制导管(5)带有特制端口和控制开关。
所述的橡胶塞(4)和储液瓶瓶塞(6)的尺寸分别与具支锥形瓶(2)和储液瓶(8)的瓶口尺寸相吻合。
所述的储液瓶(8)可用底部大上部小的饮料瓶或酒瓶。
所述的特制导管(5)可用医用输液导管,也可用橡胶管。
所述的铁架台(1),具支锥形瓶(2),铁夹(3),橡胶塞(4),铁圈(7)可用实验室已有的仪器。
自制教具:启普发生器
说明:该教具可以来制备不需加热且反应物为固体和液体的反应,如实验室制二氧化碳、氢气可以本套装置。
本套适合化学仪器、药品短缺的薄弱学校学,亦可作为化学兴趣小组的手工。
仪器用品: 500ml硬质可乐瓶、1.5L高装饮料瓶、输液器、铁夹、胶塞(或橡皮泥)各一个,细铜丝10cm。
制作方法:
将小饮料瓶从瓶底以上3厘米处剪断,并借助沸水使其牢固地塞入上半截瓶,然后在瓶底烫8个孔。
大饮料瓶从中间截断,下半部分保留,并用铜丝将两部分固定,接上点滴管,一个造价低廉的启普发生器就成功了。
使用方法:
从瓶口处加固体药品,酸可从敞口处直接加入。
实验时将点滴管上的调节阀门调至开处,使滴管通畅,这样发生器的固体、液体药品就会接触,发生反应;如需使反应停止,关上阀门即可。
教师:罗廷芬
学校:黔南州贵定县盘江中学。