氩氦刀冷冻治疗恶性肿瘤的影像学分析
- 格式:pdf
- 大小:238.76 KB
- 文档页数:1
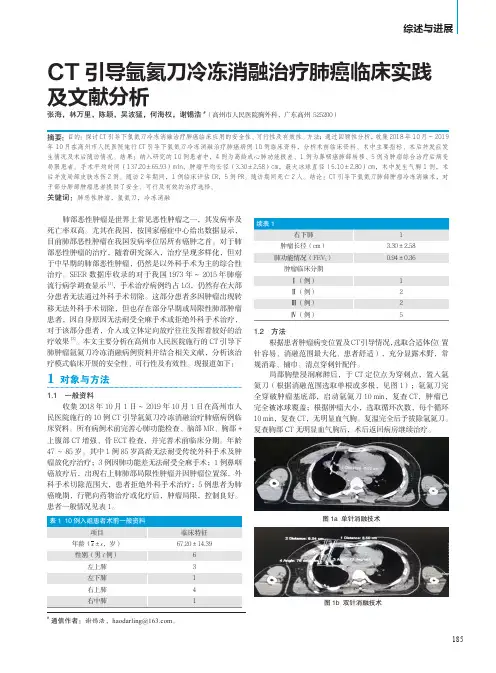
185综述与进展CT 引导氩氦刀冷冻消融治疗肺癌临床实践及文献分析张海,林万里,陈颖,吴波猛,何海权,谢锡浩#(高州市人民医院胸外科,广东高州 525200)摘要:目的:探讨CT 引导下氩氦刀冷冻消融治疗肺癌临床应用的安全性、可行性及有效性。
方法;通过回顾性分析,收集2018年10月~2019年10月在高州市人民医院施行CT 引导下氩氦刀冷冻消融治疗肺癌病例10例临床资料,分析术前临床资料、术中主要指标、术后并发症发生情况及术后随访情况。
结果:纳入研究的10例患者中,4例为高龄或心肺功能极差、1例为鼻咽癌肺部转移、5例为肿瘤综合治疗后病变局限患者。
手术平均时间(137.20±65.93)min,肿瘤平均长径(3.30±2.58)cm,最大冰球直径(5.10±2.80)cm,术中发生气胸1例,术后并发局部皮肤冻伤2例。
随访2年期间,1例临床评估CR,5例PR。
随访期间死亡2人。
结论:CT 引导下氩氦刀肺部肿瘤冷冻消融术,对于部分肺部肿瘤患者提供了安全、可行及有效的治疗选择。
关键词:肺恶性肿瘤,氩氦刀,冷冻消融肺部恶性肿瘤是世界上常见恶性肿瘤之一,其发病率及死亡率双高。
尤其在我国,按国家癌症中心给出数据显示,目前肺部恶性肿瘤在我国发病率位居所有癌肿之首。
对于肺部恶性肿瘤的治疗,随着研究深入,治疗呈现多样化,但对于中早期的肺部恶性肿瘤,仍然是以外科手术为主的综合性治疗。
SEER 数据库收录的对于我国1973年~2015年肺癌流行病学调查显示[1],手术治疗病例约占1/3,仍然存在大部分患者无法通过外科手术切除。
这部分患者多因肿瘤出现转移无法外科手术切除,但也存在部分早期或局限性肺部肿瘤患者,因自身原因无法耐受全麻手术或拒绝外科手术治疗,对于该部分患者,介入或立体定向放疗往往发挥着较好的治疗效果[2]。
本文主要分析在高州市人民医院施行的CT 引导下肺肿瘤氩氦刀冷冻消融病例资料并结合相关文献,分析该治疗模式临床开展的安全性、可行性及有效性。

射频消融,微波消融,海扶刀,氩氦刀,哪个效果好?屈立新现代微创治疗肿瘤的方法越来越多,各类“刀”五花八门,都被吹得天花乱坠。
而患者及家属没有专业医学知识,无法判断真实疗效,也不了解它的治疗风险及副作用。
我们目前了解到的“刀”就有物理消融方面的如:射频刀,氩氦刀,微波刀,海付刀以及最新出来尚未在国内应用的纳米刀;射频刀,微波刀,海扶刀都是属于热消融,其中射频刀及微波刀均使用电产生的高温杀灭肿瘤细胞,而海扶刀是通过超声聚焦加热高温杀灭肿瘤。
由于海扶刀只能在超声下进行,不适合肺肿瘤。
氩氦刀则是冷热交替消融杀灭肿瘤细胞。
其杀死肿瘤细胞是依靠反复多次迅速降温以及升温造成的细胞崩裂。
单纯的超低温冷冻可以保存组织,但是要复活细胞则需要非常缓慢的升温调控,反复超低温及复温下肿瘤细胞完全无法存活。
在这里我们只重点列出射频消融及冷冻消融。
因为它们是全世界肿瘤医生(包括中国大陆正规医院)公认权威的美国NCCN抗癌指南(2013版)中用于肺癌肝癌(含转移癌)的除外科切除手术外的唯一推荐治疗方法。
没有列出立体定向放疗是因为它对于肝癌效果甚微。
1.1射频消融治疗肿瘤:多极射频肿瘤消融术的原理是在CT、彩色B超的引导下,将多极子母针消融电极准确刺入肿瘤部位,射频消融仪在电子计算机控制下将射频脉冲能量通过多极针传导到肿瘤组织中,使肿瘤组织产生局部高温(70℃——95℃),从而达到使肿瘤组织及其邻近的可能被扩散的组织凝固坏死的目的,治疗范围约5公分。
1.2射频消融治疗肿瘤的禁区:1.贴近心脏及全身各大血管的肿瘤,热效应有可能造成严重心律失常;也可能烧穿血管造成无法控制的出现。
2.贴近胆囊,胆道,尿道,神经及胃肠道的肿瘤,这些部位如果烧穿将导致胆汁瘘,尿瘘及神经永久性损害。
3.贴近胸膜,隔膜的肿瘤如肺肿瘤肝肿瘤,胸膜烧伤可能导致严重的胸痛;而横隔膜烧穿的话有可能造成出血及隔疝。
2.1冷冻消融氩氦刀治疗肿瘤:氩氦刀冷冻消融治疗肿瘤的原理也是在CT,B超等影像引导下将多根氩氦刀探针插入肿瘤内部,氩气在针尖内急速释放,十几秒内冷冻肿瘤组织到零下120℃-零下160℃;而当氦气在针尖急速释放时,将产生急速复温快速将冰球解冻反复多次彻底杀灭肿瘤细胞。


肝细胞癌冷冻治疗术后完全消融早期MRI特征董景辉;马威;刘长春;高原智;任洪伟;李勇武;安维民【摘要】目的探讨氩氦刀冷冻治疗肝细胞癌(HCC)术后完全消融的MRI表现.方法回顾性分析经随访证实氩氦刀冷冻治疗消融完全的48例HCC患者术前及术后2~7天MRI资料,测量冷冻治疗前后病灶及其周围肝实质ADC值.结果消融后,38例T1WI呈高信号,26例T2WI呈低信号;增强扫描动脉期瘤结节均未见强化,但9例瘤结节出现门静脉晚期及延迟期强化;消融区周边均可见环形强化,25例可见消融区相邻肝包膜下斑片状强化;30例可见瘤结节周边消融区肝实质内穿行小血管强化,7例可见周围肝实质强化.冷冻治疗前后肿瘤ADC值分别为(0.80±0.33)×10-3 mm2/s、(1.26±0.54)×10-3 mm2/s,差异有统计学意义(P<0.01).结论 MRI可用于评价氩氦刀治疗肝癌的早期疗效,冷冻消融后肿瘤及周围肝实质延迟持续强化并不一定代表肿瘤残留,术后ADC值的变化可用于预测早期疗效.【期刊名称】《中国介入影像与治疗学》【年(卷),期】2014(011)010【总页数】4页(P639-642)【关键词】肝肿瘤;磁共振成像;冷冻治疗;治疗结果【作者】董景辉;马威;刘长春;高原智;任洪伟;李勇武;安维民【作者单位】中国人民解放军第302医院医学影像中心,北京100039;中国人民解放军第302医院医学影像中心,北京100039;中国人民解放军第302医院医学影像中心,北京100039;中国人民解放军第302医院医学影像中心,北京100039;中国人民解放军第302医院医学影像中心,北京100039;中国人民解放军第302医院医学影像中心,北京100039;中国人民解放军第302医院医学影像中心,北京100039【正文语种】中文【中图分类】R735.7;R445.2肝细胞癌(hepatocellular carcinoma,HCC)是严重威胁人类健康的疾病之一,发病率位居全球恶性肿瘤的第5位,而其中55%的病例发生于中国[1]。





CT导向氩氦刀治疗肺部原发肿瘤的影像表现及评估目的研究经CT导向氩氦刀靶向治疗肺部原发肿瘤前后的影像表现及临床疗效评估。
方法对73例病理确诊原发肺部肿瘤患者采用经皮肺穿刺氩氦刀靶向治疗。
所有患者术前、后均作CT扫描,测定肿瘤大小及CT值,部分病例分别于术后1、3、6个月复查CT。
结果腺癌29例和鳞癌47例,其中中央型肺癌6例(CT显示肺门区肿块),合并肺内转移转移5例,共79个病灶,单发病灶68例,多发灶5例。
氩氦刀共治疗78次。
肿瘤直径1.3-8.0cm。
其中病灶直径4cm 25个。
冷冻冰球完全覆盖瘤灶并达其边缘外1cm的20例。
冰球覆盖瘤灶体积三分之二以上的48个。
冰球覆盖瘤灶体积超过一半的11个。
肺部肿瘤冷冻后可见类圆形低密度冷冻区,与非冷冻区有明显的界限。
冷冻区中心CT值为负值,术后CT值平均下降30-50Hu,氩氦刀治疗前后肿瘤直径比较,差异有统计学意义(P<0.05)。
直径4cm 25个。
1.2 仪器:氩氦靶向手术治疗系统。
刀直径分别为2、3、5、8 mm。
可输出高压常温氩气(冷媒)或高压常温氦气(热媒)。
应用TOSHIBA Aquilion 16 层螺旋CT扫描机。
1.3 方法:充分了解影像资料中显示的肿瘤及周围组织结构的三维立体解剖关系,根据肿瘤部位和数量确定每次治疗的病灶数。
术前在肿瘤相应皮肤表面上黏贴一排状金属标记再次进行CT扫描,仔细测算、确定氩氦刀的种类、数量和方位,并最终确定刀头端进入瘤体内的位点。
设计原则要求单刀或多刀组合冷冻所形成的冰球尽可能包容瘤体组织。
冰球冷冻范围应尽可能大于肿瘤边缘1cm 以上。
1.4 手术方式:患者采卧位,于穿刺定位点行局部麻醉。
依据扫描照片所提示的进针方向、角度、深度等系列因素,把氩氦刀穿刺针刺入肺部肿瘤靶点,再将氩氦刀插入瘤体内。
启动手术系统。
先冷冻15分钟,升温10分钟,再冷冻15分钟,再升温。
术毕常规CT扫描,了解冷冻效果及有无出血、气胸。


影像学引导肺癌冷冻消融治疗专家共识(完整版)肺癌发生率逐年增加,并已经成为威胁人民健康的主要疾病。
2017年国家癌症中心统计结果显示,肺癌位居导致患者死亡疾病的第一位。
研究显示,仅有不到30%的肺癌患者可接受外科手术切除。
影像学引导肿瘤的各种消融技术在肺癌治疗中发挥着较大作用。
物理消融创伤小、安全性高及疗效可与外科手术媲美,已获得医患双方认可。
物理消融方法中,以射频和微波为代表的热消融及以氩氦刀为代表的冷消融均是在影像学引导下经皮穿刺肿瘤并以极端的温度导致肿瘤细胞坏死。
冷冻消融因治疗过程中患者痛苦小、耐受性好、影像学监测时示踪性好已被广泛接受。
影像学引导肺癌冷冻消融具有创伤小、安全性高及疗效好的优点,在肺癌的局部治疗中得到广泛应用,但同样存在并发症风险。
为明确影像学引导肺癌局部冷冻消融治疗的技术操作规范以及评估治疗效果,提高手术的安全性及疗效,特制订此共识,供临床参考。
一肺癌冷冻消融技术的特点1.1基本原理以氩-氦冷冻为代表的消融技术是目前较成熟的冷冻消融治疗技术,其主要作用机制为冷冻对靶组织及细胞的物理杀伤、肿瘤破坏微血管栓塞以及冷冻后的肿瘤组织作为抗原引起的机体免疫反应。
其主要原理为通过Joule-Thomson效应,高压氩气可使探针尖端的靶组织冷却至-140℃,导致靶细胞结冰、细胞膜破裂及细胞内容物释放引起微血管闭塞、组织缺血坏死等;而氦气可使靶组织温度从-140℃上升至20℃~40℃,通过这种温度梯度的变化以及多次冻融循环,可提高消融效果,杀灭肿瘤细胞,达到治疗肿瘤的目的。
1.2引导方式CT扫描图像质量好,成像速度快,密度分辨率及空间分辨率高,图像较直观,尤其对肺组织及病变显示具有其他影像学方法无法比拟的优势,为最常用的影像学引导方式。
MR扫描可清晰显示“冰球”大小,帮助术者准确判断冷冻范围,且术中手术器械的虚拟针影与病变图像可同时显示于同一幅图像,并实时观察手术器械与靶区病灶位置关系的动态变化。
氩氦刀冷冻消融靶向治疗中晚期恶性肿瘤的应用进展智雅婧1,郑媞2,那顺孟和2(1.内蒙古医科大学,内蒙古呼和浩特010000;2.内蒙古自治区肿瘤医院,内蒙古呼和浩特010000)摘要:恶性肿瘤具有增殖分化异常、生长不受控制、转移性及浸润性强等生物学特点,其发生与环境、生活习惯、遗传、免疫等因素有关,根据肿瘤性质、受累组织器官以及肿瘤分期不同采取针对性综合治疗。
氩氦刀是美国研制的一种引起超低温介入冷冻消融治疗设备,可对探头进行加热、制冷,在影像技术引导下对实体瘤组织进行摧毁。
氩氦刀冷冻消融治疗已广泛运用于多种肿瘤临床治疗,并取得较好效果。
本文对氩氦刀冷冻消融靶向治疗在中晚期恶性肿瘤应用作一综述。
关键词:恶性肿瘤;中晚期;氩氦刀;冷冻消融癌症在医学上是指起源于上皮组织的恶性肿瘤,其不仅影响人们的生命健康,同时,也会增加恶性肿瘤患者及社会医疗负担。
目前,恶性肿瘤的治疗方式主要有放疗、化疗、手术、免疫治疗以及中医治疗等[1-2]。
虽然放化疗药物治疗恶性肿瘤取得一定效果,但易产生不良反应或耐药性,影响临床治疗效果。
免疫治疗在多种恶性肿瘤治疗中取得较好的临床效果,但也会产生免疫治疗耐药,同时,免疫治疗不适合所有恶性肿瘤患者,导致治疗对象受限。
低温冷冻治疗疾病属于一种传统的治疗手段,有史料记载古埃及人曾用低温治疗头部复杂性骨折以及胸部炎症反应,冰冻还可有效治疗出血与水肿[3-4]。
Arnott[5]在19世纪中期时曾用不同温度的碎冰盐水用于治疗宫颈癌、乳腺癌,这也是低温冷冻技术在恶性肿瘤治疗方面的初次尝试。
随着冷冻技术的不断发展,从最初的冰发展为至今的干冰、液氮以及氩氦刀,同时,也提高了低温冷冻治疗技术的控制性。
恶性肿瘤临床主要采取手术切除治疗,但中晚期恶性肿瘤患者常伴有手术禁忌证而无法采取手术切除肿瘤治疗,只能采取姑息性治疗。
冷冻消融术具有创伤小、并发症少、禁忌证少、操作安全等特点,在多种实体瘤治疗中取得较好效果。
氩氦刀冷冻治疗恶性肿瘤的影像学分析
发表时间:2014-01-02T14:30:05.420Z 来源:《医药前沿》2013年11月第32期供稿作者:王绍龙
[导读] 治疗前要进行局部麻醉,全面掌握病变的大小、位置,而后明确冷冻探针的数量、深度和路径。
用超声进行动态引导。
王绍龙(安阳市肿瘤医院影像科 455000)
【摘要】目的探讨氩氦刀冷冻治疗恶性肿瘤在的影像学中的价值;方法分析2012年8月至2013年8月我院应用氩氦刀冷冻治疗恶性肿瘤94例患者的效果;结果经过3个月的治疗,病灶明显缩小,但是肿瘤直径超过3厘米的结果则与之相反;结论氩氦刀在治疗恶性肿瘤的术中情况较好,无明显并发症,术后恢复快。
【关键词】氩氦刀恶性肿瘤影像学
【中图分类号】R730.4 【文献标识码】A 【文章编号】2095-1752(2013)32-0188-02 随着计算机技术的不断发展,低温冷冻技术作为一种全新的治疗肿瘤的方法被广泛应用,本文选取2012年8月至2013年8月在我院进行恶性肿瘤治疗的94例患者作为研究对象,给予其低温冷冻治疗,效果较为突出,具体情况现报道如下。
1 资料与方法
1.1 一般资料
本组资料共计94例,均为2012年8月至2013年8月在我院进行恶性肿瘤治疗的患者,其中男53例,女41例,年龄37~77岁,平均53.2±2.6岁。
1.2 方法
治疗前要进行局部麻醉,全面掌握病变的大小、位置,而后明确冷冻探针的数量、深度和路径。
用超声进行动态引导。
CT引导过程中,在肿瘤的位置处用胶布团或橡皮盖进行标记,接着予以CT扫描。
在布针的时候不要对附近的关键结构或组织造成伤害,而后尽可能的消除肿瘤组织。
若肿瘤低于3厘米,那么可直接单根探针;若3~6厘米,那么要探入两根针,两针的间隔为2至3厘米。
若患者是颅脑肿瘤,那么要先进行颅骨开窗,接着在CT引导下进行冷冻治疗。
若患者的病灶较大,那么要在将探针和外鞘退出20~30毫米后,继续再治疗。
1.3 观察指标
观察冰球的大小、形成时间、冰球覆盖率、CT及超声表现以及治疗完成2星期时的病灶病理学变化和3个月病灶的缩小程度。
2 结果
2.1 冰球形成的时间
在接入氩气60秒内,温度马上下降到-130℃,在进行冷冻的过程中,温度始终在-150℃处维持着。
有88.3%的病灶在形成冰球的时间均在50秒内。
2.2 超声和CT表现
(1)超声表现:冰球初步形成时,冰球外围的横断面有弧形的强回声,纵断面有强烈的回声并轻微向前隆起,后面有轻微的声影;(2)CT表现:冷冻后马上进行扫描,冷冻部分的密度现相互下降,辩解较清晰,CT值是-10~15HU。
由于时间的增加,病灶的密度呈不均匀的增长趋势,最终钙化纤维化到高密度。
2.3 冰球大小变化
冷冻的时间在5至15分钟的时候冰球的变化是最佳显著的,而15至20分钟时其增加的幅度并不明显。
2.4 冰球覆盖率及病灶缩小率
肿瘤直径小于3厘米的冰球覆盖率很高,经过3个月的治疗,病灶明显缩小,但是肿瘤直径超过3厘米的结果则与之相反。
2.5 术中并发症
超声引导下4例肝肾间隙出血,3例肝包膜下出血,2例胆汁漏;CT引导下6例少量气胸。
没有大量气胸、出血性休克等重大并发症。
3 讨论
氩氦刀属于是低温冷冻设备的一种,主要分为导线、探针、主机三部分[1]。
经探针可将冷媒氩气导入,此时局部的温度就会迅速下降,组织就会出现变性坏死。
经实验表明,温度较低就会在细胞内形成冰晶,冰晶在较低的温度下就会杀死组织,然而,在多数情况下肿瘤组织对低温的承受能力要远远超过正常细胞。
在本次研究中,在接入氩气60秒内,温度马上下降到-130℃,在进行冷冻的过程中,温度始终在-150℃处维持着。
有88.3%的病灶在形成冰球的时间均在50秒内。
衡量冷冻效果的一个最显著的指标就是冰球的大小。
临床中认为,当冰球的边缘多余病灶1厘米时被称为最佳冷冻[2]。
但是在实际操作的过程中,是无法对内部情形进行全面观察的,所有在本次研究中选择CT和超声影像学对其进行监测,不仅能够准确的监测到冰球的变化情况,还能够及时发现术中存在问题及术后并发症。
经相关研究表明,冷冻的时间在5至15分钟的时候冰球的变化是最佳显著的,而15至20分钟时其增加的幅度并不明显。
这也就表明氩氦刀在一个周期内的最佳冷冻时间是15分钟。
经超声监测的结果与之完全吻合。
因为由于病灶的部位、形状、大小等关系各部相同,所以在进行氩氦刀治疗的过程中将所有的病灶全部切除是很不现实的问题。
此次研究中,肿瘤直径小于3厘米的冰球覆盖率很高,经过3个月的治疗,病灶明显缩小,但是肿瘤直径超过3厘米的结果则与之相反。
这也就表示小于3厘米的肿瘤采用氩氦刀进行低温冷冻治疗的效果更好。
本次研究表明,氩氦刀在治疗继发或原发肿瘤,特别是病灶位置较为特殊的选择手术难以治愈的方面效果更加明显,它的术中情况较好,无明显并发症,术后恢复快。
参考文献
[1]苏海庆, 叶海洪, 黄筱华, 等. 超声在氩氦刀冷冻治疗肝癌中的价值研究[J]. 中国医学影像技术, 2003, 19(8) : 1055-1057.
[2]王洪武, 段蕴铀, 张燕群, 等.CT 引导下经皮肺穿刺氩氦靶向治疗肺转移癌[J]. 海军总医院学报,2003,16(3): 152-155.。