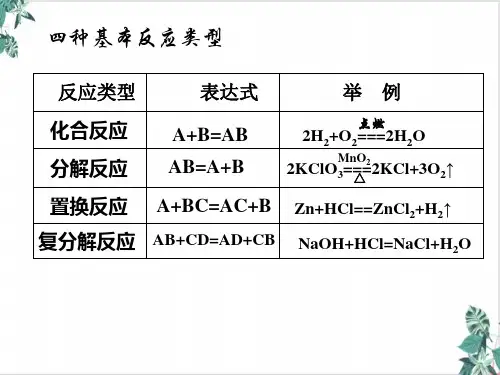
四、几种特殊的氧化还原反应
(一)部分氧化还原反应
2KMnO4 + 16HCl == 2KCl + 2MnCl2 + 5Cl2↑ + 8H2O
(二)歧化反应
Cl2 + H2O = HCl + HClO
(三)归中反应:
H2SO4(浓) + H2S = SO2↑+ S↓+ 2H2O
目录
(一) 部分氧化还原反应 在氧化还原反应中,如果还原剂只有部分被
__2_:_1 __
(三)归中反应 不同价态的同一元素化合价可升高或降低至某
一中间价态。 同种元素不同价态之间发生氧化还原 反应遵循以下归中规律:
高价+低价→相同中间价(注“可靠拢、不交叉”)
例题 2H2S+SO2=3S+2H2O
氧化产物与还原产物的物质的量之比:__2_:1___
练习:C + CO2 = 2CO n(氧化产物):n(还原产物)=__1_:_1____
2、氧化还原的实质是( ) A、有氧化剂和还原剂 B、有氧原子得失的反应 C、有元素化合价升降的反应 D、有电子得失的反应
3、下列说法下说法正确的是(
)
A、氧化剂本身被子还原,生成氧化产物
B、氧化剂是在反应中得到电子(或电子对偏向)的物质
得电子,化合价降低,被还原
氧化剂 + 还原剂 = 还原产物 + 氧化产物
(氧化性) (还原性 )
失电子,化合价升高,被氧化
2、口诀: “失, 升, 氧 , 得, 降, 还, 若 是 剂, 两 相 反 ”
3、Βιβλιοθήκη 氧化剂被还原还原产物
反 (氧化性) 得电子(化合价降低)