杂质对照品总结-- -布瓦西坦
- 格式:xlsx
- 大小:579.43 KB
- 文档页数:3

药物布瓦西坦(Brivaracetam)合成检索总结报告一、布瓦西坦(Brivaracetam)简介布瓦西坦(Brivaracetam)于2016年2月在美国上市,主要用于治疗16周岁及以上癫痫患者的局部性癫痫发作。
布瓦西坦(Brivaracetam)常见的不良反应有嗜睡、镇静、头晕、疲劳和、恶心、呕吐等等。
布瓦西坦(Brivaracetam)分子结构式如下:CAS:357336-20-0英文名称:Brivaracetam中文名称:布瓦西坦本文主要对布瓦西坦(Brivaracetam)的合成路线、关键中间体的合成方法及实验操作方法进行了文献检索并作出了总结。
二、布瓦西坦(Brivaracetam)合成路线(化合物5其他合成方法请参考总结报告)三、布瓦西坦(Brivaracetam)合成检索总结报告(一)布瓦西坦(Brivaracetam)中间体3的合成合成方法实验步骤参考文献操作方法一To a mixture ofmethyl (S)-2-aminobutanoate hydrochloride 2(5.0g,32.6mmol)and K 2CO 3(11.2g,81.7mmol)in acetone (100ml)at 0°C,compound 1(6.28g,34.3mmol)was added.After the reaction was complete by TLC,the solvents were evaporated in vacuo.The residue was added DCM (50ml)and water (50ml).The layers were separated.The aqueous layer was extracted with DCM (50ml).The combined organic layers were dried over anhydrous Na 2SO 4.Filtration and evaporation of the solvent afforded crude compound 3,which was purified by silica gel column chromatography using PE/EA (20/1)to afford the title compound 3(70%yield).WO2016/191435;(2016);(A1)English(二)布瓦西坦(Brivaracetam )中间体4的合成合成方法实验步骤参考文献操作方法一To a solution of compound 3(2.0g,7.6mmol)in anhydrous DMF (6ml),KOH (670mg,12mmol)was added portionwise at -15°C to -10°C.After the reaction was complete by HPLC,the reaction was quenched with 1N HCI.Brine (24ml)were added.The mixture was extracted with MTBE (4×20mL).The combined organic layers were washed with brine and dried over anhydrous Na 2SO 4.Filtration and evaporation of the solvent gave crude compound 4,which was purified by silica gel column chromatography using PE/EA (15/1)to afford the title compound 4(65%yield).WO2016/191435;(2016);(A1)English (三)布瓦西坦(Brivaracetam )5的合成方法一合成方法实验步骤参考文献操作方法一11.0g of the oil of Intermediate 4was added to 100mL of DMF,80mL of ammonia water was added,and the mixture was stirred at room temperature for 15h.After completion,it should be diluted with water,extracted three times with dichloromethane,combined with organic phase,washed twice with water,dried and concentrated.8.9g of bovistamCN108947883;(2018);(A)Chinese。
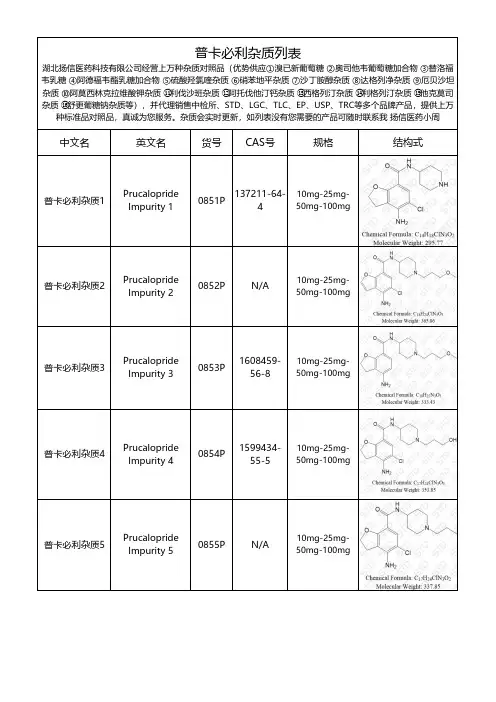
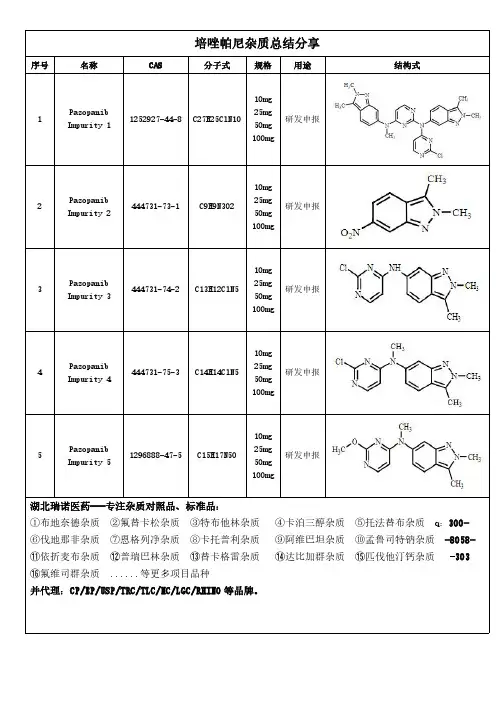
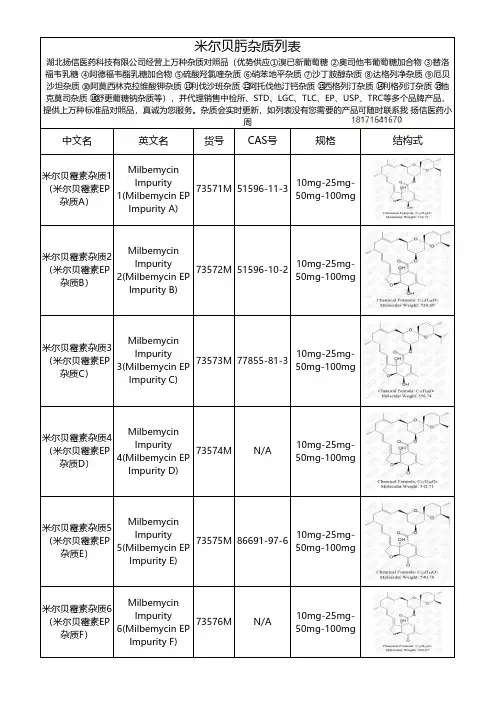

杂质对照品工作总结作为实验室中重要的一部分,杂质对照品的工作对于保证实验结果的准确性和可靠性起着关键作用。
在过去的一段时间里,我们对杂质对照品的工作进行了总结和反思,希望能够在今后的工作中更加精益求精,提高实验室的整体水平。
首先,我们深入了解了不同类型的杂质对照品的特点和用途,包括有机杂质、无机杂质、重金属杂质等。
我们认识到不同类型的杂质对照品在实验过程中起着不同的作用,需要有针对性地选择和使用。
因此,我们在选用杂质对照品时更加注重其适用性和代表性,确保实验结果的准确性。
其次,我们对杂质对照品的存储和管理进行了规范和优化。
我们建立了完善的杂质对照品管理制度,明确了责任人和管理流程,确保了杂质对照品的存储环境和条件符合要求。
同时,我们也加强了对杂质对照品的定期检查和更新,避免了因为杂质对照品过期或变质导致的实验结果不准确的情况。
此外,我们还加强了对杂质对照品的使用和操作规范的培训和指导。
我们认识到实验人员的操作技能和规范程度对于杂质对照品的使用效果和实验结果的准确性有着直接的影响。
因此,我们加强了对实验人员的培训和指导,提高了实验人员的操作技能和规范程度,确保了杂质对照品的正确使用和实验结果的准确性。
最后,我们还加强了对杂质对照品的质量控制和质量评价。
我们建立了完善的质量控制体系,确保了杂质对照品的质量符合要求。
同时,我们还加强了对杂质对照品的质量评价,及时发现和解决存在的问题,提高了杂质对照品的质量和可靠性。
总的来说,杂质对照品的工作是实验室工作中不可或缺的一部分,对于保证实验结果的准确性和可靠性起着关键作用。
我们将继续加强对杂质对照品的工作,不断提高实验室的整体水平,为科学研究和实验结果的准确性和可靠性做出更大的贡献。
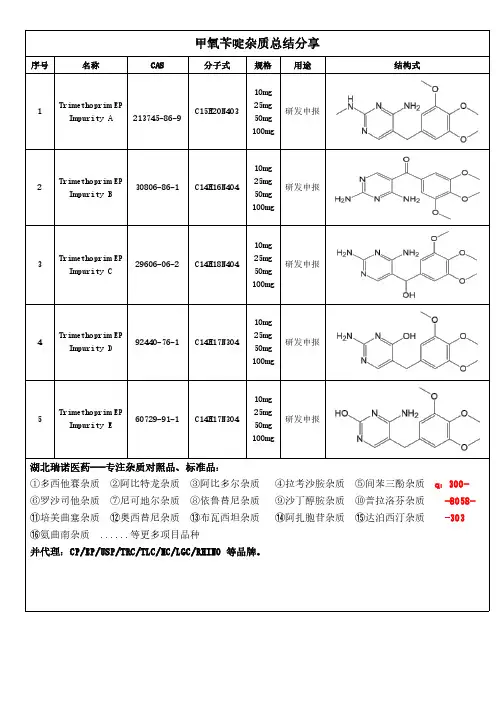
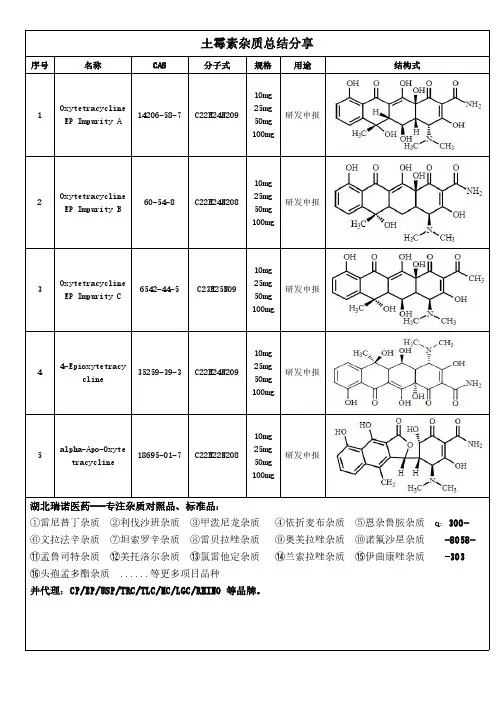
甲氧苄啶杂质总结分享
序号
名称
CAS
分子式
规格用途
结构式
1
Trimethoprim EP Impurity A
213745-86-9
C15H20N4O310mg 25mg 50mg 100mg
研发申报
2
Trimethoprim EP Impurity B
30806-86-1C14H16N4O4
10mg 25mg 50mg 100mg
研发申报
3
Trimethoprim EP Impurity C
29606-06-2C14H18N4O4
10mg 25mg 50mg 100mg
研发申报
4
Trimethoprim EP Impurity D
92440-76-1C14H17N3O4
10mg 25mg 50mg 100mg
研发申报
5
Trimethoprim EP Impurity E
60729-91-1C14H17N3O4
10mg 25mg 50mg 100mg
研发申报
湖北瑞诺医药---专注杂质对照品、标准品:①多西他赛杂质②阿比特龙杂质③阿比多尔杂质④拉考沙胺杂质⑤间苯三酚杂质q:300-
⑥罗沙司他杂质⑦尼可地尔杂质⑧依鲁替尼杂质⑨沙丁醇胺杂质⑩普拉洛芬杂质-8058-⑪培美曲塞杂质⑫奥西替尼杂质⑬布瓦西坦杂质
⑭阿扎胞苷杂质
⑮达泊西汀杂质
-303
⑯氨曲南杂质
......等更多项目品种
并代理:CP/EP/USP/TRC/TLC/MC/LGC/RHINO 等品牌。
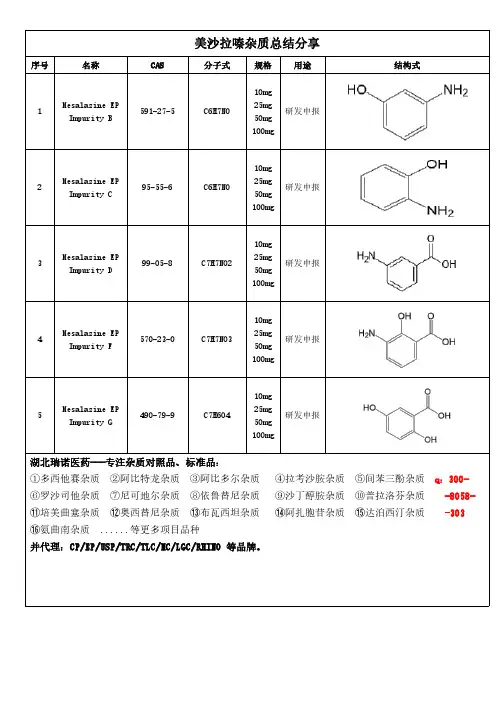
美沙拉嗪杂质总结分享
序号
名称
CAS
分子式
规格用途
结构式
1
Mesalazine EP Impurity B
591-27-5C6H7NO 10mg 25mg 50mg 100mg
研发申报
2
Mesalazine EP Impurity C
95-55-6C6H7NO
10mg 25mg 50mg 100mg
研发申报
3
Mesalazine EP Impurity D
99-05-8C7H7NO2
10mg 25mg 50mg 100mg
研发申报
4
Mesalazine EP Impurity F
570-23-0C7H7NO3
10mg 25mg 50mg 100mg
研发申报
5
Mesalazine EP Impurity G
490-79-9C7H6O4
10mg 25mg 50mg 100mg
研发申报
湖北瑞诺医药---专注杂质对照品、标准品:①多西他赛杂质②阿比特龙杂质③阿比多尔杂质④拉考沙胺杂质⑤间苯三酚杂质q:300-
⑥罗沙司他杂质⑦尼可地尔杂质⑧依鲁替尼杂质⑨沙丁醇胺杂质⑩普拉洛芬杂质-8058-⑪培美曲塞杂质⑫奥西替尼杂质⑬布瓦西坦杂质
⑭阿扎胞苷杂质
⑮达泊西汀杂质
-303
⑯氨曲南杂质
......等更多项目品种
并代理:CP/EP/USP/TRC/TLC/MC/LGC/RHINO 等品牌。
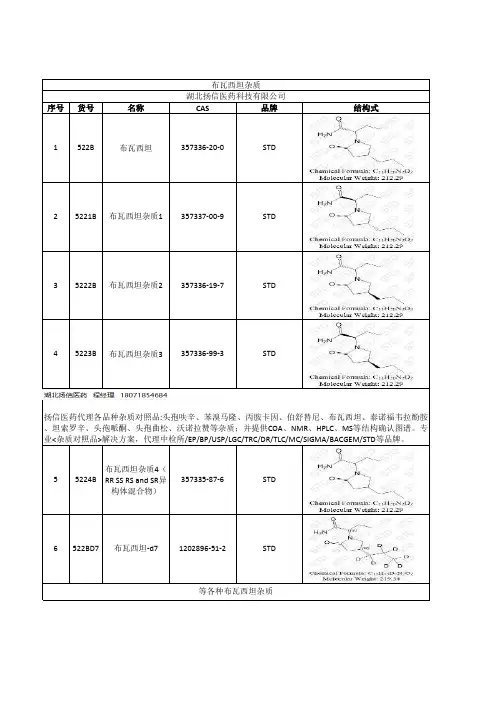
序号货号名称CAS 品牌结构式1522B 布瓦西坦357336-20-0STD
25221B 布瓦西坦杂质1357337-00-9STD
35222B 布瓦西坦杂质2357336-19-7STD
45223B 布瓦西坦杂质3357336-99-3STD
55224B 布瓦西坦杂质4(RR SS RS and SR 异
构体混合物)357335-87-6STD
6522BD7布瓦西坦-d7*******-51-2STD
布瓦西坦杂质湖北扬信医药科技有限公司扬信医药代理各品种杂质对照品:头孢呋辛、苯溴马隆、丙胺卡因、伯舒替尼、布瓦西坦、泰诺福韦拉酚胺、坦索罗辛、头孢哌酮、头孢曲松、沃诺拉赞等杂质;并提供COA 、NMR 、HPLC 、MS 等结构确认图谱。
专业<杂质对照品>解决方案,代理中检所/EP/BP/USP/LGC/TRC/DR/TLC/MC/SIGMA/BACGEM/STD 等品牌。
等各种布瓦西坦杂质。


国食药监注…2010‟ 387 号附件:化学药品CTD格式申报资料撰写要求23456CTD格式申报主要研究信息汇总表(制剂)2.3.P.5 制剂的质量控制2.3.P.5.1质量标准按下述表格方式提供质量标准。
如具有放行标准和货架期标准,应分别进行说明。
质量标准详细信息参见申报资料3.2.P.5.1(注明页码)。
2.3.P.5.2 分析方法列明各色谱方法的色谱条件:降解产物、残留溶剂、含量等。
列明溶出度检查的溶出条件、定量方法等。
分析方法详细信息参见申报资料3.2.P.5.2(注明页码)。
举例:列明各色谱方法的具体条件72.3.P.5.3分析方法的验证以表格形式逐项总结验证结果。
示例如下:有关物质方法学验证结果详细信息参见申报资料3.2.P.5.3(注明页码)。
举例含量测定方法学验证总结82.3.P.5.4 批检验报告三个连续批次(批号:)的检验报告参见申报资料3.2.P.5.4(注明页码)。
举例:2.3.P.5.5 杂质分析以列表的方式列明产品中可能含有的杂质。
示例如下:9杂质情况分析详细信息参见申报资料3.2.P.5.5(注明页码)。
2.3.P.5.6 质量标准制定依据质量标准制定依据参见申报资料3.2.P.5.6(注明页码)。
2.3.P.6 对照品药典对照品:来源、批号。
自制对照品:简述含量和纯度标定的方法及结果。
2.3.P.7 稳定性2.3.P.7.1稳定性总结(1)试验样品(2)研究内容10常规稳定性考察结果使用中产品稳定性研究结果2.3.P.7.2 上市后的稳定性承诺和稳定性方案详细信息参见申报资料3.2.P.7.2(注明页码)。
基于目前稳定性研究结果,拟定包装材料、贮藏条件和有效期如下:2.3.P.7.3 稳定性数据按以下例表简述研究结果,详细信息参见申报资料3.2.P.7.2(注明页码)。
说明:对于选用CTD格式提交申报资料的申请人,除按照“CTD 格式申报资料撰写要求”整理、提交药学部分的研究资料和图谱外,还应基于申报资料填写本表,并提交电子版。
扬信医药
布瓦西坦货号规格结构式API522B10/25/50/100mg
杂质15221B10/25/50/100mg
杂质25222B10/25/50/100mg
杂质35223B10/25/50/100mg
杂质45224B10/25/50/100mg
杂质55225B10/25/50/100mg
杂质65226B10/25/50/100mg
杂质75227B10/25/50/100mg
杂质85228B10/25/50/100mg
杂质95229B10/25/50/100mg
杂质1052210B10/25/50/100mg。
更多相关杂质现货提供,欢迎联系咨询
用途:新药研发、项目报批
提供各种对照品解决方案 :泊沙康唑杂质、替卡格雷杂质、依折麦布杂质、普瑞巴林杂质、拉米夫定杂质、氨氯地平杂质、利伐沙班杂质、克林霉素磷酸酯杂质、瑞舒伐他汀杂质、阿德福韦酯杂质、恩替卡韦杂质、替诺福韦杂质等;
并代理中检所/EP/BP/USP/LGC/TRC/DR/TLC/MC/SIGMA/BACHEM/STD等品牌
纯度高于98% 并提供COA、HNMR、HPLC、MS等图谱。