分光光度法测试水中的溴离子
- 格式:docx
- 大小:15.75 KB
- 文档页数:2

水中溴离子含量测定方法的研究窦妍;刘传富;鲁茹;曾辉辉【摘要】用溴酚红分光光度法和离子选择性电极法测定水中溴离子的含量.结果表明,分光光度法适用于低浓度(1.2×10-6 ~2.4×10-5 mol/L)溴溶液的测量,对于温度、显色时间等条件都有一定的要求;离子选择性电极法适用于溴离子浓度较大的溶液(10-3~10-1mol/L),除温度外,干扰离子Cl-、CO32--和SO42--对溴离子电极电位影响不大,具有外界环境影响小、方便携带、结果易得等特点.对于一些野外需要及时得到分析测试结果的研究工作,离子选择性电极法具有的优势更为明显.【期刊名称】《应用化工》【年(卷),期】2013(042)005【总页数】3页(P936-938)【关键词】溴酚红分光光度法;离子选择性电极;溴电极;溴离子标准溶液【作者】窦妍;刘传富;鲁茹;曾辉辉【作者单位】长安大学环境科学与工程学院,陕西西安710054;长安大学环境科学与工程学院,陕西西安710054;长安大学环境科学与工程学院,陕西西安710054;长安大学环境科学与工程学院,陕西西安710054【正文语种】中文【中图分类】O69;O6-33;X52溴酚红分光光度法是实验室测定水中溴离子含量的方法,在饮用天然矿泉水检验方法(GB/T 8538—1995)和地下水质检验方法(DZ/T 0064—1993)中都推荐此法,该法对溴离子的最佳测定浓度范围为1.2 ×10-6~2.4 ×10-5mol/L,实验室内温度及显色时间等对于该法都有一定的局限[1-2]。
目前在一些地区,由于石油等地下矿藏的开发,导致地下水中溴含量浓度超标,离子选择性电极法可作为一种快速简便的测定溴含量的方法,且不受样品溶液颜色、浑浊度、悬浮物或粘度等因素的影响,用少量样品即可测定,并且所需设备简单、操作方便,又适用于现场监测和批量样品的连续测试,更具有实用性[3-5]。

农垦师专学报 1997年第1期分光光度法测定溴的含量李 杰溴是化学中常用的试剂,由于其本身具有易挥发、不稳定的特点,因此使其含量的测定成为研究的中心。
在传统的化学分析中,溴含量的测定通常用氧化还原滴定法、配位滴定法、沉淀滴定法等方法来测定。
目前,在分析实验室中大多是用沉淀滴定法来测定溴的含量。
经过多年的实践,发现上述的这些测定方法存在着反应不完全,干扰离子多,分析过程繁琐以及分析结果准确度不高等一系列问题,给实验教学和学生的操作都带来诸多不便。
近几年来,经过逐步摸索,终于找到了一种可以代替传统分析法的方法来测定溴的含量,这就是分光光度法。
此方法是以H 2SO 4为介质,在一定的酸度条件下,将可溶性溴化物用KM n O 4氧化析出溴单质,用CCl 4萃取后进行吸光度的测量,得到了与传统分析法相一致的分析结果,并且具有准确、快速、简便等特点。
实验部分:1.实验目的用分光光度法和沉淀滴定法分别测定溴的含量,比较其分析结果,以证明分光光度法测定溴的含量是切实可行的。
2.实验仪器与试剂721型分光光度计、PHs -2型酸度计、3.0mol /l 的H 2SO 4溶液、0.10mol /l 的KM n O 4溶液、0.01000mol /l KBr 标准溶液、0.1000mol /l 的Br 2的标准溶液、有机溶剂CCl 4,以及分析实验中常用的玻璃仪器。
3.实验步骤3.1分光光度法测定溴含量的步骤准确移取0.01000mol /l KBr 标准溶液20.00ml 于分液漏斗中,一滴一滴加入3.0mol /l 的H 2SO 4溶液酸化,用PHs -2型酸度计控制溶液的PH 值为0.1左右,加入0.10mol /l KM n O 4溶液4ml,加入CCl 410ml,剧烈振荡5min,静止5min,放出下层黄棕色的萃取液,然后在分液漏斗中余下的水相中再加入适量的有机溶剂CCl 4,再次萃取,反复几次萃取,直到有机相CCl 4中不再有颜色(即无溴单质析出)为止,将所有CCl 4萃取液合并,然后用医用脱脂棉过滤,滤液装入1cm 的比色皿中并加盖(防止溴的挥发),以试剂KBr 作空白参比液,在482nm 处测定吸光度。

氨基黑10B退色分光光度法测定水中溴酸根离子摘要:在盐酸介质中,依据溴酸根离子氧化氨基黑10B退色的原理提出了测定水中溴酸根含量的新方法,研究了测定的最佳条件。
最大吸收波长为690 nm,BrO3-浓度在0.5~4.5 μg/mL内其浓度与吸光度呈良好线性关系,线性回归方程为A=0.153 33 C+0.026 56,相关系数为0.995 3,表观摩尔吸光系数为1.27×104 L/(cm·mol)。
该法适用于水中微量溴酸根离子测定。
关键词:氨基黑10B;溴酸根;退色;分光光度法随着人们对饮用水水质要求的提高,消毒效果较好的臭氧消毒技术在饮用水处理中的应用日益广泛。
但采用臭氧氧化处理含溴离子(Br-)水时,会产生以BrO3-为主的臭氧化副产物,而溴酸盐被国际癌症研究机构定为2B级潜在致癌物[1]。
因此,研究矿泉水中痕量BrO3-的测定方法对可饮用水的卫生监督和安全性评价具有重要意义。
水中BrO3-的测定方法较多,主要有分光光度法、荧光猝灭法、气相色谱法、高效液相色谱法等[2-8]。
氨基黑10B是一种色谱分析试剂、氧化还原指示剂和生物染色剂,其分子中的偶氮结构能与溴酸根发生氧化还原反应而使氨基黑10B发生退色反应,吸光度的降低与溴酸根加入量呈正比。
该法操作简单易懂,仪器成本较低,耗时短,是企业理想的测定水中BrO3-的方法。
1 材料与方法1.1 试剂与仪器岛津2550双光束紫外可见分光光度计(日本岛津公司);pHS-25型pH计(上海精科雷磁公司)。
氨基黑10B(AR,上海试剂二厂);盐酸(AR,天津市福晨化学试剂公司);溴酸钠(AR,国药集团上海试剂化学公司)。
氨基黑10B溶液:准确称取0.154 1 g的氨基黑10B固体置于100 mL烧杯中,用少量的二次蒸馏水溶解后,转入500 mL的容量瓶中,加二次蒸馏水至刻度线,得到5×10-4 mol/L的氨基黑10B溶液。

溴离子的测定方法
溴离子是一种常见的无机离子,它在环境监测、水质分析、生物医学等领域都有广泛的应用。
因此,溴离子的测定方法也备受关注,其中常见的有分光光度法、电化学法、离子色谱法等。
一、分光光度法
分光光度法是一种基于溴离子与某些试剂(如二苯基胺)发生反应,生成吸收波长在500nm左右的复合物,从而实现溴离子测定的方法。
在实际操作中,首先需要将样品与试剂混合,然后利用分光光度计测量吸收光强,根据标准曲线计算出溴离子的浓度。
二、电化学法
电化学法是一种运用电化学原理进行溴离子测定的方法。
其基本原理为,在电极上施加一定电势,使得样品中的溴离子发生氧化还原反应,从而在电极上发生电流变化。
常见的电化学方法有极谱法、循环伏安法等。
其中,循环伏安法的操作简单,测量准确性高,被广泛应用于溴离子测定。
三、离子色谱法
离子色谱法是一种基于溴离子在离子交换树脂上的吸附与洗脱行为,实现溴离子测定的方法。
在实际操作中,需要将样品通过离子交换树脂柱,使得溴离子在树脂上被吸附,然后通过洗脱溶液将溴离子
洗脱下来,最后通过检测器测量洗脱液中的溴离子浓度。
离子色谱法具有检测灵敏度高、准确性好等优点,被广泛应用于溴离子测定。
分光光度法、电化学法、离子色谱法都是常用的溴离子测定方法,其各自的优缺点需要根据实际情况进行选择。
在操作中,需要注意实验条件的控制,以及标准曲线的建立和质量控制等问题,以确保测定结果的可靠性和准确性。

紫外分光光度法测定水中总氮的方法验证摘要:总氮(Total Nitrogen, TN)是指水体中所有含氮化合物中的氮含量,即有机氮、氨氮、亚硝酸盐氮和硝酸盐氮的总量。
本报告对标准HJ 636—2012的检出限、测定下限、准确度和精密度等方面进行验证。
汇总相关验证数据后,对数据的合理性进行检验,将通过检验的验证数据进行汇总,编写实验室总氮方法验证报告。
关键词:紫外分光光度法;总氮;方法验证Abstract: the total nitrogen (Total Nitrogen, TN) refers to all the nitrogenous compounds of nitrogen content in water, namely, organic nitrogen, ammonia, nitrite nitrogen and nitrate nitrogen amount. The report on the standard HJ 636 - 2012 of the limit of detection, the detection limit, accuracy and precision and other aspects of verification. Collect related validation data, discusses the rationality of the test data, will pass Through the verification test data collected, prepared laboratory total nitrogen method validation report.Keywords: ultraviolet spectrophotometry; total nitrogen; method validation一、方法概述本方法依据HJ 636—2012。

实验六分光光度法测溴酚蓝的电离平衡常数摘要:由于光对物质的选择性吸收,对于一种物质来说,在一定的波长,对光的吸收会达到一个峰值,所以可以通过对特定波长的光的吸收来确定反应过程中的物质的量,进而跟踪反应的进程,实验中通过调节PH来改变反应物量,由于吸光度和光吸收物质的线性关系,所以负离子的mol分数可由(D-D1)/(D-D2)表示,而lg【(D-D1)/(D-D2)】=PH-PKa,在测定D1、D2后,再测一系列PH下的溶液的光密度,以lg D DD D--12对PH作图应为一直线,由其在横轴上的截距可求出P K a,从而可得该物质的电离平衡常数。
关键词:溴酚蓝,吸光度,PH,P Ka,电离平衡常数,分光光度计。
前言:通过对光的光度测量来跟踪反应,不会影响反应进程,不需要将物质分离出系统,而且测量结果比较精确,所以被广泛的应用在化学反应的测量中。
溴酚蓝是一种酸碱指示剂,离子态和分子态对光的吸收的强弱不同,而且其状态是受PH调节的,。
实验原理:波长为λ的单色光通过任何均匀而透明的介质时,由于物质对光的吸收作用而使透射光的强度(I)比入射光的强度(I0)要弱,其减弱的程度与所用的波长(λ)有关。
又因分子结构不相同的物质,对光的吸收有选择性,因此不同的物质在吸收光谱上所出现的吸收峰的位置及其形状,以及在某一波长范围内的吸收峰的数目和峰高都与物质的特性有关。
分光光度法是根据物质对光的选择性吸收的特性而建立的,这一特性不仅是研究物质内部结构的基础,也是定性分性、定量分析的基础。
根据贝尔—郎比定律,溶液对于单色光的吸收,遵守下列关系式:DIIK l C==⋅⋅lg0(6-1)式中,D-消光(或光密度);I/I0-透光率;K-摩尔消光系数,它是溶液的特性常数;l-被测溶液的厚度(即吸收槽的长度);C-溶液浓度。
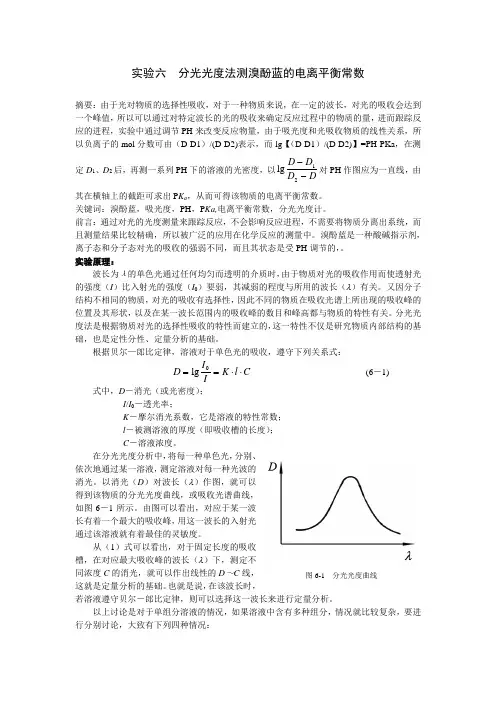
在分光光度分析中,将每一种单色光,分别、依次地通过某一溶液,测定溶液对每一种光波的消光。
以消光(D)对波长(λ)作图,就可以得到该物质的分光光度曲线,或吸收光谱曲线,如图6-1所示。



分光光度法测定甲基橙含量的新方法一、原理氯是指有组织和无组织固定污染源排放的游离氯。
含溴化钾、甲基橙的酸性溶液和氯气反应。
氯气将溴离子氧化成溴,溴能在酸性溶液中将甲基橙溶液的红色减褪,用分光光度法测定其褪色的程度来确定氯气的含量。
当采集无组织排放样品体积为30L时,方法的检出限为0.03mg/m3,定量测定的浓度范围为0.086~3.3mg/m3。
当采集有组织排气样品体积为5.0L 时,方法的检出限为0.2mg/m3,定量测定的浓度范围为0.52~20mg/m3。
游离溴有和氯相同的反应而产生正干扰,微量二氧化硫对测定有明显负干扰。
二、仪器①分光光度计:具1cm比色皿。
②多孔玻板吸收管:25ml。
③采样管:以硬质玻璃、氟树脂或氯乙烯树脂为材质,具有适当尺寸的管料的采样管。
④引气管:聚四氟乙烯或聚乙烯软管,头部装接一玻璃漏斗。
⑤连接管:聚四氟乙烯软管或内衬聚四氯乙烯薄膜的硅橡胶管。
⑥烟气采样器。
三、试剂除非另有说明,分析过程中均使用符合国家标准的分析纯试剂和蒸馏水。
①浓硫酸:ρ=1.84g/ml。
②甲基橙。
③溴化钾。
④溴酸钾;基准试剂。
⑤硫酸溶液(1+6):量取100ml浓硫酸,缓慢地、边倒边搅拌加入到600ml水中。
⑥甲基橙吸收贮备液:称取0.1000g甲基橙,溶解于100ml 40~50℃的水中,冷却至室温,加无水乙醇20ml,移入1000ml 容量瓶中,加水稀释至刻度,混匀。
此溶液放置暗处可保存半年。
⑦甲基橙吸收使用液:用吸管移取甲基橙吸收贮备液250ml,置于1000m容量瓶中,加入500ml(1+6)硫酸溶液,再加入5.0g溴化钾,溶解后用水稀释至刻度,混匀。
⑧溴酸钾标准贮备液C(1/6KBrO3)=1.41×10-1mol/L:称取1.9627溴酸钾,用少量水溶解,移入500ml容量瓶中,加水稀释至刻度,混匀。
此溴酸钾标准贮备溶液每毫升相当于5.00mg 氯。
放置暗处,可保存半年。

ABTS分光光度法测定水中微量二溴海因中的有效溴盛平;蒲韵竹;黄鑫;高乃云【摘要】为检测水中低浓度二溴海因(DBDMH),基于有效溴与2,2'-连氮-双(3-乙基苯并噻唑-6-磺酸)(ABTS)在pH=2条件下产生绿色稳定存在的ABTS·+自由基的原理,使用ABTS显色分光光度法在405 nm测定二溴海因中的有效溴.该方法在0.08~1.61 mg/L有效溴范围内线性良好,最低检测限为0.02 mg/L.二溴海因水解产生的氨氮对测定影响很小.【期刊名称】《净水技术》【年(卷),期】2010(029)006【总页数】4页(P72-75)【关键词】二溴海因;2,2'-连氮-双(3-乙基苯并噻唑-6-磺酸)(ABTS);有效溴;水处理【作者】盛平;蒲韵竹;黄鑫;高乃云【作者单位】第二军医大学长征医院,上海,200003;上海大学环境与化学工程学院,上海,200444;上海大学环境与化学工程学院,上海,200444;同济大学污染控制与资源化研究国家重点实验室,上海,200092【正文语种】中文【中图分类】X830.21,3-二溴-5,5-二甲基海因简称二溴海因(1,3-dibromo-5,5-dimethylhydantoin,DBDMH)是广谱、高效的缓释消毒剂,其杀菌效率是常规含氯消毒剂的40倍以上[1]。
在冷却水处理、游泳池用水净化、医院用品消毒等方面均获得了广泛的应用。
由于海因类消毒剂本身的不稳定性,直接检测的报道较少。
陈强等[2]通过检测消毒剂中的二甲基海因进而换算得到消毒剂含量。
也有用化学发光法直接测定海因类消毒剂,检测限较低[3]。
而且化学发光法对仪器要求较高,同时消毒剂水解产生的有效氯和有效溴都会引起化学发光,对体系有一定的干扰。
另一种方法是以碘量法为代表的检测消毒剂水解产生的有效溴或有效氯浓度。
本文中有效溴包括游离溴HBrO,以及游离溴与少量NH3反应形成的溴胺(以+1价溴计)。
DZ/T 0064.46—202X地下水质分析方法第46部分:溴化物的测定溴酚红分光光度法警示——使用本部分的人员应有正规实验室工作的实践经验。
本部分并未指出所有可能的安全问题。
使用者有责任采取适当的安全和健康措施,并保证符合国家有关法规规定的条件。
1 范围DZ/T 0064的本部分规定了溴酚红分光光度法测定地下水中溴化物的方法。
DZ/T 0064的本部分适用于地下水水资源调查、评价、监测和利用等水样中溴化物的测定。
本方法定量限为0.10 mg/L,测定范围为0.10 mg/L~2.0 mg/L。
溴化物含量高于此范围可稀释后测定。
2 规范性引用文件下列文件对于本文件的应用是必不可少的。
凡是注日期的引用文件,仅所注日期的版本适用于本文件。
凡是不注日期的引用文件,其最新版本(包括所有的修改单)适用于本文件。
GB/T 6682 分析实验室用水规格和试验方法DZ/T 0130 地质矿产实验室测试质量管理规范3 原理pH值在4.4~5时,用氯胺T做氧化剂,将溴离子氧化为游离溴,再与酚红作用形成四溴酚红。
溶液颜色随溴离子浓度不同而呈黄绿色至紫色,其吸光度与溴离子浓度呈线性关系,借此进行测定。
4 试剂或材料除非另有说明,分析时均使用符合国家标准的分析纯试剂。
4.1 纯水,符合GB/T 6682规定的二级水。
4.2 乙酸-乙酸铵缓冲溶液(pH=4.6):用乙酸溶液[c(CH3COOH)=2 mol/L]与氢氧化钠溶液[c(NaOH)=1 mol/L]等体积混合,冷至室温。
4.3 酚红溶液(0.24 g/L):称取酚红0.024 g与碳酸钠0.12 g于同一小烧杯中,加入约20 mL纯水使其溶解,再用纯水稀释至100 mL。
4.4 氯胺T溶液(2 g/L):称取氯胺T(C7H7SO2NClNa·3H2O)0.1 g溶于50 mL纯水中,临用时配制。
4.5 硫代硫酸钠溶液(25 g/L):称取硫代硫酸钠(Na2S2O3·5H2O)2.5 g溶于100 mL纯水中。
溴乙烷中溴离子的鉴定1.引言1.1 概述概述溴乙烷是一种常见的有机化合物,其化学式为C2H5Br。
其中,溴离子(Br-)是成分之一。
溴离子在溴乙烷中起着重要的化学作用,因此,对溴乙烷中溴离子的鉴定成为一项关键的研究内容。
溴离子是一种阴离子,带有一价负电荷。
它在化学反应中具有很高的活性,因此容易与其他物质发生反应。
溴离子的存在与否对于溴乙烷的性质和用途具有重要影响。
为了进行准确的鉴定,科学家们开发了多种检测方法。
这些方法包括物理方法和化学方法。
物理方法主要包括光谱分析、质谱分析等,通过检测溴离子的吸收或散射光谱特征来确定其存在与否。
化学方法则主要利用溴离子与特定试剂之间的反应进行检测,如溴离子与银离子反应生成白色沉淀等。
本文将对溴乙烷中溴离子的鉴定方法进行综述,并总结每种方法的优缺点。
同时,我们将对鉴定结果进行讨论和分析,以期对溴乙烷中溴离子的鉴定有更深入的了解。
最后,我们对未来可能的研究方向进行展望。
总之,溴乙烷中溴离子的鉴定对于理解该有机化合物的性质和用途至关重要。
通过本文的阐述,我们将探讨各种鉴定方法的优缺点,并为进一步的研究提供参考。
1.2 文章结构文章结构部分的内容可以根据以下模板进行编写:文章结构部分提供了关于整篇文章的组织和结构的说明,以帮助读者更好地理解文章的内容和逻辑关系。
本文的结构安排如下:第一部分是引言,主要包括概述、文章结构和目的。
概述部分对溴乙烷中溴离子的鉴定进行简要介绍,引起读者的兴趣并说明该领域的重要性。
文章结构部分说明了本文的整体组织结构,使读者能够清楚地了解该文档的内容分布。
目的部分明确了本文的研究目标和意义,指导读者理解和阅读本文的动力。
第二部分是正文,主要包括溴离子的性质和检测方法。
溴离子的性质部分描述了溴离子的化学特性、物理性质和常见的化学反应。
通过全面了解溴离子的性质,有助于为后续的鉴定方法提供基础知识。
溴离子的检测方法部分介绍了目前常用的鉴定溴离子的实验方法和仪器设备。
收稿日期:2020 ̄04 ̄05ꎮ作者简介:胡建军(1992 ̄)ꎬ男ꎬ浙江绍兴人ꎬ大学本科ꎬ初级工程师ꎬ目前从事工艺研发工作ꎮdoi:10.3969/j.issn.1008 ̄8261.2020.03.014总溴含量的测定方法胡建军(绍兴汉青环保科技有限公司ꎬ浙江绍兴312300)摘要:研究了PTA行业中总溴含量的测定方法ꎬ通过Na2S2O8 ̄NaOH体系对样品进行消解后ꎬ用抗坏血酸还原高价态无机溴ꎬ而后通过电位滴定法滴定消解产物中的溴离子来测定样品中的总溴含量ꎮ通过一些标准样品的测试和某PTA生产厂家的残渣浆料的验证ꎬ均有很高的符合度ꎬ认为该方法可以用于PTA行业中的总溴含量测定ꎮ关键词:PTAꎻ总溴含量ꎻ对苯二甲酸ꎻ消解ꎻ电位滴定法中图分类号:TQ245.12㊀㊀文献标识码:A㊀㊀文章编号:1008 ̄8261(2020)03 ̄0046 ̄020㊀前言精对苯二甲酸(PTA)是合成聚酯纤维和塑料的重要原料ꎬPTA的工业化生产中ꎬ采用的是以对二甲苯为原料ꎬ在催化剂作用下进行空气氧化ꎮ使用到的催化剂为乙酸钴㊁乙酸锰和氢溴酸ꎬ该氧化反应的机理一般认为是自由基氧化机理[1]ꎬ溴的作用是引发反应ꎬ相当于是氧化反应的导火索ꎬ溴浓度越高越有利于反应的引发和加快反应ꎮ但是同时ꎬ溴浓度的提高会使乙酸的燃烧反应加剧ꎬ消耗大ꎬ且会引起设备腐蚀[2]ꎬ同时也会对下游废水处理中的微生物处理过程产生负面影响ꎮ因而ꎬ必须合理的控制溴的浓度ꎮ按照文献中的报道ꎬPTA催化氧化母液中含有的溴组成非常复杂ꎬ有溴离子ꎬ溴的有机化合物和游离溴等ꎬ它们对反应均有催化作用[3]ꎮ因此ꎬ准确的测定总溴含量对溴浓度的控制有着非常重要的意义ꎮ若是采用常规的电位滴定法只能对溴离子进行测试ꎬ目前还有提出使用X射线荧光光谱仪(XRF)进行总溴含量测定[2]ꎬ然而用该法测试亦有缺点ꎬ第1对物理设备要求高ꎬ需要有X射线荧光光谱仪ꎬ第2对测试条件的把控要求高ꎬ需要选择合适的激发电位和谱线等ꎬ因而导致其测试结果偏差较大ꎮ根据«HJ636 ̄2012水质总氮的测定碱性过硫酸钾消解紫外分光光度法»中提到的ꎬ在一定温度下ꎬ碱性过硫酸钾溶液消解样品中的有机物使氮转化为硝酸盐ꎬ而后采用紫外分光光度法进行定量测试ꎮ众所周知的是ꎬ消解的作用是破坏样品中的有机物ꎬ使待测元素转化为无机态ꎬ因而消解过程一般是针对有机物ꎬ而非只对有机物中的某些特定结构起作用ꎬ正如«HJ636 ̄2012水质总氮的测定碱性过硫酸钾消解紫外分光光度法»中提到的ꎬ在碱性过硫酸钾消解紫外分光光度法下ꎬ可以测定样品中大部分有机含氮化合物中的氮ꎬ也就是可以消解掉大部分有机物ꎬ因而如果在有机物中存在溴ꎬ亦可以认为在消解后可以转化为易于测定的无机溴ꎬ如果消解后是溴离子ꎬ则可以用电位滴定法进行定量分析ꎬ如果是高价态的溴ꎬ如次溴酸根㊁溴酸根等ꎬ只要加入合适的还原剂将其还原为溴离子即可以用电位滴定法进行定量分析ꎮ1㊀实验部分1.1㊀主要仪器及试剂COD消解器 姜堰市银河仪器厂ꎻAgNO3ꎬNaClꎬNaOHꎬNa2S2O8ꎬ浓硝酸ꎬ冰乙酸ꎬ抗坏血酸ꎬ4 ̄溴苯甲酸ꎬ4 ̄溴甲基苯甲酸ꎬ溴乙酸 分析纯试剂ꎻ消解管ꎬ玻璃烧杯ꎬ电位计ꎬ双盐桥电极ꎬ银电极ꎬ磁力搅拌器等ꎮ1.2㊀测试方法配制AgNO3溶液和标准NaCl溶液ꎬ用标准NaCl溶液以电位滴定法标定AgNO3溶液的浓度ꎬ实验所用AgNO3溶液标定后浓度为0.01mol/kgꎮ配制Na2S2O8 ̄NaOH溶液ꎬ实验所用Na2S2O8浓度为40g/LꎬNaOH为15g/Lꎬ先单独配制2种溶液而后混合并进行定容ꎮ将4 ̄溴苯甲酸ꎬ4 ̄溴甲基苯甲酸和溴乙酸配制成溶液ꎬ4 ̄苯甲酸和4 ̄溴甲基苯甲酸微溶于水ꎬ因而在配制时加入了适量的NaOH以确保样品溶解ꎮ取5mLNa2S2O8 ̄NaOH溶液ꎬ分别取适量4 ̄溴㊀第33卷第3期㊀2020 ̄05㊀聚酯工业㊀PolyesterIndustryVol.33No.3㊀May.2020㊀苯甲酸溶液㊁4 ̄溴甲基苯甲酸溶液和溴乙酸溶液放入消解管ꎬ并对消解管进行封口处理ꎬ而后在120ħ下消解60minꎮ将浓硝酸稀释成wt=10%的硝酸溶液ꎬ配制0.1mol/L的抗坏血酸溶液ꎮ取10mL冰乙酸和5mL抗坏血酸加入到烧杯中ꎬ加入消解后的全部液体ꎬ并且用去离子水润洗消解管ꎬ润洗的液体也全部加入到烧杯中ꎬ而后将烧杯置于磁力搅拌器上搅拌5min等待高价溴在抗坏血酸作用下转化成溴离子ꎮ往烧杯中加入3mLwt=10%硝酸溶液ꎬ用标定过的AgNO3进行溴离子电位滴定ꎮ根据滴定曲线计算样品中的总溴元素含量ꎮ2㊀结果及讨论上文中所述的几种样品的测试结果如下ꎮ表1㊀总溴含量测试结果1Table1㊀Totalbrominecontenttestresult1编号样品名称总溴理论量/g总溴实测量/g偏差/%14 ̄溴苯甲酸0.0026820.002659-0.8624 ̄溴甲基苯甲酸0.0025130.002495-0.723溴乙酸0.0074020.007379-0.31以上测试中选择了几种有代表性的物质ꎬ4 ̄溴苯甲酸为苯环上的取代ꎬ4 ̄溴甲基苯甲酸为苄基位的取代ꎬ溴乙酸为烃基位的取代ꎬ根据测试结果可以看出ꎬ使用Na2S2O8 ̄NaOH体系进行消解ꎬ均可以很好的将以上几种有机溴转化为无机溴ꎬ在抗坏血酸作用下还原成溴离子ꎬ进行电位滴定得到的溴离子结果与样品中的总溴含量符合度很高ꎮ以上测试并未考虑到不溶性物质的情况ꎬ而在PTA行业中测试对象大都以浆料形式存在ꎬ因而补充了PTA残渣浆料的总溴含量测定实验ꎮ取某PTA生产厂家的残渣浆料进行Na2S2O8 ̄NaOH体系进行消解ꎬ而后对消解后的产物进行电位滴定测定溴离子含量ꎬ同时以使用X射线荧光光谱仪(XRF)对残渣浆料加溴化钾内标的方式测试的结果作为比较ꎬ结果如下ꎮ表2㊀总溴含量测试结果2Table2㊀Totalbrominecontenttsetresult2编号样品名称总溴浓度/(mg kg-1)测试方法1某厂家残渣浆料2878.40Na2S2O8消解 ̄电位滴定2某厂家残渣浆料2988.20XRF内标法由测试结果可见ꎬ使用2种方法测试得到的结果非常接近ꎬ若以XRF内标法测试的结果为真实值ꎬ则使用Na2S2O8消解 ̄电位滴定测试的结果偏差为 ̄3.67%ꎬ再结合表1中的标准样品测试结果ꎬ则完全有理由可以认定Na2S2O8消解 ̄电位滴定法适用于PTA行业中的总溴含量测试ꎬ且其测试方法的便捷以及测试结果的准确度有着比现有方法更大的优势ꎮ3㊀结语PTA行业中的总溴含量测定ꎬ可以使用Na2S2O8 ̄NaOH体系对样品进行消解后ꎬ在酸性条件下用抗坏血酸还原高价态的溴ꎬ而后进行溴离子电位滴定ꎬ可以准确地测试出样品中的总溴含量ꎮ参考文献:[1]㊀HindMEꎬTurnerJAꎬUreAM.ProcessfortheProductionofTe ̄rephthalicAcid[P].US5563293ꎬ1995 ̄06 ̄06.[2]㊀常毓巍ꎬ杨敬军ꎬ薛月霞.X ̄荧光光谱仪测定溶液中总溴浓度[J].兰州大学报(自然科学版)ꎬ2006ꎬ42(1):127 ̄128.[3]㊀仲军实.PTA生产中铁离子对氧化反应的影响[J].合成纤维工业ꎬ2003ꎬ26(5):24 ̄25.DeterminationoftotalbrominecontentHUJian ̄jun(ShaoxingHanqingEnvironmentalProtectionTechnologyCo.ꎬLtd.Shaoxing312300ꎬChina)Abstract:ThedeterminationmethodofTotalBromineContentinPTAindustrywasstudied.AfterthesamplewasdigestedbyNa2S2O8NaOHsystemꎬthehighvalenceinorganicbrominewasreducedbyascorbicacidꎬandthenthetotalbrominecontentinthesamplewasdeterminedbypotentiometrictitrationofbromineioninthedigestionprod ̄uct.ThroughthetestofsomestandardsamplesandtheverificationofPTAmanufacturer'sresidueslurryꎬithasahighdegreeofcompliance.ItisconsideredthatthismethodcanbeusedforthedeterminationofTotalBromineCon ̄tentinPTAindustry.Keywords:PTAꎻtotalbrominecontentꎻterephthalicacidꎻdigestionꎻpotentiometrictitration74第3期胡建军:DSC分析在聚酯生产中的应用。
氯胺T氧化-酚红分光光度法测定含碘卤水中溴陈玉锋;庄志萍;左明辉【摘要】卤水中微量溴离子常采用荧光素分光光度法测定[1],该法对时间的要求较为严格,操作较繁琐,测定含碘卤水中的溴离子重现性较差。
酚红分光光度法测定[2]卤水中的溴离子,碘对其测定干扰较大。
本工作在文献[3]基础上,采取措施消除碘的干扰,【期刊名称】《理化检验-化学分册》【年(卷),期】2012(048)004【总页数】2页(P477-478)【关键词】分光光度法测定;溴离子;卤水;含碘;酚红;氯胺T;氧化;荧光素【作者】陈玉锋;庄志萍;左明辉【作者单位】牡丹江师范学院化学化工学院,牡丹江157012;牡丹江师范学院化学化工学院,牡丹江157012;牡丹江师范学院化学化工学院,牡丹江157012【正文语种】中文【中图分类】O657.32卤水中微量溴离子常采用荧光素分光光度法测定[1],该法对时间的要求较为严格,操作较繁琐,测定含碘卤水中的溴离子重现性较差。
酚红分光光度法测定[2]卤水中的溴离子,碘对其测定干扰较大。
本工作在文献[3]基础上,采取措施消除碘的干扰,采用酚红分光光度法测定含碘卤水中溴离子。
VIS 7200型可见分光光度计,雷磁PHS-3C型精密pH计。
溴离子标准溶液:称取已于120℃干燥恒重后的溴化钾1.489 0 g,用少量去离子水溶解后,转入1 L容量瓶中,用去离子水稀至刻度,摇匀。
此溶液含溴离子 1.000 g·L-1。
所用试剂为分析纯,试验用水为去离子水。
1.2.1 标准曲线的绘制取一系列溴离子标准溶液于50 mL容量瓶中,用水稀至30 mL,加入pH 4.60的乙酸-乙酸钠缓冲溶液 1.00 mL,0.24 g·L-1酚红溶液 0.40 mL,充分摇匀,加入2 g·L-1氯胺 T 溶液 1.00 mL,摇动1 min,立即加入25 g·L-1硫代硫酸钠溶液1.00 mL,摇动,用水定容,摇匀。
化学检测工作站策划书为提高产品质量和性能,满足客户需要,促进研发成果,并结合目前实验室的测定项目和实验条件,质量部门需要在保证物理测试结果准确性的同时进行必要的化学测试实验。
首先将检测目标锁定在阻燃剂,添加剂,抗氧剂三个方面,根据其他公司的检测标准,应将增添化学检测指标定为基础的,必要的,操作简单,故在这三种物质当中我们需要增加的检测指标有元素的含量,1.元素含量1.1溴含量:溴含量的检测主要是在溴系阻燃剂中得以应有,溴含量主要分为三个部分:溴元素的含量,有机溴含量,游离溴含量。
目前公司利用ROSH测定的溴含量为溴元素的含量,而有机溴含量和游离溴含量又是判断溴系阻燃剂的主要指标,有必要对此进行检测。
1.1.1有机溴含量:是指在在阻燃剂中作为官能团上的溴。
测量方法:电位滴定法试剂:OP-10乳化剂;40%氢氧化钾溶液;氢氧化钠;1:1硝酸溶液;0.1mol/1硝酸银标准溶液;仪器:50ml 镍坩锅;调压电炉(2000W);25ml 酸式滴定管;电位滴定仪(216型银电极和217型双盐桥饱和甘汞电极);分析天平(准确致0.0002g)胶头滴管,250ml烧杯,玻璃棒,3个250ml锥形瓶。
检测原理:利用高温碱熔法,将有机溴转化为无机溴,再用硝酸银溶液对溴离子进行滴定,产生溴化银沉淀,随着加入体积的变化,离子浓度也产生变化,溶液电动势也随之改变,根据二级微商法△2E/△V2=0进行计算,进而计算出终点的滴定体积V,再进行空白试验得到滴定体积V0。
根据计算公式Xi={[C·(V-VO)×0.0799]/m}×100%,得到有机溴含量。
1.1.2游离溴含量指在阻燃剂中未被反应或已经分离出来的单质溴。
测量方法:氧化还原滴定法试剂:10g/l碘化钾溶液;0.1mol/l硫代硫酸钠标准溶液;0.002mol/l硫代硫酸钠标准溶液;溴苯。
仪器:天平(准确度为0.01g);恒温加热磁力搅拌器,3个250ml锥形瓶,空气冷凝器,500ml烧杯,50ml量筒,玻璃棒,检测原理:游离溴置换出碘化钾中的碘,单质碘遇到淀粉使溶液变蓝,滴定的硫代硫酸钠与单质碘反应,使溶液褪色,根据方程式,反应过程中硫代硫酸钠与单质碘物质量的比值为2:1,根据消耗的硫代硫酸钠的体积,求出碘的物质的量,进而求出溴的物质的量,然后求出质量。
水中溴离子的测定
1 方法提要
在PH4.4~5时,用氯胺T作氧化剂,将溴离子氧化为游离溴,再与酚红反应生成四溴酚红溶液,其颜色随溴离子含量的增大呈黄绿色至紫色,在590nm波长比色测定。
2 仪器和设备
紫外或可见光分光光度计。
3 试剂准备
3.1 乙酸-乙酸钠缓冲溶液:称取164g乙酸钠(CH3COONa·3H2O) 溶于适量纯水中,加8
4.0mL乙酸(ρ20=1.05g/mL),用纯水稀释至 1L。
3.2 酚红溶液:称取0.024g酚红〔C6H4SO2OC(C6H4-4-OH)2〕和0.12g 碳酸钠(Na2CO3) 于烧杯中,用纯水溶解,稀释至100mL。
3.3 氯胺T溶液(2g/L,需用棕色瓶冷藏保存):称取0.20g氯胺T 〔对甲苯磺酰氯胺钠(CH3C6H4SO2NClNa·3H2O) 〕溶于纯水中,稀释至100mL。
贮于棕色瓶中,冷藏保存。
3.4 硫代硫酸钠溶液(25g/L):称取2.5g硫代硫酸钠(Na2S2O3·5H2O) 溶于纯水中,稀释至100mL。
3.5 溴化物标准贮备溶液(0.1000mg/mL):购买。
配制为溴化物标准使用溶液 (10.00mg/L)待用。
4 分析步骤
4.1 样品测定
吸取10.00mL水样或稀释后取10mL水样于25mL比色管中,加0.50mL乙酸-乙酸钠缓冲溶液,3滴酚红溶液,摇匀。
再加入0.40mL 氯胺T溶液,立即摇匀。
放置1 min后(准确计时),加入0.40mL硫代硫酸钠溶液摇匀,使溶液脱氯。
放置5min后,用1cm比色皿,以试剂空白作参比,在590nm波长处,测量吸光度。
4.2 校准曲线的绘制
吸取溴化物标准使用溶液 0, 1.00, 2.00, 4.00, 6.00,8.00, 10.0mL 于一系列25mL比色管中,用纯水稀释至10mL。
以下操作同样品测试。
以比色管中溴化物的含量(mg)为横坐标,吸光度为纵坐标绘制校准曲线。
5 分析结果的表述
C(Br-)=m/V
式中:C(Br-)──水样中溴化物的质量浓度,mg/L;
m──从校准曲线上查得的比色管中溴化物的含量,μg;
V──所取水样的体积,mL。