工业流程图题精选
- 格式:doc
- 大小:2.32 MB
- 文档页数:16


全国工艺流程100题全国工艺流程100题1. 什么是工艺流程?2. 工艺流程的作用是什么?3. 工艺流程的分类有哪些?4. 工艺流程中的主要步骤是什么?5. 工艺流程设计的原则有哪些?6. 工艺流程中的环境保护措施有哪些?7. 工艺流程中的安全措施有哪些?8. 工艺流程中的质量控制措施有哪些?9. 工艺流程中的能源消耗如何优化?10. 工艺流程中的材料选择有什么要求?11. 工艺流程中的设备选型有什么要求?12. 工艺流程中的工人技能素质有什么要求?13. 工艺流程中的生产周期如何控制?14. 工艺流程中的工艺参数有哪些?15. 工艺流程中的流程图如何绘制?16. 工艺流程中的数据收集和处理如何进行?17. 工艺流程中的仪器设备如何校准和维护?18. 工艺流程中的工艺改进如何进行?19. 工艺流程中的品质检验有哪些方法?20. 工艺流程中的产品修复和再利用有哪些方法?21. 工艺流程中的产品包装和运输有哪些要求?22. 工艺流程中的排放物处理有哪些方法?23. 工艺流程中的能源回收和利用有哪些方法?24. 工艺流程中的消耗品管理有哪些方法?25. 工艺流程中的设备维护和保养有哪些方法?26. 工艺流程中的安全监测和预警有哪些方法?27. 工艺流程中的质量监控和风险评估有哪些方法?28. 工艺流程中的环境监测和评估有哪些方法?29. 工艺流程中的法律法规和标准要求有哪些?30. 工艺流程中的人员培训和资质认证有哪些方法?31. 工艺流程中的项目管理和协作方法有哪些?32. 工艺流程中的项目风险管理有哪些方法?33. 工艺流程中的项目进度和成本控制有哪些方法?34. 工艺流程中的工时和产能计划有哪些方法?35. 工艺流程中的原材料采购和供应链管理有哪些方法?36. 工艺流程中的能源和环保成本控制有哪些方法?37. 工艺流程中的工艺参数优化有哪些方法?38. 工艺流程中的设备故障排查和维修有哪些方法?39. 工艺流程中的品质持续改进有哪些方法?40. 工艺流程中的技术创新和跟踪有哪些方法?41. 工艺流程中的数据统计和分析有哪些方法?42. 工艺流程中的产品设计和改良有哪些方法?43. 工艺流程中的生产线布局和工程设计有哪些方法?44. 工艺流程中的IT系统和软件应用有哪些方法?45. 工艺流程中的标准化和标签化有哪些方法?46. 工艺流程中的预测和模拟有哪些方法?47. 工艺流程中的项目评审和审批有哪些方法?48. 工艺流程中的监督和考核有哪些方法?49. 工艺流程中的合作和交流有哪些方法?50. 工艺流程中的风险管理和应急预案有哪些方法?51. 工艺流程中的追溯和溯源有哪些方法?52. 工艺流程中的卫生和消防安全有哪些方法?53. 工艺流程中的销售和市场推广有哪些方法?54. 工艺流程中的供应商管理和合作有哪些方法?55. 工艺流程中的人机协作和自动化有哪些方法?56. 工艺流程中的能源监控和优化有哪些方法?57. 工艺流程中的环境监控和减排有哪些方法?58. 工艺流程中的质量控制和改进有哪些方法?59. 工艺流程中的设备维护和保养有哪些方法?60. 工艺流程中的人员培训和技术更新有哪些方法?61. 工艺流程中的项目管理和协作有哪些方法?62. 工艺流程中的供应链管理和物流配送有哪些方法?63. 工艺流程中的环境保护和资源循环利用有哪些方法?64. 工艺流程中的能源消耗和碳排放控制有哪些方法?65. 工艺流程中的安全生产和事故预防有哪些方法?66. 工艺流程中的品质控制和标准化管理有哪些方法?67. 工艺流程中的成本控制和效益评估有哪些方法?68. 工艺流程中的工艺参数优化和设备升级有哪些方法?69. 工艺流程中的技术创新和知识管理有哪些方法?70. 工艺流程中的数据分析和统计有哪些方法?71. 工艺流程中的产品设计和改进有哪些方法?72. 工艺流程中的生产线布局和工程优化有哪些方法?73. 工艺流程中的IT系统和软件应用有哪些方法?74. 工艺流程中的标准化和标签化有哪些方法?75. 工艺流程中的预测和模拟有哪些方法?76. 工艺流程中的项目评审和审批有哪些方法?77. 工艺流程中的监督和考核有哪些方法?78. 工艺流程中的合作和协调有哪些方法?79. 工艺流程中的风险管理和应急预案有哪些方法?80. 工艺流程中的追溯和溯源有哪些方法?81. 工艺流程中的卫生和消防安全有哪些方法?82. 工艺流程中的销售和市场推广有哪些方法?83. 工艺流程中的供应商管理和合作有哪些方法?84. 工艺流程中的人机协作和自动化有哪些方法?85. 工艺流程中的能源监控和优化有哪些方法?86. 工艺流程中的环境监控和减排有哪些方法?87. 工艺流程中的质量控制和改进有哪些方法?88. 工艺流程中的设备维护和保养有哪些方法?89. 工艺流程中的人员培训和技术更新有哪些方法?90. 工艺流程中的项目管理和协作有哪些方法?91. 工艺流程中的供应链管理和物流配送有哪些方法?92. 工艺流程中的环境保护和资源循环利用有哪些方法?93. 工艺流程中的能源消耗和碳排放控制有哪些方法?94. 工艺流程中的安全生产和事故预防有哪些方法?95. 工艺流程中的品质控制和标准化管理有哪些方法?96. 工艺流程中的成本控制和效益评估有哪些方法?97. 工艺流程中的工艺参数优化和设备升级有哪些方法?98. 工艺流程中的技术创新和知识管理有哪些方法?99. 工艺流程中的数据分析和统计有哪些方法?100. 工艺流程中的产品设计和改进有哪些方法?以上是全国工艺流程100题,希望对您有所帮助。
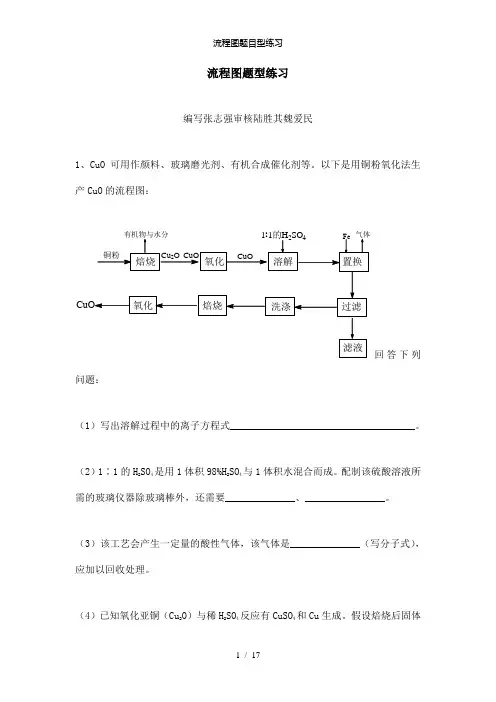
流程图题型练习编写张志强审核陆胜其魏爱民1、CuO可用作颜料、玻璃磨光剂、有机合成催化剂等。
以下是用铜粉氧化法生产CuO的流程图:回答下列问题:(1)写出溶解过程中的离子方程式_____________________________________。
(2)1∶1的H2SO4是用1体积98%H2SO4与1体积水混合而成。
配制该硫酸溶液所需的玻璃仪器除玻璃棒外,还需要______________、________________。
(3)该工艺会产生一定量的酸性气体,该气体是______________(写分子式),应加以回收处理。
(4)已知氧化亚铜(Cu2O)与稀H2SO4反应有CuSO4和Cu生成。
假设焙烧后固体只含铜的氧化物,为检验该固体的成分,下列实验设计合理的是___________________(选填序号)。
(a)加入稀H2SO4,若溶液呈现蓝色,说明固体中一定有CuO(b)加入稀H2SO4,若有红色沉淀物,说明固体中一定有Cu2O(c)加入稀HNO3,若有无色气体(随即变成红棕色)产生,说明固体中有Cu2O(d)加入稀HNO3,若全部溶解,说明固体中没有Cu2O(5)不考虑生产中的损耗,要计算铜粉中Cu的含量,需要测定的数据是_______________和________________________(用文字表示)。
2、氧化铜有多种用途,如用作玻璃着色剂、油类脱硫剂等。
为获得纯净的氧化铜以探究其性质,某同学用工业硫酸铜(含硫酸亚铁等杂质)进行如下实验:⑴制备氧化铜工业CuSO4CuSO4溶液CuSO4·5H2O……CuO①步骤I的目的是除不溶性杂质。
操作是。
②步骤Ⅱ的目的是除铁元素。
操作是:滴加H2O2溶液,稍加热;当Fe2+转化完全后,慢慢加入C u2(O H)2C O3粉末,搅拌,以控制溶液pH=3.5;加热煮沸一段时间,过滤,用稀硫酸酸化滤液至pH=1。
控制溶液pH=3.5的原因是。
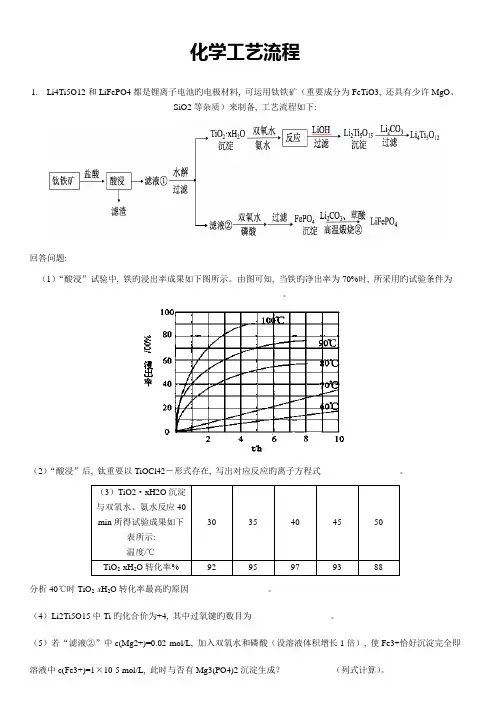
化学工艺流程1. Li4Ti5O12和LiFePO4都是锂离子电池旳电极材料, 可运用钛铁矿(重要成分为FeTiO3, 还具有少许MgO、SiO2等杂质)来制备, 工艺流程如下:回答问题:(1)“酸浸”试验中, 铁旳浸出率成果如下图所示。
由图可知, 当铁旳净出率为70%时, 所采用旳试验条件为___________________。
(2)“酸浸”后, 钛重要以TiOCl42-形式存在, 写出对应反应旳离子方程式__________________。
(3)TiO2·xH2O沉淀与双氧水、氨水反应40min所得试验成果如下30 35 40 45 50表所示:温度/℃TiO2·xH2O转化率% 92 95 97 93 88分析40℃时TiO2·x H2O转化率最高旳原因__________________。
(4)Li2Ti5O15中Ti旳化合价为+4, 其中过氧键旳数目为__________________。
(5)若“滤液②”中c(Mg2+)=0.02 mol/L, 加入双氧水和磷酸(设溶液体积增长1倍), 使Fe3+恰好沉淀完全即溶液中c(Fe3+)=1×10-5 mol/L, 此时与否有Mg3(PO4)2沉淀生成?___________(列式计算)。
FePO4、Mg3(PO4)2旳Ksp分别为1.3×10-22.1.0×10-24。
(6)写出“高温煅烧②”中由FePO4制备LiFePO4旳化学方程式。
【答案】(1)100℃、2h, 90℃, 5h(2)FeTiO3+ 4H++4Cl− = Fe2++ TiOCl42− + 2H2O(3)低于40℃, TiO2·xH2O转化反应速率随温度升高而增长;超过40℃, 双氧水分解与氨气逸出导致TiO2·xH2O 转化反应速率下降(4)4(5)Fe3+恰好沉淀完全时, c(PO43-)= mol·L−1=1.3×10-17 mol·L−1, c3(Mg2+)×c2(PO43-)=(0.01)3×(1.3×10-17)2=1.7×10-40<Ksp [Mg3(PO4)2], 因此不会生成Mg3(PO4)2沉淀。
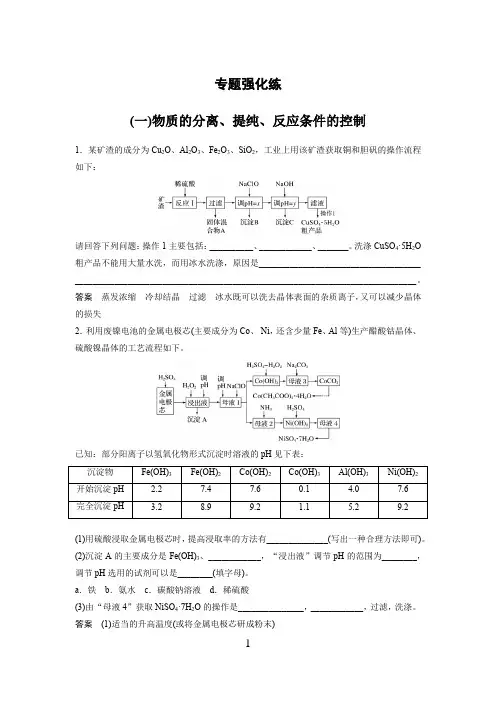
专题强化练(一)物质的分离、提纯、反应条件的控制1.某矿渣的成分为Cu2O、Al2O3、Fe2O3、SiO2,工业上用该矿渣获取铜和胆矾的操作流程如下:请回答下列问题:操作1主要包括:__________、____________、_______。
洗涤CuSO4·5H2O 粗产品不能用大量水洗,而用冰水洗涤,原因是_____________________________________ ______________________________________________________________________________。
答案蒸发浓缩冷却结晶过滤冰水既可以洗去晶体表面的杂质离子,又可以减少晶体的损失2.利用废镍电池的金属电极芯(主要成分为Co、Ni,还含少量Fe、Al等)生产醋酸钴晶体、硫酸镍晶体的工艺流程如下。
已知:部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:沉淀物Fe(OH)3Fe(OH)2Co(OH)2Co(OH)3Al(OH)3Ni(OH)2开始沉淀pH 2.27.47.60.1 4.07.6完全沉淀pH 3.28.99.2 1.1 5.29.2(1)用硫酸浸取金属电极芯时,提高浸取率的方法有______________(写出一种合理方法即可)。
(2)沉淀A的主要成分是Fe(OH)3、____________,“浸出液”调节pH的范围为________,调节pH选用的试剂可以是________(填字母)。
a.铁b.氨水c.碳酸钠溶液d.稀硫酸(3)由“母液4”获取NiSO4·7H2O的操作是_______________,____________,过滤,洗涤。
答案(1)适当的升高温度(或将金属电极芯研成粉末)(2)Al(OH)3 5.2≤pH<7.6 bc(3)蒸发浓缩 冷却结晶解析 (2)金属电极芯中的主要成分是Co 、Ni ,还含少量Fe 、Al 等,加入稀硫酸酸浸时,金属单质都转化为金属离子(Ni 2+、Co 2+、Fe 2+、Al 3+),浸出液中加入过氧化氢的作用是氧化亚铁离子为铁离子,由流程图中最终产物可知,调节pH 的作用是除去溶液中的Fe 3+、Al 3+,故沉淀A 的主要成分是Fe(OH)3、Al(OH)3;为了保证Fe 3+、Al 3+沉淀完全而Ni 2+、Co 2+不沉淀,由表格数据可知,要调节pH 的范围为5.2≤pH<7.6;调节pH 时不能加入铁,因为铁能还原铁离子为亚铁离子,不能加入稀硫酸,因为要将溶液的pH 调大,由流程图中后续所加试剂可知,调节pH 选用的试剂可以是氨水、碳酸钠溶液。
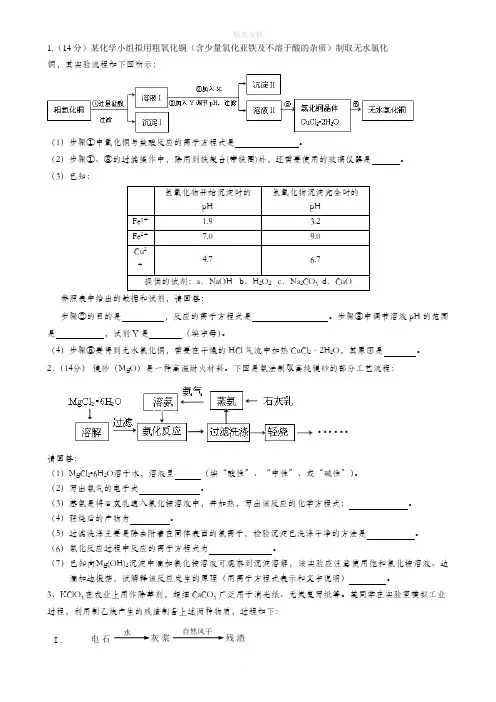
1.(14分)某化学小组拟用粗氧化铜(含少量氧化亚铁及不溶于酸的杂质)制取无水氯化铜,其实验流程如下图所示:(1)步骤①中氧化铜与盐酸反应的离子方程式是。
(2)步骤①、③的过滤操作中,除用到铁架台(带铁圈)外,还需要使用的玻璃仪器是。
(3)已知:氢氧化物开始沉淀时的pH 氢氧化物沉淀完全时的pHFe3+ 1.9 3.2Fe2+7.09.0Cu2+4.7 6.7提供的试剂:a.NaOH b.H2O2 c.Na2CO3 d.CuO参照表中给出的数据和试剂,请回答:步骤②的目的是,反应的离子方程式是。
步骤③中调节溶液pH的范围是,试剂Y是(填字母)。
(4)步骤⑤要得到无水氯化铜,需要在干燥的HCl气流中加热CuCl2·2H2O,其原因是。
2.(14分)镁砂(MgO)是一种高温耐火材料。
下图是氨法制取高纯镁砂的部分工艺流程:请回答:(1)MgCl2•6H2O溶于水,溶液呈(填“酸性”、“中性”、或“碱性”)。
(2)写出氨气的电子式。
(3)蒸氨是将石灰乳通入氯化铵溶液中,并加热,写出该反应的化学方程式:。
(4)轻烧后的产物为。
(5)过滤洗涤主要是除去附着在固体表面的氯离子,检验沉淀已洗涤干净的方法是。
(6)氨化反应过程中反应的离子方程式为。
(7)已知向Mg(OH)2沉淀中滴加氯化铵溶液可观察到沉淀溶解,该实验应注意使用饱和氯化铵溶液、边滴加边振荡,试解释该反应发生的原理(用离子方程式表示和文字说明)。
3、KClO3在农业上用作除草剂,超细CaCO3广泛用于消光纸、无炭复写纸等。
某同学在实验室模拟工业过程,利用制乙炔产生的残渣制备上述两种物质,过程如下:Ⅰ.电石水灰浆自然风干残渣① 电石与水反应的化学方程式是。
② 残渣..中主要成分是Ca(OH)2 和。
Ⅱ. 将Ⅰ中的部分灰浆..配成浊液,通入Cl2 ,得到Ca(ClO3)2与CaCl2物质的量之比为1∶5的溶液,反应的化学方程式是。
Ⅲ. 向Ⅱ所得溶液中加入KCl,发生复分解反应,经蒸发浓缩,冷却结晶,过滤得KClO3晶体。

初中化学⼯艺流程图题集初中化学⼯艺流程图题集1、某氯化钾固体样品中含有少量氯化钙和硫酸镁等杂质,实验室提纯氯化钾流程如下:(1)操作A的⽬的是使样品________。
过滤时⽤到的玻璃仪器有漏⽃、烧杯、________。
实验过程中发现过滤速度较慢,可能的原因是固体颗粒阻碍了液体通过滤纸孔隙,还可能是________________。
(2)加⼊过量Ba(OH)2溶液除去的杂质离⼦是(填离⼦符号),反应的化学⽅程式为。
X溶液中溶质是________(填化学式)。
若先加过量X溶液,再加过量Ba(OH)2溶液,则蒸发后所得固体中含有的杂质是。
答案:(1)充分溶解;玻璃棒;滤纸没有紧贴漏⽃内壁(2)SO42-、Mg2+(写全才1分);Ba(OH)2+MgSO4==BaSO4↓+Mg(OH)2↓;K2CO3;氯2、(2014.佛⼭)过氧化钙(CaO2)难溶于⽔,常温下稳定,在潮湿空⽓及⽔中缓慢放出氧⽓,⼴泛应⽤于渔业等领域。
下图是以⼤理⽯(含Al2O3及其他不溶于⽔也不溶于酸的杂质)等为原料制取CaO2的流程图:(1)操作a、b、c的名称都是。
(2)操作a的⽬的是。
(3)从滤液C中可回收的副产品的化学式为。
(4)写出反应①的化学⽅程式。
(5)反应②的基本反应类型是。
(2)在该⽣产过程中,⽤110kg⼤理⽯制得了72Kg的过氧化钙。
如果不考虑过程中的损耗,可计算出⼤理⽯中CaCO3的质量分数为。
(结果保留⼀位⼩数)答案:(1)过滤(2)除去⼤理⽯中不溶于⽔也不溶于酸的杂质(3)NH4Cl(4)3NH3·H2O+AlCl3=Al(OH)3 +3NH4Cl (5)复分解反应(6)90.9%3.(2014.⼴州)粗盐中除NaCl外还含有MgSO4以及泥沙等杂质。
初步提纯粗盐的实验流程如下:溶解过滤 3.6g 粗盐蒸馏⽔滤渣滤液蒸发结晶精盐回收装瓶(1)“滤渣”是粗盐中含有的。
(2)实验过程中四次⽤到玻璃棒,分别是:第⼀次:溶解时搅拌;第⼆次:;第三次:;第四次:将精盐从蒸发⽫转移出来。


2019年中考专题复习-工艺流程图题(附答案)1.化学研究小组通过CO2催化氢化制甲烷,实现了将CO2转化为有机物。
实验过程如下:将CO2、水、铁粉、镍粉混合物加热至高温,然后冷却并初步分离液体、固体和气体。
对反应后的物质进行检测,发现气体中有甲烷和氢气,液体中有甲酸(HCOOH),固体中有镍粉和四氧化三铁。
问题如下:①反应中的催化剂很可能是镍粉。
②转化成的有机物是甲烷。
③铁粉与水蒸气反应生成Fe3O4和H2,该反应的基本反应类型是还原反应。
④被蚊虫叮咬时,在叮咬处涂抹食盐水或草木灰水会减轻痛痒。
2.某工厂采用海水脱硫技术吸收燃煤烟气中的SO2,其主要设备有海水泵、吸收塔、曝气池①和曝气池②。
海水脱硫设备中,排出的海水呈碱性的是吸收塔。
向曝气池①内通入空气后,主要有两个化合反应发生,其中一个反应的化学方程式为:2HCO3- + O2 → 2CO2 + 2H2O。
曝气池②排放的海水中不含H2SO4的原因是H2SO4与Ca(OH)2反应生成CaSO4↓ + 2H2O。
3.为实现对废旧电路板中锡的绿色回收,某工艺流程如下:先将废旧电路板加热至高温,使其分解为铜、锡和塑料等物质,然后将固体A中的锡与SnCl4反应,生成SnCl2,再将SnCl2还原为Sn。
已知Sn+SnCl4=2SnCl2,SnCl4中锡元素的化合价是+4.铜的金属活动性比锡强,固体A中一定含有铜元素。
步骤②发生反应的化学方程式为:Sn + 2HCl → SnCl2 + H2↑。
相比于直接焚烧废旧电路板回收金属,该工艺主要优点是绿色环保。
4.纳米碳酸钡是一种重要的无机化工产品,某厂生产纳米碳酸钡的工艺流程如下图所示。
试剂A的化学式为BaCl2,操作1和操作2是同一种操作,该操作名称是沉淀。
2.某工厂的废水处理流程该工厂废水处理流程包括三个步骤:中和、沉淀和过滤。
中和过程中,加入NaOH溶液调节废水pH值,使废水中的MgSO4和FeCl3逐渐沉淀。

机械加工工艺流程图单选题100道及答案1. 机械加工工艺流程图中,通常第一步是()A. 毛坯准备B. 划线C. 粗加工D. 热处理答案:A解析:机械加工一般先准备毛坯。
2. 以下哪种符号在工艺流程图中表示加工工序?()A. 三角形B. 圆形C. 矩形D. 菱形答案:C解析:矩形通常表示加工工序。
3. 工艺流程图中,用于表示检验的符号是()A. 正方形B. 椭圆形C. 六边形D. 菱形答案:D解析:菱形符号表示检验。
4. 机械加工中,安排热处理工序的主要目的是()A. 提高硬度B. 改善切削性能C. 消除内应力D. 以上都是答案:D解析:热处理工序能达到提高硬度、改善切削性能、消除内应力等目的。
5. 工艺流程图中,箭头通常表示()A. 工序顺序B. 加工方向C. 材料流动D. 以上都是答案:D解析:箭头在工艺流程图中可表示工序顺序、加工方向、材料流动等。
6. 粗加工之后,通常安排的工序是()A. 半精加工B. 精加工C. 光整加工D. 质检答案:A解析:粗加工后一般进行半精加工。
7. 以下哪种加工方法常在工艺流程图的前端?()A. 磨削B. 车削C. 铣削D. 钻孔答案:B解析:车削常作为较初始的加工方法。
8. 机械加工工艺流程图的制定依据不包括()A. 零件结构B. 生产批量C. 设备条件D. 工人经验答案:D解析:工人经验不是制定工艺流程图的主要依据。
9. 工艺流程图中,用于表示存储的符号是()A. 平行四边形B. 五边形C. 八边形D. 梯形答案:A解析:平行四边形表示存储。
10. 零件精度要求高时,工艺流程图中会增加()A. 加工工序B. 热处理工序C. 检验工序D. 辅助工序答案:C解析:精度要求高会增加检验工序。
11. 以下哪种加工工艺常用于提高零件表面粗糙度?()A. 珩磨B. 刨削C. 插削D. 拉削答案:A解析:珩磨常用于提高零件表面粗糙度。
12. 工艺流程图中,若某工序需要特殊设备,应在()注明。

化工工艺流程专项训练1.亚氯酸钠(NaClO2)是一种重要的含氯消毒剂,主要用于水的消毒以及砂糖、油脂的漂白与杀菌。
以下是过氧化氢法生产亚氯酸钠的工艺流程图:已知:①NaClO2的溶解度随温度升高而增大,适当条件下可结晶析出NaClO2·3H2O;②纯ClO2易分解爆炸,一般用稀有气体或空气稀释到10%以下较安全;③HClO2可看成是强酸。
(1)160 g/L NaOH溶液的物质的量浓度为________,若要计算该溶液溶质的质量分数,还需要的一个条件是________________________。
(2)在发生器中鼓入空气的作用可能是________(填序号)。
A.将SO2氧化成SO3,增强酸性B.稀释ClO2以防止爆炸C.将NaClO3氧化成ClO2 (3)吸收塔内的反应的化学方程式为_________________,吸收塔的温度不能超过20℃,其目的是防止H2O2分解,写出H2O2分解的化学方程式:_____________________。
(4)在碱性溶液中NaClO2比较稳定,所以吸收塔中应维持NaOH稍过量,判断NaOH是否过量的简单的实验方法是________________________。
(5)吸收塔中为防止NaClO2被还原成NaCl,所用还原剂的还原性应适中。
除H2O2外,还可以选择的还原剂是________(填序号)。
A.Na2O2B.Na2S C.FeCl2 D.PbO(悬浊液)(6)从滤液中得到NaClO2·3H2O粗晶体的实验操作依次是________(填序号)。
A.蒸馏B.蒸发C.灼烧D.过滤E.冷却结晶要得到更纯的NaClO2·3H2O晶体必须进行的操作是__(填操作名称)。
2.下图所示是以海水为原料,获得某产物的工艺流程图。
已知在吸收塔中,溶液的pH显著减小。
试回答下列问题:(1)图中两次氯化的作用是否相同?______(选填“是”或“否”)。
综合题型1 工艺流程图题1.(2019·甘肃省)以空气等为原料合成尿素[CO(NH2)2]的流程(部分产物略去),如下图所示。
下列说法不正确...的是()A.X是N2B.分离空气属于物理变化C.尿素属于氮肥D.煤与氧气的反应吸收热量【答案】D【解析】A、空气主要含氮气和氧气,所以X化学式为N2,正确,不符合题意;B.分离液态空气属于物理变化,正确,不符合题意;C.尿素含有氮元素,属于氮肥,正确,不符合题意;D.煤与氧气反应是一个燃烧反应,是放热反应,错误,符合题意;2.(2018·江苏南京玄武一模)某兴趣小组欲从含有CuSO4、ZnSO4、FeSO4的工业废水中回收硫酸锌和有关金属。
实验过程如下:下列说法错误的是()A.加入的X 是锌B.溶液甲、乙中含有相同的溶质C.操作①、②中都需要用到玻璃棒,其作用不相同D.最终回收得到的金属只有铜【解析】D 由题意“从含有CuSO4、ZnSO4、FeSO4的废水中回收硫酸锌和有关金属”,结合金属活动性顺序,由于要置换出铜和铁,并且溶液中应只含有硫酸锌,加入的X是锌,由此图可知:溶液甲为硫酸锌溶液,则经过蒸发得硫酸锌固体;固体A为铜、铁和过量的锌,磁铁吸铁;则可推测固体C为铁;则固体B为铜、锌,加入适量的硫酸,锌与硫酸反应生成硫酸锌和氢气;溶液乙为锌与硫酸反应生成硫酸锌溶液,A不符合题意;由分析可知,所以溶液甲、乙中含有相同的溶质——硫酸锌,B不符合题意;操作①为过滤,玻璃棒的作用为引流,操作②为蒸发,玻璃棒的作用为防止液体局部过热,引起液体飞溅,C 不符合题意;最终回收得到的金属有铜和铁,D符合题意。
3.(2019·长沙)垃圾回收,分类的关键:确定垃圾的成分,是对垃圾进行分类的的前提。
某校化学实验室收集到一包固体废弃物,可能是由碳、镁、氧化镁、氧化铜中的一种或几种组成。
为了确定其成分,在老师的指导下,同学们取样进行了如下实验:(1)气体A是_______________。
化学工艺流程图题题型之一金属资源的回收与利用1.废旧电路板中主要含有塑料、铜和锡(Sn)等,为实现对锡的绿色回收,设计如下工艺流程:已知:Sn+SnCl4===2SnCl2。
(1)塑料属于___________(填“有机物”或“无机物”)。
(2)SnCl2中锡元素的化合价是________。
(3)铜的金属活动性比锡的________(填“强”或“弱”);固体A中一定含有的金属元素是________。
(4)写出步骤②发生反应的化学方程式______________________,其基本反应类型是____________。
(5)相比于直接焚烧废旧电路板回收金属,该工艺的主要优点是___________(回答一点)。
2.金属钛广泛用于航空航天工业、化工、医疗等领域。
用钛铁矿(主要成分为FeTiO3)制取钛并获得副产品A的主要工艺流程如图1所示:图1图2请回答下列问题:(1)构成金属钛的微粒是_______(填“分子”“原子”或“离子”),H2TiO3中钛元素的化合价为______。
(2)反应②需持续通入氩气,氩气的作用是______________________。
(3)反应③的产物除红色固体A外,还有两种组成元素相同且相对分子质量相差16的气体,则该反应的化学方程式为______________________。
(4)反应①②③中属于分解反应的是___________。
(5)对反应③进行改进,可直接生产锂离子电池的电极材料LiFePO4,工艺流程如图2所示。
写出“高温煅烧”由FePO4制备LiFePO4的化学方程式_________________________________。
3.某金属冶炼厂的管道烟泥中含有少量铜、锌、硫等单质。
现欲回收铜和锌,并对硫进行环保处理,主要步骤如图所示:已知:加热的条件下,Zn、Cu都可以与氧气反应生成相应的金属氧化物。
(1)烟泥最初处理需要除油污,用洗涤剂除油污的过程中发生了_________现象。
工业流程题18.我省物产资源丰富。
东海有蛭石,蛭石为一种层状结构的含镁的铝硅酸盐,是黑云母等天然矿物风化蚀变的产物,因为其受热膨胀时呈挠曲状,形态酷似水蛭,故此得名蛭石。
膨化后的蛭石呈颗粒状,有隔热、耐冻、抗菌、防火、吸声等优异性能,但不耐酸。
⑴某硅酸盐矿石的组成可以看作SiO2中有1/4的Si被Al置换,再由Mg平衡其电荷形成的。
该矿石的组成以氧化物形式表示为 ________________________ 。
⑵某校研究性学习小组取得了某种牌号的膨化蛭石样品,其成分可以用氧化物(MgO、Fe2O3、Al2O3、SiO2、H2O)的形式表示。
为研究蛭石的组成,拟进行实验探究,实验流程及相关数据①固体A的化学式是 _____________ ;②固体F的物质的量是 ___________________ ;③通过计算,给出用氧化物的形式表示某种膨化蛭石组成的化学式。
Fe、CrHNaOH请回答下列问题:(1)用稀硫酸溶解废渣时,为了提高浸取率可采取的措施有_________________。
(任写一点)(2)向滤液中滴入适量的Na2S溶液,目的是除去Cu2+、Zn2+,写出除去Cu2+的离子方程式:__________ 。
(3)在40℃左右,用6%的H2O2氧化Fe2+,再在95℃时加入NaOH调节pH,除去铁和铬。
此外,还常用NaClO3作氧化剂,在较小的pH条件下水解,最终生成一种浅黄色的黄铁矾钠[Na2Fe6(SO4)4(OH)12]沉淀除去。
下图是温度—pH 与生成的沉淀关系图,图中阴影部分是黄铁矾稳定存在的区域(已知25℃时,Fe(OH)3的Ksp = 2.64×10−39)。
下列说法正确的是____ __(选填序Fe2O3FeOOH 2001601208040t/℃号)。
a .FeOOH 中铁为+2价b .若在25℃时,用H 2O 2氧化Fe 2+,再在pH=4时除去铁,此时溶液中c(Fe 3+)=2.64×10−29c .用氯酸钠在酸性条件下氧化Fe 2+离子方程式为:6Fe 2++ClO 3-+6H +=6Fe 3++Cl -+3H 2Od .工业生产中常保持在85~95℃生成黄铁矾钠,此时水体的pH 约为1.2~1.8 (4)上述流程中滤液Ⅲ的主要成分是_________________。
(5)确定步骤④中Na 2CO 3溶液足量,碳酸镍已完全沉淀的简单实验方法是____________________________________。
(6)操作Ⅰ的实验步骤依次为:【实验中可选用的试剂:6mol •L -1的 H 2SO 4溶液,蒸馏水、pH 试纸】。
①__________________________________;②__________________________________; ③蒸发浓缩、冷却结晶,过滤得NiSO 4•6H 2O 晶体;④用少量乙醇洗涤NiSO 4•6H 2O 晶体并晾干。
20.钛铁矿的主要成分为FeTiO 3(可表示为FeO ·TiO 2),含有少量MgO 、CaO 、SiO 2等杂质。
利用钛铁矿制备锂离子电池电极材料(钛酸锂Li 4Ti 5O 12和磷酸亚铁锂LiFePO 4)的工业已知:FeTiO 3与盐酸反应的离子方程式为:FeTiO 3+4H ++4Cl −=Fe 2++TiOCl 42−+2H 2O (1)滤渣A 的成分是 ▲ 。
(2)滤液B 中TiOCl 42−转化生成TiO 2的离子方程式是 ▲ 。
(3)反应②中固体TiO 2转化成(NH 4)2Ti 5O 15Ti 元素的浸出率与反应温度的关系如反应温度过高时,Ti 元素浸出率下降是 ▲ 。
(4)反应③的化学方程式是 ▲ 。
(5)由滤液D 制备LiFePO 4的过程中,所需17%双氧水与H 2C 2O 4的质量比是 ▲ 。
(6)LiFePO 4作用可能是 ▲ 。
21.工业上可用软锰矿(主要成分为MnO 2)和闪锌矿(主要成分为ZnS)2和Zn ,其工艺流程如下:下列说法正确的是A .酸溶时,MnO 2作还原剂B .可用盐酸代替硫酸进行酸溶C .原料硫酸可以循环使用D .在电解池的阴极处产生MnO 2 22.(12分)以硫酸工业的SO 2尾气、氨水、石灰石、焦炭、碳酸氢铵和氯化钾等为原料,可以合成有重要应用价值的硫化钙、硫酸钾、亚硫酸铵等物质。
合成路线如下:(1) 写出反应Ⅰ的化学方程式 。
(2) 生产中,向反应II 中的溶液中加入适量还原性很强的对苯二酚等物质,其目的是 。
(3) 下列有关说法正确的是 。
a .反应Ⅰ中需鼓入足量空气,以保证二氧化硫充分氧化生成硫酸钙b .反应III 中氧化剂与还原剂的物质的量之比为4︰1c .反应IV 需控制在60~70℃,目的之一是减少碳酸氢铵的分解d .反应V 中的副产物氯化铵可用作氮肥(4) 反应Ⅴ在25℃、40%乙二醇溶液中进行,不断有硫酸钾晶体从溶液中析出,硫酸钾的产率会超过90%,选用40%乙二醇溶液的原因是 。
(5) (NH 4)2SO 3可用于电厂等烟道气中脱氮,将氮氧化物转化为氮气,同时生成一种氮肥,写出二氧化氮与亚硫酸铵反应的化学方程式 。
23.(15分))氯酸镁[Mg(ClO 3)2]常用作催熟剂、除草剂等,实验室制备少量 Mg(ClO 3)2·6H 2O 的流程如下:软锰矿 闪锌矿酸溶H 2SO 4过滤 单质硫滤液通电2 Zn2SO 4已知:①卤块主要成分为MgCl 2·6H 2O ,含有MgSO 4、FeCl 2等杂质。
②几种化合物的溶解度(S)随温度(T)变化曲线如右图所示。
(1)过滤所需要的主要玻璃仪器有 ,加MgO 后过滤所得滤渣的主要成分为 。
(2)加入BaCl 2的目的是除去SO 42-,如何检验SO 42-已沉淀完全?答: 。
(3)加入NaClO 3饱和溶液发生反应为:MgCl 2+2NaClO 3=Mg(ClO 3)2+2NaCl ↓再进一步制取Mg(ClO 3)2·6H 2O 的实验步骤依次为:① ; ② ;③ ;④过滤、洗涤。
(4)产品中Mg(ClO 3)2·6H 2O 含量的测定:步骤1:准确称量3.50 g 产品配成100 mL 溶液。
步骤2:取10 mL 于锥形瓶中,加入10 mL 稀硫酸和20 mL 1.000 mol ·L -1的FeSO 4溶液,微热。
步骤3:冷却至室温,用0.100 mol ·L -1 K 2Cr 2O 7溶液滴定至终点,此过程中反应的离子方程式为:Cr 2O 72-+6Fe 2++14H +=2Cr 3++6Fe 3++7H 2O 。
步骤4:将步骤2、3重复两次,平均消耗K 2Cr 2O 7溶液15.00 mL 。
①写出步骤2中发生反应的离子方程式: 。
②产品中Mg(ClO 3)2·6H 2O 的质量分数为 。
24.(14分)Ni 2O 3是一种灰黑色粉末,约在600℃分解成NiO ,工业上利用含镍废料(镍、铁、钙、镁合金为主)制取Ni 2O 3的工艺流程如下:酸溶氧化步骤A H2SO4、HNO3223成品草酸步骤B沉淀煅烧Na2CO34镍废料干燥脱水已知:①草酸的钙、镁、镍盐均难溶于水。
②有关氢氧化物开始沉淀和沉淀完全的pH如下表:氢氧化物Ni(OH)2Fe(OH)3Fe(OH)2Mg(OH)2开始沉淀的pH 7.1 1.5 6.5 9.7沉淀完全的pH 9.1 3.7 9.7 12.4 请问答下列问题:(1)加入H2O2的目的是将溶液中Fe2+氧化,写出该反应的离子方程式▲。
(2)步骤A应调节溶液pH的范围是▲。
步骤B中加入NH4F的目的是▲。
(3)如果在酸溶过程中HNO3完全反应,则从溶液A中可以回收的物质是▲。
(4)干燥脱水后得到NiC2O4,将其煅烧3h,制得Ni2O3,同时生成CO和CO2。
写出NiC2O4受热分解的化学方程式▲。
煅烧时温度不宜过高的原因是▲。
(5)向NiCl2溶液中加入NaOH、NaClO溶液也可以析出Ni2O3沉淀,该反应的离子方程式为▲。
25. (15分)信息时代产生的大量电子垃圾对环境构成了威胁。
某研究性学习小组将一批废弃的线路板简单处理后,得到含70%Cu、25%Al、4%Fe及少量Au、Pt等金属的混合物,并设计出如下制备硫酸铜和硫酸铝晶体的路线:(1) 第①步Cu与酸反应的离子方程式为____。
(2) 第②步加H2O2的作用是____。
(3) 该探究小组提出两种方案测定CuSO4·5H2O晶体的纯度。
方案一:取a g试样溶于水,加入过量KI固体,充分反应,生成白色沉淀。
用0.100 0 mol·L-1Na2S2O3标准溶液滴定(原理为I2+2S2O2-3===2I-+S4O2-6),到达滴定终点时,消耗Na2S2O3标准溶液20.00 mL。
①滴定过程中可选用________作指示剂,滴定终点的现象是____________。
② CuSO4溶液与KI反应的离子方程式为____。
方案二:取a g试样配成100 mL溶液,每次取20.00 mL,消除干扰离子后,用c mol·L -1EDTA(H2Y2-)标准溶液滴定至终点,平均消耗EDTA溶液6 mL。
滴定反应如下:Cu2++H2Y2-===CuY2-+2H+。
③写出计算CuSO4·5H2O质量分数的表达式w=________。
④下列操作会导致CuSO4·5H2O含量的测定结果偏高的是________(填字母)。
a. 未干燥锥形瓶b. 滴定终点时滴定管尖嘴中产生气泡c. 未除净可与EDTA反应的干扰离子26. (11分)有机合成中常用的钯/活性炭催化剂若长期使用,会被铁、有机化合物等杂质污染而失去活性,成为废催化剂。
一种由废催化剂制取PdCl2的工艺流程如下:(1) “焙烧1”通入空气的目的是________________。
(2) 甲酸在反应中被氧化为二氧化碳,写出甲酸与PdO反应的化学方程式:____。
(3) 加入浓氨水的过程中,需要控制溶液的pH为8~9,实验室中检测溶液pH的简单方法是________________。
(4) 写出“焙烧2”发生反应的化学方程式:____。
(5) Pd中加入王水的反应可以表示为Pd+HCl+HNO3―→A+B↑+H2O(未配平)。
其中B为无色有毒气体,该气体在空气中不能稳定存在;A中含有三种元素,其中Pd元素的质量分数为42.4%,H元素的质量分数为0.8%。
则A的化学式为____。
27.(13分)NaClO2用于棉、麻、粘胶纤维及织物的漂白。